初中化学九年级下粤教版 溶液的酸碱性 导学案
文档属性
| 名称 | 初中化学九年级下粤教版 溶液的酸碱性 导学案 |
|
|
| 格式 | zip | ||
| 文件大小 | 114.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-03-11 00:00:00 | ||
图片预览

文档简介
溶液的酸碱性导学案
酸碱中和反应过程中溶液pH变化情况
【学习目标】认识清楚酸碱中和反应过程中溶液酸碱性的变化情况。
【学习重点】1. pH与生命活动。
2.用pH来表示酸碱中和反应变化过程。
【学习内容】
酸碱中和反应过程中溶液pH变化情况
5. pH与生命活动
(1).胃酸(主要成分是盐酸)(2).乳酸(3).土壤的酸碱性。
6.pH的变化
在pH<7的溶液中加水,则溶液酸性减弱,pH增大,pH变化如右图1
在pH>7的溶液中加水,则溶液碱性减弱,pH减小,pH变化如右图2
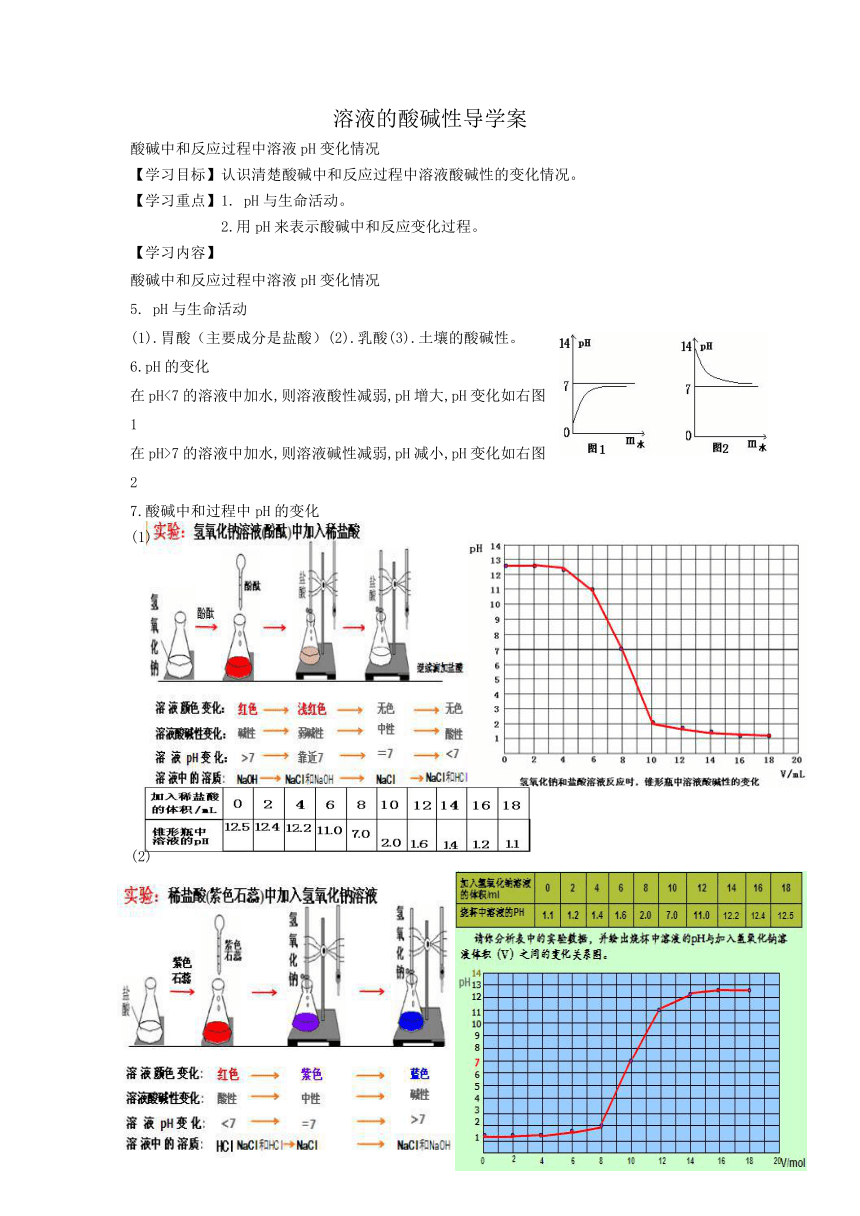
7.酸碱中和过程中pH的变化
(1)
(2)
(3)
【课堂反馈】
______________________________________________________________________________________________________________________________________________________________
【课堂练习】—1
1.某溶液的pH=8,为了使其pH降低应该 ( )
A. 滴加稀硫酸 B. 滴加NaOH C. 加水 D. 倒出一半溶液
2.一些食物的近似pH如下:番茄4.0~4.4;苹果2.9~3.3;
牛奶6.3~6.6;鸡蛋清7.6~8.0。则下列说法中不正确的是 ( )
A. 胃酸过多的人应少食苹果 B. 番茄汁属酸性食品
C. 牛奶和鸡蛋清均为碱性食品 D. 苹果汁酸性比牛奶强
3.下列物质放入或通入水中,能使pH增大的是 ( )
A. NaCl B. 白醋 C. 干冰 D. 生石灰
4.右表中为家庭中一些常见物质的pH:
蚊子、蜂、蚂蚁等昆虫叮咬人时,会向人体注入一种叫蚁酸(具有酸的性质)的物质,使皮肤红肿、痛痒。要消除这种症状,可在叮咬处涂抹一些家庭中的常见物。它是下列中的( )
A. 火碱溶液 B. 食盐水 C. 牙膏或肥皂水 D. 食醋
5.下列物质能跟盐酸发生中和反应的是 ( )
A. 锌粒 B. 氢氧化钠溶液 C. 氧化铜 D. 碳酸钠溶液
6.苯甲酸(C6H5COOH)可用作食品防腐剂,其酸性比醋酸强,下列对苯甲酸性质的推测不合理的是 ( )
A. 苯甲酸溶液的pH小于7 B. 苯甲酸溶液的pH大于7
C. 苯甲酸溶液能使紫色石蕊试液变红 D. 苯甲酸溶液不能使无色酚酞试液变色
7.有一块农田不长庄稼,经测定是酸性太强,可以适当施入 ( )
A. 石灰石 B. 熟石灰 C. 草木灰 D. 氮肥
8.下列物质中,不宜用作治疗胃酸(含稀盐酸)过多的药物是 ( )
A.NaHCO3 B.NaOH C.Al(OH)3 D.墨鱼骨粉(含CaCO3)
9.下面是几种作物生长时对土壤pH值要求的最佳范围:茶5~5.5;西瓜6;大豆6~7,甜菜7~7.5;如果某地区经常降酸雨,以上作物最不适宜种植的是 ( )
A. 茶 B. 西瓜 C. 大豆 D. 甜菜
【教学体会及注意事项】
______________________________________________________________________________________________________________________________________________________
酸碱中和反应过程中溶液pH变化情况
【学习目标】认识清楚酸碱中和反应过程中溶液酸碱性的变化情况。
【学习重点】1. pH与生命活动。
2.用pH来表示酸碱中和反应变化过程。
【学习内容】
酸碱中和反应过程中溶液pH变化情况
5. pH与生命活动
(1).胃酸(主要成分是盐酸)(2).乳酸(3).土壤的酸碱性。
6.pH的变化
在pH<7的溶液中加水,则溶液酸性减弱,pH增大,pH变化如右图1
在pH>7的溶液中加水,则溶液碱性减弱,pH减小,pH变化如右图2
7.酸碱中和过程中pH的变化
(1)
(2)
(3)
【课堂反馈】
______________________________________________________________________________________________________________________________________________________________
【课堂练习】—1
1.某溶液的pH=8,为了使其pH降低应该 ( )
A. 滴加稀硫酸 B. 滴加NaOH C. 加水 D. 倒出一半溶液
2.一些食物的近似pH如下:番茄4.0~4.4;苹果2.9~3.3;
牛奶6.3~6.6;鸡蛋清7.6~8.0。则下列说法中不正确的是 ( )
A. 胃酸过多的人应少食苹果 B. 番茄汁属酸性食品
C. 牛奶和鸡蛋清均为碱性食品 D. 苹果汁酸性比牛奶强
3.下列物质放入或通入水中,能使pH增大的是 ( )
A. NaCl B. 白醋 C. 干冰 D. 生石灰
4.右表中为家庭中一些常见物质的pH:
蚊子、蜂、蚂蚁等昆虫叮咬人时,会向人体注入一种叫蚁酸(具有酸的性质)的物质,使皮肤红肿、痛痒。要消除这种症状,可在叮咬处涂抹一些家庭中的常见物。它是下列中的( )
A. 火碱溶液 B. 食盐水 C. 牙膏或肥皂水 D. 食醋
5.下列物质能跟盐酸发生中和反应的是 ( )
A. 锌粒 B. 氢氧化钠溶液 C. 氧化铜 D. 碳酸钠溶液
6.苯甲酸(C6H5COOH)可用作食品防腐剂,其酸性比醋酸强,下列对苯甲酸性质的推测不合理的是 ( )
A. 苯甲酸溶液的pH小于7 B. 苯甲酸溶液的pH大于7
C. 苯甲酸溶液能使紫色石蕊试液变红 D. 苯甲酸溶液不能使无色酚酞试液变色
7.有一块农田不长庄稼,经测定是酸性太强,可以适当施入 ( )
A. 石灰石 B. 熟石灰 C. 草木灰 D. 氮肥
8.下列物质中,不宜用作治疗胃酸(含稀盐酸)过多的药物是 ( )
A.NaHCO3 B.NaOH C.Al(OH)3 D.墨鱼骨粉(含CaCO3)
9.下面是几种作物生长时对土壤pH值要求的最佳范围:茶5~5.5;西瓜6;大豆6~7,甜菜7~7.5;如果某地区经常降酸雨,以上作物最不适宜种植的是 ( )
A. 茶 B. 西瓜 C. 大豆 D. 甜菜
【教学体会及注意事项】
______________________________________________________________________________________________________________________________________________________
