实验活动6 酸、碱的化学性质(课件19页)
文档属性
| 名称 | 实验活动6 酸、碱的化学性质(课件19页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 11.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-09 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
第十单元 酸和碱
实验活动6 酸、碱的化学性质
人教版九年级上册
新课讲解【实验目的】1.加深对酸和碱的主要性质的认识。2.通过实验解释生活中的一些现象。【实验用品】试管、药匙、蒸发皿、玻璃棒、酒精灯、铁架台(带铁圈)、坩埚钳、胶头滴管、火柴。稀盐酸、稀硫酸、稀氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液、pH试纸、生锈的铁钉。注意:酸和碱有腐蚀性,实验时应注意安全!
新课讲解
【实验步骤】
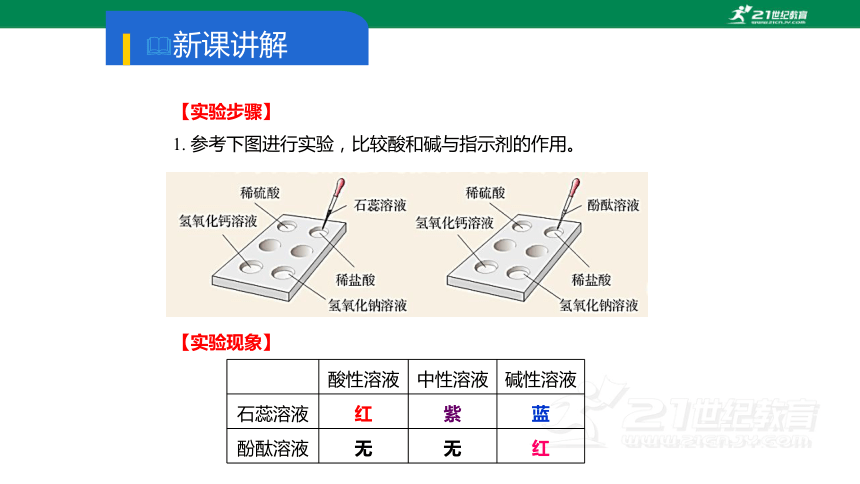
1. 参考下图进行实验,比较酸和碱与指示剂的作用。
新课讲解
【实验步骤】
1. 参考下图进行实验,比较酸和碱与指示剂的作用。
新课讲解
【实验步骤】
1. 参考下图进行实验,比较酸和碱与指示剂的作用。
酸性溶液 中性溶液 碱性溶液
石蕊溶液 红 紫 蓝
酚酞溶液 无 无 红
【实验现象】
新课讲解
2. 取两个生锈的铁钉放入两支试管中,然后加入约2mL稀盐酸,观察现象。当观察到铁钉表面的锈去掉变得光亮时,取出,洗净。继续观察另一支试管中的现象,过一段时间将铁钉取出,洗净。比较两支铁钉。
新课讲解
2. 取两个生锈的铁钉放入两支试管中,然后加入约2mL稀盐酸,观察现象。当观察到铁钉表面的锈去掉变得光亮时,取出,洗净。继续观察另一支试管中的现象,过一段时间将铁钉取出,洗净。比较两支铁钉。
【实验现象】
铁锈的主要成分为氧化铁,氧化铁能与稀盐酸反应而溶解,溶液变为黄色;当铁锈除去后,铁会继续与稀盐酸发生反应,铁钉表面有气泡冒出。
两支铁钉相比较,后取出的铁钉明显变小了。
涉及到的化学方程式为:
Fe2O3+6HCl=2FeCl3+3H2O
Fe+2HCl=FeCl2+H2↑
新课讲解
3. 在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象。然后再向试管中加入稀盐酸,观察现象。
新课讲解
3. 在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象。然后再向试管中加入稀盐酸,观察现象。
实验内容 实验现象 化学方程式
硫酸铜溶液滴入氢氧化钠溶液 生成蓝色沉淀 CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
再加入稀盐酸 蓝色沉淀逐渐溶解 Cu(OH)2+2HCl=CuCl2+2H2O
新课讲解
4. 在试管中加入约1mL氢氧化钠溶液,滴入几滴酚酞溶液。然后边用滴管慢慢滴入稀盐酸,边不断振荡试管,至溶液颜色恰好变成无色为止。取该无色溶液约1mL,置于蒸发皿中加热,使液体蒸干,观察现象。
新课讲解
4. 在试管中加入约1mL氢氧化钠溶液,滴入几滴酚酞溶液。然后边用滴管慢慢滴入稀盐酸,边不断振荡试管,至溶液颜色恰好变成无色为止。取该无色溶液约1mL,置于蒸发皿中加热,使液体蒸干,观察现象。
【实验现象】
氢氧化钠溶液中滴加酚酞后,溶液变红色;
滴加稀盐酸,溶液的红色变浅,直至消失;
蒸发所得液体,会有白色固体析出。
涉及到的化学方程式为:
NaOH+HCl=NaCl+H2O
新课讲解
【问题与交流】
向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把的一端挑一点),然后各加入1mL水,振荡;再各滴入1~2滴酚酞溶液,观察现象。继续向其中一支试管中加入约1mL水,振荡;向另一支试管中加入约1mL稀盐酸,振荡。比较两支试管中的现象。
通过实验,可以验证氢氧化钙的哪些性质?
氢氧化钙加入水后,出现白色浑浊,说明氢氧化钙微溶于水。
加入酚酞溶液,变红色,说明氢氧化钙溶液呈碱性。
一支试管中加水,另一支试管中加稀盐酸,加入稀盐酸的试管中红色消失,说明氢氧化钙能与稀盐酸发生化学反应。
归纳小结
1、主要实验中涉及的实验基本操作的训练;
2、通过实验,进一步了解的酸和碱的化学性质。
强化训练
1、利用如图所示的实验探究物质的性质。下列叙述错误的是( )
A.②处有气泡、③处无现象,则可判断锌、铜的
金属活动性
B.①②④⑤处有明显现象,则M可能为稀盐酸
C.⑤处固体明显减少,则M可能为稀硫酸
D.⑥处反应放热,则N可能是氢氧化钠溶液
C
【解析】
A、锌和稀酸反应生成氢气,产生气泡,铜不能和稀酸反应,无明显现象,说明锌比铜活泼,正确;
B、盐酸能使石蕊试液变红色,能和锌反应生成氯化锌和氢气,能和氧化铁反应生成氯化铁和水,能和碳酸钙反应生成氯化钙、水和二氧化碳,正确;
C、碳酸钙和稀硫酸反应生成的硫酸钙微溶于水,包裹在大理石表面,阻止反应的进行,M是稀硫酸时,⑤处固体不可能明显减少,错误;
D、氢氧化钠和酸反应生成盐和水,放热,正确。
强化训练
2、下列各组物质间的反应,由于现象不明显,需要借助酸碱指示剂才能判断出反应发生的是( )
A.锌与稀盐酸 B.烧碱溶液与稀硫酸
C.氧化铁与稀硫酸 D.大理石与稀盐酸
B
【解析】
A、锌与稀盐酸反应生成氯化锌和氢气,有气体生成,现象明显,故选项错误。
B、烧碱溶液与稀硫酸反应生成硫酸钠和水,反应无明显现象,需要借助指示剂才能判断出反应发生,故选项正确。
C、氧化铁与稀硫酸反应生成硫酸铁和水,会观察到固体消失,溶液变黄,现象明显,故选项错误。
D、大理石与稀盐酸反应生成氯化钙、水和二氧化碳,有大量气泡产生,现象明显,故选项错误。
强化训练
3、以下是一个完整的实验过程,下列选项中序号所对应的现象的描述正确的是( )
【实验步骤】①取少量胆矾放在研钵内研碎;②在试管中放入少量研碎后的胆矾,并加入适量水,振荡;③另取适量氢氧化钠溶液于试管中,向其中滴加2滴酚酞溶液;④将②、③实验得到的溶液混合。
A.①蓝色块状固体变成白色粉末状固体 B.②得到无色透明的溶液
C.③酚酞溶液由无色变为红色 D.④生成蓝色的氢氧化铜沉淀
C
【解析】A、胆矾研碎,会观察到蓝色块状固体变成蓝色粉末状固体,故错误;B、在试管中放入少量研碎后的胆矾,并加入适量水,振荡,得到蓝色透明的溶液,故错误;C、氢氧化钠溶液显碱性,另取适量氢氧化钠溶液于试管中,向其中滴加2滴酚酞溶液,酚酞溶液由无色变为红色,故正确;D、将②、③实验得到的溶液混合,氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,氢氧化钠溶液加入硫酸铜溶液中产生蓝色沉淀,生成蓝色的氢氧化铜沉淀是实验结论而不是实验现象,故错误。
布置作业
通过课堂学习和本次实验,你知道了酸和碱的哪些化学性质,快总结出来吧!
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
第十单元 酸和碱
实验活动6 酸、碱的化学性质
人教版九年级上册
新课讲解【实验目的】1.加深对酸和碱的主要性质的认识。2.通过实验解释生活中的一些现象。【实验用品】试管、药匙、蒸发皿、玻璃棒、酒精灯、铁架台(带铁圈)、坩埚钳、胶头滴管、火柴。稀盐酸、稀硫酸、稀氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液、pH试纸、生锈的铁钉。注意:酸和碱有腐蚀性,实验时应注意安全!
新课讲解
【实验步骤】
1. 参考下图进行实验,比较酸和碱与指示剂的作用。
新课讲解
【实验步骤】
1. 参考下图进行实验,比较酸和碱与指示剂的作用。
新课讲解
【实验步骤】
1. 参考下图进行实验,比较酸和碱与指示剂的作用。
酸性溶液 中性溶液 碱性溶液
石蕊溶液 红 紫 蓝
酚酞溶液 无 无 红
【实验现象】
新课讲解
2. 取两个生锈的铁钉放入两支试管中,然后加入约2mL稀盐酸,观察现象。当观察到铁钉表面的锈去掉变得光亮时,取出,洗净。继续观察另一支试管中的现象,过一段时间将铁钉取出,洗净。比较两支铁钉。
新课讲解
2. 取两个生锈的铁钉放入两支试管中,然后加入约2mL稀盐酸,观察现象。当观察到铁钉表面的锈去掉变得光亮时,取出,洗净。继续观察另一支试管中的现象,过一段时间将铁钉取出,洗净。比较两支铁钉。
【实验现象】
铁锈的主要成分为氧化铁,氧化铁能与稀盐酸反应而溶解,溶液变为黄色;当铁锈除去后,铁会继续与稀盐酸发生反应,铁钉表面有气泡冒出。
两支铁钉相比较,后取出的铁钉明显变小了。
涉及到的化学方程式为:
Fe2O3+6HCl=2FeCl3+3H2O
Fe+2HCl=FeCl2+H2↑
新课讲解
3. 在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象。然后再向试管中加入稀盐酸,观察现象。
新课讲解
3. 在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象。然后再向试管中加入稀盐酸,观察现象。
实验内容 实验现象 化学方程式
硫酸铜溶液滴入氢氧化钠溶液 生成蓝色沉淀 CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
再加入稀盐酸 蓝色沉淀逐渐溶解 Cu(OH)2+2HCl=CuCl2+2H2O
新课讲解
4. 在试管中加入约1mL氢氧化钠溶液,滴入几滴酚酞溶液。然后边用滴管慢慢滴入稀盐酸,边不断振荡试管,至溶液颜色恰好变成无色为止。取该无色溶液约1mL,置于蒸发皿中加热,使液体蒸干,观察现象。
新课讲解
4. 在试管中加入约1mL氢氧化钠溶液,滴入几滴酚酞溶液。然后边用滴管慢慢滴入稀盐酸,边不断振荡试管,至溶液颜色恰好变成无色为止。取该无色溶液约1mL,置于蒸发皿中加热,使液体蒸干,观察现象。
【实验现象】
氢氧化钠溶液中滴加酚酞后,溶液变红色;
滴加稀盐酸,溶液的红色变浅,直至消失;
蒸发所得液体,会有白色固体析出。
涉及到的化学方程式为:
NaOH+HCl=NaCl+H2O
新课讲解
【问题与交流】
向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把的一端挑一点),然后各加入1mL水,振荡;再各滴入1~2滴酚酞溶液,观察现象。继续向其中一支试管中加入约1mL水,振荡;向另一支试管中加入约1mL稀盐酸,振荡。比较两支试管中的现象。
通过实验,可以验证氢氧化钙的哪些性质?
氢氧化钙加入水后,出现白色浑浊,说明氢氧化钙微溶于水。
加入酚酞溶液,变红色,说明氢氧化钙溶液呈碱性。
一支试管中加水,另一支试管中加稀盐酸,加入稀盐酸的试管中红色消失,说明氢氧化钙能与稀盐酸发生化学反应。
归纳小结
1、主要实验中涉及的实验基本操作的训练;
2、通过实验,进一步了解的酸和碱的化学性质。
强化训练
1、利用如图所示的实验探究物质的性质。下列叙述错误的是( )
A.②处有气泡、③处无现象,则可判断锌、铜的
金属活动性
B.①②④⑤处有明显现象,则M可能为稀盐酸
C.⑤处固体明显减少,则M可能为稀硫酸
D.⑥处反应放热,则N可能是氢氧化钠溶液
C
【解析】
A、锌和稀酸反应生成氢气,产生气泡,铜不能和稀酸反应,无明显现象,说明锌比铜活泼,正确;
B、盐酸能使石蕊试液变红色,能和锌反应生成氯化锌和氢气,能和氧化铁反应生成氯化铁和水,能和碳酸钙反应生成氯化钙、水和二氧化碳,正确;
C、碳酸钙和稀硫酸反应生成的硫酸钙微溶于水,包裹在大理石表面,阻止反应的进行,M是稀硫酸时,⑤处固体不可能明显减少,错误;
D、氢氧化钠和酸反应生成盐和水,放热,正确。
强化训练
2、下列各组物质间的反应,由于现象不明显,需要借助酸碱指示剂才能判断出反应发生的是( )
A.锌与稀盐酸 B.烧碱溶液与稀硫酸
C.氧化铁与稀硫酸 D.大理石与稀盐酸
B
【解析】
A、锌与稀盐酸反应生成氯化锌和氢气,有气体生成,现象明显,故选项错误。
B、烧碱溶液与稀硫酸反应生成硫酸钠和水,反应无明显现象,需要借助指示剂才能判断出反应发生,故选项正确。
C、氧化铁与稀硫酸反应生成硫酸铁和水,会观察到固体消失,溶液变黄,现象明显,故选项错误。
D、大理石与稀盐酸反应生成氯化钙、水和二氧化碳,有大量气泡产生,现象明显,故选项错误。
强化训练
3、以下是一个完整的实验过程,下列选项中序号所对应的现象的描述正确的是( )
【实验步骤】①取少量胆矾放在研钵内研碎;②在试管中放入少量研碎后的胆矾,并加入适量水,振荡;③另取适量氢氧化钠溶液于试管中,向其中滴加2滴酚酞溶液;④将②、③实验得到的溶液混合。
A.①蓝色块状固体变成白色粉末状固体 B.②得到无色透明的溶液
C.③酚酞溶液由无色变为红色 D.④生成蓝色的氢氧化铜沉淀
C
【解析】A、胆矾研碎,会观察到蓝色块状固体变成蓝色粉末状固体,故错误;B、在试管中放入少量研碎后的胆矾,并加入适量水,振荡,得到蓝色透明的溶液,故错误;C、氢氧化钠溶液显碱性,另取适量氢氧化钠溶液于试管中,向其中滴加2滴酚酞溶液,酚酞溶液由无色变为红色,故正确;D、将②、③实验得到的溶液混合,氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,氢氧化钠溶液加入硫酸铜溶液中产生蓝色沉淀,生成蓝色的氢氧化铜沉淀是实验结论而不是实验现象,故错误。
布置作业
通过课堂学习和本次实验,你知道了酸和碱的哪些化学性质,快总结出来吧!
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
同课章节目录
