江苏省栟茶高级中学高二化学必修模拟试卷
图片预览



文档简介
江苏省栟茶高级中学高二化学必修模拟试卷
可能用到的相对原子质量 H:1 C:12 N:14 O:16 Fe:56 Cu:64
单项选择题:本部分共23小题,每小题3分,共69分。在每小题的4个选项中,只有1个选项是符合要求的。
1.党的十七大报告指出:节约能源和保护环境是人类社会和谐发展的重要保证。下列做法中不符合这一要求的是( )
A.推广使用沼气、太阳能、风能等新能源,减少煤、石油等化石燃料的使用
B.研究采煤、采油新技术,提高产量以满足社会快速发展的需要
C.垃圾分类回收,并对废旧电池回收处理
D.提高汽车尾气的排放标准,减少机动车尾气污染
2.人们用DNA制造出一种臂长只有7nm的纳米镊子,这种镊子能钳起分子或原子,并对它随意组合。下列分散系中,分散质微粒直径与纳米粒具有相同数量级的是( )
A.溶液 B.胶体 C.悬浊液 D.乳浊液
3.下列有关物质分类的说法中正确的是( )
A.石油、煤、苏打都是混合物 B .烧碱、纯碱、碱石灰都是碱
C.明矾、胆矾、小苏打都是盐 D.HCl、H2SO4、NH3都是酸
4.下列有关物质用途的说法中正确的是( )
A.工业上利用氨气制硝酸属于人工固氮
B.在食品包装袋内放入生石灰可以防止食品因氧化而变质
C.氢氧化铝、碳酸镁、小苏打等可用于治疗胃酸过多
D.硅可用于制造光导纤维
5.下列化学用语正确的是( )
A.HCl的电子式: B.乙醇的分子式:C2H6O
C.磷原子结构示意图: D.乙烯的结构式:H-C=C-H
6.工业上用金红石(主要成分为TiO2)制金属钛,可通过以下反应进行:
①TiO2+2C+2Cl2 TiCl4+2CO
②TiCl4+2Mg Ti+2MgCl2
对于上述两个反应的叙述中,正确的是( )
A.都是置换反应
B.①中TiO2作氧化剂
C.每生成1mo l金属 Ti,②中转移电子数为2NA
D.②中氩气作保护气,可防止金属 Ti被氧化
7.在某无色透明的且能使石蕊试剂变红的溶液中,能共存的离子组是( )
A.Na+、K+、SO42-、HCO3- B.Na+、K+、SO42-、NO3-
C.Na+、Fe2+、Cl-、NO3- D.Fe3+、K+、ClO-、Cl-
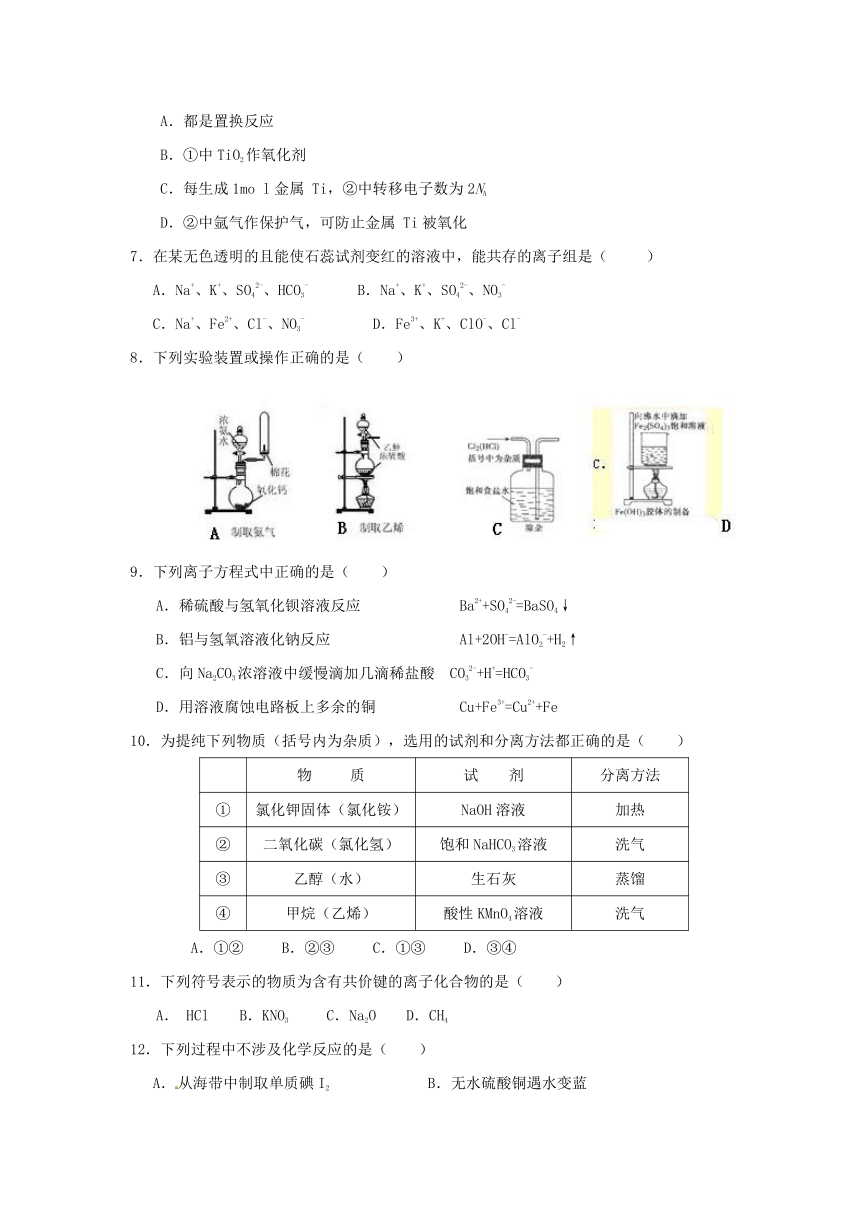
8.下列实验装置或操作正确的是( )
9.下列离子方程式中正确的是( )
A.稀硫酸与氢氧化钡溶液反应 Ba2++SO42-=BaSO4↓
B.铝与氢氧溶液化钠反应 Al+2OH-=AlO2-+H2↑
C.向Na2CO3浓溶液中缓慢滴加几滴稀盐酸 CO32-+H+=HCO3-
D.用溶液腐蚀电路板上多余的铜 Cu+Fe3+=Cu2++Fe
10.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
物 质
试 剂
分离方法
①
氯化钾固体(氯化铵)
NaOH溶液
加热
②
二氧化碳(氯化氢)
饱和NaHCO3溶液
洗气
③
乙醇(水)
生石灰
蒸馏
④
甲烷(乙烯)
酸性KMnO4溶液
洗气
A.①② B.②③ C.①③ D.③④
11.下列符号表示的物质为含有共价键的离子化合物的是( )
A. HCl B.KNO3 C.Na2O D.CH4
12.下列过程中不涉及化学反应的是( )
A.从海带中制取单质碘I2 B.无水硫酸铜遇水变蓝
C.废弃的干冰放在通风处自然升华 D.白色污染的处理:回收后高温裂解
13.下列关于甲烷和乙烯的说法中正确的是( )
A.甲烷在空气中燃烧,出现明亮的蓝紫色火焰
B.乙烯使酸性KMnO4溶液褪色是因为乙烯被酸性KMnO4溶液氧化
C.甲烷与氯气光照条件下反应生成的三氯甲烷常温下是气态
D.乙烯分子中含一个碳碳双键和两个碳氢单键
14.下列反应过程中能量变化符合如图所示的是( )
A.C+CO22CO B.Zn+H2SO4=ZnSO4+H2↑
C.CH4+2O2CO2+2H2O D.KOH+HNO3=KNO3+H2O
15.下列说法正确的是 ( )
A.H2O分子和NH3分子具有相同数目的质子总数,故属于同种元素
B.18O和16O是两种不同的核素
C.H218O和H216O属于同素异形体
D.对人体有害的氡的放射性同位素Rn,其原子中的质子数为136
16.宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2===2 Ag2S +2H2O,其中Ag是 ( )
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
17.下列关于物质的叙述中不正确的是( )
A.铝制容器不能盛装酸性溶液,可以盛装碱性溶液
B.金属钠着火时,可用细沙覆盖灭火
C.食盐是氯碱工业的基础原料
D.碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一
18.对下列有机反应类型的判断中不正确的是( )
A.CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O 取代反应
B.CH2=CH2+HOClHOCH2—CH2Cl 加成反应
C.2CH3CH2OH+O22CH3CHO+2H2O 氧化反应
D. 加成反应
19.阿伏加德罗常数约为6.02×1023mol-1,下列说法中错误的是( )
A.标准状况下,0.4gH2含氢分子数为0.2×6.02×1023
B.32gO2中含有的氧原子数为2×6.02×1023
C.1molNa2O2与足量水反应转移电子数为6.02×1023
D.标准状况下,22.4L H2O含水分子数为6.02×1023
20.有右图所示装置,下列有关说法正确的是( )
A.该装置外电路中电流由Cu棒转移到C棒
B.该装置中负极是Cu、发生还原反应
C.该装置能实验电能转化为化学能
D.该装置的总反应式为:Cu+2Fe3+=2Fe2++Cu2+
21.镁条和盐酸反应迅速产生大量的氢气,欲使反应速率减慢,可采取的措施有:①降温 ②把镁条粉碎 ③加入少许铜粉 ④加入蒸馏水使盐酸变稀 ⑤升温
A.①② B.②③⑤ C.①④ D.②④
22.X、Y、Z、W、R是5种短周期元素,其原子序数依次增加。X是元素周期表中原子半径最小的的元素, Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等,且Z在同周期中原子半径最大。下列说法正确的是 ( )
A.元素Z、W的离子具有相同的电子层排布
B.元素Y与Z可以形成化合物Z2Y2 和Z2Y,两种物质中阴阳离子个数比不同
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY< XmR
D.元素W、R的最高价氧化物的水化物都是强酸
23.一定浓度100mL的HNO3溶液中加入2.8gFe,全部溶解,得到标准状况下的NO气体1.12L,测得反应后溶液中的c(H+)=0.1mol/L。若反应前后溶液体积变化忽略不计,则下列有关判断错误的是( )
A.反应后溶液中无硝酸亚铁
B.反应前HNO3溶液的浓度为2.0mol·L-1
C.反应后溶液中c(NO3-)=1.6mol·L-1
D.反应后的溶液最多还能溶解1.61gFe
非选择题(本部分3题,共31分)
24.(15分)生活中处处有化学。
(1)合理选择饮食、正确使用药物是保证身心健康的重要方面,请填写下列空格。
水在人体内起着十分重要的作用,可以作为溶剂,调节人体体温,还是一种必不可少的反应物。请写出淀粉在人体内完全水解的反应 。人每天都要补充一定量的水,体内体液也有自己的性质,例如人的血液呈 (选填:弱酸性,中性,弱碱性)。我国居民形成了摄入蔬菜和水果偏少的习惯,一般尿液呈 (选填:弱酸性,中性,弱碱性)。
通过食物的调整,人体可以保持健康。可是如果生病了,我们还是要去医院就诊,医生所开的药一般有R标记,表示 。青霉素的种类比较多,目前临床上广泛使用的羟氨苄青霉素其俗名是 。
阿司匹林的结构简式为 具有的官能团有酯基和 (写名
称)。阿司匹林和水可缓慢水解,该反应的化学方程式为 。
(2)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础。请填写下列空格。
A.生活中的 属于传统无机硅酸盐材料。(常见的三大类)
B.合金材料钢铁里的Fe和C在潮湿的空气中因构成许多原电池而易发生电化学腐蚀,正极反应方程式为 。
C.居室装修材料如化纤地毯、三合板等均会释放出污染空气的 气体。
D. 在日常生活中可制成食品保鲜膜。
F.现代以石油化工为基础的三大合成材料是 。
地球环境日益恶化,为了保护环境人类正在尽力治理。下列说法正确的是
A.CO、甲苯、尼古丁等不是室内污染物
B.污水处理方法化学包括混凝法、中和法、沉淀法
C.“白色污染”的会危及海洋生物的生存
D.垃圾资源化的方法是分类回收法
E.为防止流感传染,可将教室门窗关闭后,用甲醛熏蒸,进行消毒
F.铅笔芯的原料的重金属铅,儿童在使用时不可用嘴吮咬铅笔,以免引起铅中毒
G.CO有毒,生有煤炉的居室,可放置数盆水这样可有效地吸收CO,以防煤气中毒
25.(6分)下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D为金属单质。(反应过程中生成的水及其他产物已略去)
请回答以下问题:
(1)B的化学式为__________。
(2)K的电子式为_______________。
(2)写出J与D反应转化为G的离子方程式_________________________________。
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式?_______。
26.(10分)工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁。
(1)工业上可用氨催化吸收法处理NOx ,反应原理如下:
4xNH3 +6 NOx (2x + 3)N2 + 6xH2O
某化学兴趣小组模拟该处理过程的实验装置如下
①装置A中发生反应的化学方程式为 。
②装置D中碱石灰的作用是 。
(2)工业上也常用Na2CO3溶液吸收法处理NOx 。已知: NO不能与Na2CO3溶液反应,。
NO + NO2 + Na2CO3 = 2NaNO2 + CO2 (I)
2NO2 + Na2CO3 = NaNO2 + NaNO3 + CO2 (II)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是 (填字母)。
A.1.8 B.1.3 C 1.6
②将1mol NOx 通入Na2CO3溶液中,被完全吸收时,溶液中生成的NO3—、NO2—两种离子的物质的量随x变化关系如右图所示: 图中线段a表示 离子随x值变化的关系;若用溶质质量分数为21.2%的 Na2CO3溶液吸收,则需要Na2CO3溶液至 g。
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为 。
(3)氨催化吸收法和Na2CO3溶液吸收法处理NOx尾气的意义是 。
江苏省栟茶高级中学高二化学必修模拟试卷答案
1
2
3
4
5
6
7
8
9
10
B
B
C
C
B
D
B
D
C
B
11
12
13
14
15
16
17
18
19
20
B
C
B
A
B
B
A
D
D
D
21
22
23
C
A
B
24.(15分)
(1)nH2O+(C6H10O5)n→ nC6H12O6
弱碱性、弱酸性、处方药、阿莫西林(或阿莫仙)
羧基(以上每空1分) (方程式略)(此空2分)
(2)玻璃、陶瓷、水泥;O2+2H2O+4e—=4OH-;
甲醛; 聚乙烯; 塑料、合成纤维、合成橡胶(以上每空1分)
(3)BC D(选对2个得1分,全对得2分,只要错选得0分)
25.(6分)(1)Fe2O3 (2)
(2)2Fe3++Fe=3Fe2+
(3)2Al+2NaOH+2H2O=2NaAlO2+3H2↑
26.(10分)
(1)①2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O
②除去气体中含有的水蒸气
(2)①B ②NO2- 250(2分)
③1.875或
(3)将有毒气体转化为无毒气体
可能用到的相对原子质量 H:1 C:12 N:14 O:16 Fe:56 Cu:64
单项选择题:本部分共23小题,每小题3分,共69分。在每小题的4个选项中,只有1个选项是符合要求的。
1.党的十七大报告指出:节约能源和保护环境是人类社会和谐发展的重要保证。下列做法中不符合这一要求的是( )
A.推广使用沼气、太阳能、风能等新能源,减少煤、石油等化石燃料的使用
B.研究采煤、采油新技术,提高产量以满足社会快速发展的需要
C.垃圾分类回收,并对废旧电池回收处理
D.提高汽车尾气的排放标准,减少机动车尾气污染
2.人们用DNA制造出一种臂长只有7nm的纳米镊子,这种镊子能钳起分子或原子,并对它随意组合。下列分散系中,分散质微粒直径与纳米粒具有相同数量级的是( )
A.溶液 B.胶体 C.悬浊液 D.乳浊液
3.下列有关物质分类的说法中正确的是( )
A.石油、煤、苏打都是混合物 B .烧碱、纯碱、碱石灰都是碱
C.明矾、胆矾、小苏打都是盐 D.HCl、H2SO4、NH3都是酸
4.下列有关物质用途的说法中正确的是( )
A.工业上利用氨气制硝酸属于人工固氮
B.在食品包装袋内放入生石灰可以防止食品因氧化而变质
C.氢氧化铝、碳酸镁、小苏打等可用于治疗胃酸过多
D.硅可用于制造光导纤维
5.下列化学用语正确的是( )
A.HCl的电子式: B.乙醇的分子式:C2H6O
C.磷原子结构示意图: D.乙烯的结构式:H-C=C-H
6.工业上用金红石(主要成分为TiO2)制金属钛,可通过以下反应进行:
①TiO2+2C+2Cl2 TiCl4+2CO
②TiCl4+2Mg Ti+2MgCl2
对于上述两个反应的叙述中,正确的是( )
A.都是置换反应
B.①中TiO2作氧化剂
C.每生成1mo l金属 Ti,②中转移电子数为2NA
D.②中氩气作保护气,可防止金属 Ti被氧化
7.在某无色透明的且能使石蕊试剂变红的溶液中,能共存的离子组是( )
A.Na+、K+、SO42-、HCO3- B.Na+、K+、SO42-、NO3-
C.Na+、Fe2+、Cl-、NO3- D.Fe3+、K+、ClO-、Cl-
8.下列实验装置或操作正确的是( )
9.下列离子方程式中正确的是( )
A.稀硫酸与氢氧化钡溶液反应 Ba2++SO42-=BaSO4↓
B.铝与氢氧溶液化钠反应 Al+2OH-=AlO2-+H2↑
C.向Na2CO3浓溶液中缓慢滴加几滴稀盐酸 CO32-+H+=HCO3-
D.用溶液腐蚀电路板上多余的铜 Cu+Fe3+=Cu2++Fe
10.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
物 质
试 剂
分离方法
①
氯化钾固体(氯化铵)
NaOH溶液
加热
②
二氧化碳(氯化氢)
饱和NaHCO3溶液
洗气
③
乙醇(水)
生石灰
蒸馏
④
甲烷(乙烯)
酸性KMnO4溶液
洗气
A.①② B.②③ C.①③ D.③④
11.下列符号表示的物质为含有共价键的离子化合物的是( )
A. HCl B.KNO3 C.Na2O D.CH4
12.下列过程中不涉及化学反应的是( )
A.从海带中制取单质碘I2 B.无水硫酸铜遇水变蓝
C.废弃的干冰放在通风处自然升华 D.白色污染的处理:回收后高温裂解
13.下列关于甲烷和乙烯的说法中正确的是( )
A.甲烷在空气中燃烧,出现明亮的蓝紫色火焰
B.乙烯使酸性KMnO4溶液褪色是因为乙烯被酸性KMnO4溶液氧化
C.甲烷与氯气光照条件下反应生成的三氯甲烷常温下是气态
D.乙烯分子中含一个碳碳双键和两个碳氢单键
14.下列反应过程中能量变化符合如图所示的是( )
A.C+CO22CO B.Zn+H2SO4=ZnSO4+H2↑
C.CH4+2O2CO2+2H2O D.KOH+HNO3=KNO3+H2O
15.下列说法正确的是 ( )
A.H2O分子和NH3分子具有相同数目的质子总数,故属于同种元素
B.18O和16O是两种不同的核素
C.H218O和H216O属于同素异形体
D.对人体有害的氡的放射性同位素Rn,其原子中的质子数为136
16.宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2===2 Ag2S +2H2O,其中Ag是 ( )
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
17.下列关于物质的叙述中不正确的是( )
A.铝制容器不能盛装酸性溶液,可以盛装碱性溶液
B.金属钠着火时,可用细沙覆盖灭火
C.食盐是氯碱工业的基础原料
D.碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一
18.对下列有机反应类型的判断中不正确的是( )
A.CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O 取代反应
B.CH2=CH2+HOClHOCH2—CH2Cl 加成反应
C.2CH3CH2OH+O22CH3CHO+2H2O 氧化反应
D. 加成反应
19.阿伏加德罗常数约为6.02×1023mol-1,下列说法中错误的是( )
A.标准状况下,0.4gH2含氢分子数为0.2×6.02×1023
B.32gO2中含有的氧原子数为2×6.02×1023
C.1molNa2O2与足量水反应转移电子数为6.02×1023
D.标准状况下,22.4L H2O含水分子数为6.02×1023
20.有右图所示装置,下列有关说法正确的是( )
A.该装置外电路中电流由Cu棒转移到C棒
B.该装置中负极是Cu、发生还原反应
C.该装置能实验电能转化为化学能
D.该装置的总反应式为:Cu+2Fe3+=2Fe2++Cu2+
21.镁条和盐酸反应迅速产生大量的氢气,欲使反应速率减慢,可采取的措施有:①降温 ②把镁条粉碎 ③加入少许铜粉 ④加入蒸馏水使盐酸变稀 ⑤升温
A.①② B.②③⑤ C.①④ D.②④
22.X、Y、Z、W、R是5种短周期元素,其原子序数依次增加。X是元素周期表中原子半径最小的的元素, Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等,且Z在同周期中原子半径最大。下列说法正确的是 ( )
A.元素Z、W的离子具有相同的电子层排布
B.元素Y与Z可以形成化合物Z2Y2 和Z2Y,两种物质中阴阳离子个数比不同
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY< XmR
D.元素W、R的最高价氧化物的水化物都是强酸
23.一定浓度100mL的HNO3溶液中加入2.8gFe,全部溶解,得到标准状况下的NO气体1.12L,测得反应后溶液中的c(H+)=0.1mol/L。若反应前后溶液体积变化忽略不计,则下列有关判断错误的是( )
A.反应后溶液中无硝酸亚铁
B.反应前HNO3溶液的浓度为2.0mol·L-1
C.反应后溶液中c(NO3-)=1.6mol·L-1
D.反应后的溶液最多还能溶解1.61gFe
非选择题(本部分3题,共31分)
24.(15分)生活中处处有化学。
(1)合理选择饮食、正确使用药物是保证身心健康的重要方面,请填写下列空格。
水在人体内起着十分重要的作用,可以作为溶剂,调节人体体温,还是一种必不可少的反应物。请写出淀粉在人体内完全水解的反应 。人每天都要补充一定量的水,体内体液也有自己的性质,例如人的血液呈 (选填:弱酸性,中性,弱碱性)。我国居民形成了摄入蔬菜和水果偏少的习惯,一般尿液呈 (选填:弱酸性,中性,弱碱性)。
通过食物的调整,人体可以保持健康。可是如果生病了,我们还是要去医院就诊,医生所开的药一般有R标记,表示 。青霉素的种类比较多,目前临床上广泛使用的羟氨苄青霉素其俗名是 。
阿司匹林的结构简式为 具有的官能团有酯基和 (写名
称)。阿司匹林和水可缓慢水解,该反应的化学方程式为 。
(2)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础。请填写下列空格。
A.生活中的 属于传统无机硅酸盐材料。(常见的三大类)
B.合金材料钢铁里的Fe和C在潮湿的空气中因构成许多原电池而易发生电化学腐蚀,正极反应方程式为 。
C.居室装修材料如化纤地毯、三合板等均会释放出污染空气的 气体。
D. 在日常生活中可制成食品保鲜膜。
F.现代以石油化工为基础的三大合成材料是 。
地球环境日益恶化,为了保护环境人类正在尽力治理。下列说法正确的是
A.CO、甲苯、尼古丁等不是室内污染物
B.污水处理方法化学包括混凝法、中和法、沉淀法
C.“白色污染”的会危及海洋生物的生存
D.垃圾资源化的方法是分类回收法
E.为防止流感传染,可将教室门窗关闭后,用甲醛熏蒸,进行消毒
F.铅笔芯的原料的重金属铅,儿童在使用时不可用嘴吮咬铅笔,以免引起铅中毒
G.CO有毒,生有煤炉的居室,可放置数盆水这样可有效地吸收CO,以防煤气中毒
25.(6分)下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D为金属单质。(反应过程中生成的水及其他产物已略去)
请回答以下问题:
(1)B的化学式为__________。
(2)K的电子式为_______________。
(2)写出J与D反应转化为G的离子方程式_________________________________。
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式?_______。
26.(10分)工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁。
(1)工业上可用氨催化吸收法处理NOx ,反应原理如下:
4xNH3 +6 NOx (2x + 3)N2 + 6xH2O
某化学兴趣小组模拟该处理过程的实验装置如下
①装置A中发生反应的化学方程式为 。
②装置D中碱石灰的作用是 。
(2)工业上也常用Na2CO3溶液吸收法处理NOx 。已知: NO不能与Na2CO3溶液反应,。
NO + NO2 + Na2CO3 = 2NaNO2 + CO2 (I)
2NO2 + Na2CO3 = NaNO2 + NaNO3 + CO2 (II)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是 (填字母)。
A.1.8 B.1.3 C 1.6
②将1mol NOx 通入Na2CO3溶液中,被完全吸收时,溶液中生成的NO3—、NO2—两种离子的物质的量随x变化关系如右图所示: 图中线段a表示 离子随x值变化的关系;若用溶质质量分数为21.2%的 Na2CO3溶液吸收,则需要Na2CO3溶液至 g。
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为 。
(3)氨催化吸收法和Na2CO3溶液吸收法处理NOx尾气的意义是 。
江苏省栟茶高级中学高二化学必修模拟试卷答案
1
2
3
4
5
6
7
8
9
10
B
B
C
C
B
D
B
D
C
B
11
12
13
14
15
16
17
18
19
20
B
C
B
A
B
B
A
D
D
D
21
22
23
C
A
B
24.(15分)
(1)nH2O+(C6H10O5)n→ nC6H12O6
弱碱性、弱酸性、处方药、阿莫西林(或阿莫仙)
羧基(以上每空1分) (方程式略)(此空2分)
(2)玻璃、陶瓷、水泥;O2+2H2O+4e—=4OH-;
甲醛; 聚乙烯; 塑料、合成纤维、合成橡胶(以上每空1分)
(3)BC D(选对2个得1分,全对得2分,只要错选得0分)
25.(6分)(1)Fe2O3 (2)
(2)2Fe3++Fe=3Fe2+
(3)2Al+2NaOH+2H2O=2NaAlO2+3H2↑
26.(10分)
(1)①2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O
②除去气体中含有的水蒸气
(2)①B ②NO2- 250(2分)
③1.875或
(3)将有毒气体转化为无毒气体
同课章节目录
