人教版化学九下第十单元课题2 酸和碱的中和反应(第一课时)课件(共24张PPT)
文档属性
| 名称 | 人教版化学九下第十单元课题2 酸和碱的中和反应(第一课时)课件(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-08 00:00:00 | ||
图片预览




文档简介
(共24张PPT)
人教版 化学 九年级 下册
第十单元 酸和碱
课题2 酸和碱的中和反应(第一课时)
为什么被蚊虫叮咬过之后会觉得痛痒?有什么办法消除肿痛?
蚊子咬人后,会放出一种叫做蚁酸的物质,这种物质有腐蚀性,会刺激皮肤,引起皮肤过敏、痛痒。如果被蚊虫叮咬,可以涂抹肥皂水等碱性物质。
1. 认识酸和碱的中和反应。
2.能从微观粒子运动的角度了解中和反应的原理,并会正确书写中和反应的化学方程式。
3. 了解中和反应在生产生活中的应用,由此感受化学知识对改善生活和促进社会发展的作用。
学习目标
中和反应
知识点 1
【拓展·实验】仔细观察判断下列实验,判断酸和碱之间是否发生了反应?
盐酸+氢氧化铁(氢氧化铜)
盐酸+氢氧化钠
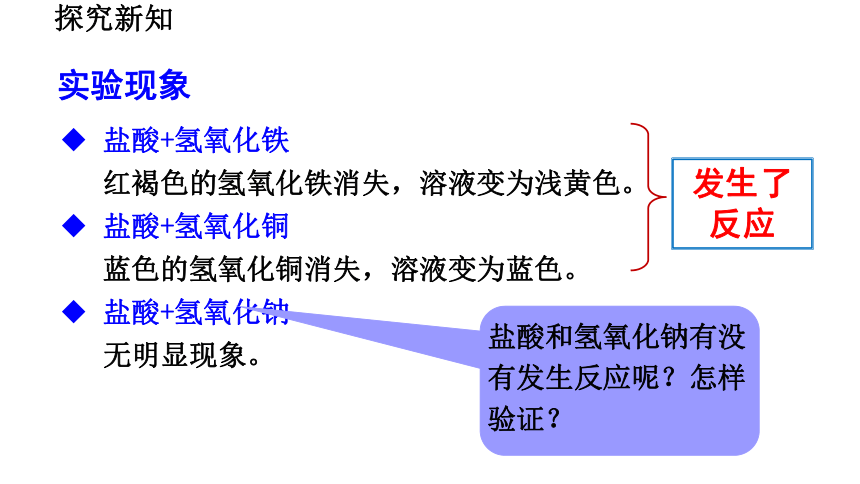
实验现象
盐酸+氢氧化铁
红褐色的氢氧化铁消失,溶液变为浅黄色。
盐酸+氢氧化铜
蓝色的氢氧化铜消失,溶液变为蓝色。
盐酸+氢氧化钠
无明显现象。
发生了反应
盐酸和氢氧化钠有没有发生反应呢?怎样验证?
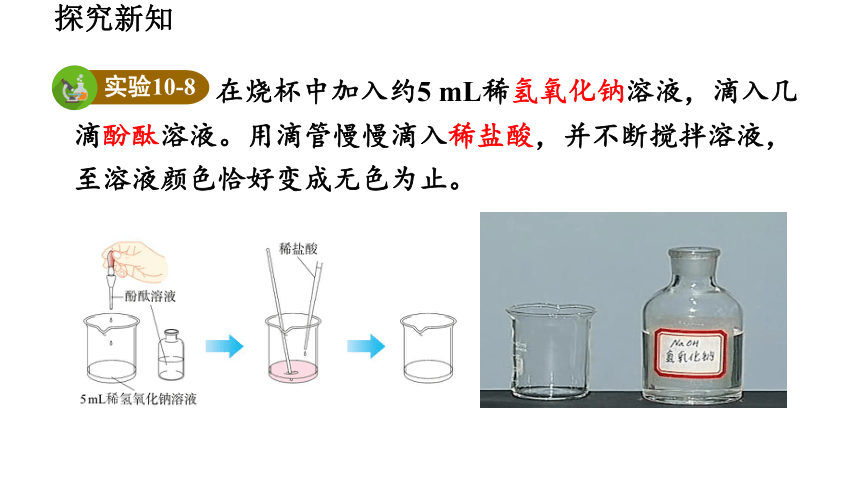
在烧杯中加入约5 mL稀氢氧化钠溶液,滴入几滴酚酞溶液。用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
实验10-8
NaOH溶液
滴入( )溶液
溶液为( )色
再滴入( )溶液
溶液为( )色
无色酚酞
红
盐酸
无
酸和碱能发生反应
实验现象
实验结论
溶液由红色变为无色,说明NaOH消失
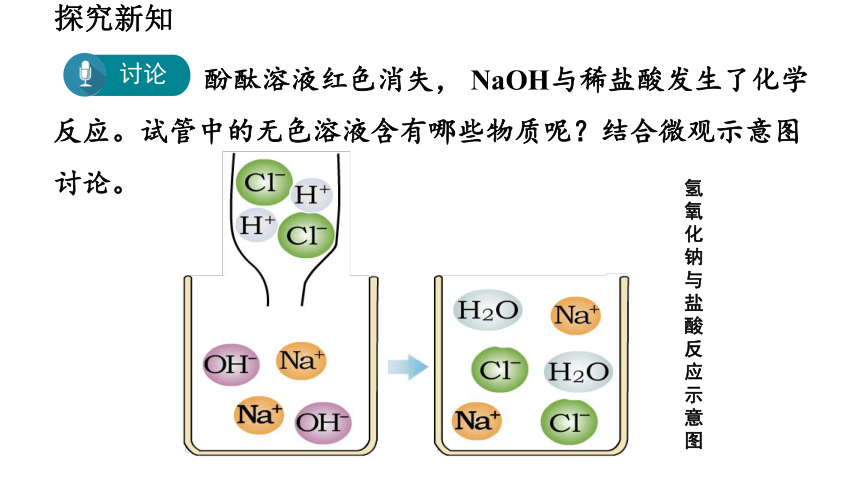
讨论
酚酞溶液红色消失, NaOH与稀盐酸发生了化学反应。试管中的无色溶液含有哪些物质呢?结合微观示意图讨论。
氢氧化钠与盐酸反应示意图
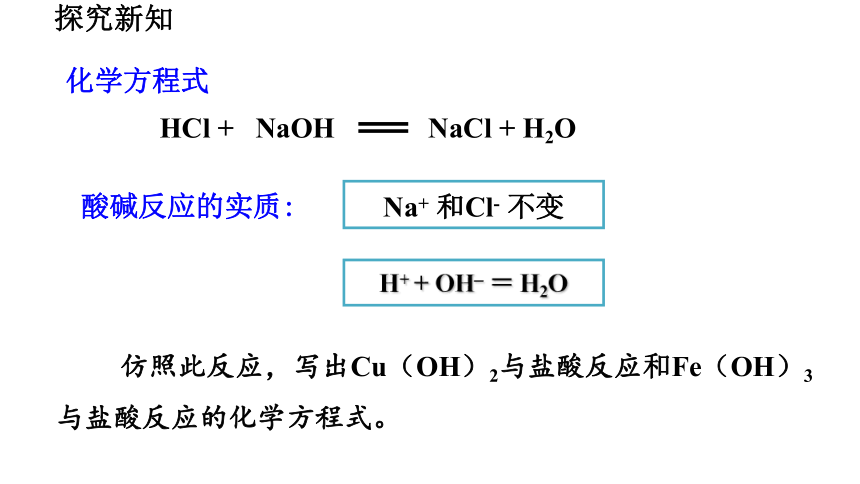
HCl + NaOH NaCl + H2O
酸碱反应的实质:
H+ + OH– = H2O
Na+ 和Cl- 不变
化学方程式
仿照此反应,写出Cu(OH)2与盐酸反应和Fe(OH)3与盐酸反应的化学方程式。
2HCl + Cu(OH)2 CuCl2 + 2H2O
3HCl + Fe(OH)3 FeCl3 + 3H2O
HCl + NaOH NaCl + H2O
碱
酸
盐
水
+
+
盐:由金属离子(或铵根离子)和酸根离子组成的化合物。
【思考】有盐和水生成的反应都是中和反应吗?
有盐和水生成的反应,不一定是中和反应。
如酸+金属氧化物→盐+水的反应不是中和反应。
上面的反应都是中和反应,你能为中和反应下个定义吗?
酸跟碱作用生成盐和水的反应,叫做中和反应。
中和反应的实质:
H+ + OH – = H2O
H2SO4 + 2NaOH === Na2SO4 + 2H2O
2HCl + Ca(OH)2 == CaCl2 +2H2O
【写一写】结合刚才所学到的知识,你能写出 ①H2SO4 (硫酸)和NaOH(氢氧化钠)反应; ②盐酸和熟石灰反应的化学方程式吗?
改良土壤的酸碱性
中性土壤
酸性土壤
熟石灰
Ca(OH)2
知识点 2
中和反应在实际中的应用
在酸性土壤中加入熟石灰
为什么常用熟石灰改良酸性土壤,而不用氢氧化钠溶液?
中性土壤
盐碱地
碱性土壤
酸性物质
中性土壤
碱性土壤
处理工厂的废水
(1)如何处理硫酸厂生产中形成的含硫酸的污水?
(2)请写出有关反应的化学方程式:
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
【想一想】
用于医药
(1)中和胃酸过多
用含有氢氧化铝的胃药中和胃酸中过多的盐酸。
化学方程式:
Al(OH)3 + 3HCl=AlCl3 + 3H2O
中和蚁酸
【思考】可不可以用NaOH来中和胃酸、蚁酸?为什么?
可涂抹一些含有碱性物质(如氨水NH3·H2O)的药水。
不可以。因为NaOH具有强的腐蚀性。
(2) 中和蚁酸
基础巩固题
1.在滴加了酚酞的氢氧化钠溶液中,逐滴加入稀盐酸至过量,溶液颜色的变化是( )
A.红色——蓝色 B.蓝色——红色
C.红色——无色 D.无色——红色
C
基础巩固题
2.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图所示。由此分析下列说法不正确的是( )
A.反应前后溶液对外不显电性
B.反应前后溶剂质量不变
C.反应后溶液呈中性
D.图中A代表水分子
B
基础巩固题
3.如图为“胃酸完全抑制剂”的标签。
(1) “胃酸完全抑制剂”主要成分中属于碱的物质是 (写化学式)。
(2)服用“胃酸完全抑制剂”后在胃内发生反应的化学反应方程式是
、
。
Mg(OH)2
Mg(OH)2+2HCl=MgCl2+2H2O
CaCO3+2HCl=CaCl2+H2O+CO2↑
1.下列说法正确的是 ( )
A. 紫色的石蕊试液可使盐酸变红
B. 中和反应一定生成盐和水
C. 生成盐和水的反应一定是中和反应
D. 氧化钙与稀盐酸能发生中和反应
B
能力提升题
2.某兴趣小组对氢氧化钡溶液和稀盐酸混合后是否发生了化学反应展开了系列实验。
【实验操作】用试管取6毫升氢氧化钡溶液,
往试管中加入6毫升稀盐酸,等分成两份。
【实验证明】(1)往其中一份混合液中滴入几滴酚酞试液,发现溶液呈无色。说明溶液中不存在的离子是 ,证明两者发生了反应。
氢氧根离子
能力提升题
【继续探究】(2)能否再设计一个实验证明盐酸中H+参加了反应?于是往混合液中滴入石蕊试液,发现变红色,溶液呈酸性,这不能证明盐酸中H+参加了反应。讨论后,形成了新的对照实验方案,将步骤补充完整:
①往盛有另一份混合液的试管中,加入足量的镁片;
② ,加入等量的镁片。
(3)证明原混合液的盐酸中H+参加了反应的现象是
。
【微观解释】(4)从微观上分析:氢氧化钡溶液和稀盐酸反应的实质是 。
取3mL相同质量分数的稀盐酸于试管中
①中产生气体比②中少
氢氧根离子和氢离子结合生成水分子
概念
中和反应
应用
酸和碱作用生成盐和水的反应。
实质
(1)改良土壤酸碱性
(2)处理工厂废水
(3)用于医药
H+ + OH – = H2O
课堂小结
人教版 化学 九年级 下册
第十单元 酸和碱
课题2 酸和碱的中和反应(第一课时)
为什么被蚊虫叮咬过之后会觉得痛痒?有什么办法消除肿痛?
蚊子咬人后,会放出一种叫做蚁酸的物质,这种物质有腐蚀性,会刺激皮肤,引起皮肤过敏、痛痒。如果被蚊虫叮咬,可以涂抹肥皂水等碱性物质。
1. 认识酸和碱的中和反应。
2.能从微观粒子运动的角度了解中和反应的原理,并会正确书写中和反应的化学方程式。
3. 了解中和反应在生产生活中的应用,由此感受化学知识对改善生活和促进社会发展的作用。
学习目标
中和反应
知识点 1
【拓展·实验】仔细观察判断下列实验,判断酸和碱之间是否发生了反应?
盐酸+氢氧化铁(氢氧化铜)
盐酸+氢氧化钠
实验现象
盐酸+氢氧化铁
红褐色的氢氧化铁消失,溶液变为浅黄色。
盐酸+氢氧化铜
蓝色的氢氧化铜消失,溶液变为蓝色。
盐酸+氢氧化钠
无明显现象。
发生了反应
盐酸和氢氧化钠有没有发生反应呢?怎样验证?
在烧杯中加入约5 mL稀氢氧化钠溶液,滴入几滴酚酞溶液。用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
实验10-8
NaOH溶液
滴入( )溶液
溶液为( )色
再滴入( )溶液
溶液为( )色
无色酚酞
红
盐酸
无
酸和碱能发生反应
实验现象
实验结论
溶液由红色变为无色,说明NaOH消失
讨论
酚酞溶液红色消失, NaOH与稀盐酸发生了化学反应。试管中的无色溶液含有哪些物质呢?结合微观示意图讨论。
氢氧化钠与盐酸反应示意图
HCl + NaOH NaCl + H2O
酸碱反应的实质:
H+ + OH– = H2O
Na+ 和Cl- 不变
化学方程式
仿照此反应,写出Cu(OH)2与盐酸反应和Fe(OH)3与盐酸反应的化学方程式。
2HCl + Cu(OH)2 CuCl2 + 2H2O
3HCl + Fe(OH)3 FeCl3 + 3H2O
HCl + NaOH NaCl + H2O
碱
酸
盐
水
+
+
盐:由金属离子(或铵根离子)和酸根离子组成的化合物。
【思考】有盐和水生成的反应都是中和反应吗?
有盐和水生成的反应,不一定是中和反应。
如酸+金属氧化物→盐+水的反应不是中和反应。
上面的反应都是中和反应,你能为中和反应下个定义吗?
酸跟碱作用生成盐和水的反应,叫做中和反应。
中和反应的实质:
H+ + OH – = H2O
H2SO4 + 2NaOH === Na2SO4 + 2H2O
2HCl + Ca(OH)2 == CaCl2 +2H2O
【写一写】结合刚才所学到的知识,你能写出 ①H2SO4 (硫酸)和NaOH(氢氧化钠)反应; ②盐酸和熟石灰反应的化学方程式吗?
改良土壤的酸碱性
中性土壤
酸性土壤
熟石灰
Ca(OH)2
知识点 2
中和反应在实际中的应用
在酸性土壤中加入熟石灰
为什么常用熟石灰改良酸性土壤,而不用氢氧化钠溶液?
中性土壤
盐碱地
碱性土壤
酸性物质
中性土壤
碱性土壤
处理工厂的废水
(1)如何处理硫酸厂生产中形成的含硫酸的污水?
(2)请写出有关反应的化学方程式:
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
【想一想】
用于医药
(1)中和胃酸过多
用含有氢氧化铝的胃药中和胃酸中过多的盐酸。
化学方程式:
Al(OH)3 + 3HCl=AlCl3 + 3H2O
中和蚁酸
【思考】可不可以用NaOH来中和胃酸、蚁酸?为什么?
可涂抹一些含有碱性物质(如氨水NH3·H2O)的药水。
不可以。因为NaOH具有强的腐蚀性。
(2) 中和蚁酸
基础巩固题
1.在滴加了酚酞的氢氧化钠溶液中,逐滴加入稀盐酸至过量,溶液颜色的变化是( )
A.红色——蓝色 B.蓝色——红色
C.红色——无色 D.无色——红色
C
基础巩固题
2.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图所示。由此分析下列说法不正确的是( )
A.反应前后溶液对外不显电性
B.反应前后溶剂质量不变
C.反应后溶液呈中性
D.图中A代表水分子
B
基础巩固题
3.如图为“胃酸完全抑制剂”的标签。
(1) “胃酸完全抑制剂”主要成分中属于碱的物质是 (写化学式)。
(2)服用“胃酸完全抑制剂”后在胃内发生反应的化学反应方程式是
、
。
Mg(OH)2
Mg(OH)2+2HCl=MgCl2+2H2O
CaCO3+2HCl=CaCl2+H2O+CO2↑
1.下列说法正确的是 ( )
A. 紫色的石蕊试液可使盐酸变红
B. 中和反应一定生成盐和水
C. 生成盐和水的反应一定是中和反应
D. 氧化钙与稀盐酸能发生中和反应
B
能力提升题
2.某兴趣小组对氢氧化钡溶液和稀盐酸混合后是否发生了化学反应展开了系列实验。
【实验操作】用试管取6毫升氢氧化钡溶液,
往试管中加入6毫升稀盐酸,等分成两份。
【实验证明】(1)往其中一份混合液中滴入几滴酚酞试液,发现溶液呈无色。说明溶液中不存在的离子是 ,证明两者发生了反应。
氢氧根离子
能力提升题
【继续探究】(2)能否再设计一个实验证明盐酸中H+参加了反应?于是往混合液中滴入石蕊试液,发现变红色,溶液呈酸性,这不能证明盐酸中H+参加了反应。讨论后,形成了新的对照实验方案,将步骤补充完整:
①往盛有另一份混合液的试管中,加入足量的镁片;
② ,加入等量的镁片。
(3)证明原混合液的盐酸中H+参加了反应的现象是
。
【微观解释】(4)从微观上分析:氢氧化钡溶液和稀盐酸反应的实质是 。
取3mL相同质量分数的稀盐酸于试管中
①中产生气体比②中少
氢氧根离子和氢离子结合生成水分子
概念
中和反应
应用
酸和碱作用生成盐和水的反应。
实质
(1)改良土壤酸碱性
(2)处理工厂废水
(3)用于医药
H+ + OH – = H2O
课堂小结
同课章节目录
