专题8 第二单元 第1课时 乙 醇 学案(含答案)
文档属性
| 名称 | 专题8 第二单元 第1课时 乙 醇 学案(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 496.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-08 00:00:00 | ||
图片预览



文档简介
第二单元 食品中的有机化合物
第1课时 乙 醇
[核心素养发展目标] 1.知道乙醇的组成、结构、物理性质及用途,培养宏观辨识与微观探析的能力。2.了解烃的衍生物的概念及官能团与性质的关系,知道有机物之间在一定条件下是可以转化的,培养变化观念与平衡思想。3.会运用乙醇的结构分析其性质,能设计实验探究乙醇的结构及性质,培养科学探究精神。
一、乙醇的物理性质及分子结构
1.乙醇
乙醇是由____________三种元素组成的有机化合物,乙醇可以与水任意比例互溶,酒类饮料中含有浓度不等的乙醇,医疗上常用体积分数为________的乙醇溶液进行消毒。
特别提醒 常用无水CuSO4检验乙醇中是否有水,常用先加生石灰再蒸馏的方法提纯乙醇。
2.乙醇的组成与结构
分子式 C2H6O
结构式
结构简式 或____________
球棍模型
空间填充模型
特别提醒 乙醇分子中含有羟基(—OH),可以看成乙烷分子中的1个氢原子被羟基取代后的产物。有机化合物分子失去一个原子或原子团剩余的部分被称为基团,如乙醇可看作乙基和羟基组成。
(1)乙醇是一种优良的有机溶剂,能溶解很多有机物和无机物( )
(2)乙烷(CH3CH3)可以看成CH4分子中的一个H原子被甲基(—CH3)所取代而生成的产物,故乙烷为烃的衍生物( )
(3)乙醇可以看作乙烷分子中氢原子被氢氧根(OH-)取代后的产物,故乙醇水溶液应呈碱性
( )
(4)为提高消毒效果,医疗上可选择体积分数为95%的乙醇溶液进行消毒( )
1.如何只用一种试剂鉴别乙醇、苯和四氯化碳?
2.如何检验乙醇中是否有水?怎样除去乙醇中的水?
1.下列有关乙醇的物理性质的应用中不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分
C.由于乙醇能够以任意比溶于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇易挥发,所以才有“酒香不怕巷子深”的说法
2.比较乙烷和乙醇的分子结构,下列说法错误的是( )
A.两个碳原子均以单键相连
B.分子里都含6个相同的氢原子
C.乙基与一个氢原子相连就是乙烷分子
D.乙基与一个羟基相连就是乙醇分子
二、乙醇的化学性质及用途
1.乙醇的化学性质
(1)乙醇与金属钠的反应——置换反应
①基础实验
实验操作
实验现象 a.钠开始沉于试管底部,最终慢慢消失,产生__________气体; b.试管内壁有______产生; c.向试管中加入澄清石灰水,石灰水______________________
实验结论 乙醇与钠反应生成______,化学方程式为________________ ____________________________________________________
②反应实质
金属钠可以保存在煤油(多种烃的混合物)中,实验表明烷烃分子中______________氢不能被金属钠置换,而乙醇分子中______________氢原子能被金属钠置换生成______气,但反应比钠与水要缓慢得多。
由结构决定性质可得,乙基对羟基的影响使得羟基氢的活性降低。
(2)氧化反应
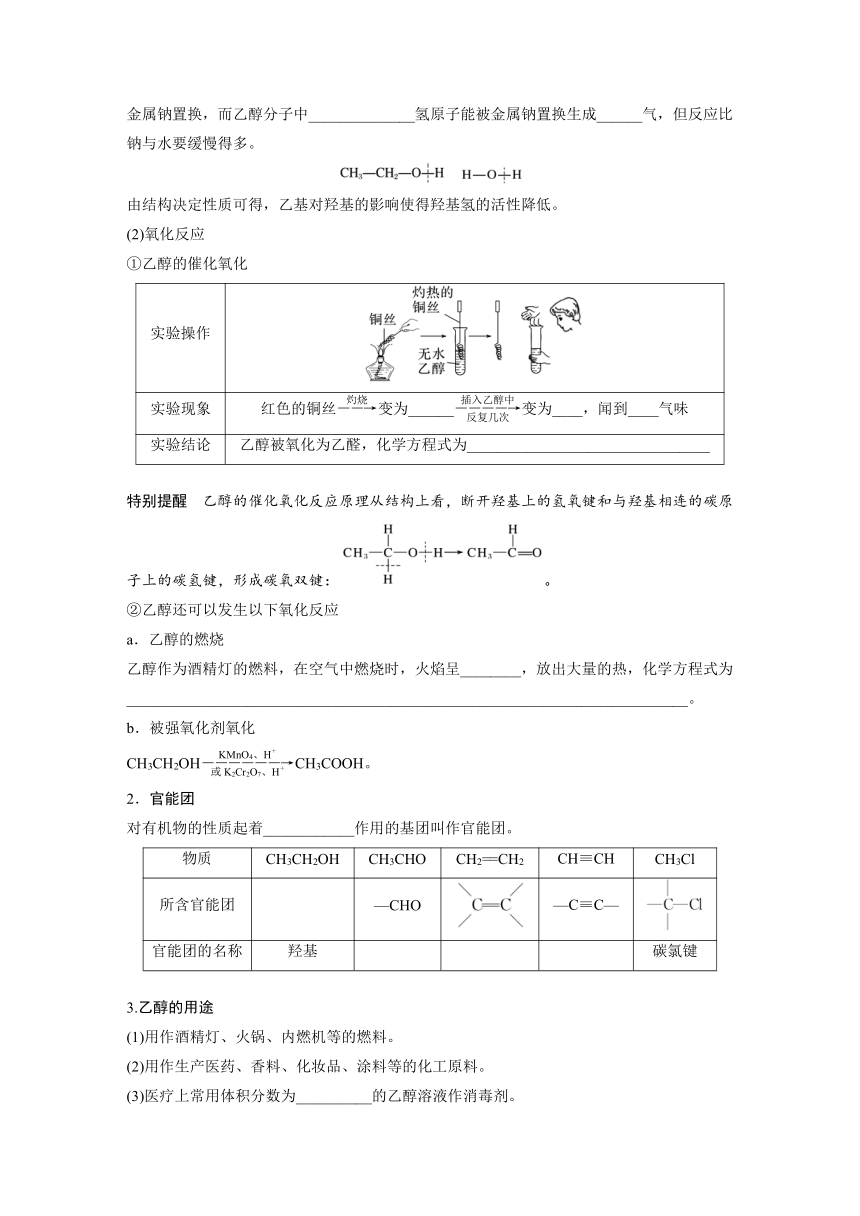
①乙醇的催化氧化
实验操作
实验现象 红色的铜丝变为______变为____,闻到____气味
实验结论 乙醇被氧化为乙醛,化学方程式为________________________________
特别提醒 乙醇的催化氧化反应原理从结构上看,断开羟基上的氢氧键和与羟基相连的碳原子上的碳氢键,形成碳氧双键:。
②乙醇还可以发生以下氧化反应
a.乙醇的燃烧
乙醇作为酒精灯的燃料,在空气中燃烧时,火焰呈________,放出大量的热,化学方程式为__________________________________________________________________________。
b.被强氧化剂氧化
CH3CH2OHCH3COOH。
2.官能团
对有机物的性质起着____________作用的基团叫作官能团。
物质 CH3CH2OH CH3CHO CH2==CH2 CH≡CH CH3Cl
所含官能团 —CHO —C≡C—
官能团的名称 羟基 碳氯键
3.乙醇的用途
(1)用作酒精灯、火锅、内燃机等的燃料。
(2)用作生产医药、香料、化妆品、涂料等的化工原料。
(3)医疗上常用体积分数为__________的乙醇溶液作消毒剂。
4.乙醛
乙醛中所含官能团为醛基(______________,可简写为____________),乙醛在适当条件下可进一步被氧气氧化,生成乙酸(CH3COOH),化学方程式为_________________________
____________________________________________________________________________。
(1)乙醇、水与钠反应的现象一样,钠都浮在液面上( )
(2)乙醇分子中羟基上的氢原子不如水中的氢原子活泼( )
(3)乙醇的分子式为C2H6O,故1 mol乙醇和足量的钠反应,可生成3 mol氢气( )
(4)乙醇能使酸性高锰酸钾溶液褪色( )
(5)乙醇的官能团为羟基,其电子式为( )
(6)乙醇能电离出H+,所以乙醇是电解质,能与NaOH溶液反应( )
(7)羟基和氢氧根离子具有相同的化学式和电子式( )
1.焊接铜器时,表面会生成黑色的氧化膜,铜匠说可以先把铜放在火上烧热,再立刻蘸一下酒精,铜会光亮如初。这一过程中发生了哪些反应?铜在反应中起到了什么作用?
2.能否催化氧化生成醛?
3.乙醇的官能团为羟基,羟基(—OH)和OH-有哪些区别和联系?请把下列表格补充完整。
名称 氢氧根离子(OH-) 羟基(—OH)
电子式
电性
稳定性
存在 ________存在于溶液或离子化合物中 ________存在,必须和其他基团或原子结合在一起
相同点 组成元素相同
1.丙烯醇(CH2==CH—CH2OH)可发生的化学反应有( )
①加成反应 ②氧化反应 ③燃烧 ④与钠反应
A.①②③ B.②③④
C.①②③④ D.①③④
2.现有甲、乙两种有机物,它们的结构简式分别为CH2==CHCH2CH2OH、。
(1)乙的分子式为____________。
(2)甲和乙中都含有的官能团为________________________________________________,
下列关于甲和乙两种有机物的叙述不正确的是________(填字母)。
a.都能与金属钠反应放出氢气
b.都能在催化剂作用下与H2反应
c.都能与NaOH溶液反应
d.甲能被催化氧化生成含—CHO的有机物
e.甲和乙与HBr、溴水发生加成反应,产物都只有一种
(1)乙醇反应时化学键的断裂
化学反应 键的断裂
与钠反应 ①
燃烧 ①②③④⑤
催化氧化 ①③
(2)醇的催化氧化反应规律(R、R′、R″代表烃基)
①凡有R—CH2OH结构的醇,在一定条件下都能被氧化成醛(R—CHO)。
②凡有R—CH(OH)—R′结构的醇,在一定条件下也能被氧化,但生成物不是醛,而是酮()。
③凡有结构的醇通常情况下不能被氧化。
1.下列有关乙醇的表述正确的是( )
A.乙醇分子中含有甲基,甲基的电子式为
B.乙醇的结构简式为C2H6O
C.乙醇分子中羟基的电子式为
D.乙醇分子的空间填充模型为
2.下列有关乙醇的说法错误的是( )
A.钠的密度大于乙醇,实验室可用乙醇保存金属钠
B.可用无水CuSO4检验工业酒精中是否含水
C.乙醇不能萃取出溴水中的溴
D.分离乙醇和水常用蒸馏的方法
3.(2022·石家庄高一月考)下列说法正确的是( )
A.乙醇分子中有—OH基团,所以乙醇溶于水后溶液显碱性
B.乙醇与钠反应可以产生氢气,所以乙醇溶于水后溶液显酸性
C.乙醇在空气中燃烧生成二氧化碳和水,说明乙醇分子中含有C、H、O三种元素
D.乙醇羟基中的氢原子比乙烷中的氢原子活泼
4.乙醇分子中的各化学键如图所示,下列关于乙醇分子在各种反应中断裂键的说法不正确的是( )
A.和金属钠反应时键①断裂
B.在铜催化共热下与O2反应时断裂①和③
C.在空气中完全燃烧时断裂①②③④⑤
D.乙醇是电解质,在水中键①断裂电离出氢离子
5.(2022·昆明高一检测)某课外活动小组的同学为了提高制取乙醛时的乙醇转化率,利用如图所示的装置进行乙醇的催化氧化实验制取乙醛,
(1)该实验常对试管甲采取的加热方式是______,其目的是_________________________。
(2)实验时,先加热玻璃管乙中的铜丝,约1分钟后鼓入空气,此时铜丝立即呈红热状态。若把酒精灯撤走,控制一定的鼓气速率,铜丝能长时间保持红热直到实验结束。
①铜丝能长时间保持红热的原因是_____________________________________________;
②控制鼓气速率的方法是_____________________________________________________。
(3)实验产物除用水吸收外,还可采用的收集方法是____________。
第二单元 食品中的有机化合物
第1课时 乙 醇
一、
1.碳、氢、氧 75%
2.CH3CH2OH C2H5OH
正误判断
(1)√ (2)× (3)× (4)×
深度思考
1.分别取少许三种液体于三支试管中,分别加入适量的水,液体不分层的是乙醇,液体分层且水在上层的是四氯化碳,液体分层且水在下层的是苯。
2.向乙醇中加入无水CuSO4粉末,若有蓝色物质生成,说明乙醇中含有水分;若无蓝色物质生成,说明乙醇中没有水分。除去乙醇中的水需要先加入生石灰吸水,再蒸馏。
应用体验
1.A [乙醇和水互溶,所以乙醇中的水不能通过分液的方法除去,而是先加入新制的生石灰,然后通过蒸馏法除去。]
2.B [乙烷和乙醇的结构简式分别为CH3CH3、CH3CH2OH,乙醇分子可以看作乙基与一个羟基相连的产物;乙醇分子的六个氢原子中,其中5个分别连接在两个碳原子上,1个连接在氧原子上,6个氢原子并不是完全相同的,B项错误。]
二、
1.(1)①无色无味 水珠 不变浑浊 氢气 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑ ②与碳原子相连的 羟基(—OH)上的 氢 (2)①黑色 红色 特殊 2CH3CH2OH+O22CH3CHO+2H2O ②a.淡蓝色 CH3CH2OH+3O22CO2+3H2O
2.决定性 —OH 醛基 碳碳双键 碳碳三键
3.(3)75%
4. —CHO 2CH3CHO+O22CH3COOH
正误判断
(1)× (2)√ (3)× (4)√ (5)× (6)× (7)×
解析 (3)乙醇分子中只有羟基上的氢原子才能和钠反应,故1 mol乙醇与足量的钠反应只生成0.5 mol氢气。
深度思考
1.2Cu+O22CuO、CH3CH2OH+CuOCH3CHO+Cu+H2O,铜作催化剂。
2.不能。该醇中羟基所连的碳原子上只有一个氢原子,不能催化氧化生成醛。
3.(10电子) (9电子) 带负电的阴离子 电中性 稳定 不稳定 能独立 不能独立
应用体验
1.C [丙烯醇中含有碳碳双键和羟基两种官能团,碳碳双键可发生①②③,羟基可发生②③④,而丙烯醇兼有两者的性质,故C项正确。]
2.(1)C6H10O (2)碳碳双键和羟基 ce
解析 甲和乙中都含有碳碳双键和—OH,所以甲和乙既有与乙烯相似的化学性质,又有与乙醇相似的化学性质。甲与乙醇相似,能被催化氧化为CH2==CHCH2CHO,甲和乙与Br2反应产物都只有一种,与HBr发生加成反应的产物都有两种。
随堂演练 知识落实
1.D [甲基的电子式为,A项错误;乙醇的结构简式为CH3CH2OH或C2H5OH,B项错误;羟基的电子式为,为中性基团,C项错误。]
2.A [钠可以和乙醇发生反应生成乙醇钠和氢气,故不能用乙醇保存金属钠,A错误;无水CuSO4可以和水反应生成蓝色晶体,故用无水CuSO4可检验工业酒精中是否含水,B正确;乙醇和水互溶,故乙醇不能萃取溴水中的溴,C正确;乙醇和水的沸点不同,故可以用蒸馏的方法分离乙醇和水,D正确。]
3.D [乙醇是非电解质,溶于水后不发生电离,因此乙醇溶液不显碱性或酸性,A、B错误;物质燃烧生成二氧化碳和水,只能说明该物质中含有C、H元素,C错误;根据乙醇能与Na反应,乙烷与Na不反应这一事实说明乙醇羟基中的氢原子比乙烷中的氢原子活泼,D正确。]
4.D [乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A项正确;乙醇催化氧化生成乙醛时,断裂①和③化学键,B项正确;乙醇完全燃烧时,化学键①②③④⑤全部断裂,C项正确;乙醇是非电解质,在水中键①不断裂,不能电离出氢离子。]
5.(1)水浴加热 加快乙醇汽化的速率 (2)①乙醇的催化氧化是放热反应 ②控制甲装置中单位时间内的气泡数 (3)将试管丁直接浸在冰水中冷却
第1课时 乙 醇
[核心素养发展目标] 1.知道乙醇的组成、结构、物理性质及用途,培养宏观辨识与微观探析的能力。2.了解烃的衍生物的概念及官能团与性质的关系,知道有机物之间在一定条件下是可以转化的,培养变化观念与平衡思想。3.会运用乙醇的结构分析其性质,能设计实验探究乙醇的结构及性质,培养科学探究精神。
一、乙醇的物理性质及分子结构
1.乙醇
乙醇是由____________三种元素组成的有机化合物,乙醇可以与水任意比例互溶,酒类饮料中含有浓度不等的乙醇,医疗上常用体积分数为________的乙醇溶液进行消毒。
特别提醒 常用无水CuSO4检验乙醇中是否有水,常用先加生石灰再蒸馏的方法提纯乙醇。
2.乙醇的组成与结构
分子式 C2H6O
结构式
结构简式 或____________
球棍模型
空间填充模型
特别提醒 乙醇分子中含有羟基(—OH),可以看成乙烷分子中的1个氢原子被羟基取代后的产物。有机化合物分子失去一个原子或原子团剩余的部分被称为基团,如乙醇可看作乙基和羟基组成。
(1)乙醇是一种优良的有机溶剂,能溶解很多有机物和无机物( )
(2)乙烷(CH3CH3)可以看成CH4分子中的一个H原子被甲基(—CH3)所取代而生成的产物,故乙烷为烃的衍生物( )
(3)乙醇可以看作乙烷分子中氢原子被氢氧根(OH-)取代后的产物,故乙醇水溶液应呈碱性
( )
(4)为提高消毒效果,医疗上可选择体积分数为95%的乙醇溶液进行消毒( )
1.如何只用一种试剂鉴别乙醇、苯和四氯化碳?
2.如何检验乙醇中是否有水?怎样除去乙醇中的水?
1.下列有关乙醇的物理性质的应用中不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分
C.由于乙醇能够以任意比溶于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇易挥发,所以才有“酒香不怕巷子深”的说法
2.比较乙烷和乙醇的分子结构,下列说法错误的是( )
A.两个碳原子均以单键相连
B.分子里都含6个相同的氢原子
C.乙基与一个氢原子相连就是乙烷分子
D.乙基与一个羟基相连就是乙醇分子
二、乙醇的化学性质及用途
1.乙醇的化学性质
(1)乙醇与金属钠的反应——置换反应
①基础实验
实验操作
实验现象 a.钠开始沉于试管底部,最终慢慢消失,产生__________气体; b.试管内壁有______产生; c.向试管中加入澄清石灰水,石灰水______________________
实验结论 乙醇与钠反应生成______,化学方程式为________________ ____________________________________________________
②反应实质
金属钠可以保存在煤油(多种烃的混合物)中,实验表明烷烃分子中______________氢不能被金属钠置换,而乙醇分子中______________氢原子能被金属钠置换生成______气,但反应比钠与水要缓慢得多。
由结构决定性质可得,乙基对羟基的影响使得羟基氢的活性降低。
(2)氧化反应
①乙醇的催化氧化
实验操作
实验现象 红色的铜丝变为______变为____,闻到____气味
实验结论 乙醇被氧化为乙醛,化学方程式为________________________________
特别提醒 乙醇的催化氧化反应原理从结构上看,断开羟基上的氢氧键和与羟基相连的碳原子上的碳氢键,形成碳氧双键:。
②乙醇还可以发生以下氧化反应
a.乙醇的燃烧
乙醇作为酒精灯的燃料,在空气中燃烧时,火焰呈________,放出大量的热,化学方程式为__________________________________________________________________________。
b.被强氧化剂氧化
CH3CH2OHCH3COOH。
2.官能团
对有机物的性质起着____________作用的基团叫作官能团。
物质 CH3CH2OH CH3CHO CH2==CH2 CH≡CH CH3Cl
所含官能团 —CHO —C≡C—
官能团的名称 羟基 碳氯键
3.乙醇的用途
(1)用作酒精灯、火锅、内燃机等的燃料。
(2)用作生产医药、香料、化妆品、涂料等的化工原料。
(3)医疗上常用体积分数为__________的乙醇溶液作消毒剂。
4.乙醛
乙醛中所含官能团为醛基(______________,可简写为____________),乙醛在适当条件下可进一步被氧气氧化,生成乙酸(CH3COOH),化学方程式为_________________________
____________________________________________________________________________。
(1)乙醇、水与钠反应的现象一样,钠都浮在液面上( )
(2)乙醇分子中羟基上的氢原子不如水中的氢原子活泼( )
(3)乙醇的分子式为C2H6O,故1 mol乙醇和足量的钠反应,可生成3 mol氢气( )
(4)乙醇能使酸性高锰酸钾溶液褪色( )
(5)乙醇的官能团为羟基,其电子式为( )
(6)乙醇能电离出H+,所以乙醇是电解质,能与NaOH溶液反应( )
(7)羟基和氢氧根离子具有相同的化学式和电子式( )
1.焊接铜器时,表面会生成黑色的氧化膜,铜匠说可以先把铜放在火上烧热,再立刻蘸一下酒精,铜会光亮如初。这一过程中发生了哪些反应?铜在反应中起到了什么作用?
2.能否催化氧化生成醛?
3.乙醇的官能团为羟基,羟基(—OH)和OH-有哪些区别和联系?请把下列表格补充完整。
名称 氢氧根离子(OH-) 羟基(—OH)
电子式
电性
稳定性
存在 ________存在于溶液或离子化合物中 ________存在,必须和其他基团或原子结合在一起
相同点 组成元素相同
1.丙烯醇(CH2==CH—CH2OH)可发生的化学反应有( )
①加成反应 ②氧化反应 ③燃烧 ④与钠反应
A.①②③ B.②③④
C.①②③④ D.①③④
2.现有甲、乙两种有机物,它们的结构简式分别为CH2==CHCH2CH2OH、。
(1)乙的分子式为____________。
(2)甲和乙中都含有的官能团为________________________________________________,
下列关于甲和乙两种有机物的叙述不正确的是________(填字母)。
a.都能与金属钠反应放出氢气
b.都能在催化剂作用下与H2反应
c.都能与NaOH溶液反应
d.甲能被催化氧化生成含—CHO的有机物
e.甲和乙与HBr、溴水发生加成反应,产物都只有一种
(1)乙醇反应时化学键的断裂
化学反应 键的断裂
与钠反应 ①
燃烧 ①②③④⑤
催化氧化 ①③
(2)醇的催化氧化反应规律(R、R′、R″代表烃基)
①凡有R—CH2OH结构的醇,在一定条件下都能被氧化成醛(R—CHO)。
②凡有R—CH(OH)—R′结构的醇,在一定条件下也能被氧化,但生成物不是醛,而是酮()。
③凡有结构的醇通常情况下不能被氧化。
1.下列有关乙醇的表述正确的是( )
A.乙醇分子中含有甲基,甲基的电子式为
B.乙醇的结构简式为C2H6O
C.乙醇分子中羟基的电子式为
D.乙醇分子的空间填充模型为
2.下列有关乙醇的说法错误的是( )
A.钠的密度大于乙醇,实验室可用乙醇保存金属钠
B.可用无水CuSO4检验工业酒精中是否含水
C.乙醇不能萃取出溴水中的溴
D.分离乙醇和水常用蒸馏的方法
3.(2022·石家庄高一月考)下列说法正确的是( )
A.乙醇分子中有—OH基团,所以乙醇溶于水后溶液显碱性
B.乙醇与钠反应可以产生氢气,所以乙醇溶于水后溶液显酸性
C.乙醇在空气中燃烧生成二氧化碳和水,说明乙醇分子中含有C、H、O三种元素
D.乙醇羟基中的氢原子比乙烷中的氢原子活泼
4.乙醇分子中的各化学键如图所示,下列关于乙醇分子在各种反应中断裂键的说法不正确的是( )
A.和金属钠反应时键①断裂
B.在铜催化共热下与O2反应时断裂①和③
C.在空气中完全燃烧时断裂①②③④⑤
D.乙醇是电解质,在水中键①断裂电离出氢离子
5.(2022·昆明高一检测)某课外活动小组的同学为了提高制取乙醛时的乙醇转化率,利用如图所示的装置进行乙醇的催化氧化实验制取乙醛,
(1)该实验常对试管甲采取的加热方式是______,其目的是_________________________。
(2)实验时,先加热玻璃管乙中的铜丝,约1分钟后鼓入空气,此时铜丝立即呈红热状态。若把酒精灯撤走,控制一定的鼓气速率,铜丝能长时间保持红热直到实验结束。
①铜丝能长时间保持红热的原因是_____________________________________________;
②控制鼓气速率的方法是_____________________________________________________。
(3)实验产物除用水吸收外,还可采用的收集方法是____________。
第二单元 食品中的有机化合物
第1课时 乙 醇
一、
1.碳、氢、氧 75%
2.CH3CH2OH C2H5OH
正误判断
(1)√ (2)× (3)× (4)×
深度思考
1.分别取少许三种液体于三支试管中,分别加入适量的水,液体不分层的是乙醇,液体分层且水在上层的是四氯化碳,液体分层且水在下层的是苯。
2.向乙醇中加入无水CuSO4粉末,若有蓝色物质生成,说明乙醇中含有水分;若无蓝色物质生成,说明乙醇中没有水分。除去乙醇中的水需要先加入生石灰吸水,再蒸馏。
应用体验
1.A [乙醇和水互溶,所以乙醇中的水不能通过分液的方法除去,而是先加入新制的生石灰,然后通过蒸馏法除去。]
2.B [乙烷和乙醇的结构简式分别为CH3CH3、CH3CH2OH,乙醇分子可以看作乙基与一个羟基相连的产物;乙醇分子的六个氢原子中,其中5个分别连接在两个碳原子上,1个连接在氧原子上,6个氢原子并不是完全相同的,B项错误。]
二、
1.(1)①无色无味 水珠 不变浑浊 氢气 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑ ②与碳原子相连的 羟基(—OH)上的 氢 (2)①黑色 红色 特殊 2CH3CH2OH+O22CH3CHO+2H2O ②a.淡蓝色 CH3CH2OH+3O22CO2+3H2O
2.决定性 —OH 醛基 碳碳双键 碳碳三键
3.(3)75%
4. —CHO 2CH3CHO+O22CH3COOH
正误判断
(1)× (2)√ (3)× (4)√ (5)× (6)× (7)×
解析 (3)乙醇分子中只有羟基上的氢原子才能和钠反应,故1 mol乙醇与足量的钠反应只生成0.5 mol氢气。
深度思考
1.2Cu+O22CuO、CH3CH2OH+CuOCH3CHO+Cu+H2O,铜作催化剂。
2.不能。该醇中羟基所连的碳原子上只有一个氢原子,不能催化氧化生成醛。
3.(10电子) (9电子) 带负电的阴离子 电中性 稳定 不稳定 能独立 不能独立
应用体验
1.C [丙烯醇中含有碳碳双键和羟基两种官能团,碳碳双键可发生①②③,羟基可发生②③④,而丙烯醇兼有两者的性质,故C项正确。]
2.(1)C6H10O (2)碳碳双键和羟基 ce
解析 甲和乙中都含有碳碳双键和—OH,所以甲和乙既有与乙烯相似的化学性质,又有与乙醇相似的化学性质。甲与乙醇相似,能被催化氧化为CH2==CHCH2CHO,甲和乙与Br2反应产物都只有一种,与HBr发生加成反应的产物都有两种。
随堂演练 知识落实
1.D [甲基的电子式为,A项错误;乙醇的结构简式为CH3CH2OH或C2H5OH,B项错误;羟基的电子式为,为中性基团,C项错误。]
2.A [钠可以和乙醇发生反应生成乙醇钠和氢气,故不能用乙醇保存金属钠,A错误;无水CuSO4可以和水反应生成蓝色晶体,故用无水CuSO4可检验工业酒精中是否含水,B正确;乙醇和水互溶,故乙醇不能萃取溴水中的溴,C正确;乙醇和水的沸点不同,故可以用蒸馏的方法分离乙醇和水,D正确。]
3.D [乙醇是非电解质,溶于水后不发生电离,因此乙醇溶液不显碱性或酸性,A、B错误;物质燃烧生成二氧化碳和水,只能说明该物质中含有C、H元素,C错误;根据乙醇能与Na反应,乙烷与Na不反应这一事实说明乙醇羟基中的氢原子比乙烷中的氢原子活泼,D正确。]
4.D [乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A项正确;乙醇催化氧化生成乙醛时,断裂①和③化学键,B项正确;乙醇完全燃烧时,化学键①②③④⑤全部断裂,C项正确;乙醇是非电解质,在水中键①不断裂,不能电离出氢离子。]
5.(1)水浴加热 加快乙醇汽化的速率 (2)①乙醇的催化氧化是放热反应 ②控制甲装置中单位时间内的气泡数 (3)将试管丁直接浸在冰水中冷却
