7.1 认识有机化合物(3课时 共162张PPT)
文档属性
| 名称 | 7.1 认识有机化合物(3课时 共162张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 95.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-08 18:20:19 | ||
图片预览










文档简介
(共162张PPT)
第七章 第一节
认识有机化合物
第一课时
名称由来
发展现状
早期发现的有机物都是从生命体内分离出来的。
随着科技的进步,很多有机物可以通过人工合成得到。
食品:糖类、油脂、蛋白质……
药物:阿司匹林、布洛芬……
材料:塑料、橡胶、纤维……
能源:煤、石油、天然气……
有机化合物
C9H8O4
CH4
C6H12O6
通过观察,你能否发现上述有机物在组成上有什么相同之处?
有机化合物
都含有C元素
C9H8O4
CH4
C6H12O6
有机化合物
通过观察,你能否发现上述有机物在组成上有什么相同之处?
有机化合物:含有C元素的化合物
1.碳酸及其盐类:H2CO3、Na2CO3、KHCO3等
2.碳的氧化物:CO、CO2
3.金属碳化物:CaC2等
4.氰化物和硫氰化物:HCN、KCN、KSCN等
5.SiC等物质
以上五类物质均为无机物。
碳元素在地壳中含量比较低,但是含碳的有机化合物种类和数量却很多。目前,人们在自然界发现和人工合成的物质已经超过一亿种,这其中绝大多数都是有机物,而且新的有机化合物还在源源不断的被发现和被合成出来,有机化合物为什么如此繁多呢?
一、碳原子成键数目探究
碳的原子结构示意图
+6
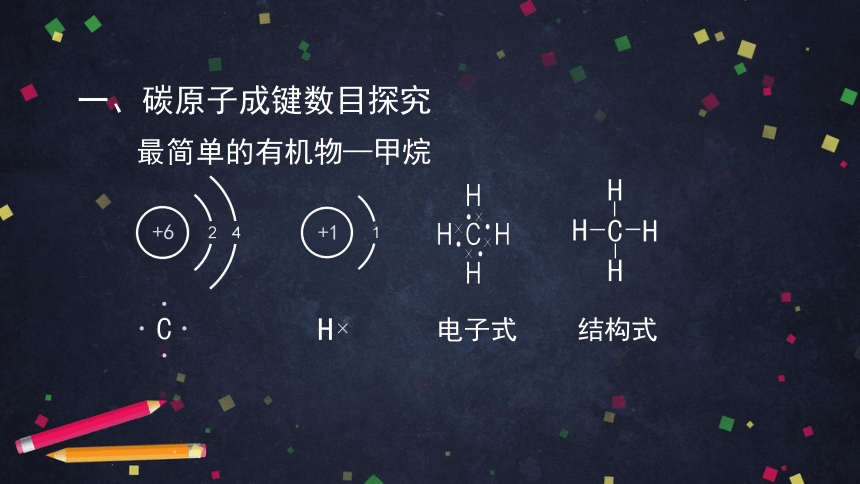
最简单的有机物—甲烷
H
×
+1
+6
一、碳原子成键数目探究
最简单的有机物—甲烷
+1
+6
电子式
一、碳原子成键数目探究
H
×
最简单的有机物—甲烷
H
×
+1
+6
电子式
结构式
一、碳原子成键数目探究
一、碳原子成键数目探究
碳原子不但可以和氢原子(H)、氯原子(Cl)形成共价键,也可以和氧原子(O)、硫原子(S)、氮原子(N)等形成共价键,原则是碳原子最终形成4个共价键。
一、碳原子成键数目探究
实验室常见的球棍模型
一、碳原子成键数目探究
一、碳原子成键数目探究
一、碳原子成键数目探究
一、碳原子成键数目探究
一、碳原子成键数目探究
C
碳原子的成键数目
4个共价键
一、碳原子成键数目探究
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
一、碳原子成键数目探究
二、碳原子之间的成键方式
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
乙烷
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
二、碳原子之间的成键方式
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
二、碳原子之间的成键方式
乙烯
乙炔
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
二、碳原子之间的成键方式
拼插思路:先确定碳骨架,再补齐氢原子
二、碳原子之间的成键方式
碳原子之间的成键方式
单键
双键
三键
二、碳原子之间的成键方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
二、碳原子之间的成键方式
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
不稳定,很少存在
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
三、碳骨架的连接方式
丙烷
丙二烯(不稳定)
丙烯
丙炔
环丙烷
三、碳骨架的连接方式
碳骨架的连接方式
链状结构
环状结构
三、碳骨架的连接方式
思考Ⅲ.提供4个碳原子,碳碳之间以单键形式连接,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅲ.提供4个碳原子,碳碳之间以单键形式连接,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅲ.提供4个碳原子,碳碳之间以单键形式连接,
你能否拼插出合理的有机化合物?
直链结构
三、碳骨架的连接方式
思考Ⅲ.提供4个碳原子,碳碳之间以单键形式连接,
你能否拼插出合理的有机化合物?
支链结构
三、碳骨架的连接方式
三、碳骨架的连接方式
C4H10
C4H10
三、碳骨架的连接方式
碳骨架的连接方式
链状结构
环状结构
直链
支链
三、碳骨架的连接方式
1.这些有机化合物分子式是什么?
C4H10
C4H6
① C4H10
③ C4H8
④ C4H8
⑦ C4H6
⑤ C4H8
⑥ C4H6
⑧ C4H8
② C4H10
⑨ C4H8
④
①
③
②
⑥
⑤
⑦
⑧
⑨
2.上述结构中,哪些是链状结构,哪些是环状结构?
④
①
③
②
⑥
⑤
⑦
⑧
⑨
链状结构:①—⑦,其中①③④⑥⑦为直链结构,②⑤为支链结构。
环状结构:⑧⑨为环状结构。
④
①
③
②
⑥
⑤
⑦
⑧
⑨
3.C原子有几种成键方式?分别在哪些分子中有所呈现?
碳骨架是链状结构,且带有支链,碳原子之间既有单键,也有双键。
碳骨架是环状和链状相结合,且碳原子之间都以单键结合。
总结
碳原子的成键数目
碳原子之间的成键方式
碳骨架的连接方式
单键
双键
三键
链状结构
环状结构
直链
支链
4个共价键
碳原子的成键特点
例.下列有关有机化合物组成的叙述正确的是( )
A.有机物只含有碳、氢两种元素
B.一氧化碳、二氧化碳是含碳化合物,所以它们是有机化合物
C.人类已知的化合物中,种类最多的是含ⅣA族元素的化合物
D.有机物只能存在于动植物体内,不能通过人工的方法合成
C
例.下列有关有机化合物组成的叙述正确的是( )
A.有机物只含有碳、氢两种元素
B.一氧化碳、二氧化碳是含碳化合物,所以它们是有机化合物
C.人类已知的化合物中,种类最多的是含ⅣA族元素的化合物
D.有机物只能存在于动植物体内,不能通过人工的方法合成
目前已知化合物中,数量和种类最多的是ⅣA族碳的化合物,下列 有关其原因,叙述不正确的是( )
A.碳原子既可以和自身,又可以和其他原子形成4个共价键
B.碳原子性质活泼,可以和多种原子形成共价键
C.碳原子之间既可以形成单键,又可以形成双键和三键
D.多个碳原子之间可以形成长度不同的链(可以有支链)和环,且
链和环之间又可以相互结合
例.
目前已知化合物中,数量和种类最多的是ⅣA族碳的化合物,下列 有关其原因,叙述不正确的是( )
A.碳原子既可以和自身,又可以和其他原子形成4个共价键
B.碳原子性质活泼,可以和多种原子形成共价键
C.碳原子之间既可以形成单键,又可以形成双键和三键
D.多个碳原子之间可以形成长度不同的链(可以有支链)和环,且
链和环之间又可以相互结合
例.
B
例.下列化合物中,不只代表一种化合物的是( )
A.CH4 B.C2H6 C.C3H8 D.C4H10
D
例.下列化合物中,不只代表一种化合物的是( )
A.CH4 B.C2H6 C.C3H8 D.C4H10
例.下图是正丁烷的球棍模型,有关该结构说法正确的是( )
A.正丁烷的分子式为C4H8
B.分子中碳骨架为支链结构
C.分子中含有4个C—C单键
D.分子中共含有13个共价键
例.下图是正丁烷的球棍模型,有关该结构说法正确的是( )
A.正丁烷的分子式为C4H8
B.分子中碳骨架为支链结构
C.分子中含有4个C—C单键
D.分子中共含有13个共价键
D
实验数据表明:甲烷分子中的5个原子不在同一平面上,分子中的C—H键的长度和强度相同,相互之间的夹角相等。
第二课时
知识回顾
有机化合物中碳原子的成键特点
C
H
H
H
H
实验数据表明:甲烷分子中的5个原子不在同一平面上,每个分子中的4个C—H键的长度和强度相同,相互之间的夹角相等。
一、甲烷的分子结构
碳原子位于正四面体的中心,4个氢原子分别位于4个顶点。4个C—H的长度和强度相同,相互之间的夹角相等。
正四面体结构
正四面体结构
不同时期提出的甲烷分子结构图示
1个C原子2个H原子
化学科学中最早的结构式
不同时期提出的甲烷分子结构图示
有组成
不是立体结构
有组成
未体现结构
有组成和化学键
不是立体结构
不同时期提出的甲烷分子结构图示
体现了甲烷的组成和空间结构
甲烷结构的正确表示
开辟立体化学新篇章
不同时期提出的甲烷分子结构图示
甲烷
与甲烷结构相似的有机化合物
搭建任务一:2个碳原子、6个氢原子
甲烷
与甲烷结构相似的有机化合物
搭建任务一:2个碳原子、6个氢原子
甲烷
与甲烷结构相似的有机化合物
搭建任务一:2个碳原子、6个氢原子
与甲烷结构相似的有机化合物
甲烷
(3)
乙烷的结构式
H
C
H
H
H
C
H
H
(2)
乙烷分子球棍模型
(上节课作品)
(1)
乙烷分子球棍模型
立体→平面的投影
搭建任务二:3个碳原子、8个氢原子
甲烷
与甲烷结构相似的有机化合物
H
C
H
H
H
C
H
H
H
C
H
与甲烷结构相似的有机化合物
搭建任务二:3个碳原子、8个氢原子
甲烷CH4
乙烷C2H6
丙烷C3H8
只含碳、氢两种元素
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
烷烃
二、烷烃
烃
C
C
碳原子数不多于10时,以甲、乙、丙、丁、戊、己、庚、 辛、壬、癸依次代表碳原子数,如丙烷;
(2) 碳原子数在10以上时,以汉字数字代表,如十一烷。
烷烃的名称:“碳原子数+烷”
对比下面三种烷烃分子的结构式和分子式,请你归纳烷烃分子式的通式?
请你归纳
甲烷CH4
乙烷C2H6
丙烷C3H8
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
通式:CnH2n+2
二、烷烃
甲烷CH4
乙烷C2H6
丙烷C3H8
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
三、同系物
结构相似,在分子组成上相差一个或若干个CH2原子团的化合物互称为同系物。
甲烷CH4
乙烷C2H6
丙烷C3H8
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
三、同系物
结构相似,在分子组成上相差一个或若干个CH2原子团的化合物互称为同系物。
甲烷CH4
乙烷C2H6
丙烷C3H8
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
请你思考1
丙烷C3H8
乙烯C2H4
下列两种物质互为同系物吗?
思考与讨论
你们书写的丁烷的结构式一样吗?为什么会出现两种结构式?
搭建任务三(丁烷):4个碳原子、10个氢原子
与甲烷结构相似的有机化合物
搭建任务三(丁烷):4个碳原子、10个氢原子
与甲烷结构相似的有机化合物
正丁烷
搭建任务三(丁烷):4个碳原子、10个氢原子
正丁烷C4H10
异丁烷C4H10
与甲烷结构相似的有机化合物
正丁烷C4H10
异丁烷C4H10
C4H10
正丁烷
熔点-138.4 ℃,沸点-0.5 ℃
C4H10
异丁烷
熔点-159.4 ℃,沸点-11.6 ℃
四、同分异构体
正丁烷C4H10
异丁烷C4H10
具有相同的分子式,但具有不同的结构的现象称为同分异构现象。
正丁烷C4H10
异丁烷C4H10
具有相同的分子式,但具有不同的结构的现象称为同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
四、同分异构体
请你观察
请你观察下面三个结构式,找出他们的相同点和不同点?
请你观察
请你观察下面三个结构式,找出他们的相同点和不同点?
C5H12
C5H12
C5H12
请你观察
请你观察下面三个结构式,找出他们的相同点和不同点?
C5H12
C5H12
C5H12
正戊烷
新戊烷
异戊烷
丁烷:2种
戊烷:3种
己烷:5种
……
癸烷:75种
烷烃的同分异构体数目规律
规律:随着碳原子数的增加,烷烃的同分异
构体的数目也就越多。
请你思考2
下面两种结构式,互为同分异构体吗?
H
Cl
C
C
Cl
Cl
Cl
H
H
H
下面两种结构式,是同分异构体吗?
请你思考2
H
Cl
C
C
Cl
Cl
Cl
H
H
H
为什么烷烃中的碳链不是一条直线,而是呈锯齿状?
碳骨架呈锯齿状
请你思考3
同系物的多样性和同分异构现象的广泛存在都是有机化合物种类繁多的原因。同系物与同分异构体之间的关系是:
互为同系物的物质 为同分异构体,互为同分异构体的物质 为同系物。
请你辨析
同系物的多样性和同分异构现象的广泛存在都是有机化合物种类繁多的原因。同系物与同分异构体之间的关系是:
互为同系物的物质 为同分异构体,互为同分异构体的物质 为同系物。
请你辨析
一定不
同系物的多样性和同分异构现象的广泛存在都是有机化合物种类繁多的原因。同系物与同分异构体之间的关系是:
互为同系物的物质 为同分异构体,互为同分异构体的物质 为同系物。
请你辨析
一定不
一定不
②CH3CHCH2CH2CH3
④CH3CH2CH2CH2CH2CH3
CH3
下列物质中,互为同分异构体的是
互为同系物的是
请你判断1
①CH3CH2CH2CH3
③CH3CH3
请你判断1
C4H10
C6H14
C2H6
C6H14
②④
②CH3CHCH2CH2CH3
④CH3CH2CH2CH2CH2CH3
CH3
①CH3CH2CH2CH3
③CH3CH3
下列物质中,互为同分异构体的是
互为同系物的是
请你判断1
①②③
①③④
和
②CH3CHCH2CH2CH3
④CH3CH2CH2CH2CH2CH3
CH3
①CH3CH2CH2CH3
③CH3CH3
下列物质中,互为同分异构体的是
互为同系物的是
②④
C4H10
C6H14
C2H6
C6H14
请你判断2
(1) CH2=CH CH3
CH2
(2) CH3 CH CH2 CH3 CH3 CH CH CH3
CH3
CH3
CH3
CH2 CH2
下列各组中的两种物质是否互为同分异构体?
和
和
请你判断2
C3H6
C3H6
(2) CH3 CH CH2 CH3 CH3 CH CH CH3
CH3
CH3
CH3
下列各组中的两种物质是否互为同分异构体?
和
C5H12
C6H14
(1) CH2=CH CH3
CH2
CH2 CH2
和
请你判断2
C3H6
C3H6
(2) CH3 CH CH2 CH3 CH3 CH CH CH3
CH3
CH3
CH3
下列各组中的两种物质是否互为同分异构体?
和
C5H12
C6H14
是
否
(1) CH2=CH CH3
CH2
CH2 CH2
和
第三课时
思考与讨论
天然气、沼气和煤层气的主要成分是甲烷;部分护肤品、医用软膏中的“凡士林”和蜡烛、蜡笔中的石蜡,其主要成分是含碳原子数较多的烷烃。请结合生活经验和初中所学的有关知识,想一想烷烃可能具有哪些性质。
烷烃的物理性质
1.烷烃均为难溶于水的无色物质。
烷烃的物理性质
名称 常温下状态 熔点/℃ 沸点/℃ 相对密度
甲烷 气 -182.5 -161.5
乙烷 气 -182.8 -88.6
丁烷 气 -138.4 -0.5 0.5788
戊烷 液 -129.7 36.0 0.6262
癸烷 液 -29.7 174.1 0.7298
十七烷 固 22.0 302.2 0.7767
烷烃的物理性质
1.烷烃均为难溶于水的无色物质。
2.烷烃的熔点、沸点、密度随着分子中碳原子数的增加(同时相
对分子质量也在增大)而升高,在常温下的状态由气态变为液
态,再到固态。
烷烃的化学性质
1.稳定性
与强酸、强碱或高锰酸钾等强氧化剂不反应
烷烃的化学性质
2.氧化反应
CH4 + 2O2 CO2 + 2H2O
点燃
C3H8 + 5O2 3CO2 + 4H2O
点燃
烷烃的化学性质
2.氧化反应
用途:用作燃料
注意:通风、严禁烟火,确保安全生产
CH4 + 2O2 CO2 + 2H2O
点燃
C3H8 + 5O2 3CO2 + 4H2O
点燃
烷烃的化学性质
3.高温分解
用途:制备化工原料和燃料
【实验7-1】甲烷与氯气的反应
如何收集甲烷?如何收集氯气?
甲烷:排水集气
氯气:排饱和NaCl溶液集气
【实验7-1】甲烷与氯气的反应
静置一段时间,观察两支试管内的现象
套上铝箔
饱和
NaCl溶液
光亮处
饱和
NaCl溶液
【实验7-1】甲烷与氯气的反应
试管内液面的变化?
物质状态变化?
气体颜色变化?
观察实验
资料
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照 试管内气体颜色变浅
试管壁上有油状液滴
试管中液面上升
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照 试管内气体颜色变浅 氯气逐渐消耗
试管壁上有油状液滴 生成不溶于水的液体
试管中液面上升 试管内气体压强减小
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照 试管内气体颜色变浅 氯气逐渐消耗
试管壁上有油状液滴 生成不溶于水的液体
试管中液面上升 试管内气体压强减小
反应过程相对缓慢 许多有机反应比较缓慢
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照 试管内气体颜色变浅 氯气逐渐消耗
试管壁上有油状液滴 生成不溶于水的液体
试管中液面上升 试管内气体压强减小
反应过程相对缓慢 许多有机反应比较缓慢
可能观察到白雾 生成HCl
烷烃的化学性质
4.取代反应
取代:取而代之、替代
C
H
H
H
H
Cl
Cl
+
烷烃的化学性质
4.取代反应
取代:取而代之、替代
C
H
H
H
H
Cl
Cl
+
H
Cl
+
产物 1
光
烷烃的化学性质
4.取代反应
取代:取而代之、替代
一氯甲烷
(气体、不溶于水)
C
H
H
H
H
Cl
Cl
+
H
Cl
+
光
C
Cl
H
H
H
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
一氯甲烷
(气体、不溶于水)
C
H
H
H
H
Cl
Cl
+
H
Cl
+
光
C
Cl
H
H
H
烷烃的化学性质
4.取代反应
二氯甲烷
(液体、不溶于水)
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
一氯甲烷
C
H
H
Cl
H
Cl
Cl
+
H
Cl
+
光
C
Cl
H
Cl
H
烷烃的化学性质
4.取代反应
三氯甲烷(氯仿)
(液体、不溶于水)
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
二氯甲烷
C
H
H
Cl
Cl
Cl
Cl
+
H
Cl
+
光
C
Cl
H
Cl
Cl
烷烃的化学性质
4.取代反应
四氯甲烷(四氯化碳)
(液体、不溶于水)
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
三氯甲烷
C
H
Cl
Cl
Cl
Cl
Cl
+
H
Cl
+
光
C
Cl
Cl
Cl
Cl
甲烷与氯气反应
动画模拟演示
资料
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
甲烷与氯气的取代反应
(1)甲烷分子中4个氢原子被氯原子逐一替代
(2)产物为混合物
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
+ Cl2
+ HCl
CH4
CH3Cl
CH2Cl2
CHCl3
CH3Cl
CH2Cl2
CHCl3
CCl4
光
+ HCl
+ Cl2
光
+ Cl2
光
+ HCl
+ Cl2
光
+ HCl
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
烷烃在一定条件下,可以与卤素单质发生取代反应
烷烃的化学性质和用途
1.稳定性
2.氧化反应
3.高温分解
4.取代反应
1.燃料
2.生产化工原料
3.有机溶剂
化学性质:
常见用途:
1.大多数有机化合物熔点较低
2.大多数有机化合物难溶于水,易溶于汽油、乙醇、苯等有机溶剂
3.大多数有机化合物容易燃烧,受热发生分解
有机化合物通性
反应原理、条件较复杂,常伴有副反应发生
有机物化学反应特点
有机化合物通性
1.大多数有机化合物熔点较低
2.大多数有机化合物难溶于水,易溶于汽油、乙醇、苯等有机溶剂
3.大多数有机化合物容易燃烧,受热发生分解
学习方法提升
烷烃代表物
甲烷
有机物化合物母体 烷烃
有机化合物
结构
结构
结构
性质
性质
性质
【课堂练习】
在一定条件下,下列物质可与甲烷发生化学反应的是( )
A. Cl2 B. 浓硫酸 C. O2 D. 高锰酸钾酸性溶液
【分析】
A.甲烷与Cl2在光照条件下可发生取代反应
B.甲烷化学性质较稳定,不与浓硫酸反应
C.甲烷可以在空气中燃烧,被O2氧化
D.甲烷化学性质较稳定,不能被高锰酸钾氧化
【课堂练习】
在一定条件下,下列物质可与甲烷发生化学反应的是( )
A. Cl2 B. 浓硫酸 C. O2 D. 高锰酸钾酸性溶液
A C
【分析】
A.甲烷与Cl2在光照条件下可发生取代反应
B.甲烷化学性质较稳定,不与浓硫酸反应
C.甲烷可以在空气中燃烧,被O2氧化
D.甲烷化学性质较稳定,不能被高锰酸钾氧化
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
该烷烃分子中 N(C) :N(H) =?
N = n NA
N(C) :N(H) = n(C) :n(H)
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
该烷烃分子中 N(C) :N(H) =?
N = n NA
N(C) :N(H) = n(C) :n(H)
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
n(CO2)
2n(H2O)
n(C)=
n(H)=
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式
【分析】
n(CO2) =
17.6 g
44 g/mol
= 0.4 mol
2n(H2O)=
9.0 g × 2
18 g/mol
=1.0 mol
该烷烃分子中碳原子与氢原子的个数比为4:10
n(C)=
n(H)=
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
该烷烃分子式为C4H10
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
该烷烃分子式为C4H10
结构简式为CH3CH2CH2CH3
CH3 CH CH3
CH3
或
【课堂练习】
下列有关说法不正确的是( )
A.天然气的主要成分为CH4
B.1 mol Cl2与1 mol CH4在光照条件下恰好完全反应,则产物
只有CH3Cl
C.反应CH3CH3 + Br2 CH3CH2Br + HBr,属于取代反应
D.CH4的二氯代物只有一种,此事实可说明CH4为正四面体结构
光
【课堂练习】
【分析】
A.天然气的主要成分为CH4
B.CH4与Cl2发生取代反应,产物为CH3Cl、CH2Cl2、CHCl3、CCl4
和HCl的混合物
【课堂练习】
【分析】
C.反应CH3CH3 + Br2 CH3CH2Br + HBr,属于取代反应
光
取代反应:
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
【课堂练习】
【分析】
D.CH4的二氯代物只有一种,此事实可说明CH4为正四面体结构
甲烷
二氯甲烷
【课堂练习】
下列有关说法不正确的是( )
A.天然气的主要成分为CH4
B.1 mol Cl2与1 mol CH4在光照条件下恰好完全反应,则产物
只有CH3Cl
C.反应CH3CH3 + Br2 CH3CH2Br + HBr,属于取代反应
D.CH4的二氯代物只有一种,此事实可说明CH4为正四面体结构
光
B
第七章 第一节
认识有机化合物
第一课时
名称由来
发展现状
早期发现的有机物都是从生命体内分离出来的。
随着科技的进步,很多有机物可以通过人工合成得到。
食品:糖类、油脂、蛋白质……
药物:阿司匹林、布洛芬……
材料:塑料、橡胶、纤维……
能源:煤、石油、天然气……
有机化合物
C9H8O4
CH4
C6H12O6
通过观察,你能否发现上述有机物在组成上有什么相同之处?
有机化合物
都含有C元素
C9H8O4
CH4
C6H12O6
有机化合物
通过观察,你能否发现上述有机物在组成上有什么相同之处?
有机化合物:含有C元素的化合物
1.碳酸及其盐类:H2CO3、Na2CO3、KHCO3等
2.碳的氧化物:CO、CO2
3.金属碳化物:CaC2等
4.氰化物和硫氰化物:HCN、KCN、KSCN等
5.SiC等物质
以上五类物质均为无机物。
碳元素在地壳中含量比较低,但是含碳的有机化合物种类和数量却很多。目前,人们在自然界发现和人工合成的物质已经超过一亿种,这其中绝大多数都是有机物,而且新的有机化合物还在源源不断的被发现和被合成出来,有机化合物为什么如此繁多呢?
一、碳原子成键数目探究
碳的原子结构示意图
+6
最简单的有机物—甲烷
H
×
+1
+6
一、碳原子成键数目探究
最简单的有机物—甲烷
+1
+6
电子式
一、碳原子成键数目探究
H
×
最简单的有机物—甲烷
H
×
+1
+6
电子式
结构式
一、碳原子成键数目探究
一、碳原子成键数目探究
碳原子不但可以和氢原子(H)、氯原子(Cl)形成共价键,也可以和氧原子(O)、硫原子(S)、氮原子(N)等形成共价键,原则是碳原子最终形成4个共价键。
一、碳原子成键数目探究
实验室常见的球棍模型
一、碳原子成键数目探究
一、碳原子成键数目探究
一、碳原子成键数目探究
一、碳原子成键数目探究
一、碳原子成键数目探究
C
碳原子的成键数目
4个共价键
一、碳原子成键数目探究
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
一、碳原子成键数目探究
二、碳原子之间的成键方式
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
乙烷
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
二、碳原子之间的成键方式
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
二、碳原子之间的成键方式
乙烯
乙炔
思考Ⅰ.提供2个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
二、碳原子之间的成键方式
拼插思路:先确定碳骨架,再补齐氢原子
二、碳原子之间的成键方式
碳原子之间的成键方式
单键
双键
三键
二、碳原子之间的成键方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
二、碳原子之间的成键方式
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
不稳定,很少存在
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅱ.提供3个碳原子,氢原子数目不限制,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
三、碳骨架的连接方式
丙烷
丙二烯(不稳定)
丙烯
丙炔
环丙烷
三、碳骨架的连接方式
碳骨架的连接方式
链状结构
环状结构
三、碳骨架的连接方式
思考Ⅲ.提供4个碳原子,碳碳之间以单键形式连接,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅲ.提供4个碳原子,碳碳之间以单键形式连接,
你能否拼插出合理的有机化合物?
三、碳骨架的连接方式
思考Ⅲ.提供4个碳原子,碳碳之间以单键形式连接,
你能否拼插出合理的有机化合物?
直链结构
三、碳骨架的连接方式
思考Ⅲ.提供4个碳原子,碳碳之间以单键形式连接,
你能否拼插出合理的有机化合物?
支链结构
三、碳骨架的连接方式
三、碳骨架的连接方式
C4H10
C4H10
三、碳骨架的连接方式
碳骨架的连接方式
链状结构
环状结构
直链
支链
三、碳骨架的连接方式
1.这些有机化合物分子式是什么?
C4H10
C4H6
① C4H10
③ C4H8
④ C4H8
⑦ C4H6
⑤ C4H8
⑥ C4H6
⑧ C4H8
② C4H10
⑨ C4H8
④
①
③
②
⑥
⑤
⑦
⑧
⑨
2.上述结构中,哪些是链状结构,哪些是环状结构?
④
①
③
②
⑥
⑤
⑦
⑧
⑨
链状结构:①—⑦,其中①③④⑥⑦为直链结构,②⑤为支链结构。
环状结构:⑧⑨为环状结构。
④
①
③
②
⑥
⑤
⑦
⑧
⑨
3.C原子有几种成键方式?分别在哪些分子中有所呈现?
碳骨架是链状结构,且带有支链,碳原子之间既有单键,也有双键。
碳骨架是环状和链状相结合,且碳原子之间都以单键结合。
总结
碳原子的成键数目
碳原子之间的成键方式
碳骨架的连接方式
单键
双键
三键
链状结构
环状结构
直链
支链
4个共价键
碳原子的成键特点
例.下列有关有机化合物组成的叙述正确的是( )
A.有机物只含有碳、氢两种元素
B.一氧化碳、二氧化碳是含碳化合物,所以它们是有机化合物
C.人类已知的化合物中,种类最多的是含ⅣA族元素的化合物
D.有机物只能存在于动植物体内,不能通过人工的方法合成
C
例.下列有关有机化合物组成的叙述正确的是( )
A.有机物只含有碳、氢两种元素
B.一氧化碳、二氧化碳是含碳化合物,所以它们是有机化合物
C.人类已知的化合物中,种类最多的是含ⅣA族元素的化合物
D.有机物只能存在于动植物体内,不能通过人工的方法合成
目前已知化合物中,数量和种类最多的是ⅣA族碳的化合物,下列 有关其原因,叙述不正确的是( )
A.碳原子既可以和自身,又可以和其他原子形成4个共价键
B.碳原子性质活泼,可以和多种原子形成共价键
C.碳原子之间既可以形成单键,又可以形成双键和三键
D.多个碳原子之间可以形成长度不同的链(可以有支链)和环,且
链和环之间又可以相互结合
例.
目前已知化合物中,数量和种类最多的是ⅣA族碳的化合物,下列 有关其原因,叙述不正确的是( )
A.碳原子既可以和自身,又可以和其他原子形成4个共价键
B.碳原子性质活泼,可以和多种原子形成共价键
C.碳原子之间既可以形成单键,又可以形成双键和三键
D.多个碳原子之间可以形成长度不同的链(可以有支链)和环,且
链和环之间又可以相互结合
例.
B
例.下列化合物中,不只代表一种化合物的是( )
A.CH4 B.C2H6 C.C3H8 D.C4H10
D
例.下列化合物中,不只代表一种化合物的是( )
A.CH4 B.C2H6 C.C3H8 D.C4H10
例.下图是正丁烷的球棍模型,有关该结构说法正确的是( )
A.正丁烷的分子式为C4H8
B.分子中碳骨架为支链结构
C.分子中含有4个C—C单键
D.分子中共含有13个共价键
例.下图是正丁烷的球棍模型,有关该结构说法正确的是( )
A.正丁烷的分子式为C4H8
B.分子中碳骨架为支链结构
C.分子中含有4个C—C单键
D.分子中共含有13个共价键
D
实验数据表明:甲烷分子中的5个原子不在同一平面上,分子中的C—H键的长度和强度相同,相互之间的夹角相等。
第二课时
知识回顾
有机化合物中碳原子的成键特点
C
H
H
H
H
实验数据表明:甲烷分子中的5个原子不在同一平面上,每个分子中的4个C—H键的长度和强度相同,相互之间的夹角相等。
一、甲烷的分子结构
碳原子位于正四面体的中心,4个氢原子分别位于4个顶点。4个C—H的长度和强度相同,相互之间的夹角相等。
正四面体结构
正四面体结构
不同时期提出的甲烷分子结构图示
1个C原子2个H原子
化学科学中最早的结构式
不同时期提出的甲烷分子结构图示
有组成
不是立体结构
有组成
未体现结构
有组成和化学键
不是立体结构
不同时期提出的甲烷分子结构图示
体现了甲烷的组成和空间结构
甲烷结构的正确表示
开辟立体化学新篇章
不同时期提出的甲烷分子结构图示
甲烷
与甲烷结构相似的有机化合物
搭建任务一:2个碳原子、6个氢原子
甲烷
与甲烷结构相似的有机化合物
搭建任务一:2个碳原子、6个氢原子
甲烷
与甲烷结构相似的有机化合物
搭建任务一:2个碳原子、6个氢原子
与甲烷结构相似的有机化合物
甲烷
(3)
乙烷的结构式
H
C
H
H
H
C
H
H
(2)
乙烷分子球棍模型
(上节课作品)
(1)
乙烷分子球棍模型
立体→平面的投影
搭建任务二:3个碳原子、8个氢原子
甲烷
与甲烷结构相似的有机化合物
H
C
H
H
H
C
H
H
H
C
H
与甲烷结构相似的有机化合物
搭建任务二:3个碳原子、8个氢原子
甲烷CH4
乙烷C2H6
丙烷C3H8
只含碳、氢两种元素
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
烷烃
二、烷烃
烃
C
C
碳原子数不多于10时,以甲、乙、丙、丁、戊、己、庚、 辛、壬、癸依次代表碳原子数,如丙烷;
(2) 碳原子数在10以上时,以汉字数字代表,如十一烷。
烷烃的名称:“碳原子数+烷”
对比下面三种烷烃分子的结构式和分子式,请你归纳烷烃分子式的通式?
请你归纳
甲烷CH4
乙烷C2H6
丙烷C3H8
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
通式:CnH2n+2
二、烷烃
甲烷CH4
乙烷C2H6
丙烷C3H8
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
三、同系物
结构相似,在分子组成上相差一个或若干个CH2原子团的化合物互称为同系物。
甲烷CH4
乙烷C2H6
丙烷C3H8
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
三、同系物
结构相似,在分子组成上相差一个或若干个CH2原子团的化合物互称为同系物。
甲烷CH4
乙烷C2H6
丙烷C3H8
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
H
C
H
H
C
H
H
H
请你思考1
丙烷C3H8
乙烯C2H4
下列两种物质互为同系物吗?
思考与讨论
你们书写的丁烷的结构式一样吗?为什么会出现两种结构式?
搭建任务三(丁烷):4个碳原子、10个氢原子
与甲烷结构相似的有机化合物
搭建任务三(丁烷):4个碳原子、10个氢原子
与甲烷结构相似的有机化合物
正丁烷
搭建任务三(丁烷):4个碳原子、10个氢原子
正丁烷C4H10
异丁烷C4H10
与甲烷结构相似的有机化合物
正丁烷C4H10
异丁烷C4H10
C4H10
正丁烷
熔点-138.4 ℃,沸点-0.5 ℃
C4H10
异丁烷
熔点-159.4 ℃,沸点-11.6 ℃
四、同分异构体
正丁烷C4H10
异丁烷C4H10
具有相同的分子式,但具有不同的结构的现象称为同分异构现象。
正丁烷C4H10
异丁烷C4H10
具有相同的分子式,但具有不同的结构的现象称为同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
四、同分异构体
请你观察
请你观察下面三个结构式,找出他们的相同点和不同点?
请你观察
请你观察下面三个结构式,找出他们的相同点和不同点?
C5H12
C5H12
C5H12
请你观察
请你观察下面三个结构式,找出他们的相同点和不同点?
C5H12
C5H12
C5H12
正戊烷
新戊烷
异戊烷
丁烷:2种
戊烷:3种
己烷:5种
……
癸烷:75种
烷烃的同分异构体数目规律
规律:随着碳原子数的增加,烷烃的同分异
构体的数目也就越多。
请你思考2
下面两种结构式,互为同分异构体吗?
H
Cl
C
C
Cl
Cl
Cl
H
H
H
下面两种结构式,是同分异构体吗?
请你思考2
H
Cl
C
C
Cl
Cl
Cl
H
H
H
为什么烷烃中的碳链不是一条直线,而是呈锯齿状?
碳骨架呈锯齿状
请你思考3
同系物的多样性和同分异构现象的广泛存在都是有机化合物种类繁多的原因。同系物与同分异构体之间的关系是:
互为同系物的物质 为同分异构体,互为同分异构体的物质 为同系物。
请你辨析
同系物的多样性和同分异构现象的广泛存在都是有机化合物种类繁多的原因。同系物与同分异构体之间的关系是:
互为同系物的物质 为同分异构体,互为同分异构体的物质 为同系物。
请你辨析
一定不
同系物的多样性和同分异构现象的广泛存在都是有机化合物种类繁多的原因。同系物与同分异构体之间的关系是:
互为同系物的物质 为同分异构体,互为同分异构体的物质 为同系物。
请你辨析
一定不
一定不
②CH3CHCH2CH2CH3
④CH3CH2CH2CH2CH2CH3
CH3
下列物质中,互为同分异构体的是
互为同系物的是
请你判断1
①CH3CH2CH2CH3
③CH3CH3
请你判断1
C4H10
C6H14
C2H6
C6H14
②④
②CH3CHCH2CH2CH3
④CH3CH2CH2CH2CH2CH3
CH3
①CH3CH2CH2CH3
③CH3CH3
下列物质中,互为同分异构体的是
互为同系物的是
请你判断1
①②③
①③④
和
②CH3CHCH2CH2CH3
④CH3CH2CH2CH2CH2CH3
CH3
①CH3CH2CH2CH3
③CH3CH3
下列物质中,互为同分异构体的是
互为同系物的是
②④
C4H10
C6H14
C2H6
C6H14
请你判断2
(1) CH2=CH CH3
CH2
(2) CH3 CH CH2 CH3 CH3 CH CH CH3
CH3
CH3
CH3
CH2 CH2
下列各组中的两种物质是否互为同分异构体?
和
和
请你判断2
C3H6
C3H6
(2) CH3 CH CH2 CH3 CH3 CH CH CH3
CH3
CH3
CH3
下列各组中的两种物质是否互为同分异构体?
和
C5H12
C6H14
(1) CH2=CH CH3
CH2
CH2 CH2
和
请你判断2
C3H6
C3H6
(2) CH3 CH CH2 CH3 CH3 CH CH CH3
CH3
CH3
CH3
下列各组中的两种物质是否互为同分异构体?
和
C5H12
C6H14
是
否
(1) CH2=CH CH3
CH2
CH2 CH2
和
第三课时
思考与讨论
天然气、沼气和煤层气的主要成分是甲烷;部分护肤品、医用软膏中的“凡士林”和蜡烛、蜡笔中的石蜡,其主要成分是含碳原子数较多的烷烃。请结合生活经验和初中所学的有关知识,想一想烷烃可能具有哪些性质。
烷烃的物理性质
1.烷烃均为难溶于水的无色物质。
烷烃的物理性质
名称 常温下状态 熔点/℃ 沸点/℃ 相对密度
甲烷 气 -182.5 -161.5
乙烷 气 -182.8 -88.6
丁烷 气 -138.4 -0.5 0.5788
戊烷 液 -129.7 36.0 0.6262
癸烷 液 -29.7 174.1 0.7298
十七烷 固 22.0 302.2 0.7767
烷烃的物理性质
1.烷烃均为难溶于水的无色物质。
2.烷烃的熔点、沸点、密度随着分子中碳原子数的增加(同时相
对分子质量也在增大)而升高,在常温下的状态由气态变为液
态,再到固态。
烷烃的化学性质
1.稳定性
与强酸、强碱或高锰酸钾等强氧化剂不反应
烷烃的化学性质
2.氧化反应
CH4 + 2O2 CO2 + 2H2O
点燃
C3H8 + 5O2 3CO2 + 4H2O
点燃
烷烃的化学性质
2.氧化反应
用途:用作燃料
注意:通风、严禁烟火,确保安全生产
CH4 + 2O2 CO2 + 2H2O
点燃
C3H8 + 5O2 3CO2 + 4H2O
点燃
烷烃的化学性质
3.高温分解
用途:制备化工原料和燃料
【实验7-1】甲烷与氯气的反应
如何收集甲烷?如何收集氯气?
甲烷:排水集气
氯气:排饱和NaCl溶液集气
【实验7-1】甲烷与氯气的反应
静置一段时间,观察两支试管内的现象
套上铝箔
饱和
NaCl溶液
光亮处
饱和
NaCl溶液
【实验7-1】甲烷与氯气的反应
试管内液面的变化?
物质状态变化?
气体颜色变化?
观察实验
资料
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照 试管内气体颜色变浅
试管壁上有油状液滴
试管中液面上升
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照 试管内气体颜色变浅 氯气逐渐消耗
试管壁上有油状液滴 生成不溶于水的液体
试管中液面上升 试管内气体压强减小
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照 试管内气体颜色变浅 氯气逐渐消耗
试管壁上有油状液滴 生成不溶于水的液体
试管中液面上升 试管内气体压强减小
反应过程相对缓慢 许多有机反应比较缓慢
【实验7-1】甲烷与氯气的反应现象及分析
实验现象 分析原因
无光照 无明显变化 无光照该反应不能发生
光照 试管内气体颜色变浅 氯气逐渐消耗
试管壁上有油状液滴 生成不溶于水的液体
试管中液面上升 试管内气体压强减小
反应过程相对缓慢 许多有机反应比较缓慢
可能观察到白雾 生成HCl
烷烃的化学性质
4.取代反应
取代:取而代之、替代
C
H
H
H
H
Cl
Cl
+
烷烃的化学性质
4.取代反应
取代:取而代之、替代
C
H
H
H
H
Cl
Cl
+
H
Cl
+
产物 1
光
烷烃的化学性质
4.取代反应
取代:取而代之、替代
一氯甲烷
(气体、不溶于水)
C
H
H
H
H
Cl
Cl
+
H
Cl
+
光
C
Cl
H
H
H
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
一氯甲烷
(气体、不溶于水)
C
H
H
H
H
Cl
Cl
+
H
Cl
+
光
C
Cl
H
H
H
烷烃的化学性质
4.取代反应
二氯甲烷
(液体、不溶于水)
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
一氯甲烷
C
H
H
Cl
H
Cl
Cl
+
H
Cl
+
光
C
Cl
H
Cl
H
烷烃的化学性质
4.取代反应
三氯甲烷(氯仿)
(液体、不溶于水)
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
二氯甲烷
C
H
H
Cl
Cl
Cl
Cl
+
H
Cl
+
光
C
Cl
H
Cl
Cl
烷烃的化学性质
4.取代反应
四氯甲烷(四氯化碳)
(液体、不溶于水)
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
三氯甲烷
C
H
Cl
Cl
Cl
Cl
Cl
+
H
Cl
+
光
C
Cl
Cl
Cl
Cl
甲烷与氯气反应
动画模拟演示
资料
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
甲烷与氯气的取代反应
(1)甲烷分子中4个氢原子被氯原子逐一替代
(2)产物为混合物
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
+ Cl2
+ HCl
CH4
CH3Cl
CH2Cl2
CHCl3
CH3Cl
CH2Cl2
CHCl3
CCl4
光
+ HCl
+ Cl2
光
+ Cl2
光
+ HCl
+ Cl2
光
+ HCl
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
烷烃的化学性质
4.取代反应
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
烷烃在一定条件下,可以与卤素单质发生取代反应
烷烃的化学性质和用途
1.稳定性
2.氧化反应
3.高温分解
4.取代反应
1.燃料
2.生产化工原料
3.有机溶剂
化学性质:
常见用途:
1.大多数有机化合物熔点较低
2.大多数有机化合物难溶于水,易溶于汽油、乙醇、苯等有机溶剂
3.大多数有机化合物容易燃烧,受热发生分解
有机化合物通性
反应原理、条件较复杂,常伴有副反应发生
有机物化学反应特点
有机化合物通性
1.大多数有机化合物熔点较低
2.大多数有机化合物难溶于水,易溶于汽油、乙醇、苯等有机溶剂
3.大多数有机化合物容易燃烧,受热发生分解
学习方法提升
烷烃代表物
甲烷
有机物化合物母体 烷烃
有机化合物
结构
结构
结构
性质
性质
性质
【课堂练习】
在一定条件下,下列物质可与甲烷发生化学反应的是( )
A. Cl2 B. 浓硫酸 C. O2 D. 高锰酸钾酸性溶液
【分析】
A.甲烷与Cl2在光照条件下可发生取代反应
B.甲烷化学性质较稳定,不与浓硫酸反应
C.甲烷可以在空气中燃烧,被O2氧化
D.甲烷化学性质较稳定,不能被高锰酸钾氧化
【课堂练习】
在一定条件下,下列物质可与甲烷发生化学反应的是( )
A. Cl2 B. 浓硫酸 C. O2 D. 高锰酸钾酸性溶液
A C
【分析】
A.甲烷与Cl2在光照条件下可发生取代反应
B.甲烷化学性质较稳定,不与浓硫酸反应
C.甲烷可以在空气中燃烧,被O2氧化
D.甲烷化学性质较稳定,不能被高锰酸钾氧化
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
该烷烃分子中 N(C) :N(H) =?
N = n NA
N(C) :N(H) = n(C) :n(H)
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
该烷烃分子中 N(C) :N(H) =?
N = n NA
N(C) :N(H) = n(C) :n(H)
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
n(CO2)
2n(H2O)
n(C)=
n(H)=
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式
【分析】
n(CO2) =
17.6 g
44 g/mol
= 0.4 mol
2n(H2O)=
9.0 g × 2
18 g/mol
=1.0 mol
该烷烃分子中碳原子与氢原子的个数比为4:10
n(C)=
n(H)=
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
该烷烃分子式为C4H10
【课堂练习】
某种烷烃完全燃烧后生成了17.6 g CO2和9.0 g H2O。请据此推测其分子式,并写出可能的结构简式。
【分析】
该烷烃分子式为C4H10
结构简式为CH3CH2CH2CH3
CH3 CH CH3
CH3
或
【课堂练习】
下列有关说法不正确的是( )
A.天然气的主要成分为CH4
B.1 mol Cl2与1 mol CH4在光照条件下恰好完全反应,则产物
只有CH3Cl
C.反应CH3CH3 + Br2 CH3CH2Br + HBr,属于取代反应
D.CH4的二氯代物只有一种,此事实可说明CH4为正四面体结构
光
【课堂练习】
【分析】
A.天然气的主要成分为CH4
B.CH4与Cl2发生取代反应,产物为CH3Cl、CH2Cl2、CHCl3、CCl4
和HCl的混合物
【课堂练习】
【分析】
C.反应CH3CH3 + Br2 CH3CH2Br + HBr,属于取代反应
光
取代反应:
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
【课堂练习】
【分析】
D.CH4的二氯代物只有一种,此事实可说明CH4为正四面体结构
甲烷
二氯甲烷
【课堂练习】
下列有关说法不正确的是( )
A.天然气的主要成分为CH4
B.1 mol Cl2与1 mol CH4在光照条件下恰好完全反应,则产物
只有CH3Cl
C.反应CH3CH3 + Br2 CH3CH2Br + HBr,属于取代反应
D.CH4的二氯代物只有一种,此事实可说明CH4为正四面体结构
光
B
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
