福建省漳州市2022-2023学年高一上学期期末教学质量检测化学试题(含答案)
文档属性
| 名称 | 福建省漳州市2022-2023学年高一上学期期末教学质量检测化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-09 00:00:00 | ||
图片预览


文档简介
漳州市2022-2023学年高一上学期期末教学质量检测
化学试题
一、选择题(本题包括12小题,每小题4分,每小题只有一个正确答案,共48分)
1.化学与生活密切相关.下列说法错误的是( )
A.焰火中的红色来源于钠盐灼烧
B.氧化镁的熔点高,是优质的耐高温材料
C.红酒中添加适量可以起到杀菌和抗氧化的作用
D.奥密克戎病毒能在空气中以气溶胶的形式传播,气溶胶属于胶体
2.2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动,其中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象.醋酸钠属于( )
A.氧化物 B.酸 C.碱 D.盐
3.反应放热且产生气体,可用于冬天石油开采.下列关于反应中相关微粒的叙述错误的是( )
A.中子数为18的氯原子为 B.Na的原子结构示意图为
C.和互为同位素 D.的电子数为10
4.用如图实验装置和方法进行相应实验,装置和现象均正确且能达到实验目的的是( )
A.收集 B.从碘水中萃取碘 C.分离沸点相差较大的液体混合物 D.蒸干溶液获得晶体
5.常温下,在无色透明溶液中,下列各组离子能大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
6.下列实验操作能达到目的的是( )
选项 实验目的 实验操作
A 除去中的 将混合气体通入NaOH溶液中
B 除去中的HCl 将混合气体分别通入盛有饱和食盐水、浓硫酸的洗气瓶
C 证明还原性 将金属钠投入溶液中
D 检验晶体中含有 取少量晶体溶于水,滴加NaOH溶液并加热,用湿润的蓝色石蕊试纸检验产生的气体
7.设为阿伏加德罗常数的值,下列说法错误的是( )
A.中质子的数目为
B.的溶液中的数目为
C.常温常压下,中原子的数目为
D.和足量Fe完全反应,转移电子的数目为
8.饮用水中的会对人类健康产生危害,为了降低饮用水中的浓度,可以在碱性条件下加入铝粉,其反应的化学方程式为.下列说法正确的是( )
A.是还原剂
B.Al被还原
C.既是氧化产物也是还原产物
D.在标准状况下,每生成时,转移的电子数目约为
9.下列离子方程式书写正确的是( )
A.过氧化钠和水反应:
B.用小苏打治疗胃酸过多:
C,稀硫酸与溶液反应:
D.向氢氧化铜悬浊液中滴加稀硫酸:
10.在探究新制饱和氯水成分及性质的实验中,下列根据实验现象得出的结论错误的是( )
A.氯水的颜色呈浅黄绿色,说明氯水中含有
B.向氯水中滴加硝酸酸化的溶液,产生白色沉淀,说明氯水中含有
C.新制氯水能使品红溶液褪色,说明具有漂白性
D.向氯水中加入粉末,有气泡产生,说明氯水呈酸性
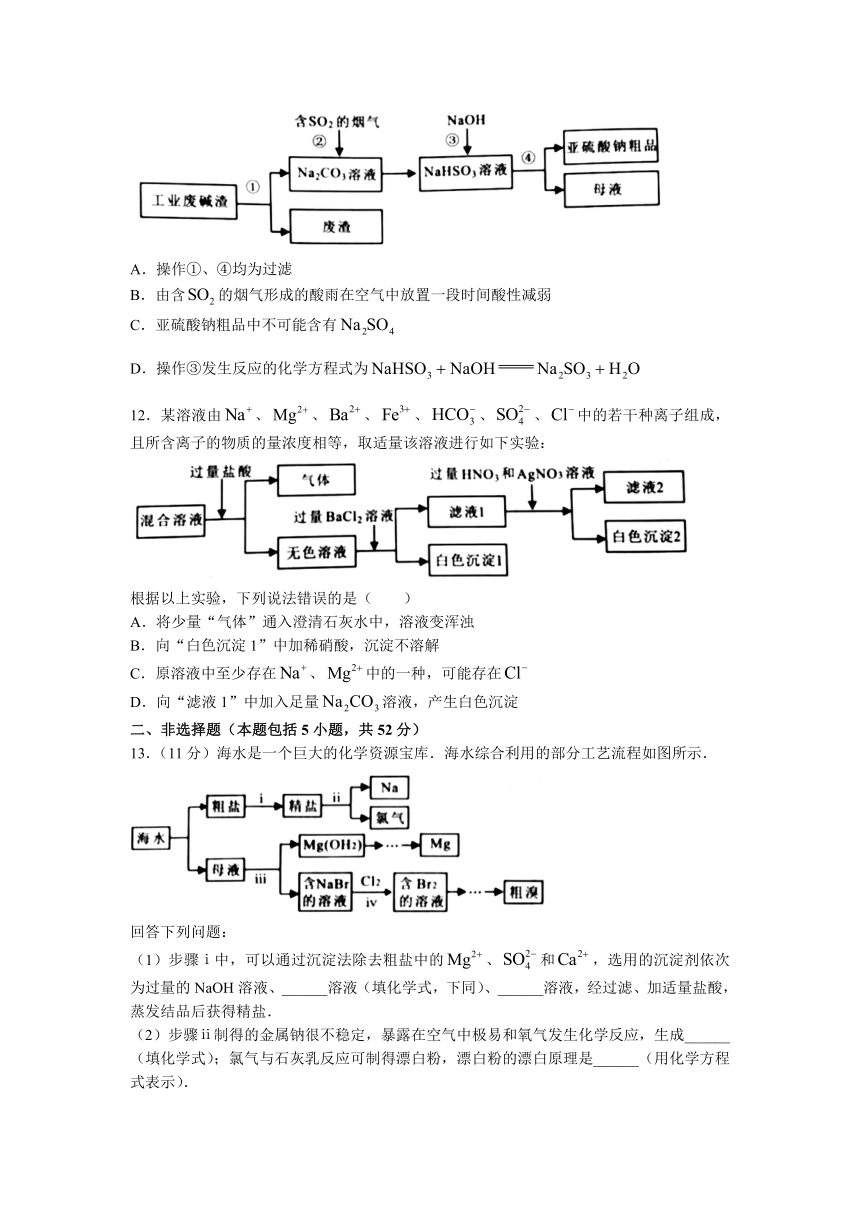
11.“以废治废”是基于“绿色化学”观念治理污染的思路.用工业废碱渣(主要成分为)吸收烟气中的,得到亚硫酸钠粗品,其工艺流程如图所示.下列说法正确的是( )
A.操作①、④均为过滤
B.由含的烟气形成的酸雨在空气中放置一段时间酸性减弱
C.亚硫酸钠粗品中不可能含有
D.操作③发生反应的化学方程式为
12.某溶液由、、、、、、中的若干种离子组成,且所含离子的物质的量浓度相等,取适量该溶液进行如下实验:
根据以上实验,下列说法错误的是( )
A.将少量“气体”通入澄清石灰水中,溶液变浑浊
B.向“白色沉淀1”中加稀硝酸,沉淀不溶解
C.原溶液中至少存在、中的一种,可能存在
D.向“滤液1”中加入足量溶液,产生白色沉淀
二、非选择题(本题包括5小题,共52分)
13.(11分)海水是一个巨大的化学资源宝库.海水综合利用的部分工艺流程如图所示.
回答下列问题:
(1)步骤ⅰ中,可以通过沉淀法除去粗盐中的、和,选用的沉淀剂依次为过量的NaOH溶液、______溶液(填化学式,下同)、______溶液,经过滤、加适量盐酸,蒸发结品后获得精盐.
(2)步骤ⅱ制得的金属钠很不稳定,暴露在空气中极易和氧气发生化学反应,生成______(填化学式);氯气与石灰乳反应可制得漂白粉,漂白粉的漂白原理是______(用化学方程式表示).
(3)步骤ⅲ中分离与含NaBr的溶液的操作名称是______,在实验室中进行该操作需要的玻璃仪器有烧杯、玻璃棒和______;通过一系列操作最后获得无水,写出由制取Mg的化学方程式______.
(4)写出步骤ⅳ主要反应的离子方程式______.
14.(14分)“价—类”二维图是预测物质性质的重要思维工具.下图为氯及其化合物的“价—类”二维图,回答下列问题:
(1)上图HCl、和HClO中,属于电解质的是______(填化学式).
(2)写出在水中的电离方程式______.
(3)写出实验室用浓盐酸和制取的化学方程式______.
(4)根据上图氯元素的化合价判断,HClO在反应中既可作氧化剂,又可作还原剂.当它作氧化剂时,理论上可能被还原为______(填标号).
A. B. C. D.
(5)和浓盐酸反应也可制得,该反应的化学方程式为:
①该反应中参加反应的HCl和被氧化的HCl的物质的量之比为______.
②请用“双线桥”法标明该反应电子转移的方向和数目.
(6)高铁酸钾是一种水处理剂,易溶于水,可对水杀菌消毒.一定条件下,向KClO与KOH的混合溶液中加入溶液,可得到和KCl,该反应的离子方程式为______.
15.(12分)在抗击新型冠状病毒的过程中,84消毒液、双氧水、75%的酒精溶液等消毒剂可有效灭活冠状病毒.某84消毒液中NaClO的物质的量浓度为,在实际使用过程中需要稀释.
(1)配制的NaClO消毒液,需要该84消毒液______mL.
(2)配制过程中需要的玻璃仪器除了烧杯、玻璃棒、量筒,还需要______、______.
(3)配制的操作顺序应是量取→______→______→______→______→摇匀(各操作只用一次,填标号).
A.定容 B.转移 C.洗涤、转移 D.稀释
(4)“转移”过程中,为了防止溶液洒出,应采取的措施是______.
(5)下列情况会使所配溶液浓度偏低的是______(填标号).
A.转移溶液前容量瓶内有少量蒸馏水
B.溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
C.定容时,俯视容量瓶的刻度线
D.定容摇匀后,发现液面降低,又补加少量水,重新达到刻度线
(6)含氯消毒剂的消毒能力可以用“有效氧”来表示,“有效氯”是指与含氯消毒剂氧化能力相当的氯气的质量.某溶液中含有(消毒过程中NaClO被还原为NaCl),该溶液的“有效氯”是______g.
16.(11分)某化学课外兴趣小组用下图所示装置制取并完成有关性质的探究.
回答下列问题:
(1)装置A中用于滴加浓硫酸的仪器名称是______,发生反应的化学方程式为______.
(2)装置B中装有饱和溶液,可暂时储存气体,装置A加热一段时间后关闭止水夹K,B中出现的现象是______.
(3)若装置D中试剂为溶液,通入一段时间后出现淡黄色浑浊,则体现的______性(填“氧化”或“还原”).
(4)若装置D中试剂为溶液,某同学预测D中溶液由棕黄色变成浅绿色,依据是______(用离子方程式表示).
(5)若装置D中试剂为品红的水溶液,通入后溶液褪色;而更换为品红的乙醇溶液,通入干燥的后无明显现象.据此推测,使品红的水溶液褪色的微粒可能是______(填微粒符号).
(6)装置E的作用是______.
17.(4分)为测定某溶液的浓度,取待测液,向其中加入过量溶液.充分反应后过滤、洗涤并干燥,得到沉淀的质量为,反应的化学方程式为.求该溶液中的物质的量浓度(请写出计算过程).
漳州市2022-2023学年高一上学期期末教学质量检测
化学试题参考答案及评分标准
一、选择题(本题包括12小题,每小题4分,每小题只有一个正确答案,共48分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 A D A A B B C D A C D C
二、非选择题(本题包括5小题,共52分)
13.(11分)
(1)
(2)
(3)过滤 漏斗
(4)
14.(14分)
(1)HCl、HClO
(2)
(3)
(4)AB
(5)①8∶5
②
(6)
15.(12分)
(1)125
(2)500mL容量瓶 胶头滴管
(3)DBCA
(4)用玻璃棒进行引流
(5)BD
(6)71
16.(11分)
(1)分液漏斗
(2)B中液面下降,长颈漏斗下端导管液面上升
(3)氧化
(4)
(5)(或、均可)
(6)吸收多余的,防止其污染环境
17.(4分)
化学试题
一、选择题(本题包括12小题,每小题4分,每小题只有一个正确答案,共48分)
1.化学与生活密切相关.下列说法错误的是( )
A.焰火中的红色来源于钠盐灼烧
B.氧化镁的熔点高,是优质的耐高温材料
C.红酒中添加适量可以起到杀菌和抗氧化的作用
D.奥密克戎病毒能在空气中以气溶胶的形式传播,气溶胶属于胶体
2.2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动,其中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象.醋酸钠属于( )
A.氧化物 B.酸 C.碱 D.盐
3.反应放热且产生气体,可用于冬天石油开采.下列关于反应中相关微粒的叙述错误的是( )
A.中子数为18的氯原子为 B.Na的原子结构示意图为
C.和互为同位素 D.的电子数为10
4.用如图实验装置和方法进行相应实验,装置和现象均正确且能达到实验目的的是( )
A.收集 B.从碘水中萃取碘 C.分离沸点相差较大的液体混合物 D.蒸干溶液获得晶体
5.常温下,在无色透明溶液中,下列各组离子能大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
6.下列实验操作能达到目的的是( )
选项 实验目的 实验操作
A 除去中的 将混合气体通入NaOH溶液中
B 除去中的HCl 将混合气体分别通入盛有饱和食盐水、浓硫酸的洗气瓶
C 证明还原性 将金属钠投入溶液中
D 检验晶体中含有 取少量晶体溶于水,滴加NaOH溶液并加热,用湿润的蓝色石蕊试纸检验产生的气体
7.设为阿伏加德罗常数的值,下列说法错误的是( )
A.中质子的数目为
B.的溶液中的数目为
C.常温常压下,中原子的数目为
D.和足量Fe完全反应,转移电子的数目为
8.饮用水中的会对人类健康产生危害,为了降低饮用水中的浓度,可以在碱性条件下加入铝粉,其反应的化学方程式为.下列说法正确的是( )
A.是还原剂
B.Al被还原
C.既是氧化产物也是还原产物
D.在标准状况下,每生成时,转移的电子数目约为
9.下列离子方程式书写正确的是( )
A.过氧化钠和水反应:
B.用小苏打治疗胃酸过多:
C,稀硫酸与溶液反应:
D.向氢氧化铜悬浊液中滴加稀硫酸:
10.在探究新制饱和氯水成分及性质的实验中,下列根据实验现象得出的结论错误的是( )
A.氯水的颜色呈浅黄绿色,说明氯水中含有
B.向氯水中滴加硝酸酸化的溶液,产生白色沉淀,说明氯水中含有
C.新制氯水能使品红溶液褪色,说明具有漂白性
D.向氯水中加入粉末,有气泡产生,说明氯水呈酸性
11.“以废治废”是基于“绿色化学”观念治理污染的思路.用工业废碱渣(主要成分为)吸收烟气中的,得到亚硫酸钠粗品,其工艺流程如图所示.下列说法正确的是( )
A.操作①、④均为过滤
B.由含的烟气形成的酸雨在空气中放置一段时间酸性减弱
C.亚硫酸钠粗品中不可能含有
D.操作③发生反应的化学方程式为
12.某溶液由、、、、、、中的若干种离子组成,且所含离子的物质的量浓度相等,取适量该溶液进行如下实验:
根据以上实验,下列说法错误的是( )
A.将少量“气体”通入澄清石灰水中,溶液变浑浊
B.向“白色沉淀1”中加稀硝酸,沉淀不溶解
C.原溶液中至少存在、中的一种,可能存在
D.向“滤液1”中加入足量溶液,产生白色沉淀
二、非选择题(本题包括5小题,共52分)
13.(11分)海水是一个巨大的化学资源宝库.海水综合利用的部分工艺流程如图所示.
回答下列问题:
(1)步骤ⅰ中,可以通过沉淀法除去粗盐中的、和,选用的沉淀剂依次为过量的NaOH溶液、______溶液(填化学式,下同)、______溶液,经过滤、加适量盐酸,蒸发结品后获得精盐.
(2)步骤ⅱ制得的金属钠很不稳定,暴露在空气中极易和氧气发生化学反应,生成______(填化学式);氯气与石灰乳反应可制得漂白粉,漂白粉的漂白原理是______(用化学方程式表示).
(3)步骤ⅲ中分离与含NaBr的溶液的操作名称是______,在实验室中进行该操作需要的玻璃仪器有烧杯、玻璃棒和______;通过一系列操作最后获得无水,写出由制取Mg的化学方程式______.
(4)写出步骤ⅳ主要反应的离子方程式______.
14.(14分)“价—类”二维图是预测物质性质的重要思维工具.下图为氯及其化合物的“价—类”二维图,回答下列问题:
(1)上图HCl、和HClO中,属于电解质的是______(填化学式).
(2)写出在水中的电离方程式______.
(3)写出实验室用浓盐酸和制取的化学方程式______.
(4)根据上图氯元素的化合价判断,HClO在反应中既可作氧化剂,又可作还原剂.当它作氧化剂时,理论上可能被还原为______(填标号).
A. B. C. D.
(5)和浓盐酸反应也可制得,该反应的化学方程式为:
①该反应中参加反应的HCl和被氧化的HCl的物质的量之比为______.
②请用“双线桥”法标明该反应电子转移的方向和数目.
(6)高铁酸钾是一种水处理剂,易溶于水,可对水杀菌消毒.一定条件下,向KClO与KOH的混合溶液中加入溶液,可得到和KCl,该反应的离子方程式为______.
15.(12分)在抗击新型冠状病毒的过程中,84消毒液、双氧水、75%的酒精溶液等消毒剂可有效灭活冠状病毒.某84消毒液中NaClO的物质的量浓度为,在实际使用过程中需要稀释.
(1)配制的NaClO消毒液,需要该84消毒液______mL.
(2)配制过程中需要的玻璃仪器除了烧杯、玻璃棒、量筒,还需要______、______.
(3)配制的操作顺序应是量取→______→______→______→______→摇匀(各操作只用一次,填标号).
A.定容 B.转移 C.洗涤、转移 D.稀释
(4)“转移”过程中,为了防止溶液洒出,应采取的措施是______.
(5)下列情况会使所配溶液浓度偏低的是______(填标号).
A.转移溶液前容量瓶内有少量蒸馏水
B.溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
C.定容时,俯视容量瓶的刻度线
D.定容摇匀后,发现液面降低,又补加少量水,重新达到刻度线
(6)含氯消毒剂的消毒能力可以用“有效氧”来表示,“有效氯”是指与含氯消毒剂氧化能力相当的氯气的质量.某溶液中含有(消毒过程中NaClO被还原为NaCl),该溶液的“有效氯”是______g.
16.(11分)某化学课外兴趣小组用下图所示装置制取并完成有关性质的探究.
回答下列问题:
(1)装置A中用于滴加浓硫酸的仪器名称是______,发生反应的化学方程式为______.
(2)装置B中装有饱和溶液,可暂时储存气体,装置A加热一段时间后关闭止水夹K,B中出现的现象是______.
(3)若装置D中试剂为溶液,通入一段时间后出现淡黄色浑浊,则体现的______性(填“氧化”或“还原”).
(4)若装置D中试剂为溶液,某同学预测D中溶液由棕黄色变成浅绿色,依据是______(用离子方程式表示).
(5)若装置D中试剂为品红的水溶液,通入后溶液褪色;而更换为品红的乙醇溶液,通入干燥的后无明显现象.据此推测,使品红的水溶液褪色的微粒可能是______(填微粒符号).
(6)装置E的作用是______.
17.(4分)为测定某溶液的浓度,取待测液,向其中加入过量溶液.充分反应后过滤、洗涤并干燥,得到沉淀的质量为,反应的化学方程式为.求该溶液中的物质的量浓度(请写出计算过程).
漳州市2022-2023学年高一上学期期末教学质量检测
化学试题参考答案及评分标准
一、选择题(本题包括12小题,每小题4分,每小题只有一个正确答案,共48分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 A D A A B B C D A C D C
二、非选择题(本题包括5小题,共52分)
13.(11分)
(1)
(2)
(3)过滤 漏斗
(4)
14.(14分)
(1)HCl、HClO
(2)
(3)
(4)AB
(5)①8∶5
②
(6)
15.(12分)
(1)125
(2)500mL容量瓶 胶头滴管
(3)DBCA
(4)用玻璃棒进行引流
(5)BD
(6)71
16.(11分)
(1)分液漏斗
(2)B中液面下降,长颈漏斗下端导管液面上升
(3)氧化
(4)
(5)(或、均可)
(6)吸收多余的,防止其污染环境
17.(4分)
同课章节目录
