化学人教版(2019)必修第二册5.2.2 氮的氧化物(共24张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册5.2.2 氮的氧化物(共24张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 26.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-11 00:00:00 | ||
图片预览







文档简介
(共24张PPT)
第二节 氮及其化合物
氮的氧化物
氮的常见的化合价有
-3、+1、+2 、+3 、+4 、+5
其氧化物有N2O、NO、N2O3、NO2、N2O4、N2O5共有六种,它们都有毒,是大气污染物。
注意:
(1)这些氧化物中只有N2O3 、N2O5是酸性氧化物,其余均为不成盐氧化物。氮的氧化物都有毒。
(2)N2O俗称“笑气”,为无色有甜味的气体,广泛应用于医药麻醉、食品加工等生产生活领域。
N
1. 物理性质
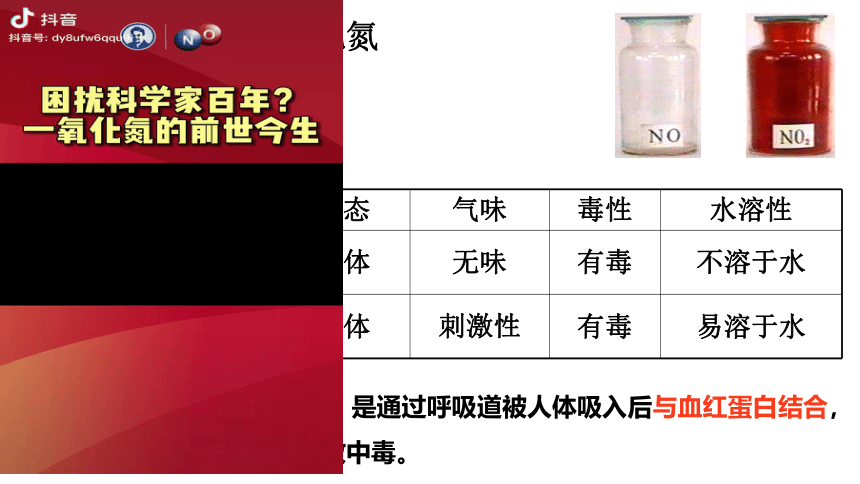
物质 颜色 状态 气味 毒性 水溶性
NO 无色 气体 无味 有毒 不溶于水
NO2 红棕色 气体 刺激性 有毒 易溶于水
一、一氧化氮和二氧化氮
NO中毒原理:与CO相似,是通过呼吸道被人体吸入后与血红蛋白结合,使其失去携带O2的能力,导致中毒。
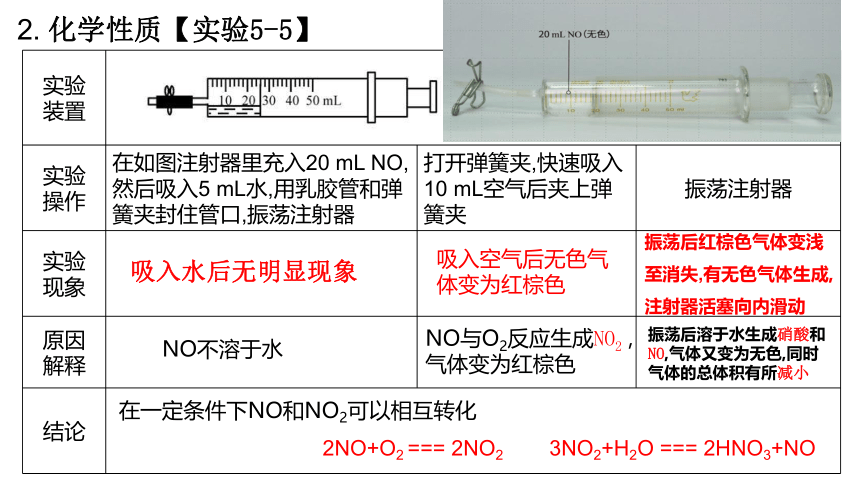
实验 装置
实验 操作 在如图注射器里充入20 mL NO,然后吸入5 mL水,用乳胶管和弹簧夹封住管口,振荡注射器 打开弹簧夹,快速吸入10 mL空气后夹上弹簧夹 振荡注射器
实验 现象
原因 解释
结论
2. 化学性质【实验5-5】
吸入水后无明显现象
吸入空气后无色气体变为红棕色
NO不溶于水
振荡后红棕色气体变浅至消失,有无色气体生成,注射器活塞向内滑动
NO与O2反应生成NO2 ,气体变为红棕色
振荡后溶于水生成硝酸和NO,气体又变为无色,同时气体的总体积有所减小
在一定条件下NO和NO2可以相互转化
2NO+O2 === 2NO2
3NO2+H2O === 2HNO3+NO
结论:
在一定条件下,NO与NO2可以相互转化
①NO→NO2:
2NO+O2====2NO2
②NO2→NO:
3NO2+H2O====2HNO3+NO
一氧化氮在常温下很容易与氧气化合,生成二氧化氮。二氧化氮溶于水时生成硝酸和一氧化氮,工业上利用这一原理生产硝酸。
(1) NO和NO2分别采用什么方法收集?
(2)NO2转化为NO的变化中,NO2只能作氧化剂吗
常温下NO能与O2反应,只能用排水法收集;NO2能与水反应生成NO,故只能用排空气法收集。
NO2与水反应转化为NO的同时生成HNO3, NO2既作氧化剂又作还原剂。
【思考与讨论P13】
NO 和 O2 混和气体溶于水的反应
2NO + O2 = 2NO2 ①
3NO2 + H2O = 2HNO3 + NO ②
① ×3 + ②×2 :
4NO + 3O2 + 2H2O = 4HNO3
NO2 和 O2 混和气体溶于水的反应
2NO + O2 = 2NO2 ②
3NO2 + H2O = 2HNO3 + NO ①
① ×2 + ② :
4NO2 + O2 + 2H2O = 4HNO3
性 质 NO NO2
物理性质
毒 性
与水反应
与氧气反应
实验室制备
收集方法
其他
对环境影响
无色、无味的有毒气体,难溶于水
红棕色、有刺激性气味的有毒气体
不反应(难溶于水)
3NO2+H2O====2HNO3+NO
2NO+O2====2NO2
不反应
铜与稀硝酸反应
铜与浓硝酸反应
常用排水法
常用向上排空气法
2NO2 N2O4
导致光化学烟雾和酸雨,破坏臭氧层
有毒(跟血红蛋白结合)
有毒
特别提示
①氮的氧化物都是大气污染物。
②空气中NO2是造成光化学烟雾的主要因素。
③空气中NO、NO2主要来源于煤和石油的燃烧、汽车尾气、硝酸工厂等。
④NO2:既有氧化性又有还原性,以氧化性为主。NO2能使湿润的淀粉 KI试纸变蓝
3. 氮氧化物对环境的污染与防治
(1)常见的污染类型
①光化学烟雾:NOx在紫外线作用下,与碳氢化合物
发生一系列光化学反应,产生了一种有毒的烟雾。
②酸雨:NOx排入大气中后,与水反应生成HNO3和
HNO2,随雨雪降到地面。
③破坏臭氧层:NO2可使平流层中的臭氧减少,导致
地面紫外线辐射量增加。
1、雾霾是指各种源排放的污染物(如SO2、NOx、NH3、 CO、VOCs、PM等),在特定的大气流场条件下,经过一系列物理化学变化过程形成的细粒子,并与水汽相互作用导致的大气消光现象。
2、PM2.5是指直径小于或者等于2.5微米的大气颗粒物的总称。雾霾成分有硫酸盐、硝酸盐、铵盐、有机物、炭黑 以及矿物粉尘等。
雾霾组成
汽车尾气的化学成分
汽车尾气所含污染物主要是: CO、碳氢化合物(CnHm) 、氮氧化合物(NO和NO2) 、SO2、颗粒物以及含铅化合物。
汽车尾气中NOx 的产生:
N2+O2 === 2NO
高温高压
2NO+O2= 2NO2
(2)常见的NOx尾气处理方法
①碱液吸收法
2NO2+2NaOH===NaNO3+NaNO2+H2O
NO2+NO+2NaOH===2NaNO2+H2O
NO2、NO的混合气体能被足量烧碱溶液完全吸收的条件是n(NO2)≥n(NO)。一般适合工业尾气中NOx处理。
②催化转化法
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体(N2)或NOx与CO在一定温度下催化转化为无毒气体(N2和CO2)。一般适用于汽车尾气的处理。
1.判断正误(正确的打“√”,错误的打“×”)
(1)由于NO极易与O2反应,且其密度与空气相差不多,因此收集NO只能用排水法( )
(2)由于NO2极易与水反应且密度比空气大,因此收集NO2只能用向上排空气法( )
(3)NO2易溶于水生成HNO3,故NO2是酸性氧化物( )
(4)N2与O2反应时,不论O2是否足量,其一步反应都只能得到NO,不能生成NO2( )
(5)NO和NO2都是有刺激性气味的有毒气体,它们都是大气污染物( )
(6)可用湿润的淀粉碘化钾试纸鉴别NO2与溴蒸气( )
√
√
√
×
×
×
(7)NO在空气中易转化为红棕色NO2。( )
(8)NO2与水的反应,NO2只作氧化剂。( )
(9)NO2是红棕色气体,Fe2O3是红棕色固体。( )
(10)NO2既有氧化性,又有还原性。( )
(11)NO和NO2的颜色、气味、水溶性不同,但它们都是有毒的气( )
(12)在实验室里,NO和NO2均用排水法收集。( )
√
√
√
√
×
×
2.NO2与水反应的化学方程式为3NO2+H2O === 2HNO3+NO,关于此反应的下列说法中正确的是( )
A.氮元素的化合价没有发生变化
B.NO2只是氧化剂
C.NO2只是还原剂
D.NO2既是氧化剂,又是还原剂
解析:NO2与H2O的反应中N的化合价既升高又降低,NO2既是氧化剂,又是还原剂。
D
3.下列对氮的氧化物的叙述中,正确的是( )
A.氮的氧化物都是无色气体
B.氮的氧化物都难溶于水
C.氮的氧化物都是酸性氧化物
D.氮的氧化物都是大气污染物
解析:NO2是红棕色,A不正确;NO2易溶于水,B不正确;NO不是酸性氧化物,C不正确;氮的氧化物均是大气污染物,D正确。
D
4.运载火箭的推进剂引燃后产生的气体主要是CO2、H2O、N2、NO,这些气体均为无色,但在卫星发射现场看到火箭喷出大量红色烟雾。产生红色烟雾的原因是( )
A.高温下N2遇空气生成NO2
B.NO遇空气生成NO2
C.CO2遇NO反应生成CO和NO2
D.NO和H2O反应生成H2和NO2
解析:根据火箭喷出的大量红色烟雾可推知其应是NO2,而高温下N2与O2不能生成NO2。
B
5.下列有关氮气的说法正确的是( )
A.氮气是由氮原子构成的双原子分子,所以化学性质不活泼
B. 1 mol N2可与3 mol H2完全反应生成2 mol NH3
C.电闪雷鸣的雨天,雨水中会含有一定量的硝酸,其中发生的反应之一是N2+2O2===2NO2
D.NO、NO2在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物
D
解析:A项,氮原子最外层5个电子,氮与氮形成三对共用电子对,达8电子的稳定结构;B项,氮气与氢气反应生成氨气是可逆反应;C项,氮气与氧气在放电的条件下生成一氧化氮;D项,NO和氧气能反应生成NO2,NO2和水反应生成NO。
6.下列关于NO、NO2性质的说法,正确的是
A.都是无色无味气体
B.都不溶于水
C.都可以用向上排空气法收集
D.NO2与水能够发生反应,而NO不能
D
解析:A.NO2为红棕色气体有刺激性气味,A错误;
B.二氧化氮与水生成硝酸和一氧化氮,B错误;
C.一氧化氮密度与空气接近、能与氧气反应,不能用向上排空气法收集,C错误;
D.NO2与水能够发生反应生成硝酸和一氧化氮,而NO不能,D正确。
7.下列关于NO2说法不正确的是
A.NO2是一种无色气体 B.NO2有刺激性气味
C.NO2易溶于水 D.NO2密度比空气大
A
解析:A.NO2是一种红棕色气体,故A错误;
B.NO2是一种红棕色有刺激性气味的气体,故B正确;
C.NO2易溶于水生成硝酸和NO,故C正确;
D.NO2相对分子质量大于29,所以密度比空气大,故D正确。
知识拓展——NO
计算机模拟的NO分子的图像
硝化甘油
— 百年历史的古老炸药和心脏病内服药
患有动脉硬化的病人,因血块堵住了动脉的血管,血肌供氧量的减少,引起胸部的疼痛,有时甚至导致心肌梗塞。服用硝化甘油,就是提供了NO,扩大了心肌血管,增大了血流量。
伊格纳罗博士和他的两位工作伙伴(芬奇戈特博士、穆拉博士)成功发现氧化氮(国内称一氧化氮)是一种可以传递信息的气体,它可以通过细胞薄膜(membrane),去调节另一细胞的功能;他们的发现,开创生物系统(biological systems)信息传递的新理论。正是这一重大发现和对氧化氮的研究使伊格纳罗博士获得1998年诺贝尔生物医学奖。
明星分子:NO
伊格纳罗
知识拓展——NO
第二节 氮及其化合物
氮的氧化物
氮的常见的化合价有
-3、+1、+2 、+3 、+4 、+5
其氧化物有N2O、NO、N2O3、NO2、N2O4、N2O5共有六种,它们都有毒,是大气污染物。
注意:
(1)这些氧化物中只有N2O3 、N2O5是酸性氧化物,其余均为不成盐氧化物。氮的氧化物都有毒。
(2)N2O俗称“笑气”,为无色有甜味的气体,广泛应用于医药麻醉、食品加工等生产生活领域。
N
1. 物理性质
物质 颜色 状态 气味 毒性 水溶性
NO 无色 气体 无味 有毒 不溶于水
NO2 红棕色 气体 刺激性 有毒 易溶于水
一、一氧化氮和二氧化氮
NO中毒原理:与CO相似,是通过呼吸道被人体吸入后与血红蛋白结合,使其失去携带O2的能力,导致中毒。
实验 装置
实验 操作 在如图注射器里充入20 mL NO,然后吸入5 mL水,用乳胶管和弹簧夹封住管口,振荡注射器 打开弹簧夹,快速吸入10 mL空气后夹上弹簧夹 振荡注射器
实验 现象
原因 解释
结论
2. 化学性质【实验5-5】
吸入水后无明显现象
吸入空气后无色气体变为红棕色
NO不溶于水
振荡后红棕色气体变浅至消失,有无色气体生成,注射器活塞向内滑动
NO与O2反应生成NO2 ,气体变为红棕色
振荡后溶于水生成硝酸和NO,气体又变为无色,同时气体的总体积有所减小
在一定条件下NO和NO2可以相互转化
2NO+O2 === 2NO2
3NO2+H2O === 2HNO3+NO
结论:
在一定条件下,NO与NO2可以相互转化
①NO→NO2:
2NO+O2====2NO2
②NO2→NO:
3NO2+H2O====2HNO3+NO
一氧化氮在常温下很容易与氧气化合,生成二氧化氮。二氧化氮溶于水时生成硝酸和一氧化氮,工业上利用这一原理生产硝酸。
(1) NO和NO2分别采用什么方法收集?
(2)NO2转化为NO的变化中,NO2只能作氧化剂吗
常温下NO能与O2反应,只能用排水法收集;NO2能与水反应生成NO,故只能用排空气法收集。
NO2与水反应转化为NO的同时生成HNO3, NO2既作氧化剂又作还原剂。
【思考与讨论P13】
NO 和 O2 混和气体溶于水的反应
2NO + O2 = 2NO2 ①
3NO2 + H2O = 2HNO3 + NO ②
① ×3 + ②×2 :
4NO + 3O2 + 2H2O = 4HNO3
NO2 和 O2 混和气体溶于水的反应
2NO + O2 = 2NO2 ②
3NO2 + H2O = 2HNO3 + NO ①
① ×2 + ② :
4NO2 + O2 + 2H2O = 4HNO3
性 质 NO NO2
物理性质
毒 性
与水反应
与氧气反应
实验室制备
收集方法
其他
对环境影响
无色、无味的有毒气体,难溶于水
红棕色、有刺激性气味的有毒气体
不反应(难溶于水)
3NO2+H2O====2HNO3+NO
2NO+O2====2NO2
不反应
铜与稀硝酸反应
铜与浓硝酸反应
常用排水法
常用向上排空气法
2NO2 N2O4
导致光化学烟雾和酸雨,破坏臭氧层
有毒(跟血红蛋白结合)
有毒
特别提示
①氮的氧化物都是大气污染物。
②空气中NO2是造成光化学烟雾的主要因素。
③空气中NO、NO2主要来源于煤和石油的燃烧、汽车尾气、硝酸工厂等。
④NO2:既有氧化性又有还原性,以氧化性为主。NO2能使湿润的淀粉 KI试纸变蓝
3. 氮氧化物对环境的污染与防治
(1)常见的污染类型
①光化学烟雾:NOx在紫外线作用下,与碳氢化合物
发生一系列光化学反应,产生了一种有毒的烟雾。
②酸雨:NOx排入大气中后,与水反应生成HNO3和
HNO2,随雨雪降到地面。
③破坏臭氧层:NO2可使平流层中的臭氧减少,导致
地面紫外线辐射量增加。
1、雾霾是指各种源排放的污染物(如SO2、NOx、NH3、 CO、VOCs、PM等),在特定的大气流场条件下,经过一系列物理化学变化过程形成的细粒子,并与水汽相互作用导致的大气消光现象。
2、PM2.5是指直径小于或者等于2.5微米的大气颗粒物的总称。雾霾成分有硫酸盐、硝酸盐、铵盐、有机物、炭黑 以及矿物粉尘等。
雾霾组成
汽车尾气的化学成分
汽车尾气所含污染物主要是: CO、碳氢化合物(CnHm) 、氮氧化合物(NO和NO2) 、SO2、颗粒物以及含铅化合物。
汽车尾气中NOx 的产生:
N2+O2 === 2NO
高温高压
2NO+O2= 2NO2
(2)常见的NOx尾气处理方法
①碱液吸收法
2NO2+2NaOH===NaNO3+NaNO2+H2O
NO2+NO+2NaOH===2NaNO2+H2O
NO2、NO的混合气体能被足量烧碱溶液完全吸收的条件是n(NO2)≥n(NO)。一般适合工业尾气中NOx处理。
②催化转化法
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体(N2)或NOx与CO在一定温度下催化转化为无毒气体(N2和CO2)。一般适用于汽车尾气的处理。
1.判断正误(正确的打“√”,错误的打“×”)
(1)由于NO极易与O2反应,且其密度与空气相差不多,因此收集NO只能用排水法( )
(2)由于NO2极易与水反应且密度比空气大,因此收集NO2只能用向上排空气法( )
(3)NO2易溶于水生成HNO3,故NO2是酸性氧化物( )
(4)N2与O2反应时,不论O2是否足量,其一步反应都只能得到NO,不能生成NO2( )
(5)NO和NO2都是有刺激性气味的有毒气体,它们都是大气污染物( )
(6)可用湿润的淀粉碘化钾试纸鉴别NO2与溴蒸气( )
√
√
√
×
×
×
(7)NO在空气中易转化为红棕色NO2。( )
(8)NO2与水的反应,NO2只作氧化剂。( )
(9)NO2是红棕色气体,Fe2O3是红棕色固体。( )
(10)NO2既有氧化性,又有还原性。( )
(11)NO和NO2的颜色、气味、水溶性不同,但它们都是有毒的气( )
(12)在实验室里,NO和NO2均用排水法收集。( )
√
√
√
√
×
×
2.NO2与水反应的化学方程式为3NO2+H2O === 2HNO3+NO,关于此反应的下列说法中正确的是( )
A.氮元素的化合价没有发生变化
B.NO2只是氧化剂
C.NO2只是还原剂
D.NO2既是氧化剂,又是还原剂
解析:NO2与H2O的反应中N的化合价既升高又降低,NO2既是氧化剂,又是还原剂。
D
3.下列对氮的氧化物的叙述中,正确的是( )
A.氮的氧化物都是无色气体
B.氮的氧化物都难溶于水
C.氮的氧化物都是酸性氧化物
D.氮的氧化物都是大气污染物
解析:NO2是红棕色,A不正确;NO2易溶于水,B不正确;NO不是酸性氧化物,C不正确;氮的氧化物均是大气污染物,D正确。
D
4.运载火箭的推进剂引燃后产生的气体主要是CO2、H2O、N2、NO,这些气体均为无色,但在卫星发射现场看到火箭喷出大量红色烟雾。产生红色烟雾的原因是( )
A.高温下N2遇空气生成NO2
B.NO遇空气生成NO2
C.CO2遇NO反应生成CO和NO2
D.NO和H2O反应生成H2和NO2
解析:根据火箭喷出的大量红色烟雾可推知其应是NO2,而高温下N2与O2不能生成NO2。
B
5.下列有关氮气的说法正确的是( )
A.氮气是由氮原子构成的双原子分子,所以化学性质不活泼
B. 1 mol N2可与3 mol H2完全反应生成2 mol NH3
C.电闪雷鸣的雨天,雨水中会含有一定量的硝酸,其中发生的反应之一是N2+2O2===2NO2
D.NO、NO2在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物
D
解析:A项,氮原子最外层5个电子,氮与氮形成三对共用电子对,达8电子的稳定结构;B项,氮气与氢气反应生成氨气是可逆反应;C项,氮气与氧气在放电的条件下生成一氧化氮;D项,NO和氧气能反应生成NO2,NO2和水反应生成NO。
6.下列关于NO、NO2性质的说法,正确的是
A.都是无色无味气体
B.都不溶于水
C.都可以用向上排空气法收集
D.NO2与水能够发生反应,而NO不能
D
解析:A.NO2为红棕色气体有刺激性气味,A错误;
B.二氧化氮与水生成硝酸和一氧化氮,B错误;
C.一氧化氮密度与空气接近、能与氧气反应,不能用向上排空气法收集,C错误;
D.NO2与水能够发生反应生成硝酸和一氧化氮,而NO不能,D正确。
7.下列关于NO2说法不正确的是
A.NO2是一种无色气体 B.NO2有刺激性气味
C.NO2易溶于水 D.NO2密度比空气大
A
解析:A.NO2是一种红棕色气体,故A错误;
B.NO2是一种红棕色有刺激性气味的气体,故B正确;
C.NO2易溶于水生成硝酸和NO,故C正确;
D.NO2相对分子质量大于29,所以密度比空气大,故D正确。
知识拓展——NO
计算机模拟的NO分子的图像
硝化甘油
— 百年历史的古老炸药和心脏病内服药
患有动脉硬化的病人,因血块堵住了动脉的血管,血肌供氧量的减少,引起胸部的疼痛,有时甚至导致心肌梗塞。服用硝化甘油,就是提供了NO,扩大了心肌血管,增大了血流量。
伊格纳罗博士和他的两位工作伙伴(芬奇戈特博士、穆拉博士)成功发现氧化氮(国内称一氧化氮)是一种可以传递信息的气体,它可以通过细胞薄膜(membrane),去调节另一细胞的功能;他们的发现,开创生物系统(biological systems)信息传递的新理论。正是这一重大发现和对氧化氮的研究使伊格纳罗博士获得1998年诺贝尔生物医学奖。
明星分子:NO
伊格纳罗
知识拓展——NO
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
