专题8 第二单元 第4课时 糖类 蛋白质和氨基酸 课件(共97张PPT)
文档属性
| 名称 | 专题8 第二单元 第4课时 糖类 蛋白质和氨基酸 课件(共97张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-10 00:00:00 | ||
图片预览








文档简介
(共97张PPT)
第4课时
DISIKESHI
糖类 / 蛋白质和氨基酸 / 随堂演练 知识落实 / 课时对点练
糖类 蛋白质和氨基酸
专题8
核心素养
发展目标
1.能从官能团的角度认识糖类、蛋白质、氨基酸的组成、结构和性质,培养宏观辨识与微观探析的能力。
2.掌握蛋白质的组成和主要性质,能设计实验探究蛋白质的性质,培养科学探究精神。
3.了解糖类、蛋白质在生产、生活中的应用,提高创新意识与社会责任。
内容索引
一、糖类
二、蛋白质和氨基酸
随堂演练 知识落实
课时对点练
糖类
一
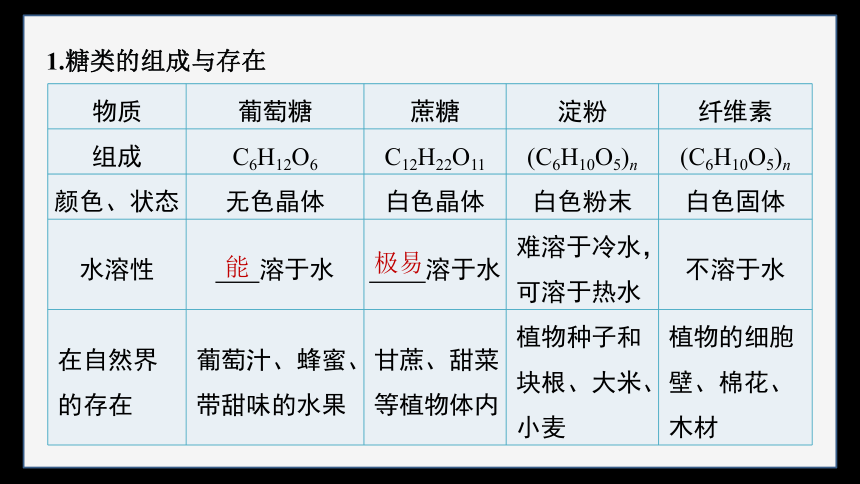
1.糖类的组成与存在
物质 葡萄糖 蔗糖 淀粉 纤维素
组成 C6H12O6 C12H22O11 (C6H10O5)n (C6H10O5)n
颜色、状态 无色晶体 白色晶体 白色粉末 白色固体
水溶性 溶于水 溶于水 难溶于冷水,可溶于热水 不溶于水
在自然界 的存在 葡萄汁、蜂蜜、带甜味的水果 甘蔗、甜菜等植物体内 植物种子和块根、大米、小麦 植物的细胞壁、棉花、木材
极易
能
特别提醒 从糖类的组成和原子数的比例来看,有些糖的组成符合Cn(H2O)m,如葡萄糖C6(H2O)6、蔗糖C12(H2O)11等,人们曾称糖类为碳水化合物;但有些糖不符合Cn(H2O)m,如脱氧核糖(C5H10O4),有些物质如乙酸(C2H4O2)符合Cn(H2O)m,但不属于糖。
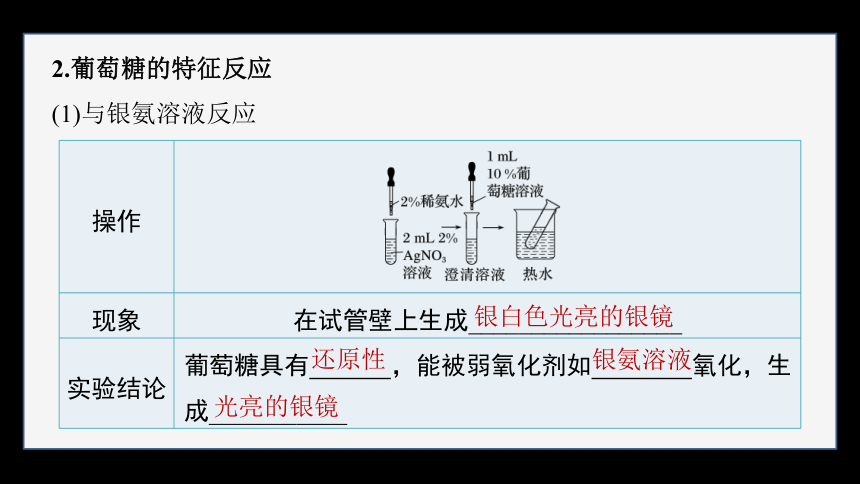
2.葡萄糖的特征反应
(1)与银氨溶液反应
操作
现象 在试管壁上生成_________________
实验结论 葡萄糖具有 ,能被弱氧化剂如 氧化,生成___________
银白色光亮的银镜
还原性
银氨溶液
光亮的银镜
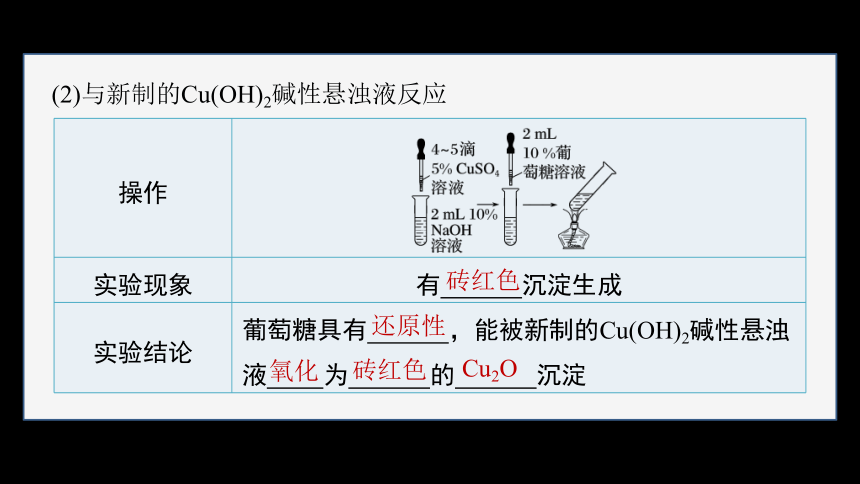
(2)与新制的Cu(OH)2碱性悬浊液反应
操作
实验现象 有 沉淀生成
实验结论 葡萄糖具有 ,能被新制的Cu(OH)2碱性悬浊液 为 的 沉淀
砖红色
还原性
氧化
砖红色
Cu2O
特别提醒 ①银氨溶液的配制:向AgNO3溶液中滴加氨水至生成的沉淀恰好完全溶解。②葡萄糖与新制的Cu(OH)2碱性悬浊液或银氨溶液反应均在碱性条件下进行。
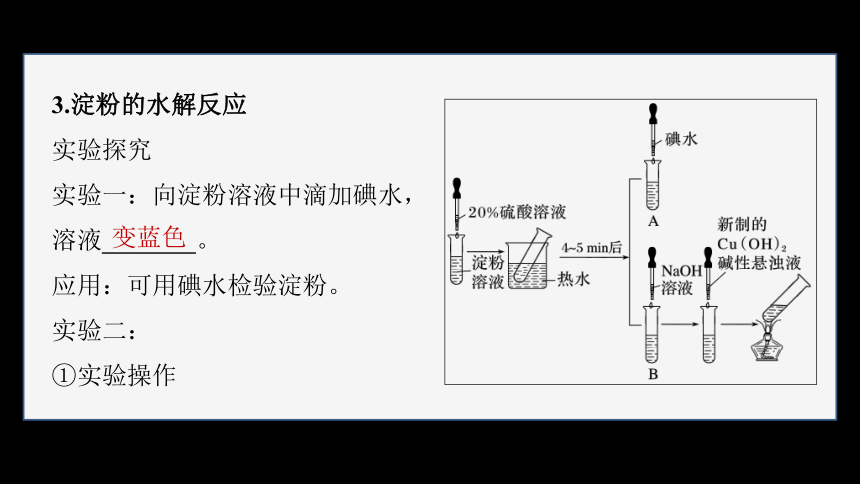
3.淀粉的水解反应
实验探究
实验一:向淀粉溶液中滴加碘水,
溶液 。
应用:可用碘水检验淀粉。
实验二:
①实验操作
变蓝色
②实验现象及结论
情况 现象A 现象B 结论
Ⅰ 溶液呈蓝色 未产生银镜 ______
Ⅱ 溶液呈蓝色 出现银镜 _________
Ⅲ 溶液不变蓝色 出现银镜 _________
未水解
部分水解
完全水解
③淀粉水解反应的化学方程式为
(C6H10O5)n+nH2O nC6H12O6
_______________________________。
淀粉 葡萄糖
4.糖类在生产、生活中的应用
(1)淀粉为人体提供能量
淀粉在淀粉酶的作用下,水解生成 , 在人体组织中缓慢氧化,放出热量,提供生命活动所需要的能量,反应的热化学方程式:_________________________________________________________。
(2)含淀粉的物质可以用来酿酒,富含纤维素的植物秸秆可以用来制造工业酒精。
葡萄糖转化为酒精的化学方程式为______________________________。
葡萄糖
葡萄糖
C6H12O6(s)+6O2(g)===6CO2(g)+6H2O(l) ΔH=-2 803 kJ·mol-1
C6H12O6 2C2H5OH+2CO2↑
(3)葡萄糖的银镜反应,或与新制的Cu(OH)2碱性悬浊液的反应可用于检验葡萄糖的存在,医学上曾用类似的反应来检验病人尿液中葡萄糖的含量是否偏高。
(1)糖类是有甜味的物质,有甜味的物质就是糖( )
(2)淀粉与纤维素的分子式相同,它们互为同分异构体( )
(3)葡萄糖分子式可表示为C6(H2O)6,则每1个葡萄糖分子中含有6个H2O( )
(4)可用新制的Cu(OH)2碱性悬浊液鉴别蔗糖和葡萄糖( )
(5)可以用KI溶液检验淀粉的存在( )
正误判断
×
×
×
×
√
深度思考
某同学设计了如下3个实验方案,用以检验淀粉的水解程度。
结论:淀粉未水解
深度思考
结论:淀粉部分水解
深度思考
题述三种方案操作是否正确?结论是否正确?说明理由。
甲__________________________________________________________
___________________________________________________________________。
乙__________________________________________________________
______________________________________________________________________________________________________________________。
甲方案操作正确,但结论错误。加入碘水溶液变蓝有两种情况:①淀粉完全没有水解;②淀粉部分水解。故不能得出淀粉尚未水解的结论
乙方案操作错误,结论也错误。应用稀碱溶液中和水解液中的稀硫酸,然后再做与新制的Cu(OH)2碱性悬浊液反应的实验。本方案中无砖红色沉淀产生,淀粉可能尚未水解,也可能完全水解或部分水解
丙__________________________。
丙方案操作正确,结论正确
淀粉已水解完全,则溶液中不再有淀粉存在,用碘水检验,溶液不会出现蓝色;淀粉尚未水解时,加入新制的Cu(OH)2碱性悬浊液煮沸,不会有砖红色沉淀产生。淀粉部分水解时,则既要用碘水检验有无淀粉的存在,又要用新制的Cu(OH)2碱性悬浊液检验有无葡萄糖的存在。
应用体验
1.大米、小麦、玉米等谷类食物中所含的营养物质主要是
A.淀粉 B.油脂 C.纤维素 D.水
√
谷类食物中所含的主要营养物质是淀粉,还含有少量的油脂、蛋白质、纤维素等。
2.某学生做葡萄糖的还原性实验将4 mL 0.5 mol·L-1的CuSO4溶液和 4 mL 0.5 mol·L-1的NaOH溶液混合后,向混合液中滴入1.0 mL 10%葡萄糖溶液,加热煮沸,结果没看到有砖红色沉淀生成。这是因为
A.葡萄糖浓度太大 B.加热时间不够
C.CuSO4溶液的量不够 D.NaOH溶液的量不够
√
葡萄糖与新制Cu(OH)2碱性悬浊液反应时,NaOH必须过量,题中n(CuSO4)=n(NaOH)=2×10-3 mol,NaOH的量不足,故看不到有砖红色沉淀生成。
3.通过实验来验证淀粉水解可生成葡萄糖,其实验包括下列操作过程,这些操作过程的正确排列顺序是
①取少量淀粉和水制成溶液 ②加热煮沸 ③加入碱液中和酸性 ④加入新制的Cu(OH)2碱性悬浊液 ⑤加入少量稀硫酸 ⑥水浴加热
A.①②⑤⑥④③ B.①⑤②④⑥③
C.①⑤⑥③④② D.①⑥④⑤③②
√
验证淀粉水解产物的实验主要有以下步骤:(1)在酸性条件下水浴加热使其水解,即①⑤⑥;
(2)加碱中和硫酸,即③;
(3)加入新制的Cu(OH)2碱性悬浊液并加热煮沸检验产物,即④②。
归纳总结
淀粉水解程度的检验
(1)实验步骤
归纳总结
(2)实验现象及结论
情况 现象A 现象B 结论
① 未出现银镜 溶液呈蓝色 淀粉未水解
② 出现银镜 溶液呈蓝色 淀粉部分水解
③ 出现银镜 溶液未呈蓝色 淀粉完全水解
返回
蛋白质和氨基酸
二
1.蛋白质的存在与组成
(1)存在
蛋白质广泛存在于生命体内,是组成 的基础物质。动物的 、____以及在人体新陈代谢中起催化作用的 、运输氧气的 、引起疾病的 和 、抵抗疾病的 中都含有蛋白质。
(2)组成
主要由 、 、 、 、硫等元素组成,是结构非常复杂的高分子化合物。
细胞
肌肉
毛皮
酶
血红蛋白
细菌
病毒
抗体
碳
氢
氧
氮
2.蛋白质的性质
按表中实验操作完成实验,并填写下表
实验操作 实验现象
蛋白质溶液 加饱和(NH4)2SO4溶液,再加蒸馏水 有 析出,加入蒸馏水____
_______
加稀硫酸,再加蒸馏水 有 析出,加入蒸馏水,___
_________
加CuSO4溶液,再加蒸馏水 有 析出,加入蒸馏水,___
_________
白色沉淀
沉淀
又溶解
白色沉淀
沉
淀不溶解
白色沉淀
沉
淀不溶解
蛋白质溶液 加甲醛溶液,再加蒸馏水 有 析出,加入蒸馏水,____
______
加热,再加蒸馏水 有 析出,加入蒸馏水,____
_______
白色沉淀
沉淀
不溶解
白色沉淀
沉淀
不溶解
(1)蛋白质的盐析
①概念:某些浓的无机盐溶液可使蛋白质的溶解度 而使其从溶液中 的过程叫盐析。
②条件:浓的轻金属盐溶液或铵盐溶液,如(NH4)2SO4溶液、Na2SO4溶液。少量的无机盐能促进蛋白质的溶解。
③特点:盐析是 过程,继续加水时,能使 , 蛋白质的生理活性。可用来分离、提纯蛋白质。
降低
析出
可逆
沉淀溶解
不影响
不可逆
(2)蛋白质的变性
①概念:在加热、强酸、强碱、重金属盐、紫外线、福尔马林(36%~40%甲醛溶液)的作用下,蛋白质原有的 或 会发生改变,其 也会随之改变,我们把这种变化称为蛋白质的变性。
②蛋白质的变性是 过程,可以利用这一性质进行杀菌消毒。
化学组成
空间结构
生理功能
不可逆
特别提醒 误食含重金属离子的溶液时,可喝生牛奶或蛋清救治。
(3)蛋白质的水解反应
氨基酸
②几种常见的氨基酸
甘氨酸(氨基乙酸):_____________;
丙氨酸(α-氨基丙酸):________________;
谷氨酸(α-氨基戊二酸):____________________________。
氨基酸分子中均含有 和 两种官能团,氨基连接在离 的氨基酸为α-氨基酸。
羧基(—COOH)
氨基(—NH2)
羧基最近的碳原子上
③氨基酸的化学性质
碱
酸
酸
碱
多肽
蛋白质
(4)蛋白质的特征反应
3.酶
(1)酶是一种具有 的物质。
(2)绝大多数酶是 。
(3)酶催化作用的特征
①专一性;②高效性;③条件温和。
催化作用
蛋白质
(1)蛋白质都是结构复杂的高分子化合物,组成元素只有C、H、O、N( )
正误判断
×
(2)蛋白质在酶的作用下,可直接水解生成各种氨基酸( )
正误判断
提示 蛋白质水解先生成多肽,多肽进一步水解,最终生成氨基酸。
×
(3)蛋白质溶液遇到盐就会变性( )
(4)蛋白质变性属于化学变化( )
正误判断
×
√
(5)向鸡蛋白溶液中加入醋酸铅溶液,生成白色沉淀,加水可重新溶解( )
正误判断
提示 加入重金属盐,蛋白质发生变性,加水沉淀也不会溶解。
×
(6)可以通过灼烧的方法鉴别真蚕丝和人造丝( )
正误判断
提示 真蚕丝灼烧有烧焦羽毛气味,而人造丝没有。
√
1.硝酸可以使蛋白质变黄,称为蛋白质的颜色反应。此“颜色反应”与钠元素的“焰色反应”有何区别?
提示 颜色反应是指某些蛋白质的黄蛋白反应,属于化学变化;而焰色反应是指钠、钾等多种金属元素被灼烧时火焰呈现的颜色,属于物理变化。
深度思考
2.为了检验过氧化氢分解酶的作用,在室温下进行如下实验:
(1)在试管A中加入3%的双氧水3 mL,再加入二氧化锰0.5 g,有气体产生。
(2)在试管B中加入3%的双氧水3 mL,再加入新鲜的鸡肝片1 g,有气体产生。
(3)在试管C中加入3%的双氧水3 mL,再加入煮熟的鸡肝片1 g,无气体产生。
(4)在试管D中加入3%的双氧水2 mL和10%的盐酸1 mL,再加入新鲜的鸡肝片1 g,无气体产生。
(5)在试管E中加入3%的双氧水2 mL和10%的氢氧化钠溶液1 mL,再加入新鲜的鸡肝片1 g,无气体产生。
通过以上实验,你能得出什么结论?
深度思考
深度思考
提示 通过以上实验可得出:
(1)MnO2和新鲜的鸡肝片都能催化过氧化氢的分解。
(2)煮熟的鸡肝片不能催化过氧化氢的分解。
(3)在较强的酸性、碱性条件下,新鲜的鸡肝片不能催化过氧化氢的分解。由此可知:新鲜鸡肝片中的过氧化氢酶在加热、强酸、强碱条件下发生变性,失去催化作用。
应用体验
1.下列关于蛋白质的叙述正确的是
A.向蛋白质溶液中分别加入NaCl溶液、CuSO4溶液,其过程均是不可逆的
B.重金属盐使蛋白质分子变性,但是吞“钡餐”(主要成分是硫酸钡)不
会引起中毒
C.温度越高,酶对某些生化反应的催化效率就越高
D.医疗上用75%的酒精杀菌消毒,是利用了酒精可以使蛋白质盐析的性质
√
向蛋白质溶液中加入NaCl溶液发生盐析,其过程是可逆的,A错误;
重金属盐使蛋白质分子变性,但是吞“钡餐”(主要成分是硫酸钡)不会引起中毒,因为硫酸钡既不溶于水也不溶于酸,且不容易被X射线透过,在医疗上可用作检查肠胃的内服药剂,B正确;
酶的活性受温度限制,超过适宜的温度时酶将失去活性,C错误;
医疗上用体积分数为75%的酒精杀菌消毒,是利用了酒精可以使蛋白质变性的性质,D错误。
2.下列关于氨基酸的说法,正确的是
①蛋白质在一定条件下能发生水解反应,最终转化为各种氨基酸
②氨基酸分子既能与酸反应,又能与碱反应
③α-氨基酸中氨基连在离羧基最近的碳原子上
④氨基酸之间在一定条件下能发生反应,生成多肽
A.只有①② B.只有①②③
C.只有①②④ D.①②③④
√
3.(1)鸡蛋清水解的最终产物是________。请以甘氨酸( )为例,
写出其与NaOH溶液反应的化学方程式:_______________________
________________。
氨基酸
蛋白质水解的最终产物是氨基酸。
+NaOH―→
+H2O
(2)市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服上的汗渍、血液及人体排放的蛋白质油渍遇到它,皆能水解除去。下列衣料中不能用加酶洗衣粉洗涤的是______
(填序号)。
①棉织品 ②毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥锦纶织品
根据题意知加酶洗衣粉能使蛋白质水解,所以含有蛋白质的衣服不能用加酶洗衣粉清洗。毛织品和蚕丝织品的主要成分是蛋白质。
②④
归纳总结
蛋白质的盐析与变性的区别
盐析 变性
含义 蛋白质在某些盐的浓溶液中因溶解度降低而析出 蛋白质在加热、酸、碱等条件下性质发生改变而聚沉
条件 轻金属盐和铵盐 紫外线照射、加热或加入某些有机化合物(甲醛、酒精)、强酸、强碱、重金属盐(如铅盐、铜盐、汞盐)等
归纳总结
特征 可逆过程,不改变蛋白质的性质和生理活性 不可逆过程,蛋白质失去生理活性
实质 溶解度降低,物理变化 结构、性质改变,化学变化
用途 分离、提纯蛋白质 杀菌消毒
返回
随堂演练 知识落实
1.葡萄糖(C6H12O6)是一种重要的营养物质,下列关于葡萄糖的说法正确的是
A.葡萄糖是一种单糖
B.葡萄糖分子中有6个碳原子、6个水分子
C.常温下,葡萄糖可与新制的氢氧化铜碱性悬浊液反应
D.1 mol葡萄糖完全燃烧需要9 mol氧气
√
1
2
3
4
1
2
3
4
葡萄糖分子中氢、氧原子个数比为2∶1,但不是以水分子的形式存在,B项错误;
葡萄糖和新制的氢氧化铜碱性悬浊液反应必须加热,C项错误;
葡萄糖的分子式可改写为C6(H2O)6,由此可判断1 mol 葡萄糖完全燃烧需要消耗6 mol氧气,D项错误。
2.中国酒文化源远流长,很多地方至今仍用传统工艺来制作米酒。家酿米酒的转化过程为
A.淀粉→蔗糖→葡萄糖→酒
B.淀粉→麦芽糖→葡萄糖→酒
C.淀粉→麦芽糖→果糖→酒
D.淀粉→蔗糖→果糖→酒
√
1
2
3
4
3.(2022·成都龙泉驿区教育科学研究院高一期中)下列实例利用了蛋白质变性原理的是
①利用过氧乙酸对环境、物品进行消毒 ②利用高温、紫外线对医疗器械进行消毒 ③蒸煮鸡蛋食用 ④松花蛋的腌制 ⑤用牛奶灌服重金属中毒的病人
A.①②③④⑤ B.①②③④
C.①②③ D.①②
√
1
2
3
4
1
2
3
4
过氧乙酸有强氧化性,能使蛋白质变性,故①正确;
高温、紫外线均能使蛋白质变性,故②正确;
加热能使蛋白质变性,故③正确;
碱能使蛋白质变性,用石灰腌制松花蛋便于保存和食用,故④正确;
重金属盐中毒的原理是其破坏了人体的蛋白质结构,牛奶的主要成分是蛋白质,服用牛奶,可防止人体本身的蛋白质被破坏,能用于解毒,故⑤正确。
4.成熟的苹果中含有淀粉、葡萄糖和无机盐等,某课外兴趣小组设计了一组实验证明某些成分的存在,请你参与并协助他们完成相关实验。
(1)用小试管取少量的苹果汁,加入______(填名称),溶液变蓝,则证明苹果中含有淀粉。
1
2
3
4
碘水
苹果中含有淀粉,淀粉遇碘单质变蓝,向苹果汁中加入碘水,溶液变蓝,则证明苹果中含有淀粉。
1
2
3
4
(2)利用含淀粉的物质可以生产醋酸。下面是生产醋酸的流程图,试回答下列问题:
B是日常生活中有特殊香味的常见有机物,在有些饮料中含有B。
①写出下列反应的化学方程式,并注明反应类型。
B与醋酸反应:________________________________________________,
属于____________反应。
B→C:______________________________________,属_____反应。
取代(或酯化)
氧化
1
2
3
4
1
2
3
4
②可用于检验A的试剂是________________________________________
_____。
新制的氢氧化铜碱性悬浊液(其他合理答案
均可)
葡萄糖中含有醛基,检验葡萄糖可用新制的氢氧化铜碱性悬浊液(或银氨溶液),加热后若生成砖红色沉淀(或水浴加热出现光亮的银镜),则说明为葡萄糖。
返回
课时对点练
题组一 糖类
1.下列关于糖类的叙述正确的是
A.含有C、H、O三种元素的有机物叫糖类
B.糖类物质均能与银氨溶液在加热时反应生成银镜
C.糖类物质都有甜味
D.糖类物质是绿色植物光合作用的产物,是动、植物所需能量的重要
来源
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
含有C、H、O三种元素的有机物很多,如CH3CH2OH、CH3COOH、CH3COOCH2CH3等,故A错误;
分子结构中含有—CHO的糖类分子才能发生银镜反应,故B错误;
并不是所有的糖类都有甜味,如淀粉、纤维素,故C错误。
2.糯米中含大量淀粉,下列有关说法正确的是
A.淀粉能与银氨溶液反应产生银镜
B.淀粉是否水解完全可以用碘水来检验
C.淀粉在碱性条件下能水解生成葡萄糖
D.糖尿病病人不宜吃粽子,因为糯米中含大量的葡萄糖会使血糖升高
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
淀粉属于高分子化合物,不能与银氨溶液反应产生银镜,A错误;
淀粉是否水解完全可以用碘水来检验,若溶液变蓝,则淀粉未水解或水解不完全,反之水解完全,B正确;
淀粉在酸或酶的催化作用下能水解生成葡萄糖,但在碱性条件下不能水解,C错误;
糖尿病病人不宜吃粽子,是因为糯米中含大量的淀粉,淀粉水解能生成葡萄糖,会使血糖升高,D错误。
3.(2022·合肥一中高一检测)下列关于检验某病人尿糖的做法正确的是
A.取尿样,加入新制的Cu(OH)2碱性悬浊液,观察发生的现象
B.取尿样,加入过量稀H2SO4,再加入新制的Cu(OH)2碱性悬浊液,
观察发生的现象
C.取尿样,加入新制的Cu(OH)2碱性悬浊液,煮沸,观察发生的现象
D.取尿样,加入Cu(OH)2固体,煮沸,观察发生的现象
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
葡萄糖的检验需在碱性条件下与新制的Cu(OH)2悬浊液或银氨溶液共热而完成。
4.2020年新疆棉花总产量达516.1万吨,占全国棉花总产量的87.3%,约占世界棉花产量的20%以上。棉花中的纤维素占比87%~90%,纤维素的化学式为(C6H10O5)n,下列关于纤维素说法正确的是
A.纤维素属于有机物
B.纤维素中碳、氢元素质量比为3∶5
C.纤维素是由碳、氢、氧三种原子构成的
D.纤维素的相对分子质量为162
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
纤维素是含碳元素的化合物,属于有机物,A正确;
纤维素中碳、氢元素质量比为(12×6)∶10=36∶5,B错误;
纤维素是由碳、氢、氧三种元素组成的,C错误;
纤维素的相对分子质量为12×6n+10n+16×5n=162n,D错误。
5.以玉米(主要成分是淀粉)为原料制备乙醇的流程如图:
下列说法不正确的是
A.C12H22O11属于二糖
B.1 mol葡萄糖可分解成3 mol乙醇
C.葡萄糖不能进一步水解
D.不能用分液操作分离乙醇和水
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
由流程图可知,玉米中淀粉在酸性条件下水解得到C12H22O11,C12H22O11在酸性条件下继续水解得到葡萄糖,葡萄糖在酒化酶的作用下转化为乙醇。淀粉在酸性条件下水解生成的C12H22O11属于二糖,A正确;
乙醇和水互溶,不可用分液操作分离,D正确。
6.某学生设计了如下实验方案用以检验淀粉水解的情况:
下列结论正确的是
A.淀粉尚有部分未水解
B.淀粉已完全水解
C.淀粉没有水解
D.淀粉已发生水解,但不知是否完全水解
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
因为混合液呈碱性,所以加碘水溶液不变蓝,不能说明溶液中不含淀粉;而加入新制的Cu(OH)2碱性悬浊液加热煮沸生成砖红色沉淀,说明其中含有葡萄糖,故结论应为淀粉已水解,但不知是否完全水解。
题组二 蛋白质和氨基酸
7.某期刊封面上有如图所示的一个分子的球棍模型,图中“棍”代表单键、双键或三键。不同颜色的“球”代表不同元素的原子,该模型图可代表的物质是
A.葡萄糖
B.酯
C.氨基酸
D.乙醇钠
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
由分子的球棍模型图,结合原子结构可知,白球代表H,蓝球代表N,绿球代表C,红球代表O。故该模型图表示的分子是H2NCH2COOH,即甘氨酸,甘氨酸是一种重要的氨基酸,故C符合题意。
8.下列有关蛋白质的性质描述说法错误的是
A.棉被和蚕丝被的主要材质均为高分子
B.从牛奶中可以提取酪素,用来制作塑料
C.消毒过程中细菌蛋白质发生了水解
D.在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会产生沉淀,
但原理不同
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
棉被和蚕丝被的主要材质分别是纤维素、蛋白质,二者均为高分子,A正确;
酪素由酪蛋白水解得到,故从牛奶中可以提取酪素,用来制作塑料,B正确;
消毒过程中细菌蛋白质发生了变性,C错误;
鸡蛋清中加入饱和Na2SO4溶液使蛋白质的溶解性降低而析出,加入CuSO4溶液使蛋白质发生变性而析出,原理不同,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
9.2018年诺贝尔化学奖获得者为弗朗西斯·阿诺德(Frances H·Amold)、乔治·史密斯(George P·Smith)及格雷戈里·温特(Gregory P·Winter)爵士。上述三位化学奖得主成功利用基因变化和选择研究出可以解决人类化学问题的蛋白质。下列关于蛋白质的组成与性质的叙述正确的是
A.蛋白质在酶的作用下水解的最终产物为氨基酸
B.向蛋白质溶液中加入CuSO4、Na2SO4浓溶液,均会使其变性
C.天然蛋白质仅由碳、氢、氧、氮四种元素组成
D.蛋白质、纤维素、油脂都是高分子化合物
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
蛋白质水解的最终产物为氨基酸,A正确;
CuSO4为重金属盐,能使蛋白质发生变性,Na2SO4浓溶液不能使蛋白质发生变性,B错误;
天然蛋白质除含C、H、O、N四种元素外还含有P、S等元素,C错误;
油脂不是高分子化合物,D错误。
10.下列关于酶的叙述中,不正确的是
A.酶是糖类物质
B.大多数酶是蛋白质
C.酶是生物体内产生的催化剂
D.酶受到高温或重金属盐作用时会变性
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
大多数酶是蛋白质,而不是糖类物质,A错误、B正确;
酶是生物体内产生的催化剂,其催化作用具有条件温和、不需要加热、高度专一、催化效率高等特点,C正确;
酶具有蛋白质的性质,当受到高温或重金属盐作用时会变性,D正确。
11.(2022·深圳高一月考)生命在于运动,而生命活动的维持离不开能量,糖类、油脂、蛋白质是基本营养物质。下列说法正确的是
A.糖类、油脂、蛋白质都能发生水解反应
B.糖尿病病人食用的“无糖饼干”主要成分为面粉,不含糖类物质
C.我国新冠疫苗安全有效,助力全球抗疫,疫苗无需经冷链运输
D.豆腐是我国古代劳动人民智慧的结晶,蛋白质在人体内水解的最终
产物为氨基酸
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
糖类有多种,例如葡萄糖等单糖不能发生水解,A错误;
面粉的主要成分为淀粉,淀粉属于糖类物质,B错误;
疫苗的主要成分为蛋白质,温度过高蛋白质易变性,应冷链运输,C错误;
豆腐的主要成分为蛋白质,在人体内经蛋白酶催化水解为氨基酸,D正确。
12.下列与化学有关的文献或诗文,理解正确的是
A.《问刘十九》中写道:“绿蚁新醅酒,红泥小火炉”,“新醅酒”即新酿
的酒,在酿酒的过程中,葡萄糖发生了水解反应
B.“独忆飞絮鹅毛下,非复青丝马尾垂”中的“飞絮”和棉花的化学成分不同
C.《天工开物》中有如下描述:“世间丝、麻、裘、褐皆具素质,而使殊颜
异色得以尚焉……”文中的“麻”“裘”在一定条件下都可以水解生成
小分子
D.《傅鹑觚集·太子少傅箴》中记载:“故近朱者赤,近墨者黑。”这里的
“朱”指的是朱砂,它是古代常用的一种红色颜料,其主要成分为Fe2O3
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
葡萄糖为单糖,不能水解,故A错误;
飞絮和棉花的化学成分都是纤维素,故B错误;
“麻”的主要成分为纤维素,“裘”的主要成分为蛋白质,都可以水解生成小分子,故C正确;
朱砂是古代常用的一种红色颜料,其主要成分是HgS,故D错误。
13.下列有关蛋白质的叙述中,不正确的是
A.蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解
B.人工合成的具有生命活性的蛋白质——结晶牛胰岛素,是1965年我
国科学家最先合成的
C.重金属盐能使蛋白质变性,所以误食重金属盐会中毒
D.浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生
颜色反应
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,为蛋白质的盐析过程,蛋白质盐析可逆,再加水会溶解,A错误;
结晶牛胰岛素是我国科学家于1965年首次合成的,属于蛋白质,B正确;
浓硝酸与部分天然蛋白质会发生颜色反应,所以浓硝酸溅在皮肤上,使皮肤呈黄色,D正确。
14.近期,英国科学家通过研究人类脑部疾病的样本,发现人脑中一种名为“突触后致密区”(PSD)的神经组织含有1 461种蛋白,该组织病变会导致痴呆等130多种脑部疾病,最新研究有望为科学家治疗脑病指明方向。下列关于蛋白质叙述正确的是
A.天然蛋白质水解的最终产物都是氨基酸
B.在蛋白质溶液中滴加饱和硫酸铵溶液可以使蛋白质变性
C.在蛋白质溶液中加入福尔马林(36%~40%甲醛溶液)产生沉淀,再加
入大量水,沉淀又溶解
D.通过盐析作用析出的蛋白质不再溶于水
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
15.应用所学知识回答下列问题:
(1)下列物质对蛋白质的化学性质具有明显影响的是________(填字母,下同)。
A.重晶石(BaSO4) B.蓝矾 C.碘酒 D.高锰酸钾 E.酒精 F.生牛奶 G.熟鸡蛋
蓝矾、碘酒、高锰酸钾、酒精等物质都能使蛋白质变性,蛋白质的变性属于化学变化。重晶石的主要成分是硫酸钡,它既不溶于水又不溶于酸,不能使蛋白质变性,对人体无毒。
BCDE
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
A.重晶石(BaSO4) B.蓝矾 C.碘酒 D.高锰酸钾 E.酒精 F.生牛奶 G.熟鸡蛋
(2)如果你发现有人误服重金属盐而出现了轻微中毒症状,需要你马上对病人进行抢救,你认为上述物质中可以应用的是_____。
生牛奶中含有较多的未变性的蛋白质,熟鸡蛋中蛋白质已经变性了。
F
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(3)当你选择物质对病人进行抢救以后,下一步的打算或做法是______。
A.建议病人尽快去医院继续治疗
B.将病人安置于通风处呼吸新鲜的空气
C.建议病人卧床休息
重金属盐中毒者服用生牛奶能降低重金属盐对人体的伤害,但这种作用是有限的。病人去医院做更有效的治疗是最佳选择。
A
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
16.鸡蛋中含有丰富的蛋白质,鸡蛋清就是一种蛋白质,它的分子直径为1~100 nm,具有某些胶体的性质。取新鲜鸡蛋的鸡蛋清溶于水制成水溶液,分装于试管中,分别进行如下实验,回答下列问题:
(1)向试管里缓慢地加入饱和的硫酸铵溶液,观察到的现象是________
____;再向试管里加入足量的蒸馏水,观察到的现象是_________。
有沉淀
析出
沉淀溶解
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
硫酸铵能够使蛋白质发生盐析,降低蛋白质的溶解度,使其以沉淀形式析出,该过程发生了物理变化,所得沉淀和原蛋白质的性质相同,所以加入足量的蒸馏水,沉淀又会溶解,是一个可逆过程。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(2)向试管里缓慢地加入硫酸铜溶液,观察到的现象是___________;再向试管里加入足量的蒸馏水,观察到的现象是___________。
有沉淀析出
沉淀不溶解
硫酸铜属于重金属盐,它能够使蛋白质发生变性,从而析出沉淀,该过程发生了化学变化,所得沉淀和原蛋白质的性质不同,所以加入足量的蒸馏水,沉淀不会溶解,是一个不可逆过程。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(3)已知蛋白质遇到浓硝酸会变黄,这个反应可以用来鉴别某些带有苯环的蛋白质。把10 mL鸡蛋清溶液和5 mL NaCl溶液的混合液体,加入用
半透膜(一种有微孔的膜,小分子或离子可以透过,胶体粒子不能透过)制成的袋内,将此袋浸入盛蒸馏水的烧杯中(如图)。2 min后,取烧杯中的液体分别进行实验。
①加入AgNO3溶液,产生的现象是________________。
有白色沉淀析出
②加入浓硝酸,产生的现象是____________。
无明显现象
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
胶体微粒不能透过半透膜,而小分子或离子能够透过半透膜,所以烧杯中含有NaCl溶液而不含鸡蛋清溶液,加入AgNO3溶液会产生AgCl白色沉淀,加入浓硝酸不会变黄。
返回
本课结束
专题8
第4课时
DISIKESHI
糖类 / 蛋白质和氨基酸 / 随堂演练 知识落实 / 课时对点练
糖类 蛋白质和氨基酸
专题8
核心素养
发展目标
1.能从官能团的角度认识糖类、蛋白质、氨基酸的组成、结构和性质,培养宏观辨识与微观探析的能力。
2.掌握蛋白质的组成和主要性质,能设计实验探究蛋白质的性质,培养科学探究精神。
3.了解糖类、蛋白质在生产、生活中的应用,提高创新意识与社会责任。
内容索引
一、糖类
二、蛋白质和氨基酸
随堂演练 知识落实
课时对点练
糖类
一
1.糖类的组成与存在
物质 葡萄糖 蔗糖 淀粉 纤维素
组成 C6H12O6 C12H22O11 (C6H10O5)n (C6H10O5)n
颜色、状态 无色晶体 白色晶体 白色粉末 白色固体
水溶性 溶于水 溶于水 难溶于冷水,可溶于热水 不溶于水
在自然界 的存在 葡萄汁、蜂蜜、带甜味的水果 甘蔗、甜菜等植物体内 植物种子和块根、大米、小麦 植物的细胞壁、棉花、木材
极易
能
特别提醒 从糖类的组成和原子数的比例来看,有些糖的组成符合Cn(H2O)m,如葡萄糖C6(H2O)6、蔗糖C12(H2O)11等,人们曾称糖类为碳水化合物;但有些糖不符合Cn(H2O)m,如脱氧核糖(C5H10O4),有些物质如乙酸(C2H4O2)符合Cn(H2O)m,但不属于糖。
2.葡萄糖的特征反应
(1)与银氨溶液反应
操作
现象 在试管壁上生成_________________
实验结论 葡萄糖具有 ,能被弱氧化剂如 氧化,生成___________
银白色光亮的银镜
还原性
银氨溶液
光亮的银镜
(2)与新制的Cu(OH)2碱性悬浊液反应
操作
实验现象 有 沉淀生成
实验结论 葡萄糖具有 ,能被新制的Cu(OH)2碱性悬浊液 为 的 沉淀
砖红色
还原性
氧化
砖红色
Cu2O
特别提醒 ①银氨溶液的配制:向AgNO3溶液中滴加氨水至生成的沉淀恰好完全溶解。②葡萄糖与新制的Cu(OH)2碱性悬浊液或银氨溶液反应均在碱性条件下进行。
3.淀粉的水解反应
实验探究
实验一:向淀粉溶液中滴加碘水,
溶液 。
应用:可用碘水检验淀粉。
实验二:
①实验操作
变蓝色
②实验现象及结论
情况 现象A 现象B 结论
Ⅰ 溶液呈蓝色 未产生银镜 ______
Ⅱ 溶液呈蓝色 出现银镜 _________
Ⅲ 溶液不变蓝色 出现银镜 _________
未水解
部分水解
完全水解
③淀粉水解反应的化学方程式为
(C6H10O5)n+nH2O nC6H12O6
_______________________________。
淀粉 葡萄糖
4.糖类在生产、生活中的应用
(1)淀粉为人体提供能量
淀粉在淀粉酶的作用下,水解生成 , 在人体组织中缓慢氧化,放出热量,提供生命活动所需要的能量,反应的热化学方程式:_________________________________________________________。
(2)含淀粉的物质可以用来酿酒,富含纤维素的植物秸秆可以用来制造工业酒精。
葡萄糖转化为酒精的化学方程式为______________________________。
葡萄糖
葡萄糖
C6H12O6(s)+6O2(g)===6CO2(g)+6H2O(l) ΔH=-2 803 kJ·mol-1
C6H12O6 2C2H5OH+2CO2↑
(3)葡萄糖的银镜反应,或与新制的Cu(OH)2碱性悬浊液的反应可用于检验葡萄糖的存在,医学上曾用类似的反应来检验病人尿液中葡萄糖的含量是否偏高。
(1)糖类是有甜味的物质,有甜味的物质就是糖( )
(2)淀粉与纤维素的分子式相同,它们互为同分异构体( )
(3)葡萄糖分子式可表示为C6(H2O)6,则每1个葡萄糖分子中含有6个H2O( )
(4)可用新制的Cu(OH)2碱性悬浊液鉴别蔗糖和葡萄糖( )
(5)可以用KI溶液检验淀粉的存在( )
正误判断
×
×
×
×
√
深度思考
某同学设计了如下3个实验方案,用以检验淀粉的水解程度。
结论:淀粉未水解
深度思考
结论:淀粉部分水解
深度思考
题述三种方案操作是否正确?结论是否正确?说明理由。
甲__________________________________________________________
___________________________________________________________________。
乙__________________________________________________________
______________________________________________________________________________________________________________________。
甲方案操作正确,但结论错误。加入碘水溶液变蓝有两种情况:①淀粉完全没有水解;②淀粉部分水解。故不能得出淀粉尚未水解的结论
乙方案操作错误,结论也错误。应用稀碱溶液中和水解液中的稀硫酸,然后再做与新制的Cu(OH)2碱性悬浊液反应的实验。本方案中无砖红色沉淀产生,淀粉可能尚未水解,也可能完全水解或部分水解
丙__________________________。
丙方案操作正确,结论正确
淀粉已水解完全,则溶液中不再有淀粉存在,用碘水检验,溶液不会出现蓝色;淀粉尚未水解时,加入新制的Cu(OH)2碱性悬浊液煮沸,不会有砖红色沉淀产生。淀粉部分水解时,则既要用碘水检验有无淀粉的存在,又要用新制的Cu(OH)2碱性悬浊液检验有无葡萄糖的存在。
应用体验
1.大米、小麦、玉米等谷类食物中所含的营养物质主要是
A.淀粉 B.油脂 C.纤维素 D.水
√
谷类食物中所含的主要营养物质是淀粉,还含有少量的油脂、蛋白质、纤维素等。
2.某学生做葡萄糖的还原性实验将4 mL 0.5 mol·L-1的CuSO4溶液和 4 mL 0.5 mol·L-1的NaOH溶液混合后,向混合液中滴入1.0 mL 10%葡萄糖溶液,加热煮沸,结果没看到有砖红色沉淀生成。这是因为
A.葡萄糖浓度太大 B.加热时间不够
C.CuSO4溶液的量不够 D.NaOH溶液的量不够
√
葡萄糖与新制Cu(OH)2碱性悬浊液反应时,NaOH必须过量,题中n(CuSO4)=n(NaOH)=2×10-3 mol,NaOH的量不足,故看不到有砖红色沉淀生成。
3.通过实验来验证淀粉水解可生成葡萄糖,其实验包括下列操作过程,这些操作过程的正确排列顺序是
①取少量淀粉和水制成溶液 ②加热煮沸 ③加入碱液中和酸性 ④加入新制的Cu(OH)2碱性悬浊液 ⑤加入少量稀硫酸 ⑥水浴加热
A.①②⑤⑥④③ B.①⑤②④⑥③
C.①⑤⑥③④② D.①⑥④⑤③②
√
验证淀粉水解产物的实验主要有以下步骤:(1)在酸性条件下水浴加热使其水解,即①⑤⑥;
(2)加碱中和硫酸,即③;
(3)加入新制的Cu(OH)2碱性悬浊液并加热煮沸检验产物,即④②。
归纳总结
淀粉水解程度的检验
(1)实验步骤
归纳总结
(2)实验现象及结论
情况 现象A 现象B 结论
① 未出现银镜 溶液呈蓝色 淀粉未水解
② 出现银镜 溶液呈蓝色 淀粉部分水解
③ 出现银镜 溶液未呈蓝色 淀粉完全水解
返回
蛋白质和氨基酸
二
1.蛋白质的存在与组成
(1)存在
蛋白质广泛存在于生命体内,是组成 的基础物质。动物的 、____以及在人体新陈代谢中起催化作用的 、运输氧气的 、引起疾病的 和 、抵抗疾病的 中都含有蛋白质。
(2)组成
主要由 、 、 、 、硫等元素组成,是结构非常复杂的高分子化合物。
细胞
肌肉
毛皮
酶
血红蛋白
细菌
病毒
抗体
碳
氢
氧
氮
2.蛋白质的性质
按表中实验操作完成实验,并填写下表
实验操作 实验现象
蛋白质溶液 加饱和(NH4)2SO4溶液,再加蒸馏水 有 析出,加入蒸馏水____
_______
加稀硫酸,再加蒸馏水 有 析出,加入蒸馏水,___
_________
加CuSO4溶液,再加蒸馏水 有 析出,加入蒸馏水,___
_________
白色沉淀
沉淀
又溶解
白色沉淀
沉
淀不溶解
白色沉淀
沉
淀不溶解
蛋白质溶液 加甲醛溶液,再加蒸馏水 有 析出,加入蒸馏水,____
______
加热,再加蒸馏水 有 析出,加入蒸馏水,____
_______
白色沉淀
沉淀
不溶解
白色沉淀
沉淀
不溶解
(1)蛋白质的盐析
①概念:某些浓的无机盐溶液可使蛋白质的溶解度 而使其从溶液中 的过程叫盐析。
②条件:浓的轻金属盐溶液或铵盐溶液,如(NH4)2SO4溶液、Na2SO4溶液。少量的无机盐能促进蛋白质的溶解。
③特点:盐析是 过程,继续加水时,能使 , 蛋白质的生理活性。可用来分离、提纯蛋白质。
降低
析出
可逆
沉淀溶解
不影响
不可逆
(2)蛋白质的变性
①概念:在加热、强酸、强碱、重金属盐、紫外线、福尔马林(36%~40%甲醛溶液)的作用下,蛋白质原有的 或 会发生改变,其 也会随之改变,我们把这种变化称为蛋白质的变性。
②蛋白质的变性是 过程,可以利用这一性质进行杀菌消毒。
化学组成
空间结构
生理功能
不可逆
特别提醒 误食含重金属离子的溶液时,可喝生牛奶或蛋清救治。
(3)蛋白质的水解反应
氨基酸
②几种常见的氨基酸
甘氨酸(氨基乙酸):_____________;
丙氨酸(α-氨基丙酸):________________;
谷氨酸(α-氨基戊二酸):____________________________。
氨基酸分子中均含有 和 两种官能团,氨基连接在离 的氨基酸为α-氨基酸。
羧基(—COOH)
氨基(—NH2)
羧基最近的碳原子上
③氨基酸的化学性质
碱
酸
酸
碱
多肽
蛋白质
(4)蛋白质的特征反应
3.酶
(1)酶是一种具有 的物质。
(2)绝大多数酶是 。
(3)酶催化作用的特征
①专一性;②高效性;③条件温和。
催化作用
蛋白质
(1)蛋白质都是结构复杂的高分子化合物,组成元素只有C、H、O、N( )
正误判断
×
(2)蛋白质在酶的作用下,可直接水解生成各种氨基酸( )
正误判断
提示 蛋白质水解先生成多肽,多肽进一步水解,最终生成氨基酸。
×
(3)蛋白质溶液遇到盐就会变性( )
(4)蛋白质变性属于化学变化( )
正误判断
×
√
(5)向鸡蛋白溶液中加入醋酸铅溶液,生成白色沉淀,加水可重新溶解( )
正误判断
提示 加入重金属盐,蛋白质发生变性,加水沉淀也不会溶解。
×
(6)可以通过灼烧的方法鉴别真蚕丝和人造丝( )
正误判断
提示 真蚕丝灼烧有烧焦羽毛气味,而人造丝没有。
√
1.硝酸可以使蛋白质变黄,称为蛋白质的颜色反应。此“颜色反应”与钠元素的“焰色反应”有何区别?
提示 颜色反应是指某些蛋白质的黄蛋白反应,属于化学变化;而焰色反应是指钠、钾等多种金属元素被灼烧时火焰呈现的颜色,属于物理变化。
深度思考
2.为了检验过氧化氢分解酶的作用,在室温下进行如下实验:
(1)在试管A中加入3%的双氧水3 mL,再加入二氧化锰0.5 g,有气体产生。
(2)在试管B中加入3%的双氧水3 mL,再加入新鲜的鸡肝片1 g,有气体产生。
(3)在试管C中加入3%的双氧水3 mL,再加入煮熟的鸡肝片1 g,无气体产生。
(4)在试管D中加入3%的双氧水2 mL和10%的盐酸1 mL,再加入新鲜的鸡肝片1 g,无气体产生。
(5)在试管E中加入3%的双氧水2 mL和10%的氢氧化钠溶液1 mL,再加入新鲜的鸡肝片1 g,无气体产生。
通过以上实验,你能得出什么结论?
深度思考
深度思考
提示 通过以上实验可得出:
(1)MnO2和新鲜的鸡肝片都能催化过氧化氢的分解。
(2)煮熟的鸡肝片不能催化过氧化氢的分解。
(3)在较强的酸性、碱性条件下,新鲜的鸡肝片不能催化过氧化氢的分解。由此可知:新鲜鸡肝片中的过氧化氢酶在加热、强酸、强碱条件下发生变性,失去催化作用。
应用体验
1.下列关于蛋白质的叙述正确的是
A.向蛋白质溶液中分别加入NaCl溶液、CuSO4溶液,其过程均是不可逆的
B.重金属盐使蛋白质分子变性,但是吞“钡餐”(主要成分是硫酸钡)不
会引起中毒
C.温度越高,酶对某些生化反应的催化效率就越高
D.医疗上用75%的酒精杀菌消毒,是利用了酒精可以使蛋白质盐析的性质
√
向蛋白质溶液中加入NaCl溶液发生盐析,其过程是可逆的,A错误;
重金属盐使蛋白质分子变性,但是吞“钡餐”(主要成分是硫酸钡)不会引起中毒,因为硫酸钡既不溶于水也不溶于酸,且不容易被X射线透过,在医疗上可用作检查肠胃的内服药剂,B正确;
酶的活性受温度限制,超过适宜的温度时酶将失去活性,C错误;
医疗上用体积分数为75%的酒精杀菌消毒,是利用了酒精可以使蛋白质变性的性质,D错误。
2.下列关于氨基酸的说法,正确的是
①蛋白质在一定条件下能发生水解反应,最终转化为各种氨基酸
②氨基酸分子既能与酸反应,又能与碱反应
③α-氨基酸中氨基连在离羧基最近的碳原子上
④氨基酸之间在一定条件下能发生反应,生成多肽
A.只有①② B.只有①②③
C.只有①②④ D.①②③④
√
3.(1)鸡蛋清水解的最终产物是________。请以甘氨酸( )为例,
写出其与NaOH溶液反应的化学方程式:_______________________
________________。
氨基酸
蛋白质水解的最终产物是氨基酸。
+NaOH―→
+H2O
(2)市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服上的汗渍、血液及人体排放的蛋白质油渍遇到它,皆能水解除去。下列衣料中不能用加酶洗衣粉洗涤的是______
(填序号)。
①棉织品 ②毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥锦纶织品
根据题意知加酶洗衣粉能使蛋白质水解,所以含有蛋白质的衣服不能用加酶洗衣粉清洗。毛织品和蚕丝织品的主要成分是蛋白质。
②④
归纳总结
蛋白质的盐析与变性的区别
盐析 变性
含义 蛋白质在某些盐的浓溶液中因溶解度降低而析出 蛋白质在加热、酸、碱等条件下性质发生改变而聚沉
条件 轻金属盐和铵盐 紫外线照射、加热或加入某些有机化合物(甲醛、酒精)、强酸、强碱、重金属盐(如铅盐、铜盐、汞盐)等
归纳总结
特征 可逆过程,不改变蛋白质的性质和生理活性 不可逆过程,蛋白质失去生理活性
实质 溶解度降低,物理变化 结构、性质改变,化学变化
用途 分离、提纯蛋白质 杀菌消毒
返回
随堂演练 知识落实
1.葡萄糖(C6H12O6)是一种重要的营养物质,下列关于葡萄糖的说法正确的是
A.葡萄糖是一种单糖
B.葡萄糖分子中有6个碳原子、6个水分子
C.常温下,葡萄糖可与新制的氢氧化铜碱性悬浊液反应
D.1 mol葡萄糖完全燃烧需要9 mol氧气
√
1
2
3
4
1
2
3
4
葡萄糖分子中氢、氧原子个数比为2∶1,但不是以水分子的形式存在,B项错误;
葡萄糖和新制的氢氧化铜碱性悬浊液反应必须加热,C项错误;
葡萄糖的分子式可改写为C6(H2O)6,由此可判断1 mol 葡萄糖完全燃烧需要消耗6 mol氧气,D项错误。
2.中国酒文化源远流长,很多地方至今仍用传统工艺来制作米酒。家酿米酒的转化过程为
A.淀粉→蔗糖→葡萄糖→酒
B.淀粉→麦芽糖→葡萄糖→酒
C.淀粉→麦芽糖→果糖→酒
D.淀粉→蔗糖→果糖→酒
√
1
2
3
4
3.(2022·成都龙泉驿区教育科学研究院高一期中)下列实例利用了蛋白质变性原理的是
①利用过氧乙酸对环境、物品进行消毒 ②利用高温、紫外线对医疗器械进行消毒 ③蒸煮鸡蛋食用 ④松花蛋的腌制 ⑤用牛奶灌服重金属中毒的病人
A.①②③④⑤ B.①②③④
C.①②③ D.①②
√
1
2
3
4
1
2
3
4
过氧乙酸有强氧化性,能使蛋白质变性,故①正确;
高温、紫外线均能使蛋白质变性,故②正确;
加热能使蛋白质变性,故③正确;
碱能使蛋白质变性,用石灰腌制松花蛋便于保存和食用,故④正确;
重金属盐中毒的原理是其破坏了人体的蛋白质结构,牛奶的主要成分是蛋白质,服用牛奶,可防止人体本身的蛋白质被破坏,能用于解毒,故⑤正确。
4.成熟的苹果中含有淀粉、葡萄糖和无机盐等,某课外兴趣小组设计了一组实验证明某些成分的存在,请你参与并协助他们完成相关实验。
(1)用小试管取少量的苹果汁,加入______(填名称),溶液变蓝,则证明苹果中含有淀粉。
1
2
3
4
碘水
苹果中含有淀粉,淀粉遇碘单质变蓝,向苹果汁中加入碘水,溶液变蓝,则证明苹果中含有淀粉。
1
2
3
4
(2)利用含淀粉的物质可以生产醋酸。下面是生产醋酸的流程图,试回答下列问题:
B是日常生活中有特殊香味的常见有机物,在有些饮料中含有B。
①写出下列反应的化学方程式,并注明反应类型。
B与醋酸反应:________________________________________________,
属于____________反应。
B→C:______________________________________,属_____反应。
取代(或酯化)
氧化
1
2
3
4
1
2
3
4
②可用于检验A的试剂是________________________________________
_____。
新制的氢氧化铜碱性悬浊液(其他合理答案
均可)
葡萄糖中含有醛基,检验葡萄糖可用新制的氢氧化铜碱性悬浊液(或银氨溶液),加热后若生成砖红色沉淀(或水浴加热出现光亮的银镜),则说明为葡萄糖。
返回
课时对点练
题组一 糖类
1.下列关于糖类的叙述正确的是
A.含有C、H、O三种元素的有机物叫糖类
B.糖类物质均能与银氨溶液在加热时反应生成银镜
C.糖类物质都有甜味
D.糖类物质是绿色植物光合作用的产物,是动、植物所需能量的重要
来源
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
含有C、H、O三种元素的有机物很多,如CH3CH2OH、CH3COOH、CH3COOCH2CH3等,故A错误;
分子结构中含有—CHO的糖类分子才能发生银镜反应,故B错误;
并不是所有的糖类都有甜味,如淀粉、纤维素,故C错误。
2.糯米中含大量淀粉,下列有关说法正确的是
A.淀粉能与银氨溶液反应产生银镜
B.淀粉是否水解完全可以用碘水来检验
C.淀粉在碱性条件下能水解生成葡萄糖
D.糖尿病病人不宜吃粽子,因为糯米中含大量的葡萄糖会使血糖升高
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
淀粉属于高分子化合物,不能与银氨溶液反应产生银镜,A错误;
淀粉是否水解完全可以用碘水来检验,若溶液变蓝,则淀粉未水解或水解不完全,反之水解完全,B正确;
淀粉在酸或酶的催化作用下能水解生成葡萄糖,但在碱性条件下不能水解,C错误;
糖尿病病人不宜吃粽子,是因为糯米中含大量的淀粉,淀粉水解能生成葡萄糖,会使血糖升高,D错误。
3.(2022·合肥一中高一检测)下列关于检验某病人尿糖的做法正确的是
A.取尿样,加入新制的Cu(OH)2碱性悬浊液,观察发生的现象
B.取尿样,加入过量稀H2SO4,再加入新制的Cu(OH)2碱性悬浊液,
观察发生的现象
C.取尿样,加入新制的Cu(OH)2碱性悬浊液,煮沸,观察发生的现象
D.取尿样,加入Cu(OH)2固体,煮沸,观察发生的现象
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
葡萄糖的检验需在碱性条件下与新制的Cu(OH)2悬浊液或银氨溶液共热而完成。
4.2020年新疆棉花总产量达516.1万吨,占全国棉花总产量的87.3%,约占世界棉花产量的20%以上。棉花中的纤维素占比87%~90%,纤维素的化学式为(C6H10O5)n,下列关于纤维素说法正确的是
A.纤维素属于有机物
B.纤维素中碳、氢元素质量比为3∶5
C.纤维素是由碳、氢、氧三种原子构成的
D.纤维素的相对分子质量为162
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
纤维素是含碳元素的化合物,属于有机物,A正确;
纤维素中碳、氢元素质量比为(12×6)∶10=36∶5,B错误;
纤维素是由碳、氢、氧三种元素组成的,C错误;
纤维素的相对分子质量为12×6n+10n+16×5n=162n,D错误。
5.以玉米(主要成分是淀粉)为原料制备乙醇的流程如图:
下列说法不正确的是
A.C12H22O11属于二糖
B.1 mol葡萄糖可分解成3 mol乙醇
C.葡萄糖不能进一步水解
D.不能用分液操作分离乙醇和水
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
由流程图可知,玉米中淀粉在酸性条件下水解得到C12H22O11,C12H22O11在酸性条件下继续水解得到葡萄糖,葡萄糖在酒化酶的作用下转化为乙醇。淀粉在酸性条件下水解生成的C12H22O11属于二糖,A正确;
乙醇和水互溶,不可用分液操作分离,D正确。
6.某学生设计了如下实验方案用以检验淀粉水解的情况:
下列结论正确的是
A.淀粉尚有部分未水解
B.淀粉已完全水解
C.淀粉没有水解
D.淀粉已发生水解,但不知是否完全水解
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
因为混合液呈碱性,所以加碘水溶液不变蓝,不能说明溶液中不含淀粉;而加入新制的Cu(OH)2碱性悬浊液加热煮沸生成砖红色沉淀,说明其中含有葡萄糖,故结论应为淀粉已水解,但不知是否完全水解。
题组二 蛋白质和氨基酸
7.某期刊封面上有如图所示的一个分子的球棍模型,图中“棍”代表单键、双键或三键。不同颜色的“球”代表不同元素的原子,该模型图可代表的物质是
A.葡萄糖
B.酯
C.氨基酸
D.乙醇钠
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
由分子的球棍模型图,结合原子结构可知,白球代表H,蓝球代表N,绿球代表C,红球代表O。故该模型图表示的分子是H2NCH2COOH,即甘氨酸,甘氨酸是一种重要的氨基酸,故C符合题意。
8.下列有关蛋白质的性质描述说法错误的是
A.棉被和蚕丝被的主要材质均为高分子
B.从牛奶中可以提取酪素,用来制作塑料
C.消毒过程中细菌蛋白质发生了水解
D.在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会产生沉淀,
但原理不同
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
棉被和蚕丝被的主要材质分别是纤维素、蛋白质,二者均为高分子,A正确;
酪素由酪蛋白水解得到,故从牛奶中可以提取酪素,用来制作塑料,B正确;
消毒过程中细菌蛋白质发生了变性,C错误;
鸡蛋清中加入饱和Na2SO4溶液使蛋白质的溶解性降低而析出,加入CuSO4溶液使蛋白质发生变性而析出,原理不同,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
9.2018年诺贝尔化学奖获得者为弗朗西斯·阿诺德(Frances H·Amold)、乔治·史密斯(George P·Smith)及格雷戈里·温特(Gregory P·Winter)爵士。上述三位化学奖得主成功利用基因变化和选择研究出可以解决人类化学问题的蛋白质。下列关于蛋白质的组成与性质的叙述正确的是
A.蛋白质在酶的作用下水解的最终产物为氨基酸
B.向蛋白质溶液中加入CuSO4、Na2SO4浓溶液,均会使其变性
C.天然蛋白质仅由碳、氢、氧、氮四种元素组成
D.蛋白质、纤维素、油脂都是高分子化合物
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
蛋白质水解的最终产物为氨基酸,A正确;
CuSO4为重金属盐,能使蛋白质发生变性,Na2SO4浓溶液不能使蛋白质发生变性,B错误;
天然蛋白质除含C、H、O、N四种元素外还含有P、S等元素,C错误;
油脂不是高分子化合物,D错误。
10.下列关于酶的叙述中,不正确的是
A.酶是糖类物质
B.大多数酶是蛋白质
C.酶是生物体内产生的催化剂
D.酶受到高温或重金属盐作用时会变性
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
大多数酶是蛋白质,而不是糖类物质,A错误、B正确;
酶是生物体内产生的催化剂,其催化作用具有条件温和、不需要加热、高度专一、催化效率高等特点,C正确;
酶具有蛋白质的性质,当受到高温或重金属盐作用时会变性,D正确。
11.(2022·深圳高一月考)生命在于运动,而生命活动的维持离不开能量,糖类、油脂、蛋白质是基本营养物质。下列说法正确的是
A.糖类、油脂、蛋白质都能发生水解反应
B.糖尿病病人食用的“无糖饼干”主要成分为面粉,不含糖类物质
C.我国新冠疫苗安全有效,助力全球抗疫,疫苗无需经冷链运输
D.豆腐是我国古代劳动人民智慧的结晶,蛋白质在人体内水解的最终
产物为氨基酸
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
糖类有多种,例如葡萄糖等单糖不能发生水解,A错误;
面粉的主要成分为淀粉,淀粉属于糖类物质,B错误;
疫苗的主要成分为蛋白质,温度过高蛋白质易变性,应冷链运输,C错误;
豆腐的主要成分为蛋白质,在人体内经蛋白酶催化水解为氨基酸,D正确。
12.下列与化学有关的文献或诗文,理解正确的是
A.《问刘十九》中写道:“绿蚁新醅酒,红泥小火炉”,“新醅酒”即新酿
的酒,在酿酒的过程中,葡萄糖发生了水解反应
B.“独忆飞絮鹅毛下,非复青丝马尾垂”中的“飞絮”和棉花的化学成分不同
C.《天工开物》中有如下描述:“世间丝、麻、裘、褐皆具素质,而使殊颜
异色得以尚焉……”文中的“麻”“裘”在一定条件下都可以水解生成
小分子
D.《傅鹑觚集·太子少傅箴》中记载:“故近朱者赤,近墨者黑。”这里的
“朱”指的是朱砂,它是古代常用的一种红色颜料,其主要成分为Fe2O3
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
葡萄糖为单糖,不能水解,故A错误;
飞絮和棉花的化学成分都是纤维素,故B错误;
“麻”的主要成分为纤维素,“裘”的主要成分为蛋白质,都可以水解生成小分子,故C正确;
朱砂是古代常用的一种红色颜料,其主要成分是HgS,故D错误。
13.下列有关蛋白质的叙述中,不正确的是
A.蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解
B.人工合成的具有生命活性的蛋白质——结晶牛胰岛素,是1965年我
国科学家最先合成的
C.重金属盐能使蛋白质变性,所以误食重金属盐会中毒
D.浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生
颜色反应
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,为蛋白质的盐析过程,蛋白质盐析可逆,再加水会溶解,A错误;
结晶牛胰岛素是我国科学家于1965年首次合成的,属于蛋白质,B正确;
浓硝酸与部分天然蛋白质会发生颜色反应,所以浓硝酸溅在皮肤上,使皮肤呈黄色,D正确。
14.近期,英国科学家通过研究人类脑部疾病的样本,发现人脑中一种名为“突触后致密区”(PSD)的神经组织含有1 461种蛋白,该组织病变会导致痴呆等130多种脑部疾病,最新研究有望为科学家治疗脑病指明方向。下列关于蛋白质叙述正确的是
A.天然蛋白质水解的最终产物都是氨基酸
B.在蛋白质溶液中滴加饱和硫酸铵溶液可以使蛋白质变性
C.在蛋白质溶液中加入福尔马林(36%~40%甲醛溶液)产生沉淀,再加
入大量水,沉淀又溶解
D.通过盐析作用析出的蛋白质不再溶于水
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
15.应用所学知识回答下列问题:
(1)下列物质对蛋白质的化学性质具有明显影响的是________(填字母,下同)。
A.重晶石(BaSO4) B.蓝矾 C.碘酒 D.高锰酸钾 E.酒精 F.生牛奶 G.熟鸡蛋
蓝矾、碘酒、高锰酸钾、酒精等物质都能使蛋白质变性,蛋白质的变性属于化学变化。重晶石的主要成分是硫酸钡,它既不溶于水又不溶于酸,不能使蛋白质变性,对人体无毒。
BCDE
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
A.重晶石(BaSO4) B.蓝矾 C.碘酒 D.高锰酸钾 E.酒精 F.生牛奶 G.熟鸡蛋
(2)如果你发现有人误服重金属盐而出现了轻微中毒症状,需要你马上对病人进行抢救,你认为上述物质中可以应用的是_____。
生牛奶中含有较多的未变性的蛋白质,熟鸡蛋中蛋白质已经变性了。
F
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(3)当你选择物质对病人进行抢救以后,下一步的打算或做法是______。
A.建议病人尽快去医院继续治疗
B.将病人安置于通风处呼吸新鲜的空气
C.建议病人卧床休息
重金属盐中毒者服用生牛奶能降低重金属盐对人体的伤害,但这种作用是有限的。病人去医院做更有效的治疗是最佳选择。
A
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
16.鸡蛋中含有丰富的蛋白质,鸡蛋清就是一种蛋白质,它的分子直径为1~100 nm,具有某些胶体的性质。取新鲜鸡蛋的鸡蛋清溶于水制成水溶液,分装于试管中,分别进行如下实验,回答下列问题:
(1)向试管里缓慢地加入饱和的硫酸铵溶液,观察到的现象是________
____;再向试管里加入足量的蒸馏水,观察到的现象是_________。
有沉淀
析出
沉淀溶解
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
硫酸铵能够使蛋白质发生盐析,降低蛋白质的溶解度,使其以沉淀形式析出,该过程发生了物理变化,所得沉淀和原蛋白质的性质相同,所以加入足量的蒸馏水,沉淀又会溶解,是一个可逆过程。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(2)向试管里缓慢地加入硫酸铜溶液,观察到的现象是___________;再向试管里加入足量的蒸馏水,观察到的现象是___________。
有沉淀析出
沉淀不溶解
硫酸铜属于重金属盐,它能够使蛋白质发生变性,从而析出沉淀,该过程发生了化学变化,所得沉淀和原蛋白质的性质不同,所以加入足量的蒸馏水,沉淀不会溶解,是一个不可逆过程。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(3)已知蛋白质遇到浓硝酸会变黄,这个反应可以用来鉴别某些带有苯环的蛋白质。把10 mL鸡蛋清溶液和5 mL NaCl溶液的混合液体,加入用
半透膜(一种有微孔的膜,小分子或离子可以透过,胶体粒子不能透过)制成的袋内,将此袋浸入盛蒸馏水的烧杯中(如图)。2 min后,取烧杯中的液体分别进行实验。
①加入AgNO3溶液,产生的现象是________________。
有白色沉淀析出
②加入浓硝酸,产生的现象是____________。
无明显现象
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
胶体微粒不能透过半透膜,而小分子或离子能够透过半透膜,所以烧杯中含有NaCl溶液而不含鸡蛋清溶液,加入AgNO3溶液会产生AgCl白色沉淀,加入浓硝酸不会变黄。
返回
本课结束
专题8
