专题8 第一单元 第1课时 天然气的利用 甲烷 课件(共73张PPT)
文档属性
| 名称 | 专题8 第一单元 第1课时 天然气的利用 甲烷 课件(共73张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-10 00:00:00 | ||
图片预览










文档简介
(共73张PPT)
第1课时
DIYIKESHI
甲烷的组成与结构 / 甲烷的化学性质 / 随堂演练 知识落实 / 课时对点练
天然气的利用 甲烷
专题8
核心素养
发展目标
1.认识甲烷的组成和结构特点。会书写甲烷的分子式、结构式及电子式,形成“结构决定性质”的观念,培养宏观辨识与微观探析的能力。
2.知道甲烷能发生氧化反应和取代反应,掌握取代反应的概念,能通过分析、推理等方法,判断有机物的取代反应,培养证据推理的能力。
内容索引
一、甲烷的组成与结构
二、甲烷的化学性质
随堂演练 知识落实
课时对点练
甲烷的组成与结构
一
1.甲烷
甲烷是一种 色、 味、 溶于水的气体,熔、沸点 、密度比空气 。甲烷是 的主要成分, 的水合物外形似冰,被称为“可燃冰”。
无
无
难
低
小
天然气
天然气
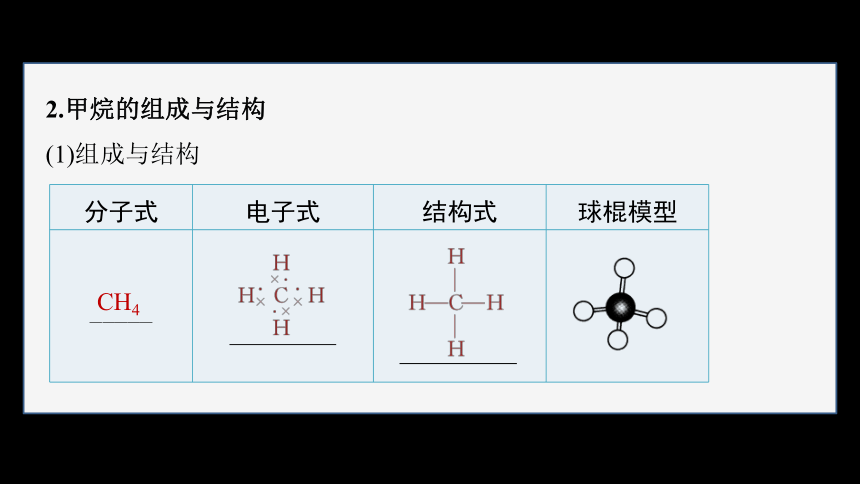
2.甲烷的组成与结构
(1)组成与结构
分子式 电子式 结构式 球棍模型
_____
CH4
(2)结构特点
碳原子位于中心,与4个氢原子形成完全相同的4个C—H共价键,相邻C—H共价键的夹角为109°28′,具有 空间结构。
正四面体
正误判断
(1)甲烷分子中碳原子最外层有4个电子,可以形成4个共价键( )
(2)已知甲烷为正四面体结构,可推知CCl4也为正四面体结构( )
(3)天然气就是纯净的甲烷气体( )
(4)16 g CH4分子中含有2NA个C—H键( )
(5)甲烷和四氯化碳的分子中各原子均达到8电子稳定结构( )
√
√
×
×
×
已知标准状况下,甲烷的密度是0.717 g·L-1。
(1)甲烷的相对分子质量是多少?
深度思考
提示 由M=ρ·22.4 L·mol-1得,M(甲烷)≈16 g·mol-1,即甲烷的相对分子质量为16。
(2)甲烷中含碳元素的质量分数为75%,含氢元素的质量分数为25%,求甲烷的分子式。
深度思考
应用体验
1.下列叙述与甲烷无关的是
A.天然气、沼气、可燃冰的主要成分
B.“西气东输”工程中运输的气体的主要成分
C.造成“光化学烟雾”的气体
D.煤矿中瓦斯爆炸
√
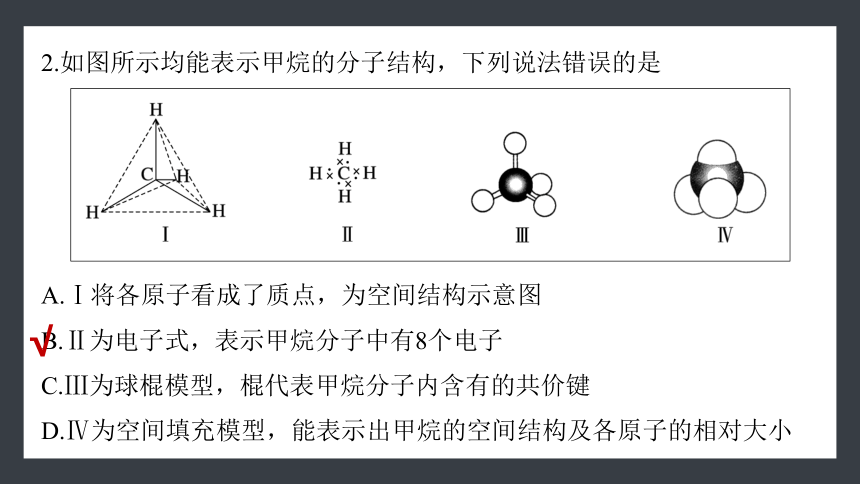
2.如图所示均能表示甲烷的分子结构,下列说法错误的是
A.Ⅰ将各原子看成了质点,为空间结构示意图
B.Ⅱ为电子式,表示甲烷分子中有8个电子
C.Ⅲ为球棍模型,棍代表甲烷分子内含有的共价键
D.Ⅳ为空间填充模型,能表示出甲烷的空间结构及各原子的相对大小
√
Ⅱ表示电子式,但略去了碳原子的内层电子,甲烷分子中应含有10个电子。
归纳总结
一个碳原子与其他4个原子以4个单键相结合时:
(1)如果这4个原子相同,分别在四面体的顶点上,则构成正四面体;
(2)如果这4个原子不相同,则分别在四面体的顶点上,但不是正四面体;
(3)无论这4个原子是否相同,都不可能在同一平面上,并且最多有3个原子共面。
返回
甲烷的化学性质
二
1.稳定性
CH4性质稳定,不与 、 、 等物质反应。
2.氧化反应
点燃甲烷气体,观察燃烧现象,并检验燃烧产物。
(1)猜想:根据甲烷(CH4)的组成,其燃烧后可能会生成 和 。
强酸
强碱
KMnO4
CO2
H2O
(2)实验验证
燃烧现象 检验产物 方法 现象 结论
___________ 在火焰上方罩一个干燥的烧杯 烧杯内壁有水珠产生 _________
在火焰上方罩一个涂有澄清石灰水的烧杯 烧杯内壁变浑浊 ___________
_____
淡蓝色火焰
生成了水
生成了二氧
化碳
(3)实验结论
经测定,1 mol CH4完全燃烧生成 和 ,放出890 kJ的热,热化学方程式为 ,因此,甲烷是一种高效而洁净的燃料。
液态水
二氧化碳
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
3.取代反应
(1)实验探究
实验装置与操作
用排饱和食盐水法收集 体积的氯气和 体积的甲烷
气体,用灯光照射瓶中的混合气体
实验 现象 集气瓶内黄绿色气体颜色逐渐变浅,集气瓶内壁有_________
出现,瓶中有少量白雾,且瓶内液面 ,水槽中有固体析出
实验 结论 CH4与Cl2需在 条件下发生化学反应,有关化学方程式为
CH4+Cl2 ;
CH3Cl+Cl2 ;
CH2Cl2+Cl2 ;
CHCl3+Cl2 ———————————————————————
油状液体
上升
光照
CH3Cl(一氯甲烷)+HCl
CH2Cl2(二氯甲烷)+HCl
CHCl3(三氯甲烷或氯仿)+HCl
CCl4(四氯甲烷或四氯化碳)+HCl
特别提醒:
①水溶性:CH3Cl、CH2Cl2、CHCl3、CCl4均不溶于水。
②状态:常温下除CH3Cl是气体,其余三种均为油状液体。
(2)取代反应
①概念:有机化合物分子中的某种原子(或原子团)被另一种__________
所取代的反应。
②特点:
a.反应条件,在光照条件下,甲烷与气态纯卤素单质发生取代反应。
b.连续反应,甲烷分子中的氢原子被氯原子逐步取代,反应一旦开始,后续反应立即进行,且各步反应可同时进行。
③因为有机化学反应的副产物较多,所以写化学方程式时用“→”连接反应物和目标产物。
原子(或原
子团)
正误判断
(1)甲烷性质稳定,与任何氧化剂都不反应( )
(2)CH4和Cl2按体积比1∶1混合,发生取代反应生成的产物只有两种( )
(3)CH4和Cl2发生取代反应时,每生成1 mol HCl,则有1 mol Cl2参加反应
( )
(4)CH4分子为正四面体结构,因此其生成物CH3Cl、CH2Cl2、CHCl3和CCl4都为正四面体结构( )
(5)取代反应和置换反应都是物质中某些原子或原子团被其他原子或原子团代替,因此本质相同( )
×
×
√
×
×
1.若甲烷分子中的一个氢原子被氯原子取代,生成的CH3Cl还是四面体结构吗?
深度思考
提示 CH3Cl中3个H和1个Cl仍分别位于四面体的4个顶点,仍为四面体结构,但不是正四面体结构。
2.甲烷中每有1 mol氢原子被取代,消耗Cl2的物质的量是多少?
深度思考
提示 1 mol。
应用体验
1.下列物质在一定条件下能与甲烷发生取代反应的是
A.氯气 B.酸性高锰酸钾溶液
C.氢氧化钠溶液 D.溴水
√
A项,氯气在光照条件下与甲烷可以发生取代反应;
B项,酸性高锰酸钾溶液不能氧化甲烷,也不能与甲烷发生取代反应;
C项,氢氧化钠溶液与甲烷不反应;
D项,溴水与甲烷不反应。
2.在光照条件下,将1 mol CH4与Cl2反应,得到四种有机产物CH3Cl、CH2Cl2、CHCl3、CCl4的物质的量之比为1∶2∶3∶4,则消耗Cl2的物质的量为
A.0.5 mol B.1.25 mol
C.2.5 mol D.3 mol
√
四种有机产物的物质的量之比为n(CH3Cl)∶n(CH2Cl2)∶n(CHCl3)∶n(CCl4)
=1∶2∶3∶4,则四种取代物的物质的量分别为n(CH3Cl)=0.1 mol,n(CH2Cl2)=0.2 mol,n(CHCl3)=0.3 mol,n(CCl4)=0.4 mol,发生取代反应时,一半的Cl进入HCl,消耗氯气的物质的量为0.1 mol+2×
0.2 mol+3×0.3 mol+4×0.4 mol=3 mol。
归纳总结
甲烷的取代反应
返回
随堂演练 知识落实
1.甲烷是天然气的主要成分,是一种高效、低耗、污染小的清洁能源。下列有关甲烷的说法正确的是
①甲烷是一种正四面体结构的分子
②甲烷分子中所有原子均满足最外层8电子结构
③0.5 mol CH4完全燃烧时消耗1 mol O2
④1 mol CH4完全生成CCl4,最多消耗2 mol Cl2
A.①② B.③④ C.①③ D.②④
√
1
2
3
4
1
2
3
4
①甲烷是一种正四面体结构的分子,正确;
③1 mol CH4完全燃烧时消耗2 mol O2,则0.5 mol CH4完全燃烧时消耗1 mol O2,正确;
④根据取代反应的特点,1 mol CH4完全生成CCl4,最多消耗4 mol Cl2,错误。
2.(2022·成都龙泉驿区教育科学研究院高一期中)若甲烷与氯气的体积之比为1∶1,则得到的产物为
A.CH3Cl HCl
B.CCl4 HCl
C.CH3Cl CH2Cl2
D.CH3Cl CH2Cl2 CHCl3 CCl4 HCl
√
1
2
3
4
1
2
3
4
3.将标准状况下的11.2 L甲烷和22.4 L氧气混合点燃,恢复到原状态后,气体的体积为
A.11.2 L B.22.4 L C.33.6 L D.44.8 L
√
1
2
3
4
CH4+2O2 CO2+2H2O(l)
起始/mol 0.5 1 0 0
转化/mol 0.5 1 0.5 1
最终/mol 0 0 0.5 1
注意CO2为气体,H2O为液体。
4.(2018·全国卷Ⅱ,9)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是
1
2
3
4
√
1
2
3
4
甲烷与氯气在光照条件下发生取代反应,黄绿色的氯气减少,因此试管内气体颜色逐渐变浅;反应生成的HCl极易溶于水,使试管内气体压强减小,因此试管内液面上升;生成的CH2Cl2、CHCl3、CCl4均为无色
油状液体,附着在试管壁上,因此试管壁上出现无色油状液滴;生成的HCl气体遇到水蒸气溶解生成盐酸小液滴,形成白雾,因此试管中有少量白雾。综合上述现象,答案选D项。
返回
课时对点练
题组一 甲烷的组成与结构
1.下列关于甲烷的说法错误的是
A.分子式:CH4
B.可作为清洁燃料
C.球棍模型:
D.可使酸性KMnO4溶液褪色
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
甲烷的分子式为CH4,故A正确;
甲烷完全燃烧生成二氧化碳和水,不产生空气污染物,可作为清洁燃料,故B正确;
甲烷为正四面体结构,碳原子的半径大于氢原子的半径,球棍模型为
,故C正确;
甲烷化学性质稳定,不能使酸性KMnO4溶液褪色,故D错误。
2.下列关于甲烷的说法不正确的是
A.甲烷分子具有正四面体结构
B.甲烷是无色、无味的气体
C.甲烷是最简单的有机化合物
D.甲烷能使溴水褪色
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
通常情况下,甲烷是一种无色、无味的气体,难溶于水,密度比空气小,故B正确;
仅含碳氢单键的甲烷不能与溴水反应,溶液不会褪色,故D错误。
3.下图是CH4、CCl4、CH3Cl分子的球棍模型,下列说法正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
A.CH4、CCl4和CH3Cl都是正四面体结构
B.CH4、CCl4都是正四面体结构
C.CH4和CCl4中的化学键完全相同
D.CH4、CCl4的结构相同,性质也相同
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
CCl4与CH4的分子结构相似,为正四面体结构,CH3Cl中的C—H键和C—Cl键不同,不是正四面体结构,而是四面体结构。
4.(2022·江西省临川第二中学高一期中)能证明CH4分子的空间结构为正四面体形而非平面正方形的事实是
A.CH2Cl2只有一种结构
B.CH3Cl分子只有一种结构
C.C原子距离四个H原子的距离一样
D.CH4分子中的四个碳氢键一样
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
若CH4分子的空间结构为平面正方形,CH2Cl2应有2种结构,而实际上CH2Cl2只有一种结构,说明CH4分子的空间结构为正四面体形,故选A;
无论CH4分子的空间结构为正四面体形还是平面正方形,CH3Cl分子都只有一种结构,故不选B;
无论CH4分子的空间结构为正四面体形还是平面正方形,C原子距离四个H原子的距离一样,故不选C;
无论CH4分子的空间结构为正四面体形还是平面正方形,CH4分子中的四个碳氢键一样,故不选D。
题组二 甲烷的性质
5.在我国的南海、东海海底已发现天然气(含甲烷等)的水合物,它易燃烧,外形似冰,被称为可燃冰。可燃冰的开采,有助于缓解人类面临的能源危机。下列说法正确的是
①甲烷是“西气东输”的主要成分 ②在相同条件下,甲烷的密度大于空气的密度 ③甲烷难溶于水 ④可燃冰是一种极具潜力的能源
A.①②③ B.②③④ C.①③④ D.①②④
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
6.(2022·河北石家庄二十三中高一期中)最新研究发现,火星大气层中含有甲烷。下列说法错误的是
A.甲烷是一种共价化合物
B.可燃冰释放出的气体中含有甲烷
C.甲烷能发生氧化反应和取代反应
D.等物质的量的CH4与Cl2在光照下的反应产物只有CH3Cl和HCl
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
甲烷是由碳元素和氢元素组成的共价化合物,A项正确;
可燃冰是由水和甲烷在高压、低温条件下形成的类冰状结晶物质,可燃冰释放出的气体为甲烷,B项正确;
等物质的量的CH4和Cl2在光照下发生取代反应,属于连锁反应,生成4种氯代产物,同时生成HCl,D项错误。
7.下列反应中,属于取代反应的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
CaCO3高温下生成CaO和CO2,属于分解反应,A不符合题意;
Zn与硫酸反应属于置换反应,B不符合题意;
CH4与O2反应属于氧化反应,C不符合题意;
CH3CH3与Cl2反应生成CH3CH2Cl,可看成是CH3CH3中1个H原子被Cl原子取代,属于取代反应,D符合题意。
8.(2022·上海市延安中学高一期末)1 mol甲烷和1 mol氯气在光照条件下充分反应,产物中物质的量最多的是
A.CH3Cl B.HCl
C.CH2Cl2 D.CHCl3
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
甲烷和氯气在光照条件下发生取代反应,可生成有机物CH3Cl、CH2Cl2、CHCl3、CCl4,每一步反应都生成HCl,所以生成物中物质的量最多的是HCl,故B正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
9.下列关于甲烷的说法正确的是
A.甲烷是含碳元素质量分数最高的有机物
B.1 mol甲烷与1 mol氯气反应恰好生成1 mol一氯甲烷
C.CH2Cl2为正四面体结构
D.沼气的主要成分是甲烷,常用作清洁燃料
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
有机物中C原子呈四价,1个C原子最多结合4个H原子,甲烷是含氢元素质量分数最高的有机物,A错;
1 mol甲烷与1 mol氯气发生取代反应,伴随副反应的发生,生成多种氯代物,生成的一氯甲烷的物质的量小于1 mol,B错;
甲烷分子中,1个碳原子与4个氢原子形成共价键,4个共价键完全相同,且向空间4个方向伸展,所以甲烷为正四面体结构,而CH2Cl2相当于甲烷分子中的2个氢原子替换成2个氯原子,所以不是正四面体结构,应为四面体结构,C错。
10.将甲烷与一定量的氯气混合于一试管中,倒立于盛有饱和食盐水的水槽中(如图所示),对于此反应,有关叙述不正确的是
A.该反应的生成物只有四种
B.该反应的条件是光照
C.该反应结束后试管内液面上升(冷却到室温)
D.该反应属于取代反应
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
甲烷和氯气反应的生成物有一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢5种,故A错误;
该反应氯气中的氯原子取代了甲烷中的氢原子,属于取代反应,反应条件是光照,故B、D正确;
该反应生成了液态的二氯甲烷、三氯甲烷、四氯化碳,使气体的量减少,且生成的氯化氢气体极易溶于水,试管内压强减小,液面上升(冷却到室温),故C正确。
11.(2022·辽宁同泽高中高一阶段练习)以下关于甲烷的说法中,正确的是
①一氯甲烷分子具有四面体结构 ②二氯甲烷有两种 ③甲烷与Cl2在光照条件下发生取代,取代1 mol H需0.5 mol Cl2 ④甲烷分子中四个C—H键,任意两个共价键之间的键角均相等
A.②③④ B.②③
C.①④ D.①③
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
一氯甲烷分子为甲烷中一个H原子被Cl取代,CH3Cl的结构不对称,为四面体结构,故①正确;
甲烷为正四面体结构,所以二氯甲烷只有一种,故②错误;
甲烷与氯气发生一氯取代的化学方程式为CH4+Cl2 CH3Cl+HCl,取代1 mol H需1 mol Cl2,故③错误;
甲烷分子中四个碳氢键完全相同,任意两个碳氢键之间的键角均相等,故④正确。
12.鉴别甲烷、一氧化碳和氢气三种无色气体的方法是
A.通入溴水中→通入澄清石灰水中
B.点燃→罩上涂有澄清石灰水的烧杯
C.点燃→罩上干燥的冷烧杯→罩上涂有澄清石灰水的烧杯
D.点燃→罩上涂有澄清石灰水的烧杯→通入溴水中
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
13.标准状况下,44.8 L CH4与一定量Cl2在光照条件下发生取代反应,待反应完全后,测得四种有机取代产物的物质的量相等,则消耗Cl2的物质的量为
A.1 mol B.2 mol
C.4 mol D.5 mol
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
标准状况下,44.8 L CH4的物质的量为2 mol,2 mol甲烷完全与氯气发生取代反应,生成相同物质的量的四种取代物,所以每种取代物的物质的量是0.5 mol,在甲烷和氯气的取代反应中,被取代的氢原子的物质的量与消耗的氯气的物质的量相等,所以生成0.5 mol一氯甲烷需要0.5 mol氯气,生成0.5 mol二氯甲烷需要1 mol氯气,生成0.5 mol三氯甲烷需要1.5 mol氯气,生成0.5 mol四氯化碳需要2 mol氯气,所以总共消耗氯气的物质的量为0.5 mol+1 mol+1.5 mol+2 mol=5 mol。
14.取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是
A.反应过程中试管内黄绿色逐渐消失,试管壁上
有油珠产生
B.甲烷和Cl2反应后的产物有4种
C.盛放饱和食盐水的水槽底部不会有晶体析出
D.CH4和Cl2完全反应后液面上升,液体充满试管
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
Cl2被消耗后,黄绿色消失,生成的CH2Cl2、CHCl3、CCl4均为油状液体,所以试管壁上有油珠产生,A项正确;
CH4与Cl2反应生成4种有机物和1种无机物,共有5种产物,B项错误;
CH4与Cl2反应生成HCl,HCl溶于饱和食盐水会有NaCl晶体析出,C项错误;
取代产物CH2Cl2、CHCl3、CCl4是油状液体,而CH3Cl是气体,不溶于饱和食盐水,故液体不会充满试管,D项错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
15.如图所示,U形管的左端是被水和胶塞封闭的甲烷和氯气(体积比为1∶4)的混合气体,假设氯气在水中的溶解度可以忽略。将封闭有甲烷和氯气混合气体的一端放置在有光的地方,让混合气体缓慢地反应一段时间。
(1)假设甲烷与氯气充分反应,且只产生一种有机物,请写出其化学
方程式:__________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
因CH4和Cl2的体积之比为1∶4,若充分反应且只产生一种有机物,则CH4中的四个H原子可完全被取代,生成CCl4和HCl。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(2)经过几个小时的反应后,U形管右端的液面变化是______(填字母)。
A.升高 B.降低
C.不变 D.无法确定
B
甲烷和氯气在光照条件下发生取代反应生成的一氯甲烷为不溶于水的气体,其他三种有机产物均为油状液体,且生成的氯化氢气体易溶于水,故甲烷和氯气的反应为气体的物质的量减少的反应,会导致U形管右端液面降低,左端液面升高。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(3)若水中含有Na2SiO3,则在U形管左端会观察到的现象是___________
_________。
有白色胶状
因U形管左侧生成的HCl溶于水后发生反应:2HCl+Na2SiO3===H2SiO3↓+2NaCl,所以会观察到U形管左端有白色胶状沉淀生成。
沉淀生成
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(4)右端玻璃管的作用是__________。
平衡气压
在U形管右侧插入一支玻璃管的目的是连通大气,平衡气压。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
16.如图是某同学利用注射器设计的简易实验装置。甲注射器中注入10 mL CH4,同温同压下乙注射器中注入50 mL Cl2,将乙注射器中的气体推入甲注射器中,光照一段时间使气体在甲注射器中反应。
(1)下列是某同学预测的实验现象:
①气体最终变为无色
②实验过程中,甲注射器活塞向右移动
③甲注射器内壁有油珠
④产生火花
其中正确的是_______(填序号)。
②③
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
该注射器里氯气与甲烷的体积之比为5∶1,氯气过量,最终剩余的气体中仍有氯气,不会变为无色。该反应进行缓慢,不会产生火花。产物中只有氯化氢和一氯甲烷为气体,二氯甲烷、三氯甲烷和四氯甲烷为液体,所以气体的总物质的量减小,内部压强减小,甲注射器活塞向右移动。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(2)甲注射器中发生反应的化学反应类型为__________。
取代反应
甲烷分子中的四个氢原子可被氯原子逐一取代,故甲注射器中发生的是取代反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(3)反应后,甲注射器中剩余气体最好用_____(填字母)吸收。
A.水 B.氢氧化钠溶液
C.硝酸银溶液 D.饱和食盐水
B
剩余气体中含有氯气和氯化氢,最好用氢氧化钠溶液吸收。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(4)反应后,若将甲注射器中的物质推入盛有适量AgNO3溶液的小试管中会观察到____________________________;若再向其中滴入几滴紫色石蕊试液,观察到__________________。
液体分为两层,产生白色沉淀
溶液先变红后褪色
生成的HCl会与AgNO3反应生成AgCl白色沉淀,同时因CH2Cl2、CHCl3、CCl4不溶于水,可以看到液体分为两层;若加入几滴紫色石蕊试液,溶液会先变红后褪色。
返回
本课结束
专题8
第1课时
DIYIKESHI
甲烷的组成与结构 / 甲烷的化学性质 / 随堂演练 知识落实 / 课时对点练
天然气的利用 甲烷
专题8
核心素养
发展目标
1.认识甲烷的组成和结构特点。会书写甲烷的分子式、结构式及电子式,形成“结构决定性质”的观念,培养宏观辨识与微观探析的能力。
2.知道甲烷能发生氧化反应和取代反应,掌握取代反应的概念,能通过分析、推理等方法,判断有机物的取代反应,培养证据推理的能力。
内容索引
一、甲烷的组成与结构
二、甲烷的化学性质
随堂演练 知识落实
课时对点练
甲烷的组成与结构
一
1.甲烷
甲烷是一种 色、 味、 溶于水的气体,熔、沸点 、密度比空气 。甲烷是 的主要成分, 的水合物外形似冰,被称为“可燃冰”。
无
无
难
低
小
天然气
天然气
2.甲烷的组成与结构
(1)组成与结构
分子式 电子式 结构式 球棍模型
_____
CH4
(2)结构特点
碳原子位于中心,与4个氢原子形成完全相同的4个C—H共价键,相邻C—H共价键的夹角为109°28′,具有 空间结构。
正四面体
正误判断
(1)甲烷分子中碳原子最外层有4个电子,可以形成4个共价键( )
(2)已知甲烷为正四面体结构,可推知CCl4也为正四面体结构( )
(3)天然气就是纯净的甲烷气体( )
(4)16 g CH4分子中含有2NA个C—H键( )
(5)甲烷和四氯化碳的分子中各原子均达到8电子稳定结构( )
√
√
×
×
×
已知标准状况下,甲烷的密度是0.717 g·L-1。
(1)甲烷的相对分子质量是多少?
深度思考
提示 由M=ρ·22.4 L·mol-1得,M(甲烷)≈16 g·mol-1,即甲烷的相对分子质量为16。
(2)甲烷中含碳元素的质量分数为75%,含氢元素的质量分数为25%,求甲烷的分子式。
深度思考
应用体验
1.下列叙述与甲烷无关的是
A.天然气、沼气、可燃冰的主要成分
B.“西气东输”工程中运输的气体的主要成分
C.造成“光化学烟雾”的气体
D.煤矿中瓦斯爆炸
√
2.如图所示均能表示甲烷的分子结构,下列说法错误的是
A.Ⅰ将各原子看成了质点,为空间结构示意图
B.Ⅱ为电子式,表示甲烷分子中有8个电子
C.Ⅲ为球棍模型,棍代表甲烷分子内含有的共价键
D.Ⅳ为空间填充模型,能表示出甲烷的空间结构及各原子的相对大小
√
Ⅱ表示电子式,但略去了碳原子的内层电子,甲烷分子中应含有10个电子。
归纳总结
一个碳原子与其他4个原子以4个单键相结合时:
(1)如果这4个原子相同,分别在四面体的顶点上,则构成正四面体;
(2)如果这4个原子不相同,则分别在四面体的顶点上,但不是正四面体;
(3)无论这4个原子是否相同,都不可能在同一平面上,并且最多有3个原子共面。
返回
甲烷的化学性质
二
1.稳定性
CH4性质稳定,不与 、 、 等物质反应。
2.氧化反应
点燃甲烷气体,观察燃烧现象,并检验燃烧产物。
(1)猜想:根据甲烷(CH4)的组成,其燃烧后可能会生成 和 。
强酸
强碱
KMnO4
CO2
H2O
(2)实验验证
燃烧现象 检验产物 方法 现象 结论
___________ 在火焰上方罩一个干燥的烧杯 烧杯内壁有水珠产生 _________
在火焰上方罩一个涂有澄清石灰水的烧杯 烧杯内壁变浑浊 ___________
_____
淡蓝色火焰
生成了水
生成了二氧
化碳
(3)实验结论
经测定,1 mol CH4完全燃烧生成 和 ,放出890 kJ的热,热化学方程式为 ,因此,甲烷是一种高效而洁净的燃料。
液态水
二氧化碳
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
3.取代反应
(1)实验探究
实验装置与操作
用排饱和食盐水法收集 体积的氯气和 体积的甲烷
气体,用灯光照射瓶中的混合气体
实验 现象 集气瓶内黄绿色气体颜色逐渐变浅,集气瓶内壁有_________
出现,瓶中有少量白雾,且瓶内液面 ,水槽中有固体析出
实验 结论 CH4与Cl2需在 条件下发生化学反应,有关化学方程式为
CH4+Cl2 ;
CH3Cl+Cl2 ;
CH2Cl2+Cl2 ;
CHCl3+Cl2 ———————————————————————
油状液体
上升
光照
CH3Cl(一氯甲烷)+HCl
CH2Cl2(二氯甲烷)+HCl
CHCl3(三氯甲烷或氯仿)+HCl
CCl4(四氯甲烷或四氯化碳)+HCl
特别提醒:
①水溶性:CH3Cl、CH2Cl2、CHCl3、CCl4均不溶于水。
②状态:常温下除CH3Cl是气体,其余三种均为油状液体。
(2)取代反应
①概念:有机化合物分子中的某种原子(或原子团)被另一种__________
所取代的反应。
②特点:
a.反应条件,在光照条件下,甲烷与气态纯卤素单质发生取代反应。
b.连续反应,甲烷分子中的氢原子被氯原子逐步取代,反应一旦开始,后续反应立即进行,且各步反应可同时进行。
③因为有机化学反应的副产物较多,所以写化学方程式时用“→”连接反应物和目标产物。
原子(或原
子团)
正误判断
(1)甲烷性质稳定,与任何氧化剂都不反应( )
(2)CH4和Cl2按体积比1∶1混合,发生取代反应生成的产物只有两种( )
(3)CH4和Cl2发生取代反应时,每生成1 mol HCl,则有1 mol Cl2参加反应
( )
(4)CH4分子为正四面体结构,因此其生成物CH3Cl、CH2Cl2、CHCl3和CCl4都为正四面体结构( )
(5)取代反应和置换反应都是物质中某些原子或原子团被其他原子或原子团代替,因此本质相同( )
×
×
√
×
×
1.若甲烷分子中的一个氢原子被氯原子取代,生成的CH3Cl还是四面体结构吗?
深度思考
提示 CH3Cl中3个H和1个Cl仍分别位于四面体的4个顶点,仍为四面体结构,但不是正四面体结构。
2.甲烷中每有1 mol氢原子被取代,消耗Cl2的物质的量是多少?
深度思考
提示 1 mol。
应用体验
1.下列物质在一定条件下能与甲烷发生取代反应的是
A.氯气 B.酸性高锰酸钾溶液
C.氢氧化钠溶液 D.溴水
√
A项,氯气在光照条件下与甲烷可以发生取代反应;
B项,酸性高锰酸钾溶液不能氧化甲烷,也不能与甲烷发生取代反应;
C项,氢氧化钠溶液与甲烷不反应;
D项,溴水与甲烷不反应。
2.在光照条件下,将1 mol CH4与Cl2反应,得到四种有机产物CH3Cl、CH2Cl2、CHCl3、CCl4的物质的量之比为1∶2∶3∶4,则消耗Cl2的物质的量为
A.0.5 mol B.1.25 mol
C.2.5 mol D.3 mol
√
四种有机产物的物质的量之比为n(CH3Cl)∶n(CH2Cl2)∶n(CHCl3)∶n(CCl4)
=1∶2∶3∶4,则四种取代物的物质的量分别为n(CH3Cl)=0.1 mol,n(CH2Cl2)=0.2 mol,n(CHCl3)=0.3 mol,n(CCl4)=0.4 mol,发生取代反应时,一半的Cl进入HCl,消耗氯气的物质的量为0.1 mol+2×
0.2 mol+3×0.3 mol+4×0.4 mol=3 mol。
归纳总结
甲烷的取代反应
返回
随堂演练 知识落实
1.甲烷是天然气的主要成分,是一种高效、低耗、污染小的清洁能源。下列有关甲烷的说法正确的是
①甲烷是一种正四面体结构的分子
②甲烷分子中所有原子均满足最外层8电子结构
③0.5 mol CH4完全燃烧时消耗1 mol O2
④1 mol CH4完全生成CCl4,最多消耗2 mol Cl2
A.①② B.③④ C.①③ D.②④
√
1
2
3
4
1
2
3
4
①甲烷是一种正四面体结构的分子,正确;
③1 mol CH4完全燃烧时消耗2 mol O2,则0.5 mol CH4完全燃烧时消耗1 mol O2,正确;
④根据取代反应的特点,1 mol CH4完全生成CCl4,最多消耗4 mol Cl2,错误。
2.(2022·成都龙泉驿区教育科学研究院高一期中)若甲烷与氯气的体积之比为1∶1,则得到的产物为
A.CH3Cl HCl
B.CCl4 HCl
C.CH3Cl CH2Cl2
D.CH3Cl CH2Cl2 CHCl3 CCl4 HCl
√
1
2
3
4
1
2
3
4
3.将标准状况下的11.2 L甲烷和22.4 L氧气混合点燃,恢复到原状态后,气体的体积为
A.11.2 L B.22.4 L C.33.6 L D.44.8 L
√
1
2
3
4
CH4+2O2 CO2+2H2O(l)
起始/mol 0.5 1 0 0
转化/mol 0.5 1 0.5 1
最终/mol 0 0 0.5 1
注意CO2为气体,H2O为液体。
4.(2018·全国卷Ⅱ,9)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是
1
2
3
4
√
1
2
3
4
甲烷与氯气在光照条件下发生取代反应,黄绿色的氯气减少,因此试管内气体颜色逐渐变浅;反应生成的HCl极易溶于水,使试管内气体压强减小,因此试管内液面上升;生成的CH2Cl2、CHCl3、CCl4均为无色
油状液体,附着在试管壁上,因此试管壁上出现无色油状液滴;生成的HCl气体遇到水蒸气溶解生成盐酸小液滴,形成白雾,因此试管中有少量白雾。综合上述现象,答案选D项。
返回
课时对点练
题组一 甲烷的组成与结构
1.下列关于甲烷的说法错误的是
A.分子式:CH4
B.可作为清洁燃料
C.球棍模型:
D.可使酸性KMnO4溶液褪色
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
甲烷的分子式为CH4,故A正确;
甲烷完全燃烧生成二氧化碳和水,不产生空气污染物,可作为清洁燃料,故B正确;
甲烷为正四面体结构,碳原子的半径大于氢原子的半径,球棍模型为
,故C正确;
甲烷化学性质稳定,不能使酸性KMnO4溶液褪色,故D错误。
2.下列关于甲烷的说法不正确的是
A.甲烷分子具有正四面体结构
B.甲烷是无色、无味的气体
C.甲烷是最简单的有机化合物
D.甲烷能使溴水褪色
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
通常情况下,甲烷是一种无色、无味的气体,难溶于水,密度比空气小,故B正确;
仅含碳氢单键的甲烷不能与溴水反应,溶液不会褪色,故D错误。
3.下图是CH4、CCl4、CH3Cl分子的球棍模型,下列说法正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
A.CH4、CCl4和CH3Cl都是正四面体结构
B.CH4、CCl4都是正四面体结构
C.CH4和CCl4中的化学键完全相同
D.CH4、CCl4的结构相同,性质也相同
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
CCl4与CH4的分子结构相似,为正四面体结构,CH3Cl中的C—H键和C—Cl键不同,不是正四面体结构,而是四面体结构。
4.(2022·江西省临川第二中学高一期中)能证明CH4分子的空间结构为正四面体形而非平面正方形的事实是
A.CH2Cl2只有一种结构
B.CH3Cl分子只有一种结构
C.C原子距离四个H原子的距离一样
D.CH4分子中的四个碳氢键一样
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
若CH4分子的空间结构为平面正方形,CH2Cl2应有2种结构,而实际上CH2Cl2只有一种结构,说明CH4分子的空间结构为正四面体形,故选A;
无论CH4分子的空间结构为正四面体形还是平面正方形,CH3Cl分子都只有一种结构,故不选B;
无论CH4分子的空间结构为正四面体形还是平面正方形,C原子距离四个H原子的距离一样,故不选C;
无论CH4分子的空间结构为正四面体形还是平面正方形,CH4分子中的四个碳氢键一样,故不选D。
题组二 甲烷的性质
5.在我国的南海、东海海底已发现天然气(含甲烷等)的水合物,它易燃烧,外形似冰,被称为可燃冰。可燃冰的开采,有助于缓解人类面临的能源危机。下列说法正确的是
①甲烷是“西气东输”的主要成分 ②在相同条件下,甲烷的密度大于空气的密度 ③甲烷难溶于水 ④可燃冰是一种极具潜力的能源
A.①②③ B.②③④ C.①③④ D.①②④
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
6.(2022·河北石家庄二十三中高一期中)最新研究发现,火星大气层中含有甲烷。下列说法错误的是
A.甲烷是一种共价化合物
B.可燃冰释放出的气体中含有甲烷
C.甲烷能发生氧化反应和取代反应
D.等物质的量的CH4与Cl2在光照下的反应产物只有CH3Cl和HCl
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
甲烷是由碳元素和氢元素组成的共价化合物,A项正确;
可燃冰是由水和甲烷在高压、低温条件下形成的类冰状结晶物质,可燃冰释放出的气体为甲烷,B项正确;
等物质的量的CH4和Cl2在光照下发生取代反应,属于连锁反应,生成4种氯代产物,同时生成HCl,D项错误。
7.下列反应中,属于取代反应的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
CaCO3高温下生成CaO和CO2,属于分解反应,A不符合题意;
Zn与硫酸反应属于置换反应,B不符合题意;
CH4与O2反应属于氧化反应,C不符合题意;
CH3CH3与Cl2反应生成CH3CH2Cl,可看成是CH3CH3中1个H原子被Cl原子取代,属于取代反应,D符合题意。
8.(2022·上海市延安中学高一期末)1 mol甲烷和1 mol氯气在光照条件下充分反应,产物中物质的量最多的是
A.CH3Cl B.HCl
C.CH2Cl2 D.CHCl3
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
甲烷和氯气在光照条件下发生取代反应,可生成有机物CH3Cl、CH2Cl2、CHCl3、CCl4,每一步反应都生成HCl,所以生成物中物质的量最多的是HCl,故B正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
9.下列关于甲烷的说法正确的是
A.甲烷是含碳元素质量分数最高的有机物
B.1 mol甲烷与1 mol氯气反应恰好生成1 mol一氯甲烷
C.CH2Cl2为正四面体结构
D.沼气的主要成分是甲烷,常用作清洁燃料
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
有机物中C原子呈四价,1个C原子最多结合4个H原子,甲烷是含氢元素质量分数最高的有机物,A错;
1 mol甲烷与1 mol氯气发生取代反应,伴随副反应的发生,生成多种氯代物,生成的一氯甲烷的物质的量小于1 mol,B错;
甲烷分子中,1个碳原子与4个氢原子形成共价键,4个共价键完全相同,且向空间4个方向伸展,所以甲烷为正四面体结构,而CH2Cl2相当于甲烷分子中的2个氢原子替换成2个氯原子,所以不是正四面体结构,应为四面体结构,C错。
10.将甲烷与一定量的氯气混合于一试管中,倒立于盛有饱和食盐水的水槽中(如图所示),对于此反应,有关叙述不正确的是
A.该反应的生成物只有四种
B.该反应的条件是光照
C.该反应结束后试管内液面上升(冷却到室温)
D.该反应属于取代反应
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
甲烷和氯气反应的生成物有一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢5种,故A错误;
该反应氯气中的氯原子取代了甲烷中的氢原子,属于取代反应,反应条件是光照,故B、D正确;
该反应生成了液态的二氯甲烷、三氯甲烷、四氯化碳,使气体的量减少,且生成的氯化氢气体极易溶于水,试管内压强减小,液面上升(冷却到室温),故C正确。
11.(2022·辽宁同泽高中高一阶段练习)以下关于甲烷的说法中,正确的是
①一氯甲烷分子具有四面体结构 ②二氯甲烷有两种 ③甲烷与Cl2在光照条件下发生取代,取代1 mol H需0.5 mol Cl2 ④甲烷分子中四个C—H键,任意两个共价键之间的键角均相等
A.②③④ B.②③
C.①④ D.①③
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
一氯甲烷分子为甲烷中一个H原子被Cl取代,CH3Cl的结构不对称,为四面体结构,故①正确;
甲烷为正四面体结构,所以二氯甲烷只有一种,故②错误;
甲烷与氯气发生一氯取代的化学方程式为CH4+Cl2 CH3Cl+HCl,取代1 mol H需1 mol Cl2,故③错误;
甲烷分子中四个碳氢键完全相同,任意两个碳氢键之间的键角均相等,故④正确。
12.鉴别甲烷、一氧化碳和氢气三种无色气体的方法是
A.通入溴水中→通入澄清石灰水中
B.点燃→罩上涂有澄清石灰水的烧杯
C.点燃→罩上干燥的冷烧杯→罩上涂有澄清石灰水的烧杯
D.点燃→罩上涂有澄清石灰水的烧杯→通入溴水中
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
13.标准状况下,44.8 L CH4与一定量Cl2在光照条件下发生取代反应,待反应完全后,测得四种有机取代产物的物质的量相等,则消耗Cl2的物质的量为
A.1 mol B.2 mol
C.4 mol D.5 mol
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
标准状况下,44.8 L CH4的物质的量为2 mol,2 mol甲烷完全与氯气发生取代反应,生成相同物质的量的四种取代物,所以每种取代物的物质的量是0.5 mol,在甲烷和氯气的取代反应中,被取代的氢原子的物质的量与消耗的氯气的物质的量相等,所以生成0.5 mol一氯甲烷需要0.5 mol氯气,生成0.5 mol二氯甲烷需要1 mol氯气,生成0.5 mol三氯甲烷需要1.5 mol氯气,生成0.5 mol四氯化碳需要2 mol氯气,所以总共消耗氯气的物质的量为0.5 mol+1 mol+1.5 mol+2 mol=5 mol。
14.取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是
A.反应过程中试管内黄绿色逐渐消失,试管壁上
有油珠产生
B.甲烷和Cl2反应后的产物有4种
C.盛放饱和食盐水的水槽底部不会有晶体析出
D.CH4和Cl2完全反应后液面上升,液体充满试管
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
Cl2被消耗后,黄绿色消失,生成的CH2Cl2、CHCl3、CCl4均为油状液体,所以试管壁上有油珠产生,A项正确;
CH4与Cl2反应生成4种有机物和1种无机物,共有5种产物,B项错误;
CH4与Cl2反应生成HCl,HCl溶于饱和食盐水会有NaCl晶体析出,C项错误;
取代产物CH2Cl2、CHCl3、CCl4是油状液体,而CH3Cl是气体,不溶于饱和食盐水,故液体不会充满试管,D项错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
15.如图所示,U形管的左端是被水和胶塞封闭的甲烷和氯气(体积比为1∶4)的混合气体,假设氯气在水中的溶解度可以忽略。将封闭有甲烷和氯气混合气体的一端放置在有光的地方,让混合气体缓慢地反应一段时间。
(1)假设甲烷与氯气充分反应,且只产生一种有机物,请写出其化学
方程式:__________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
因CH4和Cl2的体积之比为1∶4,若充分反应且只产生一种有机物,则CH4中的四个H原子可完全被取代,生成CCl4和HCl。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(2)经过几个小时的反应后,U形管右端的液面变化是______(填字母)。
A.升高 B.降低
C.不变 D.无法确定
B
甲烷和氯气在光照条件下发生取代反应生成的一氯甲烷为不溶于水的气体,其他三种有机产物均为油状液体,且生成的氯化氢气体易溶于水,故甲烷和氯气的反应为气体的物质的量减少的反应,会导致U形管右端液面降低,左端液面升高。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(3)若水中含有Na2SiO3,则在U形管左端会观察到的现象是___________
_________。
有白色胶状
因U形管左侧生成的HCl溶于水后发生反应:2HCl+Na2SiO3===H2SiO3↓+2NaCl,所以会观察到U形管左端有白色胶状沉淀生成。
沉淀生成
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(4)右端玻璃管的作用是__________。
平衡气压
在U形管右侧插入一支玻璃管的目的是连通大气,平衡气压。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
16.如图是某同学利用注射器设计的简易实验装置。甲注射器中注入10 mL CH4,同温同压下乙注射器中注入50 mL Cl2,将乙注射器中的气体推入甲注射器中,光照一段时间使气体在甲注射器中反应。
(1)下列是某同学预测的实验现象:
①气体最终变为无色
②实验过程中,甲注射器活塞向右移动
③甲注射器内壁有油珠
④产生火花
其中正确的是_______(填序号)。
②③
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
该注射器里氯气与甲烷的体积之比为5∶1,氯气过量,最终剩余的气体中仍有氯气,不会变为无色。该反应进行缓慢,不会产生火花。产物中只有氯化氢和一氯甲烷为气体,二氯甲烷、三氯甲烷和四氯甲烷为液体,所以气体的总物质的量减小,内部压强减小,甲注射器活塞向右移动。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(2)甲注射器中发生反应的化学反应类型为__________。
取代反应
甲烷分子中的四个氢原子可被氯原子逐一取代,故甲注射器中发生的是取代反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(3)反应后,甲注射器中剩余气体最好用_____(填字母)吸收。
A.水 B.氢氧化钠溶液
C.硝酸银溶液 D.饱和食盐水
B
剩余气体中含有氯气和氯化氢,最好用氢氧化钠溶液吸收。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(4)反应后,若将甲注射器中的物质推入盛有适量AgNO3溶液的小试管中会观察到____________________________;若再向其中滴入几滴紫色石蕊试液,观察到__________________。
液体分为两层,产生白色沉淀
溶液先变红后褪色
生成的HCl会与AgNO3反应生成AgCl白色沉淀,同时因CH2Cl2、CHCl3、CCl4不溶于水,可以看到液体分为两层;若加入几滴紫色石蕊试液,溶液会先变红后褪色。
返回
本课结束
专题8
