2.1.1 共价键 课件(共23张PPT)
文档属性
| 名称 | 2.1.1 共价键 课件(共23张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-12 00:00:00 | ||
图片预览








文档简介
(共23张PPT)
第1课时 共价键
知识回顾:
1. 什么是共价键?
2. 通常哪些元素之间可以形成共价键?
3. 共价键是如何形成的?
类型:
共价键
极性共价键
非极性共价键
4. 用电子式表示共价键的形成过程:HCl、Cl2
学与问
你能用电子式表示H2、Cl2分子的形成过程吗?
一、共价键的形成
用电子式表示H2、Cl2分子的形成过程 我们必修中已学过。本书中我们刚学了电子云和原子轨道,今天我们将从电子云和原子轨道的角度进一步理解共价键。
1. σ键的形成
现代物质结构理论认为 共价键的形成是由于成键原子电子云的重叠
H
H
(1)(s-s σ键)
电子云在两个原子核间重叠,意味着电子出现在核间的概率增大,电子带负电,因而可以形象的说,核间电子好比在核间架起一座带负电的桥梁,把带正电的两个原子核“黏结”在一起了。
用电子云来描述共价键的形成过程
σ键的特征:以形成化学键的两原子核的连线做为轴旋转操作,共价键电子云的图形不变,称为轴对称。
(2)p-p σ键的形成
Cl
Cl
Cl Cl
思考与交流
请你用电子式表示HCl分子的形成过程;
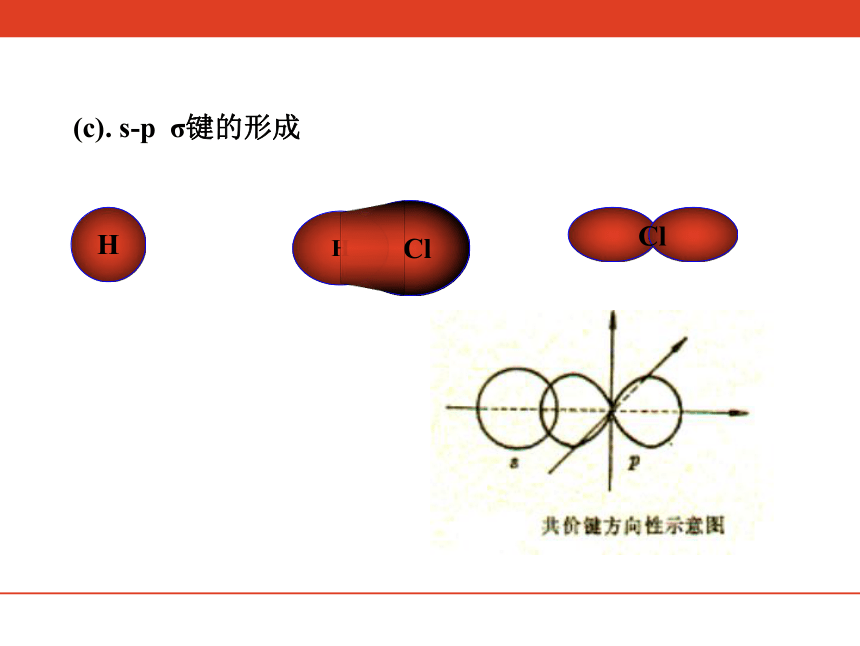
(c). s-p σ键的形成
H
Cl
Cl
H
σ键:“头碰头”
x
s—s
x
px—s
x
px—px
轴对称
形成σ键的电子称为σ电子。
2. π键的形成
键特点:两个原子轨道以平行或“肩并肩” 方式重叠;原子重叠的部分分别位于两原子核构成平面的两侧,如果以它们之间包含原子核的平面为镜面,它们互为镜像,称为镜像对称
由于 键重叠程度要比 键小,所以 键的强度要比 键大。
“肩并肩”
形成π键的电子称为π电子。
由原子轨道相互重叠形成的σ键和π键
总称价键轨道。
价键轨道
描述价键轨道的理论称为价键理论。
价键理论的要点
1.电子配对原理
2.最大重叠原理
两原子各自提供1个自旋方向相反的未成对电子彼此配对。
两个原子轨道重叠部分越大,两核间电子的概率密度越大,形成的共价键越牢固,分子越稳定。
思考与交流
能否有H3、H2Cl、Cl3分子的形成?
二、共价键的特征
1. 共价键具有饱和性
按照价键理论的电子配对原理,一个原子有几个未成对电子,便可和几个自旋相反的电子配对成键,这就共价键的“饱和性”。H 原子、Cl原子都只有一个未成对电子,因而只能形成H2、HCl、Cl2分子,不能形成H3、H2Cl、Cl3分子
2. 共价键具有方向性
按照价键理论的电子云最大重叠原理,P电子云
沿X、 Y 、 Z轴方向伸展。当电子云沿X、 Y 、 Z
轴方向重叠时,重叠程度最大。
小结
σ键 π键
成键方向
电子云形状
牢固程度
成键判断规律
沿轴方向“头碰头”
平行方向“肩并肩”
轴对称
镜像对称
强度大,不易断裂
强度较小,易断裂
共价单键是σ键,共价双键中一个是 σ键,另一个是π键,共价三键中一个是σ键,另两个为π键。
类型
特征
乙烷、乙烯和乙炔分子中的共价键分别有几个σ键和几个π键组成?
乙烷分子中由7个σ键组成;乙烯分子中由5个σ键和1个π键组成;乙炔分子中由3个σ键和2个π键组成。
1. 氮分子中的化学键是( )
A. 3个σ键 B. 1个σ键,2个π键
C. 3个π键 D. 1个σ键,1个π键
B
随堂练习
2. 下列说法中正确的是( )
A. p轨道之间以“肩并肩”重叠可形成σ键
B. p轨道之间以“头对头”重叠可形成π键
C. s和p轨道以“头对头”重叠可形成σ键
D. 共价键是两个原子轨道以“头对头”重叠形成的
C
3. 在氯化氢分子中,形成共价键的原子轨道是( )
A. 氯原子的2p轨道和氢原子的1s轨道
B. 氯原子的2p轨道和氢原子的2p轨道
C. 氯原子的3p轨道和氢原子的1s轨道
D. 氯原子的3p轨道和氢原子的3p轨道
C
7
3
4. 某有机物的结构简式为 :
CH2=CHC≡CH
则分子中 有 个σ键, 个π键
我的收获是.............
1. σ键与π键的形成方式有何不同,有何形象的比喻?
2. σ键与π键在对称上有何不同
3. σ键的类型
4. 哪些共价键是σ键,哪些共价键是π键
5. 什么是价键轨道
本节内容结束
第1课时 共价键
知识回顾:
1. 什么是共价键?
2. 通常哪些元素之间可以形成共价键?
3. 共价键是如何形成的?
类型:
共价键
极性共价键
非极性共价键
4. 用电子式表示共价键的形成过程:HCl、Cl2
学与问
你能用电子式表示H2、Cl2分子的形成过程吗?
一、共价键的形成
用电子式表示H2、Cl2分子的形成过程 我们必修中已学过。本书中我们刚学了电子云和原子轨道,今天我们将从电子云和原子轨道的角度进一步理解共价键。
1. σ键的形成
现代物质结构理论认为 共价键的形成是由于成键原子电子云的重叠
H
H
(1)(s-s σ键)
电子云在两个原子核间重叠,意味着电子出现在核间的概率增大,电子带负电,因而可以形象的说,核间电子好比在核间架起一座带负电的桥梁,把带正电的两个原子核“黏结”在一起了。
用电子云来描述共价键的形成过程
σ键的特征:以形成化学键的两原子核的连线做为轴旋转操作,共价键电子云的图形不变,称为轴对称。
(2)p-p σ键的形成
Cl
Cl
Cl Cl
思考与交流
请你用电子式表示HCl分子的形成过程;
(c). s-p σ键的形成
H
Cl
Cl
H
σ键:“头碰头”
x
s—s
x
px—s
x
px—px
轴对称
形成σ键的电子称为σ电子。
2. π键的形成
键特点:两个原子轨道以平行或“肩并肩” 方式重叠;原子重叠的部分分别位于两原子核构成平面的两侧,如果以它们之间包含原子核的平面为镜面,它们互为镜像,称为镜像对称
由于 键重叠程度要比 键小,所以 键的强度要比 键大。
“肩并肩”
形成π键的电子称为π电子。
由原子轨道相互重叠形成的σ键和π键
总称价键轨道。
价键轨道
描述价键轨道的理论称为价键理论。
价键理论的要点
1.电子配对原理
2.最大重叠原理
两原子各自提供1个自旋方向相反的未成对电子彼此配对。
两个原子轨道重叠部分越大,两核间电子的概率密度越大,形成的共价键越牢固,分子越稳定。
思考与交流
能否有H3、H2Cl、Cl3分子的形成?
二、共价键的特征
1. 共价键具有饱和性
按照价键理论的电子配对原理,一个原子有几个未成对电子,便可和几个自旋相反的电子配对成键,这就共价键的“饱和性”。H 原子、Cl原子都只有一个未成对电子,因而只能形成H2、HCl、Cl2分子,不能形成H3、H2Cl、Cl3分子
2. 共价键具有方向性
按照价键理论的电子云最大重叠原理,P电子云
沿X、 Y 、 Z轴方向伸展。当电子云沿X、 Y 、 Z
轴方向重叠时,重叠程度最大。
小结
σ键 π键
成键方向
电子云形状
牢固程度
成键判断规律
沿轴方向“头碰头”
平行方向“肩并肩”
轴对称
镜像对称
强度大,不易断裂
强度较小,易断裂
共价单键是σ键,共价双键中一个是 σ键,另一个是π键,共价三键中一个是σ键,另两个为π键。
类型
特征
乙烷、乙烯和乙炔分子中的共价键分别有几个σ键和几个π键组成?
乙烷分子中由7个σ键组成;乙烯分子中由5个σ键和1个π键组成;乙炔分子中由3个σ键和2个π键组成。
1. 氮分子中的化学键是( )
A. 3个σ键 B. 1个σ键,2个π键
C. 3个π键 D. 1个σ键,1个π键
B
随堂练习
2. 下列说法中正确的是( )
A. p轨道之间以“肩并肩”重叠可形成σ键
B. p轨道之间以“头对头”重叠可形成π键
C. s和p轨道以“头对头”重叠可形成σ键
D. 共价键是两个原子轨道以“头对头”重叠形成的
C
3. 在氯化氢分子中,形成共价键的原子轨道是( )
A. 氯原子的2p轨道和氢原子的1s轨道
B. 氯原子的2p轨道和氢原子的2p轨道
C. 氯原子的3p轨道和氢原子的1s轨道
D. 氯原子的3p轨道和氢原子的3p轨道
C
7
3
4. 某有机物的结构简式为 :
CH2=CHC≡CH
则分子中 有 个σ键, 个π键
我的收获是.............
1. σ键与π键的形成方式有何不同,有何形象的比喻?
2. σ键与π键在对称上有何不同
3. σ键的类型
4. 哪些共价键是σ键,哪些共价键是π键
5. 什么是价键轨道
本节内容结束
