人教版九年级化学下册第九单元课题3《溶液的浓度》(课件26页)
文档属性
| 名称 | 人教版九年级化学下册第九单元课题3《溶液的浓度》(课件26页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 27.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-15 00:00:00 | ||
图片预览






文档简介
课题3 溶液的浓度
第1课时 溶质的质量分数
1. 认识溶质的质量分数的概念;能进行溶质质量分数的简单计算。
2.学会配制一定溶质质量分数溶液的方法。
3. 学会严谨求实的科学学习方法,培养具体问题具体分析的能力。
素养目标
导入新课
生理盐水对大家来说并不陌生,它是不是溶液?
标签上的这个0.9%是什么意思?
这个0.9%是指溶液的浓度,那么如何来定量表示溶液的组成?
两杯等量的水中分别加入1块和2块大小相同的方糖,完全溶解后,两杯糖水的甜度一样吗?如何定量表示溶液的浓稀?
导入新课
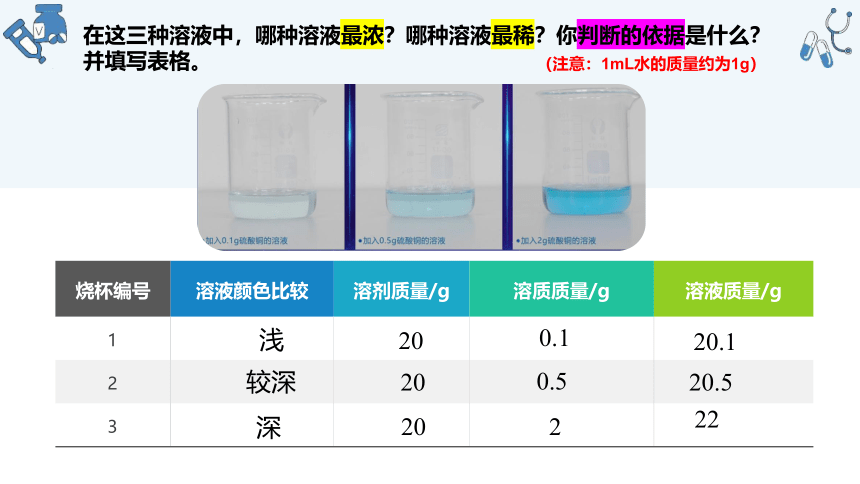
实验 9 – 7 配制三种浓稀不同的硫酸铜溶液
在室温下,向三个小烧杯中各加入20mL水,然后分别加入0.1g、0.5g、2g无水硫酸铜,用玻璃棒搅拌,使硫酸铜全部溶解,比较三种硫酸铜溶液。
烧杯编号
溶液颜色比较
溶剂质量/g
溶质质量/g
溶液质量/g
1
2
3
浅
较深
深
20
20
20
0.1
0.5
2
20.1
20.5
22
在这三种溶液中,哪种溶液最浓?哪种溶液最稀?你判断的依据是什么?并填写表格。
(注意:1mL水的质量约为1g)
对有颜色的溶液来说,可以根据颜色的深浅区分溶液是浓还是稀。但这种方法比较粗略,特别是无色溶液,不能准确地表明一定量的溶液里究竟含有多少溶质。
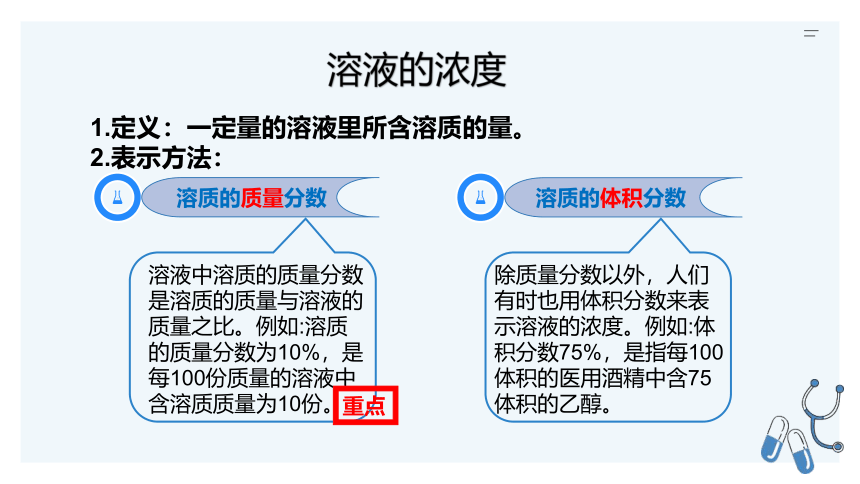
溶液的浓度
1.定义:一定量的溶液里所含溶质的量。
2.表示方法:
溶质的质量分数
溶质的体积分数
溶液中溶质的质量分数是溶质的质量与溶液的质量之比。例如:溶质的质量分数为10%,是每100份质量的溶液中含溶质质量为10份。
除质量分数以外,人们有时也用体积分数来表示溶液的浓度。例如:体积分数75%,是指每100体积的医用酒精中含75体积的乙醇。
重点
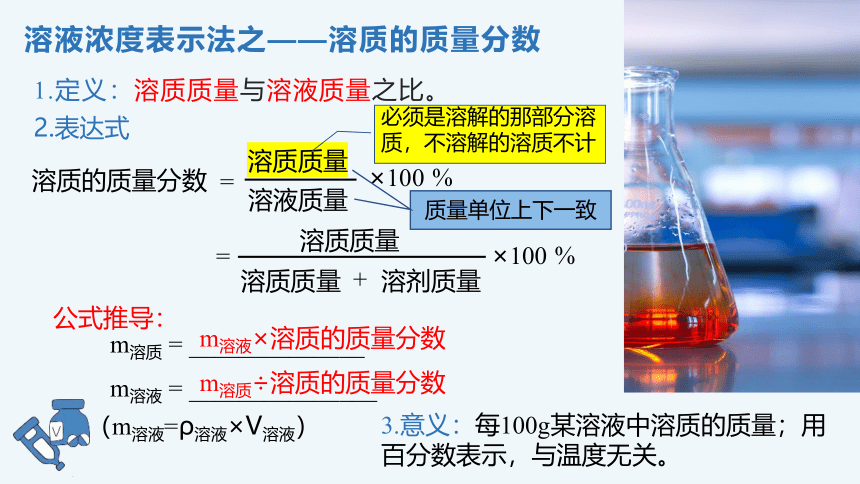
1.定义:溶质质量与溶液质量之比。
溶液浓度表示法之——溶质的质量分数
2.表达式
%
×100
+
=
溶剂质量
溶质质量
溶质质量
=
溶液质量
溶质质量
溶质的质量分数
%
×100
公式推导:
m溶质 = ______________
m溶液 = _______________
m溶液×溶质的质量分数
m溶质÷溶质的质量分数
3.意义:每100g某溶液中溶质的质量;用百分数表示,与温度无关。
必须是溶解的那部分溶质,不溶解的溶质不计
(m溶液=ρ溶液×V溶液)
质量单位上下一致
思考与交流
食盐的质量占整个溶液质量的5%
每5g食盐溶于95g水形成的溶液
100g食盐溶液中含有食盐5g
m食盐:m水:m食盐溶液
=5:95:100
“5%的NaCl溶液”的含义
练一练
在实验9-7中,三种硫酸铜溶液中溶质的质量分数各是多少?把计算结果填在表中。
烧杯编号
溶液颜色比较
溶剂质量/g
溶质质量/g
溶液质量/g
溶质的质量分数
1
浅
20
0.1
20.1
2
较深
20
0.5
20.5
3
深
20
2.0
22.0
=
溶液质量
溶质质量
溶质的质量分数
%
×100
0.5%
2.44%
9.09%
{5940675A-B579-460E-94D1-54222C63F5DA}溶质质量/g
溶剂(水)质量/g
现象
溶液中溶质的质量分数
10
90
20
80
10%
20%
完全溶解
完全溶解
实验 9 – 8 配制两种质量分数不同的氯化钠溶液
实验 9 – 8
质量分数与溶解度的关系
已知20oC时,氯化钠的溶解度是36g。有人说“20oC时氯化钠饱和溶液中溶质的质量分数为36%。”这种说法对吗?为什么?
温度
溶质的质量
溶剂的质量
溶液的质量
20℃
36g
100g
100g+36g
36g
100g+36g
100%
×
=26.5%
不对,质量分数=
区别?
溶解度 ?
溶质的质量分数 ?
概念 ?
一定温度时,100g溶剂中最多溶解溶质的质量 ?
任意溶液中,溶质质量与溶液质量之比 ?
应用范围?
m溶质与m溶剂 ?
m溶质与m溶液 ?
条件 ?
一定温度
不定温度 ?
状态 ?
饱和状态 ?
可饱和,可不饱和 ?
单位 ?
g ?
无单位 ?
溶解度S
100g+溶解度S
×????????????%
?
饱和溶液中的
溶质的质量分数
=
在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?
例题1
=126Kg
【解】
= 溶液质量×溶质的质量分数
=150Kg×6%
=24Kg
溶剂质量
=溶液质量-溶质的质量
=150Kg-24Kg
答:配制150kg质量分数为16%的氯化钠溶液需24 kg氯化钠和126 kg水。
=
溶液质量
溶质质量
溶质的质量分数
%
×100
溶质质量
解析:先利用溶解度判断溶液是否饱和,未溶解不计入
18g
即m溶质=18g,m溶液=68g
20℃时,NaCl的溶解度是36克。现有50克水放入20克NaCl,求:所得溶液的溶质质量分数。
例题2
现有一瓶98%的浓硫酸,你能帮我将它变成质量分数为20%的硫酸吗?
溶液的稀释
1.实质:溶液稀释前后溶质的质量不变。
2.表达式:
m×a%=(m+c)×b%
稀释前溶液的溶质质量分数
稀释后溶液的溶质质量分数
稀释前溶液的质量
加水的质量
3.注意事项:
①所设的物理量是质量;
②未知量Χ后不带单位;
③解题过程中数字后写单位;
④最后要写答。
化学实验室现在有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?
例题3
溶液稀释前后,溶质的质量不变。
稀释公式:m浓×c浓% = m稀×c稀% =(m浓+m水)×c稀%
解:设需要加水的质量为x
50g×98% =(50g+x) ×20%
x = 245g
答:需要水的质量为195g。
法二:
解:设稀释后溶液的质量为x
100g × 98% = x × 20%
x = 245g
需要水的质量=245g-50g=195g
答:需要水的质量为195g。
法一:
将溶质的质量分数运用于化学方程式的计算
【例题4】 100g某硫酸溶液恰好与13g锌完全反应,试计算这种硫酸中溶质的质量分数。
解:设这种硫酸中溶质的质量为x。
Zn + H2SO4 = ZnSO4 + H2↑
65 98
13g x
13g x
65 98
x = 19.6 g
溶质的质量分数 = × 100% =19.6%
19.6g
100g
答:这种硫酸溶液中溶质的质量分数为19.6%。
拓展延伸
生命之水
●Spirytus Rektyfikowany是一款原产于波兰的伏特加,被西方人称为“生命之水”。
●经过了反复70回以上的蒸馏,达到96%的酒精度数,是世界上纯度最高的烈酒。
●白酒的"度数”指的是白酒中酒精的含量。这里的含量不是指质量分数,而是体积分数。
●例如: 96度(96°)的酒表示100 mL酒中含有96mL
酒精,体积分数也是一种表示溶液组成的方法。
课堂小结
溶质的质量分数
简单计算
概念
溶质质量与溶液质量之比
溶质的质量分数=
溶质质量
溶液质量
100%
×
公式
溶液的稀释
溶质质量分数的简单计算
随堂训练
1. 对“10%的氯化钠溶液”含义的解释错误的是( )
A. 100 g氯化钠溶液中溶解了10 g氯化钠
B. 100 g水中溶解了10 g氯化钠
C. 将10 g氯化钠溶解于90 g水中得到的溶液
D. 溶液中氯化钠与水的质量比为1 ∶9
B
随堂训练
2. 现配制50 g质量分数为10%的氢氧化钠溶液,需称量氢氧化钠的质量为( )
A. 10 g B. 5 g C. 0.5 g D. 15 g
B
3.现需要将溶质质量分数为40%的氢氧化钠溶液稀释为40 g溶质质量分数为5%的氢氧化钠溶液。此时,需要水的体积为( )
A.38 mL B.36 mL C.35 mL D.37 mL
C
随堂训练
4.甲、乙、丙三种物质的溶解度曲线如图K9-3-1所示。下列说法不正确的是( )
A.t1 ℃时,甲和丙的溶解度相等
B. 降低温度可使丙的不饱和溶液
变成饱和溶液
C.甲中含有少量乙时,可采用降温
结晶的方法提纯甲
D.t2 ℃时,向80 g水中加入20 g甲,溶解后其溶质质量分数为20%
B
随堂训练
5.现有某温度下的硝酸钾溶液35 g,若将其蒸干,得到7 g硝酸钾,则该溶液中溶质的质量分数为________。
(1)若将上述溶液取出2 mL,则剩余溶液的溶质质量分数为
________。
(2)若往上述溶液中加入21 g水,所得溶液的溶质质量分数
为_______。
(3)若往上述溶液中加入3 g硝酸钾,搅拌后完全溶解,所得
溶液的溶质质量分数为________。
(4)若往上述溶液中加入45 g 12%的硝酸钾溶液,所得溶液
的溶质质量分数为________。
20%
12.5%
26.3%
15.5%
20%
第1课时 溶质的质量分数
1. 认识溶质的质量分数的概念;能进行溶质质量分数的简单计算。
2.学会配制一定溶质质量分数溶液的方法。
3. 学会严谨求实的科学学习方法,培养具体问题具体分析的能力。
素养目标
导入新课
生理盐水对大家来说并不陌生,它是不是溶液?
标签上的这个0.9%是什么意思?
这个0.9%是指溶液的浓度,那么如何来定量表示溶液的组成?
两杯等量的水中分别加入1块和2块大小相同的方糖,完全溶解后,两杯糖水的甜度一样吗?如何定量表示溶液的浓稀?
导入新课
实验 9 – 7 配制三种浓稀不同的硫酸铜溶液
在室温下,向三个小烧杯中各加入20mL水,然后分别加入0.1g、0.5g、2g无水硫酸铜,用玻璃棒搅拌,使硫酸铜全部溶解,比较三种硫酸铜溶液。
烧杯编号
溶液颜色比较
溶剂质量/g
溶质质量/g
溶液质量/g
1
2
3
浅
较深
深
20
20
20
0.1
0.5
2
20.1
20.5
22
在这三种溶液中,哪种溶液最浓?哪种溶液最稀?你判断的依据是什么?并填写表格。
(注意:1mL水的质量约为1g)
对有颜色的溶液来说,可以根据颜色的深浅区分溶液是浓还是稀。但这种方法比较粗略,特别是无色溶液,不能准确地表明一定量的溶液里究竟含有多少溶质。
溶液的浓度
1.定义:一定量的溶液里所含溶质的量。
2.表示方法:
溶质的质量分数
溶质的体积分数
溶液中溶质的质量分数是溶质的质量与溶液的质量之比。例如:溶质的质量分数为10%,是每100份质量的溶液中含溶质质量为10份。
除质量分数以外,人们有时也用体积分数来表示溶液的浓度。例如:体积分数75%,是指每100体积的医用酒精中含75体积的乙醇。
重点
1.定义:溶质质量与溶液质量之比。
溶液浓度表示法之——溶质的质量分数
2.表达式
%
×100
+
=
溶剂质量
溶质质量
溶质质量
=
溶液质量
溶质质量
溶质的质量分数
%
×100
公式推导:
m溶质 = ______________
m溶液 = _______________
m溶液×溶质的质量分数
m溶质÷溶质的质量分数
3.意义:每100g某溶液中溶质的质量;用百分数表示,与温度无关。
必须是溶解的那部分溶质,不溶解的溶质不计
(m溶液=ρ溶液×V溶液)
质量单位上下一致
思考与交流
食盐的质量占整个溶液质量的5%
每5g食盐溶于95g水形成的溶液
100g食盐溶液中含有食盐5g
m食盐:m水:m食盐溶液
=5:95:100
“5%的NaCl溶液”的含义
练一练
在实验9-7中,三种硫酸铜溶液中溶质的质量分数各是多少?把计算结果填在表中。
烧杯编号
溶液颜色比较
溶剂质量/g
溶质质量/g
溶液质量/g
溶质的质量分数
1
浅
20
0.1
20.1
2
较深
20
0.5
20.5
3
深
20
2.0
22.0
=
溶液质量
溶质质量
溶质的质量分数
%
×100
0.5%
2.44%
9.09%
{5940675A-B579-460E-94D1-54222C63F5DA}溶质质量/g
溶剂(水)质量/g
现象
溶液中溶质的质量分数
10
90
20
80
10%
20%
完全溶解
完全溶解
实验 9 – 8 配制两种质量分数不同的氯化钠溶液
实验 9 – 8
质量分数与溶解度的关系
已知20oC时,氯化钠的溶解度是36g。有人说“20oC时氯化钠饱和溶液中溶质的质量分数为36%。”这种说法对吗?为什么?
温度
溶质的质量
溶剂的质量
溶液的质量
20℃
36g
100g
100g+36g
36g
100g+36g
100%
×
=26.5%
不对,质量分数=
区别?
溶解度 ?
溶质的质量分数 ?
概念 ?
一定温度时,100g溶剂中最多溶解溶质的质量 ?
任意溶液中,溶质质量与溶液质量之比 ?
应用范围?
m溶质与m溶剂 ?
m溶质与m溶液 ?
条件 ?
一定温度
不定温度 ?
状态 ?
饱和状态 ?
可饱和,可不饱和 ?
单位 ?
g ?
无单位 ?
溶解度S
100g+溶解度S
×????????????%
?
饱和溶液中的
溶质的质量分数
=
在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?
例题1
=126Kg
【解】
= 溶液质量×溶质的质量分数
=150Kg×6%
=24Kg
溶剂质量
=溶液质量-溶质的质量
=150Kg-24Kg
答:配制150kg质量分数为16%的氯化钠溶液需24 kg氯化钠和126 kg水。
=
溶液质量
溶质质量
溶质的质量分数
%
×100
溶质质量
解析:先利用溶解度判断溶液是否饱和,未溶解不计入
18g
即m溶质=18g,m溶液=68g
20℃时,NaCl的溶解度是36克。现有50克水放入20克NaCl,求:所得溶液的溶质质量分数。
例题2
现有一瓶98%的浓硫酸,你能帮我将它变成质量分数为20%的硫酸吗?
溶液的稀释
1.实质:溶液稀释前后溶质的质量不变。
2.表达式:
m×a%=(m+c)×b%
稀释前溶液的溶质质量分数
稀释后溶液的溶质质量分数
稀释前溶液的质量
加水的质量
3.注意事项:
①所设的物理量是质量;
②未知量Χ后不带单位;
③解题过程中数字后写单位;
④最后要写答。
化学实验室现在有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?
例题3
溶液稀释前后,溶质的质量不变。
稀释公式:m浓×c浓% = m稀×c稀% =(m浓+m水)×c稀%
解:设需要加水的质量为x
50g×98% =(50g+x) ×20%
x = 245g
答:需要水的质量为195g。
法二:
解:设稀释后溶液的质量为x
100g × 98% = x × 20%
x = 245g
需要水的质量=245g-50g=195g
答:需要水的质量为195g。
法一:
将溶质的质量分数运用于化学方程式的计算
【例题4】 100g某硫酸溶液恰好与13g锌完全反应,试计算这种硫酸中溶质的质量分数。
解:设这种硫酸中溶质的质量为x。
Zn + H2SO4 = ZnSO4 + H2↑
65 98
13g x
13g x
65 98
x = 19.6 g
溶质的质量分数 = × 100% =19.6%
19.6g
100g
答:这种硫酸溶液中溶质的质量分数为19.6%。
拓展延伸
生命之水
●Spirytus Rektyfikowany是一款原产于波兰的伏特加,被西方人称为“生命之水”。
●经过了反复70回以上的蒸馏,达到96%的酒精度数,是世界上纯度最高的烈酒。
●白酒的"度数”指的是白酒中酒精的含量。这里的含量不是指质量分数,而是体积分数。
●例如: 96度(96°)的酒表示100 mL酒中含有96mL
酒精,体积分数也是一种表示溶液组成的方法。
课堂小结
溶质的质量分数
简单计算
概念
溶质质量与溶液质量之比
溶质的质量分数=
溶质质量
溶液质量
100%
×
公式
溶液的稀释
溶质质量分数的简单计算
随堂训练
1. 对“10%的氯化钠溶液”含义的解释错误的是( )
A. 100 g氯化钠溶液中溶解了10 g氯化钠
B. 100 g水中溶解了10 g氯化钠
C. 将10 g氯化钠溶解于90 g水中得到的溶液
D. 溶液中氯化钠与水的质量比为1 ∶9
B
随堂训练
2. 现配制50 g质量分数为10%的氢氧化钠溶液,需称量氢氧化钠的质量为( )
A. 10 g B. 5 g C. 0.5 g D. 15 g
B
3.现需要将溶质质量分数为40%的氢氧化钠溶液稀释为40 g溶质质量分数为5%的氢氧化钠溶液。此时,需要水的体积为( )
A.38 mL B.36 mL C.35 mL D.37 mL
C
随堂训练
4.甲、乙、丙三种物质的溶解度曲线如图K9-3-1所示。下列说法不正确的是( )
A.t1 ℃时,甲和丙的溶解度相等
B. 降低温度可使丙的不饱和溶液
变成饱和溶液
C.甲中含有少量乙时,可采用降温
结晶的方法提纯甲
D.t2 ℃时,向80 g水中加入20 g甲,溶解后其溶质质量分数为20%
B
随堂训练
5.现有某温度下的硝酸钾溶液35 g,若将其蒸干,得到7 g硝酸钾,则该溶液中溶质的质量分数为________。
(1)若将上述溶液取出2 mL,则剩余溶液的溶质质量分数为
________。
(2)若往上述溶液中加入21 g水,所得溶液的溶质质量分数
为_______。
(3)若往上述溶液中加入3 g硝酸钾,搅拌后完全溶解,所得
溶液的溶质质量分数为________。
(4)若往上述溶液中加入45 g 12%的硝酸钾溶液,所得溶液
的溶质质量分数为________。
20%
12.5%
26.3%
15.5%
20%
同课章节目录
