第3章物质的性质与转化检测题(含答案)高一上学期化学鲁科版(2019)必修第一册
文档属性
| 名称 | 第3章物质的性质与转化检测题(含答案)高一上学期化学鲁科版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 464.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-16 00:00:00 | ||
图片预览




文档简介
第三章 物质的性质与转化 检测题
一、单选题
1.足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积的O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入50mL4mol·L-1NaOH溶液,则Cu2+恰好完全沉淀。下列说法正确的是
A.此反应过程中转移的电子为0.3mol
B.混合气体中含NO2(标准状况)1.12L
C.参加反应的HNO3是0.4mol
D.消耗氧气(标准状况)的体积为1.68L
2.下列关于浓硫酸的性质叙述正确的是
A.加热时与铜反应只体现酸性 B.干燥氢气体现脱水性
C.使白纸变黑体现吸水性 D.加热时与碳反应体现强氧化性
3.下列物质的转化在给定条件下能实现的是
①铝土矿
②盐卤(含)溶液无水
③
④
⑤NaCl溶液无水
⑥溶液
A.③⑥ B.③⑤⑥ C.①④⑤ D.①③⑥
4.下列有关离子方程式书写正确的是
A.铵明矾溶液中滴加少量NaOH 溶液:
B.磁铁矿石溶于稀硝酸:
C.向碳酸氢钠溶液中通人氯气:
D.IBr在KOH溶液中发生非氧化还原反应:
5.下列说法正确的是
A.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
B.NH3液化时吸收大量的热,因此,氨气常用作制冷剂
C.CO2、NO2或SO2都会导致酸雨的形成,NO2能导致“光化学烟雾”
D.活性炭、SO2、Na2O2都能使品红溶液褪色,原理不同
6.在给定条件下,下列所示的转化关系不能实现的是
A.Fe Fe2O3 FeCl2
B.C CO2 H2CO3
C.AlAl2O3 NaAlO2
D.Na Na2O2Na2CO3
7.下列使用稀硫酸或浓硫酸的方法正确的是
A.浓硫酸和乙醇加热到170°C制乙烯
B.常温下浓硫酸和铁制硫酸铁
C.稀硫酸和铜加热制备二氧化硫
D.稀硫酸和氯化钠固体共热制备氯化氢
8.下列关于SO2的性质用途叙述错误的是
A.SO2不能用作食品添加剂
B.SO2可用于杀菌消毒
C.SO2能使品红褪色
D.工业上常用SO2来漂白纸浆、毛、丝等
9.下列关于铁及其化合物的说法正确的是
A.红热的铁能与水蒸气反应,生成和
B.在空气中充分灼烧得到FeO
C.FeO是一种黑色粉末,不稳定,在空气中受热,迅速转化成红棕色粉末
D.过量铁与氯气或者稀盐酸反应均可制得
10.对于硝酸的物理性质,下列叙述错误的是
A.可以与水以任意比互溶 B.不易挥发
C.有刺激性气味 D.无色液体
11.下列有关自然界中氮循环的说法错误的是
A.工业合成氨属于人工固氮
B.豆科植物可实现生物固氮
C.氨和铵盐在硝化细菌作用下被还原
D.含氮无机物与有机氮可以相互转化
12.在一定条件下,将 6 体积的 NO2(不考虑 NO2 转化为 N2O4)和一定体积的 NO 置于试管中,并将试管倒置于盛有水的水槽中,待试管内液面不变后再通入 4.5 体积的 O2 充分反应后,剩余 1.5 体积气体,则原 NO 体积可能为:①3 体积 ;②4 体积;③5 体积;④5.5 体积;⑤2体积
A.①或⑤ B.②或⑤ C.④或⑤ D.②或③
13.是一种常见的化肥,其溶解度随着温度的升高而增大,某工厂用石膏、、和制备的工艺流程如图:
下列说法正确的是
A.通入和的顺序可以互换
B.操作2为将滤液蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可得
C.步骤②中反应的离子方程式为
D.通入的和均应过量,且工艺流程中可循环利用
14.如图所示装置中,试管内的FeI2溶液中滴有KSCN溶液,实验中控制通入Cl2的速度,试管内先观察到紫色,后观察到血红色。下列说法正确的是
A.若Cl2中含较多HCl,则实验过程中会产生倒吸现象
B.通入足量Cl2后,振荡试管,下层变紫色,上层变血红色
C.该实验可验证氧化性:Cl2>I2>Fe3+
D.试管内反应的离子方程式可表示为2Fe2++2I-+2Cl2=I2+2Fe3++4Cl-
二、填空题
15.(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式是_______;常用澄清石灰水检验 CO2 气体的离子方程式是_______。
(2)表面附有铁锈 ( 成分是 Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是_______。反应片刻后,可观察到有气体产生,其离子方程式是_______。
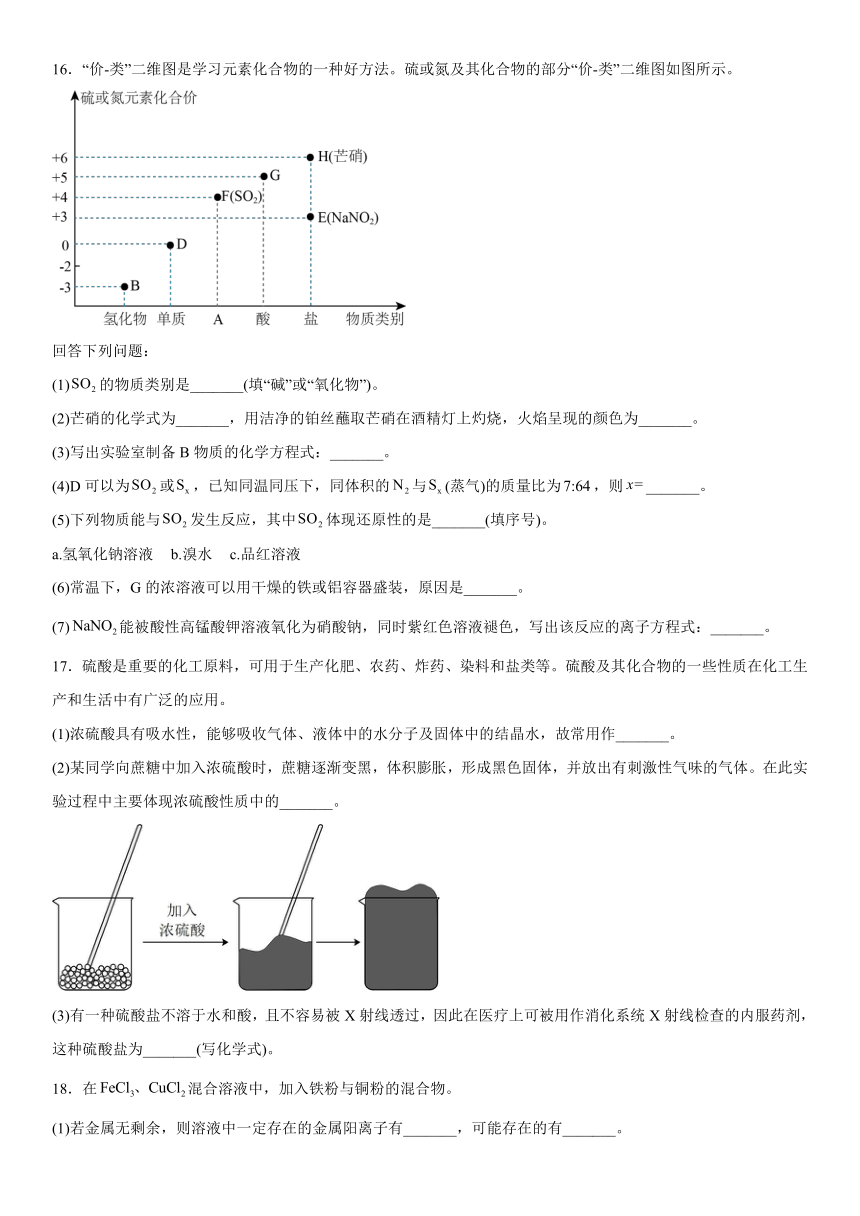
16.“价-类”二维图是学习元素化合物的一种好方法。硫或氮及其化合物的部分“价-类”二维图如图所示。
回答下列问题:
(1)的物质类别是_______(填“碱”或“氧化物”)。
(2)芒硝的化学式为_______,用洁净的铂丝蘸取芒硝在酒精灯上灼烧,火焰呈现的颜色为_______。
(3)写出实验室制备B物质的化学方程式:_______。
(4)D可以为或,已知同温同压下,同体积的与(蒸气)的质量比为,则_______。
(5)下列物质能与发生反应,其中体现还原性的是_______(填序号)。
a.氢氧化钠溶液 b.溴水 c.品红溶液
(6)常温下,G的浓溶液可以用干燥的铁或铝容器盛装,原因是_______。
(7)能被酸性高锰酸钾溶液氧化为硝酸钠,同时紫红色溶液褪色,写出该反应的离子方程式:_______。
17.硫酸是重要的化工原料,可用于生产化肥、农药、炸药、染料和盐类等。硫酸及其化合物的一些性质在化工生产和生活中有广泛的应用。
(1)浓硫酸具有吸水性,能够吸收气体、液体中的水分子及固体中的结晶水,故常用作_______。
(2)某同学向蔗糖中加入浓硫酸时,蔗糖逐渐变黑,体积膨胀,形成黑色固体,并放出有刺激性气味的气体。在此实验过程中主要体现浓硫酸性质中的_______。
(3)有一种硫酸盐不溶于水和酸,且不容易被X射线透过,因此在医疗上可被用作消化系统X射线检查的内服药剂,这种硫酸盐为_______(写化学式)。
18.在混合溶液中,加入铁粉与铜粉的混合物。
(1)若金属无剩余,则溶液中一定存在的金属阳离子有_______,可能存在的有_______。
(2)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有_______,一定不存在_______。
(3)若剩余固体中只有铜,则溶液中一定存在的金属阳离子有_______,可能存在的有_______,一定不存在_______。
19.某无色溶液中可能含有H+、NH、Mg2+、Fe3+、Al3+、SO、HCO等离子,当向溶液中加入一定浓度NaOH溶液时,生成沉淀的物质的量随加入NaOH溶液的体积关系如图所示。
请回答下列问题:
(1)该无色溶液中一定不存在的离子有___________;
(2)ab段生成的沉淀的化学式为___________;
(3)bc段表明溶液中有___________(填离子符号),检验该离子的实验操作及现象是___________;
(4)cd段沉淀减少的离子方程式为___________;
(5)原溶液中一定含有的离子的物质的量之比为___________。[按题中给出离子的顺序写比例,格式如:n(H+):n(NH):n(Mg2+)=1:1:1]
20.铁的氧化物的比较
化学式
俗名 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有磁性)
溶解性 难溶于水 难溶于水 难溶于水
铁的化合价 _______ _______ _______
稳定性 不稳定 稳定 稳定
与反应的离子方程式 _______ _______
与的反应(炼铁原理)
21.“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”,减少废气的排放是环境保护的重要内容之一、
(1)氮氧化物是形成光化学烟雾的主要元凶,利用碱液吸收法可以有效地吸收氮氧化物,发生的反应有、。若某混合气体中含amolNO和bmolNO2,用NaOH溶液吸收时,要使气体完全被吸收,则a与b需满足的关系为___________,气体完全被吸收后测得溶液中NaNO2和NaNO3的物质的量之比为4∶1,则混合气体中NO的体积分数为___________。
(2)煤燃烧时排放的烟气中含有SO2和NOx,用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2和NaOH溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下表所示(其他极微量离子忽略不计):
离子 Na+ SO NO H+ Cl-
浓度/(mol/L) 3.0×10-3 y 8.8×10-4 3.8×10-4 1.0×10-3
①SO2和NaClO2溶液反应的离子方程式为___________。
②表中y=___________。
(3)工业生产硫酸也会产生SO2。硫铁矿(FeS2)煅烧的化学方程式为___________;当有11.2L(标准状况) SO2气体生成时,反应中转移的电子数为___________NA。
参考答案:
1.B
【分析】向所得硝酸铜溶液中加入50mL4mol·L-1NaOH溶液,则Cu2+恰好完全沉淀,可知硝酸铜的物质的量是0.1mol,据此分析解题。
【详解】A.向所得硝酸铜溶液中加入50mL4mol·L-1NaOH溶液,则Cu2+恰好完全沉淀,根据反应可知Cu2+的物质的量是0.1mol,所以此反应过程中转移的电子为0.2mol,故A错误;
B.设NO2、NO的物质的量分别是x、y,根据元素守恒 ,根据电子守恒;解方程可知,NO2、NO的物质的量分别是0.05mol、0.05mol,混合气体中含NO2(标准状况)1.12L,故B正确;
C.参加反应的铜的物质的量是0.1mol,则表现酸性的硝酸0.2mol,混合气体的物质的量是0.1mol,则被还原的硝酸是0.1mol,参加反应的HNO3是0.3mol,故C错误;
D.参加反应的铜的物质的量是0.1mol,根据转移电子守恒,可知2Cu~O2,消耗氧气(标准状况)的体积为0.05mol×22.4L/mol=1.12L,故D错误;
故选B。
2.D
【详解】A.加热时与铜与浓硫酸反应既体现酸性,又表现了强氧化,故A错误;
B.浓硫酸干燥氢气,体现了浓硫酸具有吸水性,故B错误;
C.浓硫酸能够使白纸变黑,说明浓硫酸具脱水性,故C错误;
D.浓硫酸与非金属单质碳反应只体现浓硫酸的强氧化性,故D正确;
故答案:C。
3.A
【详解】①铝土矿与氢氧化钠反应生成偏铝酸钠,偏铝酸钠溶液通入足量的盐酸,生成氯化铝,得不到氢氧化铝,故①错误;
②盐卤(含MgCl2)与石灰乳反应生成氢氧化镁,氢氧化镁与盐酸反应生成氯化镁溶液,但由于Mg2+水解Mg2++2H2O Mg(OH)2+2H+,加热蒸发HCl挥发,平衡向右移动,所以得不到无水MgCl2,故②错误;
③氨催化氧化生成一氧化氮和水,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸,符合各步转化,故③正确;
④硫在氧气中燃烧只能生成二氧化硫,不能生成三氧化硫,故④错误;
⑤电解氯化钠溶液可以得到氯气,氯气与铁反应生成FeCl3,不是,故⑤错误;
⑥SiO2与氢氧化钠反应Na2SiO3,Na2SiO3溶液中通二氧化碳发生反应生成H2SiO3,故⑥正确;
综上所述选A。
4.D
【详解】A.由能与氨水反应可知,结合的能力强于,故滴加少量NaOH溶液,先反应,A项错误;
B.硝酸会将氧化为,B项错误;
C.次氯酸的酸性弱于碳酸,次氯酸与不反应,最终产物中次氯酸应写分子式,C项错误;
D.IBr中碘元素为+1价,溴元素为-1价,发生非氧化还原反应生成和,D项正确。
故选D。
5.D
【详解】A.三种气体都是大气污染物,NO易与空气中的氧气反应生成NO2,在空气中不能稳定存在,A项错误;
B.液态NH3汽化时吸收大量的热,因此,液氨常用作制冷剂,B项错误;
C.酸雨与二氧化硫和氮的氧化物有关,与二氧化碳无关,二氧化碳与温室效应有关,C项错误;
D.活性炭因吸附使品红褪色、SO2因发生化合反应使品红褪色、Na2O2因强氧化性使品红溶液褪色,原理不同,D项正确;
答案选D。
6.A
【详解】A.Fe与水蒸气在高温下反应产生Fe3O4,不是Fe2O3,Fe2O3与HCl反应产生FeCl3,不是FeCl2,因此不能在给定条件下实现物质的转化关系,A符合题意;
B.C与足量O2在点燃时反应产生CO2,CO2能够溶于水,与水反应产生H2CO3,能在给定条件下实现物质的转化关系,B不符合题意;
C.Al能够与O2反应产生Al2O3,Al2O3是两性氧化物,能够NaOH溶液反应产生NaAlO2,能在给定条件下实现物质的转化关系,C不符合题意;
D.Na与O2在加热时反应产生Na2O2,Na2O2与CO2反应产生Na2CO3和O2,D不符合题意;
故选A。
7.A
【详解】A.浓硫酸和乙醇加热到170°C,分子内脱水发生消去反应制备乙烯,故A正确;
B.常温下浓硫酸与铁发生钝化,不能制备硫酸铁,故B错误;
C.稀硫酸和铜不反应,故C错误;
D.浓硫酸和氯化钠固体共热制备氯化氢,故D错误;
故答案为A。
8.A
【详解】A.二氧化硫有毒,可以用作一定范围内的食品添加剂,但必需严格按照国家有关范围和标准使用,否则影响人体健康,A错误;
B.二氧化硫与水反应生成的酸可使蛋白质变性,SO2可用于杀菌消毒,B正确;
C.SO2具有漂白性,能使品红褪色,C正确;
D.工业上常用二氧化硫来漂白纸浆、丝毛、草帽等,此外二氧化硫还能够抑制霉菌和细菌的滋生,D正确;
答案选A。
9.A
【详解】A.铁与水蒸气在高温下生成Fe3O4和H2,故A正确;
B.氢氧化亚铁具有还原性,在空气中灼烧氧气将+2价Fe氧化+3价Fe,最终不能得到FeO,故B错误;
C.FeO是一种黑色粉末,不稳定,在空气里加热,最终被氧化成黑色的Fe3O4,故C错误;
D.铁无论过量还是不足,与氯气在加热条件下反应,均生成FeCl3,故D错误;
答案为A。
10.B
【详解】硝酸是一种无色,可以与水以任意比互溶,易挥发的液体,有刺激性气味,B项错误,故选B。
11.C
【详解】A.氮的固定分为三类:植物的根瘤菌固氮称为生物固氮、放电条件下生成一氧化氮为高能固氮、工业合成氨反应属于人工固氮,A正确;
B.豆科植物可将大气中的N2转化为NH3,从而实现生物固氮,B正确;
C.氨和铵盐在硝化细菌作用下最终转化为硝酸根离子,氮元素价态升高,被氧化,C不正确;
D.由二氧化碳与氨在一定条件下反应可制得尿素,从而实现含氮无机物与有机氮的转化,蛋白质在动物体内消化可生成氨,实现有机氮向含氮无机物的转化,D正确;
故选C。
12.C
【分析】根据4NO2+O2+2H2O=4HNO3、4NO+3O2+2H2O=4HNO3,剩余1.5体积气体,可能为NO,也可能为氧气,以此来计算。
【详解】
则一定体积的NO和3体积的氧气发生4NO+3O2+2H2O=4HNO3
①若剩余气体为NO,则由反应可知,消耗NO为4体积,则原NO的体积为1.5+4=5.5体积;
②若剩余气体为氧气,则4NO+3O2+2H2O=4HNO3中反应的氧气为1.5体积,则原NO的体积为=2体积,
故选C。
13.B
【详解】A.由于微溶于水,易溶于水,应先通入足量,使溶液呈碱性,然后再通入适量,反应的化学方程式为,通入和的顺序不可以互换,选项A错误;
B.向硫酸钙悬浊液中通入足量的氨气,使溶液呈碱性,再通入适量的二氧化碳利于反应的进行,硫酸钙与氨气、水和二氧化碳反应生成了硫酸铵和碳酸钙沉淀。操作2是溶液中得到溶质固体的过程,需要蒸发浓缩、冷却结晶、过滤、洗涤、干燥等,可得,选项B正确;
C.硫酸钙与氨气、水和二氧化碳反应生成了硫酸铵和碳酸钙沉淀,物质发生的主要化学反应为,反应的离子方程式为,选项C错误;
D.反应过程中二氧化碳参与反应生成硫酸铵和碳酸钙,碳酸钙分解生成二氧化碳,工艺流程中产生的可循环利用,通入足量,通适量二氧化碳,否则碳酸钙溶解,选项D错误。
答案选B。
14.B
【分析】碘化亚铁溶液通入氯气,先观察到紫色,说明氯气先将碘离子氧化成碘单质,然后观察到血红色,说明氯气将亚铁离子氧化成Fe3+,据此分析;
【详解】A.根据图象,导管下端在四氯化碳溶液中,HCl不溶于四氯化碳,不能发生倒吸,故A错误;
B.通入足量的氯气后,振荡试管,因四氯化碳的密度大于水,且不与水互溶,四氯化碳在下层,水层在上层,碘单质易溶于四氯化碳,即下层显紫色,Fe3+在水层,即上层显红色,故B正确;
C.根据上述分析,氯气先氧化成碘离子,再氧化亚铁离子,说明氯气的氧化性最强,碘离子的还原性强于亚铁离子,从而推出Fe3+的氧化性强于I2,故C错误;
D.根据上述分析,氯气先氧化碘离子,将碘离子氧化完后,再与亚铁离子反应,题中所给离子方程式是先氧化亚铁离子,因此离子方程式可以是2Fe2++4I-+3Cl2=2I2+2Fe3++6Cl-,故D错误;
答案为B。
15. CaCO3+2H+=Ca2++H2O+CO2↑ Ca2++2OH-+CO2=CaCO3↓+H2O Fe2O3+6H+=2Fe3++3H2O Fe+2H+=Fe2++H2↑
【分析】碳酸钙与盐酸反应生成氯化钙、二氧化碳和水;用澄清石灰水检验 CO2 气体,澄清石灰水变浑浊,生成碳酸钙;表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始时氧化铁与稀硫酸反应生成硫酸铁和水,片刻后,可观察到有气体产生,是铁与稀硫酸反应生成硫酸亚铁和氢气,据此书写反应的离子方程式。
【详解】(1)碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,反应的离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑; 用澄清石灰水检验 CO2 气体,澄清石灰水变浑浊,生成碳酸钙和水,反应的离子方程式为Ca2++2OH-+CO2=CaCO3↓+H2O,故答案为:CaCO3+2H+=Ca2++H2O+CO2↑; Ca2++2OH-+CO2=CaCO3↓+H2O;
(2)表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始时氧化铁与稀硫酸反应生成硫酸铁和水,反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O ,反应片刻后,可观察到有气体产生,是铁与稀硫酸反应生成硫酸亚铁和氢气,反应的离子方程式为Fe+2H+=Fe2++H2↑,故答案为:Fe2O3+6H+=2Fe3++3H2O;Fe+2H+=Fe2++H2↑。
16.(1)氧化物
(2) 黄色
(3)
(4)8
(5)漂白性
(6)常温下,铁或铝被浓硝酸氧化,生成一层致密的氧化物薄膜,这层薄膜阻止了酸与内层金属的进一步反应(合理即可)
(7)
【解析】(1)
的物质类别是氧化物;
(2)
芒硝的化学式为,芒硝在酒精灯上灼烧,火焰呈现的颜色为黄色;
(3)
实验室制备氨气反应的化学方程式为;
(4)
D可以为或,已知同温同压下,同体积的与(蒸气)的物质的量相同,则,解得:;
(5)
与氢氧化钠溶液反应,体现其酸性氧化物的性质,与溴水反应体现其还原性,与品红溶液反应,体现其漂白性;
(6)
常温下,浓硝酸可以用干燥的铁或铝容器盛装,是因为常温下,铁或铝被浓硝酸氧化,生成一层致密的氧化物薄膜,这层薄膜阻止了酸与内层金属的进一步反应;
(7)
能被酸性高锰酸钾溶液氧化为硝酸钠,同时紫红色溶液褪色,该反应的离子方程式为。
17.(1)干燥剂
(2)脱水性、强氧化性
(3)BaSO4
【解析】(1)
浓硫酸具有吸水性,能够吸收气体、液体中的水分子及固体中的结晶水,故常用作干燥剂,故答案为:干燥剂;
(2)
蔗糖逐渐变黑,体现了浓硫酸的脱水性,体积膨胀,并放出有刺激性气味的气体SO2,体现了浓硫酸的强氧化性,故答案为:脱水性、强氧化性;
(3)
BaSO4不溶于胃酸,在医疗上可被用作消化系统X射线检查的内服药剂,俗称钡餐,故答案为:BaSO4。
18.(1)
(2)
(3)
【分析】向铁铜的混合粉末中加入溶液,由于铁的还原性比铜的强,氯化铁的氧化性比氯化铜强,故最先发生反应2Fe3++Fe=3Fe2+,还可能发生2Fe3++Cu=2Fe2++Cu2+、Fe+Cu2+=Fe2++Cu,据此回答。
【详解】(1)若金属无剩余,则2Fe3++Fe=3Fe2+、2Fe3++Cu=2Fe2++Cu2+必定发生,溶液中一定存在的金属阳离子有,可能存在的有。
(2)若剩余固体中有铁和铜,则溶液中不存在,反应2Fe3++Fe=3Fe2+ 、Fe+Cu2+=Fe2++Cu必定发生,则溶液中一定存在的金属阳离子有,一定不存在。
(3)若剩余固体中只有铜,则溶液中不存在,反应2Fe3++Fe=3Fe2+必定发生,溶液中一定存在的金属阳离子有,可能存在的有,一定不存在。
19.(1)Fe3+、HCO
(2)Al(OH)3、Mg(OH)2
(3) NH 取少量待测液加入浓的NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,说明溶液有NH3 H2O
(4)Al(OH)3+OH-═AlO+2H2O
(5)n(H+):n(NH):n(Mg2+):n(Al3+):n(SO)=2:4:3:2:9
【分析】无色溶液,则一定不含Fe3+,加入NaOH溶液后,在0-a段没有生成沉淀,说明溶液中一定存在H+或HCO离子,由于后面有沉淀生成及部分沉淀溶解可知,溶液中一定存在Al3+,由于HCO和Al3+会发生双水解而不能共存,则只能存在H+,a-b段生成沉淀消耗了6a体积氢氧化钠,又c-d段部分沉淀溶解,可知溶液中一定存在Mg2+、Al3+,根据图象Al(OH)3的物质的量与剩余的沉淀的物质的量相等,由OH-~AlO可知消耗溶解氢氧化铝消耗了a体积氢氧化钠,所以生成氢氧化铝沉淀消耗了3a体积氢氧化钠,Mg2+生成的沉淀的量也消耗3a体积氢氧化钠,b-c段沉淀的物质的量不变,说明氢氧根离子与铵离子发生了反应,即溶液中一定存在NH,根据溶液呈电中性可知,溶液中一定存在SO;综上所述,原溶液中含有的阳离子是H+、NH、Mg2+、Al3+、SO,一定不存在Fe3+、HCO,据此分析解答。
(1)
含Fe3+溶液为黄色,由分析可知,该无色溶液中一定不存在的离子有Fe3+、HCO;
(2)
根据以上分析,溶液中一定存在Mg2+、Al3+,所以ab段生成沉淀的化学式为:Al(OH)3、Mg(OH)2,故答案为:Al(OH)3、Mg(OH)2;
(3)
b-c段沉淀的物质的量不变,说明加入的NaOH与原溶液中的NH反应生成NH3 H2O,证明溶液中含NH,检验该离子的实验操作及现象是:取少量待测液加入浓的NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,说明溶液有NH3 H2O,故答案为:NH;取少量待测液加入浓的NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,说明溶液有NH3 H2O;
(4)
cd段沉淀减少是氢氧化铝与氢氧化钠反应,反应的离子方程式为:Al(OH)3+OH-═AlO+2H2O,故答案为:Al(OH)3+OH-═AlO+2H2O;
(5)
原溶液中含有的阳离子是H+、NH、Mg2+、Al3+,根据消耗的氢氧化钠的物质的量可以认为n(H+)=a,n(Al3+)=a,n(Mg2+)=1.5a,n(NH)=2a,根据电荷守恒,n(SO)=4.5a,n(H+):n(NH):n(Mg2+):n(Al3+):n(SO)=2:4:3:2:9,故答案为:n(H+):n(NH):n(Mg2+):n(Al3+):n(SO)=2:4:3:2:9。
20. 、
【详解】根据化合物中化合价代数和为0可知,中Fe元素化合价为+2价,中Fe元素化合价为+3价,可以看成,故Fe元素化合价为+2、+3价,与氢离子反应的离子方程式为,与氢离子反应的离子方程式为。
21.(1) a≤b 30%
(2)
(3) 4FeS2+11O22Fe2O3+8SO2 2.75
【分析】(1)
由题意可知,NO2能被NaOH溶液吸收,NO和NO2按1∶1的比例能被NaOH溶液吸收,NO不能被NaOH溶液吸收,故n(NO2)≥n(NO)即可,即a≤b;设混合气中NO、NO2物质的量分别为x、y,根据反应NO+NO2+2NaOH=2NaNO2+H2O,该反应消耗NO2物质的量为x,生成NaNO2物质的量为2x,则反应2NO2+2NaOH=NaNO2+NaNO3+H2O消耗NO2物质的量为(y-x),生成NaNO2、NaNO3物质的量都为,溶液中NaNO2和NaNO3的物质的量之比为4∶1,则(2x+):=4:1,解得x:y=3:7,故混合气体中NO物质的量分数为30%,即混合气体中NO的体积分数为30%;答案为:a≤b;30%。
(2)
①根据表中离子可知,SO2被氧化成,被还原成Cl-,结合得失电子守恒、电荷守恒、原子守恒,SO2和NaClO2反应的离子方程式为2SO2++2H2O=2+Cl-+4H+;答案为:2SO2++2H2O=2+Cl-+4H+。
②溶液中的电荷守恒为c(Na+)+c(H+)=2c()+c()+c(Cl-)+c(OH-),3×10-3mol/L+3.8×10-4mol/L=2ymol/L+8.8×10-4mol/L+1×10-3mol/L+mol/L,解得y=7.5×10-4;答案为7.5×10-4。
(3)
煅烧硫铁矿生成Fe2O3和SO2,反应的化学方程式为4FeS2+11O22Fe2O3+8SO2;反应中生成8molSO2时转移44mol电子,标准状况下11.2LSO2物质的量为0.5mol,则转移电子数为=2.75mol,转移电子数为2.75NA;答案为:4FeS2+11O22Fe2O3+8SO2;2.75。
一、单选题
1.足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积的O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入50mL4mol·L-1NaOH溶液,则Cu2+恰好完全沉淀。下列说法正确的是
A.此反应过程中转移的电子为0.3mol
B.混合气体中含NO2(标准状况)1.12L
C.参加反应的HNO3是0.4mol
D.消耗氧气(标准状况)的体积为1.68L
2.下列关于浓硫酸的性质叙述正确的是
A.加热时与铜反应只体现酸性 B.干燥氢气体现脱水性
C.使白纸变黑体现吸水性 D.加热时与碳反应体现强氧化性
3.下列物质的转化在给定条件下能实现的是
①铝土矿
②盐卤(含)溶液无水
③
④
⑤NaCl溶液无水
⑥溶液
A.③⑥ B.③⑤⑥ C.①④⑤ D.①③⑥
4.下列有关离子方程式书写正确的是
A.铵明矾溶液中滴加少量NaOH 溶液:
B.磁铁矿石溶于稀硝酸:
C.向碳酸氢钠溶液中通人氯气:
D.IBr在KOH溶液中发生非氧化还原反应:
5.下列说法正确的是
A.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
B.NH3液化时吸收大量的热,因此,氨气常用作制冷剂
C.CO2、NO2或SO2都会导致酸雨的形成,NO2能导致“光化学烟雾”
D.活性炭、SO2、Na2O2都能使品红溶液褪色,原理不同
6.在给定条件下,下列所示的转化关系不能实现的是
A.Fe Fe2O3 FeCl2
B.C CO2 H2CO3
C.AlAl2O3 NaAlO2
D.Na Na2O2Na2CO3
7.下列使用稀硫酸或浓硫酸的方法正确的是
A.浓硫酸和乙醇加热到170°C制乙烯
B.常温下浓硫酸和铁制硫酸铁
C.稀硫酸和铜加热制备二氧化硫
D.稀硫酸和氯化钠固体共热制备氯化氢
8.下列关于SO2的性质用途叙述错误的是
A.SO2不能用作食品添加剂
B.SO2可用于杀菌消毒
C.SO2能使品红褪色
D.工业上常用SO2来漂白纸浆、毛、丝等
9.下列关于铁及其化合物的说法正确的是
A.红热的铁能与水蒸气反应,生成和
B.在空气中充分灼烧得到FeO
C.FeO是一种黑色粉末,不稳定,在空气中受热,迅速转化成红棕色粉末
D.过量铁与氯气或者稀盐酸反应均可制得
10.对于硝酸的物理性质,下列叙述错误的是
A.可以与水以任意比互溶 B.不易挥发
C.有刺激性气味 D.无色液体
11.下列有关自然界中氮循环的说法错误的是
A.工业合成氨属于人工固氮
B.豆科植物可实现生物固氮
C.氨和铵盐在硝化细菌作用下被还原
D.含氮无机物与有机氮可以相互转化
12.在一定条件下,将 6 体积的 NO2(不考虑 NO2 转化为 N2O4)和一定体积的 NO 置于试管中,并将试管倒置于盛有水的水槽中,待试管内液面不变后再通入 4.5 体积的 O2 充分反应后,剩余 1.5 体积气体,则原 NO 体积可能为:①3 体积 ;②4 体积;③5 体积;④5.5 体积;⑤2体积
A.①或⑤ B.②或⑤ C.④或⑤ D.②或③
13.是一种常见的化肥,其溶解度随着温度的升高而增大,某工厂用石膏、、和制备的工艺流程如图:
下列说法正确的是
A.通入和的顺序可以互换
B.操作2为将滤液蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可得
C.步骤②中反应的离子方程式为
D.通入的和均应过量,且工艺流程中可循环利用
14.如图所示装置中,试管内的FeI2溶液中滴有KSCN溶液,实验中控制通入Cl2的速度,试管内先观察到紫色,后观察到血红色。下列说法正确的是
A.若Cl2中含较多HCl,则实验过程中会产生倒吸现象
B.通入足量Cl2后,振荡试管,下层变紫色,上层变血红色
C.该实验可验证氧化性:Cl2>I2>Fe3+
D.试管内反应的离子方程式可表示为2Fe2++2I-+2Cl2=I2+2Fe3++4Cl-
二、填空题
15.(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式是_______;常用澄清石灰水检验 CO2 气体的离子方程式是_______。
(2)表面附有铁锈 ( 成分是 Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是_______。反应片刻后,可观察到有气体产生,其离子方程式是_______。
16.“价-类”二维图是学习元素化合物的一种好方法。硫或氮及其化合物的部分“价-类”二维图如图所示。
回答下列问题:
(1)的物质类别是_______(填“碱”或“氧化物”)。
(2)芒硝的化学式为_______,用洁净的铂丝蘸取芒硝在酒精灯上灼烧,火焰呈现的颜色为_______。
(3)写出实验室制备B物质的化学方程式:_______。
(4)D可以为或,已知同温同压下,同体积的与(蒸气)的质量比为,则_______。
(5)下列物质能与发生反应,其中体现还原性的是_______(填序号)。
a.氢氧化钠溶液 b.溴水 c.品红溶液
(6)常温下,G的浓溶液可以用干燥的铁或铝容器盛装,原因是_______。
(7)能被酸性高锰酸钾溶液氧化为硝酸钠,同时紫红色溶液褪色,写出该反应的离子方程式:_______。
17.硫酸是重要的化工原料,可用于生产化肥、农药、炸药、染料和盐类等。硫酸及其化合物的一些性质在化工生产和生活中有广泛的应用。
(1)浓硫酸具有吸水性,能够吸收气体、液体中的水分子及固体中的结晶水,故常用作_______。
(2)某同学向蔗糖中加入浓硫酸时,蔗糖逐渐变黑,体积膨胀,形成黑色固体,并放出有刺激性气味的气体。在此实验过程中主要体现浓硫酸性质中的_______。
(3)有一种硫酸盐不溶于水和酸,且不容易被X射线透过,因此在医疗上可被用作消化系统X射线检查的内服药剂,这种硫酸盐为_______(写化学式)。
18.在混合溶液中,加入铁粉与铜粉的混合物。
(1)若金属无剩余,则溶液中一定存在的金属阳离子有_______,可能存在的有_______。
(2)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有_______,一定不存在_______。
(3)若剩余固体中只有铜,则溶液中一定存在的金属阳离子有_______,可能存在的有_______,一定不存在_______。
19.某无色溶液中可能含有H+、NH、Mg2+、Fe3+、Al3+、SO、HCO等离子,当向溶液中加入一定浓度NaOH溶液时,生成沉淀的物质的量随加入NaOH溶液的体积关系如图所示。
请回答下列问题:
(1)该无色溶液中一定不存在的离子有___________;
(2)ab段生成的沉淀的化学式为___________;
(3)bc段表明溶液中有___________(填离子符号),检验该离子的实验操作及现象是___________;
(4)cd段沉淀减少的离子方程式为___________;
(5)原溶液中一定含有的离子的物质的量之比为___________。[按题中给出离子的顺序写比例,格式如:n(H+):n(NH):n(Mg2+)=1:1:1]
20.铁的氧化物的比较
化学式
俗名 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有磁性)
溶解性 难溶于水 难溶于水 难溶于水
铁的化合价 _______ _______ _______
稳定性 不稳定 稳定 稳定
与反应的离子方程式 _______ _______
与的反应(炼铁原理)
21.“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”,减少废气的排放是环境保护的重要内容之一、
(1)氮氧化物是形成光化学烟雾的主要元凶,利用碱液吸收法可以有效地吸收氮氧化物,发生的反应有、。若某混合气体中含amolNO和bmolNO2,用NaOH溶液吸收时,要使气体完全被吸收,则a与b需满足的关系为___________,气体完全被吸收后测得溶液中NaNO2和NaNO3的物质的量之比为4∶1,则混合气体中NO的体积分数为___________。
(2)煤燃烧时排放的烟气中含有SO2和NOx,用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2和NaOH溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下表所示(其他极微量离子忽略不计):
离子 Na+ SO NO H+ Cl-
浓度/(mol/L) 3.0×10-3 y 8.8×10-4 3.8×10-4 1.0×10-3
①SO2和NaClO2溶液反应的离子方程式为___________。
②表中y=___________。
(3)工业生产硫酸也会产生SO2。硫铁矿(FeS2)煅烧的化学方程式为___________;当有11.2L(标准状况) SO2气体生成时,反应中转移的电子数为___________NA。
参考答案:
1.B
【分析】向所得硝酸铜溶液中加入50mL4mol·L-1NaOH溶液,则Cu2+恰好完全沉淀,可知硝酸铜的物质的量是0.1mol,据此分析解题。
【详解】A.向所得硝酸铜溶液中加入50mL4mol·L-1NaOH溶液,则Cu2+恰好完全沉淀,根据反应可知Cu2+的物质的量是0.1mol,所以此反应过程中转移的电子为0.2mol,故A错误;
B.设NO2、NO的物质的量分别是x、y,根据元素守恒 ,根据电子守恒;解方程可知,NO2、NO的物质的量分别是0.05mol、0.05mol,混合气体中含NO2(标准状况)1.12L,故B正确;
C.参加反应的铜的物质的量是0.1mol,则表现酸性的硝酸0.2mol,混合气体的物质的量是0.1mol,则被还原的硝酸是0.1mol,参加反应的HNO3是0.3mol,故C错误;
D.参加反应的铜的物质的量是0.1mol,根据转移电子守恒,可知2Cu~O2,消耗氧气(标准状况)的体积为0.05mol×22.4L/mol=1.12L,故D错误;
故选B。
2.D
【详解】A.加热时与铜与浓硫酸反应既体现酸性,又表现了强氧化,故A错误;
B.浓硫酸干燥氢气,体现了浓硫酸具有吸水性,故B错误;
C.浓硫酸能够使白纸变黑,说明浓硫酸具脱水性,故C错误;
D.浓硫酸与非金属单质碳反应只体现浓硫酸的强氧化性,故D正确;
故答案:C。
3.A
【详解】①铝土矿与氢氧化钠反应生成偏铝酸钠,偏铝酸钠溶液通入足量的盐酸,生成氯化铝,得不到氢氧化铝,故①错误;
②盐卤(含MgCl2)与石灰乳反应生成氢氧化镁,氢氧化镁与盐酸反应生成氯化镁溶液,但由于Mg2+水解Mg2++2H2O Mg(OH)2+2H+,加热蒸发HCl挥发,平衡向右移动,所以得不到无水MgCl2,故②错误;
③氨催化氧化生成一氧化氮和水,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸,符合各步转化,故③正确;
④硫在氧气中燃烧只能生成二氧化硫,不能生成三氧化硫,故④错误;
⑤电解氯化钠溶液可以得到氯气,氯气与铁反应生成FeCl3,不是,故⑤错误;
⑥SiO2与氢氧化钠反应Na2SiO3,Na2SiO3溶液中通二氧化碳发生反应生成H2SiO3,故⑥正确;
综上所述选A。
4.D
【详解】A.由能与氨水反应可知,结合的能力强于,故滴加少量NaOH溶液,先反应,A项错误;
B.硝酸会将氧化为,B项错误;
C.次氯酸的酸性弱于碳酸,次氯酸与不反应,最终产物中次氯酸应写分子式,C项错误;
D.IBr中碘元素为+1价,溴元素为-1价,发生非氧化还原反应生成和,D项正确。
故选D。
5.D
【详解】A.三种气体都是大气污染物,NO易与空气中的氧气反应生成NO2,在空气中不能稳定存在,A项错误;
B.液态NH3汽化时吸收大量的热,因此,液氨常用作制冷剂,B项错误;
C.酸雨与二氧化硫和氮的氧化物有关,与二氧化碳无关,二氧化碳与温室效应有关,C项错误;
D.活性炭因吸附使品红褪色、SO2因发生化合反应使品红褪色、Na2O2因强氧化性使品红溶液褪色,原理不同,D项正确;
答案选D。
6.A
【详解】A.Fe与水蒸气在高温下反应产生Fe3O4,不是Fe2O3,Fe2O3与HCl反应产生FeCl3,不是FeCl2,因此不能在给定条件下实现物质的转化关系,A符合题意;
B.C与足量O2在点燃时反应产生CO2,CO2能够溶于水,与水反应产生H2CO3,能在给定条件下实现物质的转化关系,B不符合题意;
C.Al能够与O2反应产生Al2O3,Al2O3是两性氧化物,能够NaOH溶液反应产生NaAlO2,能在给定条件下实现物质的转化关系,C不符合题意;
D.Na与O2在加热时反应产生Na2O2,Na2O2与CO2反应产生Na2CO3和O2,D不符合题意;
故选A。
7.A
【详解】A.浓硫酸和乙醇加热到170°C,分子内脱水发生消去反应制备乙烯,故A正确;
B.常温下浓硫酸与铁发生钝化,不能制备硫酸铁,故B错误;
C.稀硫酸和铜不反应,故C错误;
D.浓硫酸和氯化钠固体共热制备氯化氢,故D错误;
故答案为A。
8.A
【详解】A.二氧化硫有毒,可以用作一定范围内的食品添加剂,但必需严格按照国家有关范围和标准使用,否则影响人体健康,A错误;
B.二氧化硫与水反应生成的酸可使蛋白质变性,SO2可用于杀菌消毒,B正确;
C.SO2具有漂白性,能使品红褪色,C正确;
D.工业上常用二氧化硫来漂白纸浆、丝毛、草帽等,此外二氧化硫还能够抑制霉菌和细菌的滋生,D正确;
答案选A。
9.A
【详解】A.铁与水蒸气在高温下生成Fe3O4和H2,故A正确;
B.氢氧化亚铁具有还原性,在空气中灼烧氧气将+2价Fe氧化+3价Fe,最终不能得到FeO,故B错误;
C.FeO是一种黑色粉末,不稳定,在空气里加热,最终被氧化成黑色的Fe3O4,故C错误;
D.铁无论过量还是不足,与氯气在加热条件下反应,均生成FeCl3,故D错误;
答案为A。
10.B
【详解】硝酸是一种无色,可以与水以任意比互溶,易挥发的液体,有刺激性气味,B项错误,故选B。
11.C
【详解】A.氮的固定分为三类:植物的根瘤菌固氮称为生物固氮、放电条件下生成一氧化氮为高能固氮、工业合成氨反应属于人工固氮,A正确;
B.豆科植物可将大气中的N2转化为NH3,从而实现生物固氮,B正确;
C.氨和铵盐在硝化细菌作用下最终转化为硝酸根离子,氮元素价态升高,被氧化,C不正确;
D.由二氧化碳与氨在一定条件下反应可制得尿素,从而实现含氮无机物与有机氮的转化,蛋白质在动物体内消化可生成氨,实现有机氮向含氮无机物的转化,D正确;
故选C。
12.C
【分析】根据4NO2+O2+2H2O=4HNO3、4NO+3O2+2H2O=4HNO3,剩余1.5体积气体,可能为NO,也可能为氧气,以此来计算。
【详解】
则一定体积的NO和3体积的氧气发生4NO+3O2+2H2O=4HNO3
①若剩余气体为NO,则由反应可知,消耗NO为4体积,则原NO的体积为1.5+4=5.5体积;
②若剩余气体为氧气,则4NO+3O2+2H2O=4HNO3中反应的氧气为1.5体积,则原NO的体积为=2体积,
故选C。
13.B
【详解】A.由于微溶于水,易溶于水,应先通入足量,使溶液呈碱性,然后再通入适量,反应的化学方程式为,通入和的顺序不可以互换,选项A错误;
B.向硫酸钙悬浊液中通入足量的氨气,使溶液呈碱性,再通入适量的二氧化碳利于反应的进行,硫酸钙与氨气、水和二氧化碳反应生成了硫酸铵和碳酸钙沉淀。操作2是溶液中得到溶质固体的过程,需要蒸发浓缩、冷却结晶、过滤、洗涤、干燥等,可得,选项B正确;
C.硫酸钙与氨气、水和二氧化碳反应生成了硫酸铵和碳酸钙沉淀,物质发生的主要化学反应为,反应的离子方程式为,选项C错误;
D.反应过程中二氧化碳参与反应生成硫酸铵和碳酸钙,碳酸钙分解生成二氧化碳,工艺流程中产生的可循环利用,通入足量,通适量二氧化碳,否则碳酸钙溶解,选项D错误。
答案选B。
14.B
【分析】碘化亚铁溶液通入氯气,先观察到紫色,说明氯气先将碘离子氧化成碘单质,然后观察到血红色,说明氯气将亚铁离子氧化成Fe3+,据此分析;
【详解】A.根据图象,导管下端在四氯化碳溶液中,HCl不溶于四氯化碳,不能发生倒吸,故A错误;
B.通入足量的氯气后,振荡试管,因四氯化碳的密度大于水,且不与水互溶,四氯化碳在下层,水层在上层,碘单质易溶于四氯化碳,即下层显紫色,Fe3+在水层,即上层显红色,故B正确;
C.根据上述分析,氯气先氧化成碘离子,再氧化亚铁离子,说明氯气的氧化性最强,碘离子的还原性强于亚铁离子,从而推出Fe3+的氧化性强于I2,故C错误;
D.根据上述分析,氯气先氧化碘离子,将碘离子氧化完后,再与亚铁离子反应,题中所给离子方程式是先氧化亚铁离子,因此离子方程式可以是2Fe2++4I-+3Cl2=2I2+2Fe3++6Cl-,故D错误;
答案为B。
15. CaCO3+2H+=Ca2++H2O+CO2↑ Ca2++2OH-+CO2=CaCO3↓+H2O Fe2O3+6H+=2Fe3++3H2O Fe+2H+=Fe2++H2↑
【分析】碳酸钙与盐酸反应生成氯化钙、二氧化碳和水;用澄清石灰水检验 CO2 气体,澄清石灰水变浑浊,生成碳酸钙;表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始时氧化铁与稀硫酸反应生成硫酸铁和水,片刻后,可观察到有气体产生,是铁与稀硫酸反应生成硫酸亚铁和氢气,据此书写反应的离子方程式。
【详解】(1)碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,反应的离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑; 用澄清石灰水检验 CO2 气体,澄清石灰水变浑浊,生成碳酸钙和水,反应的离子方程式为Ca2++2OH-+CO2=CaCO3↓+H2O,故答案为:CaCO3+2H+=Ca2++H2O+CO2↑; Ca2++2OH-+CO2=CaCO3↓+H2O;
(2)表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始时氧化铁与稀硫酸反应生成硫酸铁和水,反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O ,反应片刻后,可观察到有气体产生,是铁与稀硫酸反应生成硫酸亚铁和氢气,反应的离子方程式为Fe+2H+=Fe2++H2↑,故答案为:Fe2O3+6H+=2Fe3++3H2O;Fe+2H+=Fe2++H2↑。
16.(1)氧化物
(2) 黄色
(3)
(4)8
(5)漂白性
(6)常温下,铁或铝被浓硝酸氧化,生成一层致密的氧化物薄膜,这层薄膜阻止了酸与内层金属的进一步反应(合理即可)
(7)
【解析】(1)
的物质类别是氧化物;
(2)
芒硝的化学式为,芒硝在酒精灯上灼烧,火焰呈现的颜色为黄色;
(3)
实验室制备氨气反应的化学方程式为;
(4)
D可以为或,已知同温同压下,同体积的与(蒸气)的物质的量相同,则,解得:;
(5)
与氢氧化钠溶液反应,体现其酸性氧化物的性质,与溴水反应体现其还原性,与品红溶液反应,体现其漂白性;
(6)
常温下,浓硝酸可以用干燥的铁或铝容器盛装,是因为常温下,铁或铝被浓硝酸氧化,生成一层致密的氧化物薄膜,这层薄膜阻止了酸与内层金属的进一步反应;
(7)
能被酸性高锰酸钾溶液氧化为硝酸钠,同时紫红色溶液褪色,该反应的离子方程式为。
17.(1)干燥剂
(2)脱水性、强氧化性
(3)BaSO4
【解析】(1)
浓硫酸具有吸水性,能够吸收气体、液体中的水分子及固体中的结晶水,故常用作干燥剂,故答案为:干燥剂;
(2)
蔗糖逐渐变黑,体现了浓硫酸的脱水性,体积膨胀,并放出有刺激性气味的气体SO2,体现了浓硫酸的强氧化性,故答案为:脱水性、强氧化性;
(3)
BaSO4不溶于胃酸,在医疗上可被用作消化系统X射线检查的内服药剂,俗称钡餐,故答案为:BaSO4。
18.(1)
(2)
(3)
【分析】向铁铜的混合粉末中加入溶液,由于铁的还原性比铜的强,氯化铁的氧化性比氯化铜强,故最先发生反应2Fe3++Fe=3Fe2+,还可能发生2Fe3++Cu=2Fe2++Cu2+、Fe+Cu2+=Fe2++Cu,据此回答。
【详解】(1)若金属无剩余,则2Fe3++Fe=3Fe2+、2Fe3++Cu=2Fe2++Cu2+必定发生,溶液中一定存在的金属阳离子有,可能存在的有。
(2)若剩余固体中有铁和铜,则溶液中不存在,反应2Fe3++Fe=3Fe2+ 、Fe+Cu2+=Fe2++Cu必定发生,则溶液中一定存在的金属阳离子有,一定不存在。
(3)若剩余固体中只有铜,则溶液中不存在,反应2Fe3++Fe=3Fe2+必定发生,溶液中一定存在的金属阳离子有,可能存在的有,一定不存在。
19.(1)Fe3+、HCO
(2)Al(OH)3、Mg(OH)2
(3) NH 取少量待测液加入浓的NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,说明溶液有NH3 H2O
(4)Al(OH)3+OH-═AlO+2H2O
(5)n(H+):n(NH):n(Mg2+):n(Al3+):n(SO)=2:4:3:2:9
【分析】无色溶液,则一定不含Fe3+,加入NaOH溶液后,在0-a段没有生成沉淀,说明溶液中一定存在H+或HCO离子,由于后面有沉淀生成及部分沉淀溶解可知,溶液中一定存在Al3+,由于HCO和Al3+会发生双水解而不能共存,则只能存在H+,a-b段生成沉淀消耗了6a体积氢氧化钠,又c-d段部分沉淀溶解,可知溶液中一定存在Mg2+、Al3+,根据图象Al(OH)3的物质的量与剩余的沉淀的物质的量相等,由OH-~AlO可知消耗溶解氢氧化铝消耗了a体积氢氧化钠,所以生成氢氧化铝沉淀消耗了3a体积氢氧化钠,Mg2+生成的沉淀的量也消耗3a体积氢氧化钠,b-c段沉淀的物质的量不变,说明氢氧根离子与铵离子发生了反应,即溶液中一定存在NH,根据溶液呈电中性可知,溶液中一定存在SO;综上所述,原溶液中含有的阳离子是H+、NH、Mg2+、Al3+、SO,一定不存在Fe3+、HCO,据此分析解答。
(1)
含Fe3+溶液为黄色,由分析可知,该无色溶液中一定不存在的离子有Fe3+、HCO;
(2)
根据以上分析,溶液中一定存在Mg2+、Al3+,所以ab段生成沉淀的化学式为:Al(OH)3、Mg(OH)2,故答案为:Al(OH)3、Mg(OH)2;
(3)
b-c段沉淀的物质的量不变,说明加入的NaOH与原溶液中的NH反应生成NH3 H2O,证明溶液中含NH,检验该离子的实验操作及现象是:取少量待测液加入浓的NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,说明溶液有NH3 H2O,故答案为:NH;取少量待测液加入浓的NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,说明溶液有NH3 H2O;
(4)
cd段沉淀减少是氢氧化铝与氢氧化钠反应,反应的离子方程式为:Al(OH)3+OH-═AlO+2H2O,故答案为:Al(OH)3+OH-═AlO+2H2O;
(5)
原溶液中含有的阳离子是H+、NH、Mg2+、Al3+,根据消耗的氢氧化钠的物质的量可以认为n(H+)=a,n(Al3+)=a,n(Mg2+)=1.5a,n(NH)=2a,根据电荷守恒,n(SO)=4.5a,n(H+):n(NH):n(Mg2+):n(Al3+):n(SO)=2:4:3:2:9,故答案为:n(H+):n(NH):n(Mg2+):n(Al3+):n(SO)=2:4:3:2:9。
20. 、
【详解】根据化合物中化合价代数和为0可知,中Fe元素化合价为+2价,中Fe元素化合价为+3价,可以看成,故Fe元素化合价为+2、+3价,与氢离子反应的离子方程式为,与氢离子反应的离子方程式为。
21.(1) a≤b 30%
(2)
(3) 4FeS2+11O22Fe2O3+8SO2 2.75
【分析】(1)
由题意可知,NO2能被NaOH溶液吸收,NO和NO2按1∶1的比例能被NaOH溶液吸收,NO不能被NaOH溶液吸收,故n(NO2)≥n(NO)即可,即a≤b;设混合气中NO、NO2物质的量分别为x、y,根据反应NO+NO2+2NaOH=2NaNO2+H2O,该反应消耗NO2物质的量为x,生成NaNO2物质的量为2x,则反应2NO2+2NaOH=NaNO2+NaNO3+H2O消耗NO2物质的量为(y-x),生成NaNO2、NaNO3物质的量都为,溶液中NaNO2和NaNO3的物质的量之比为4∶1,则(2x+):=4:1,解得x:y=3:7,故混合气体中NO物质的量分数为30%,即混合气体中NO的体积分数为30%;答案为:a≤b;30%。
(2)
①根据表中离子可知,SO2被氧化成,被还原成Cl-,结合得失电子守恒、电荷守恒、原子守恒,SO2和NaClO2反应的离子方程式为2SO2++2H2O=2+Cl-+4H+;答案为:2SO2++2H2O=2+Cl-+4H+。
②溶液中的电荷守恒为c(Na+)+c(H+)=2c()+c()+c(Cl-)+c(OH-),3×10-3mol/L+3.8×10-4mol/L=2ymol/L+8.8×10-4mol/L+1×10-3mol/L+mol/L,解得y=7.5×10-4;答案为7.5×10-4。
(3)
煅烧硫铁矿生成Fe2O3和SO2,反应的化学方程式为4FeS2+11O22Fe2O3+8SO2;反应中生成8molSO2时转移44mol电子,标准状况下11.2LSO2物质的量为0.5mol,则转移电子数为=2.75mol,转移电子数为2.75NA;答案为:4FeS2+11O22Fe2O3+8SO2;2.75。
