3.2.2酚 课件(共35张PPT)
文档属性
| 名称 | 3.2.2酚 课件(共35张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-16 00:00:00 | ||
图片预览







文档简介
第二节 醇 酚
第二课时 酚
第三章 烃的衍生物
浓度很低的某些酚类溶液(与水的比例通常在 1:20 ~1:40),可以用来消毒杀菌。
在19世纪初,医院的设备很差,那时缺少麻醉药和消毒剂,许多病人死于手术后的伤口感染中。在英国的爱丁堡有一家医院,一名叫李斯特的的外科医生,发现在化工厂附近的污水沟里,沟水清澈,浮在水面上的草根很少腐烂。原来,就是从化工厂流出的石炭酸(苯酚)混杂在沟水里,石炭酸是化工厂提炼煤焦油时排出的“废弃物”。李斯特用石炭酸对手术器械、纱布等一系列用品进行了消毒,病人手术后伤口化脓、感染的现象立即减少了,死亡率大大下降。由此,爱丁堡医院手术伤口感染率一度成为全世界外科医院中最低的。这一发现使苯酚成为一种强有力的外科消毒剂,李斯特也因此被誉为“外科消毒之父”。同时使苯酚首次声名远扬。
是谁使苯酚声名远扬?
“外科消毒之父”-
约瑟夫·李斯特
了解酚典型代表物的组成、结构特点及性质。
能列举事实说明有机分子中集团之间存在相互影响。
学习目标
HO
OH
OH
OH
OCH3
CH2
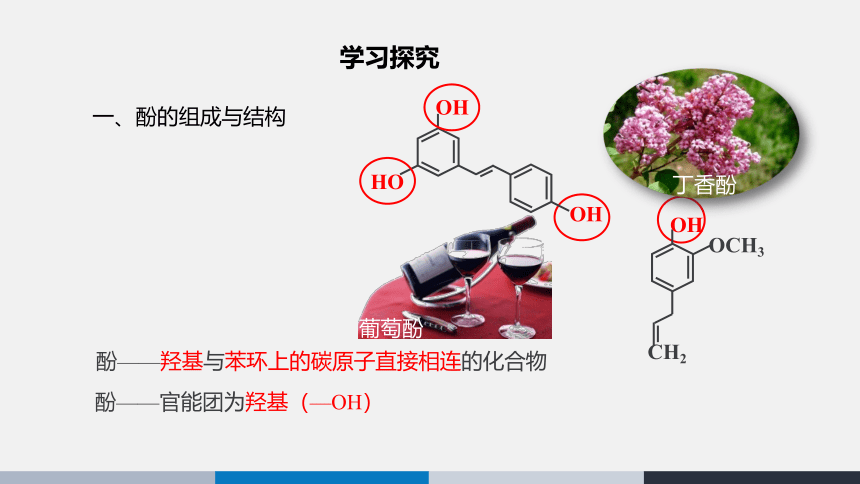
葡萄酚
丁香酚
一、酚的组成与结构
酚——羟基与苯环上的碳原子直接相连的化合物
酚——官能团为羟基(—OH)
学习探究
二、苯酚的组成、结构与性质
1.组成与结构
苯酚是一元酚,是酚类化合物最简单的,其官能团为羟基(—OH)。
名称
苯酚,俗称石灰酸
分子式
C6H6O
官能团
—OH
结构特点
羟基与苯环直接相连
2.物理性质
(1)纯净的苯酚是无色晶体,有特殊气味,放置时间较长的苯酚,因部分被空气中的O2氧化而呈粉红色,所以保存时要密封。
(2)苯酚室温下在水中的溶解度为9.2 g,当温度高于65 ℃时能与水混溶,苯酚易溶于有机溶剂。熔点为43℃
(3)苯酚有毒,对皮肤有腐蚀性,如不慎沾到皮肤上,应立即用乙醇冲洗,再用水冲洗。
医院常用的“来苏水”消毒剂便是苯酚钠盐的稀溶液。
思考:常温下将苯酚溶于水,会有什么现象?加热苯酚和水的混合物,会发生什么现象?再冷却该混合物至室温,会发生什么现象?
苯酚乳浊液
加热
溶解度增大
苯酚澄清溶液
冷却
溶解度下降
苯酚乳浊液
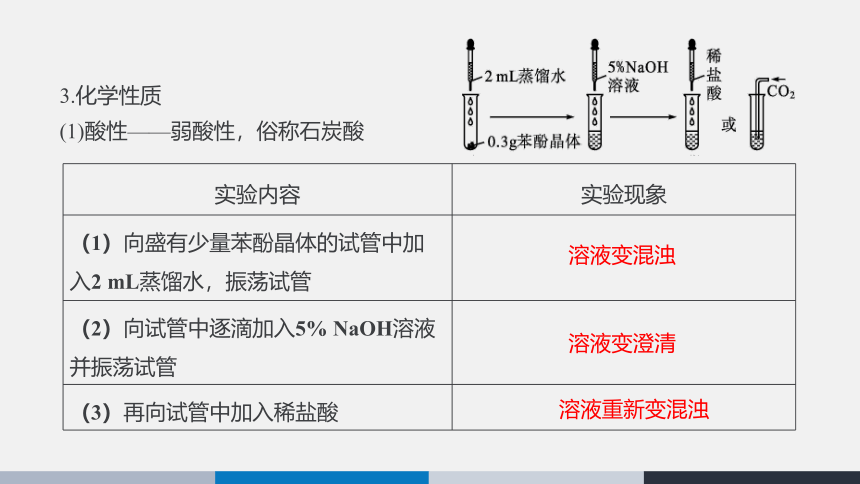
3.化学性质
(1)酸性——弱酸性,俗称石炭酸
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}实验内容
实验现象
(1)向盛有少量苯酚晶体的试管中加入2 mL蒸馏水,振荡试管
(2)向试管中逐滴加入5% NaOH溶液并振荡试管
(3)再向试管中加入稀盐酸
溶液变混浊
溶液变澄清
溶液重新变混浊
加入氢氧化钠溶液
加入稀盐酸
苯酚能与碱反应,体现酸性。因此,苯酚俗称石炭酸。
但是不能使酸碱指示剂变色
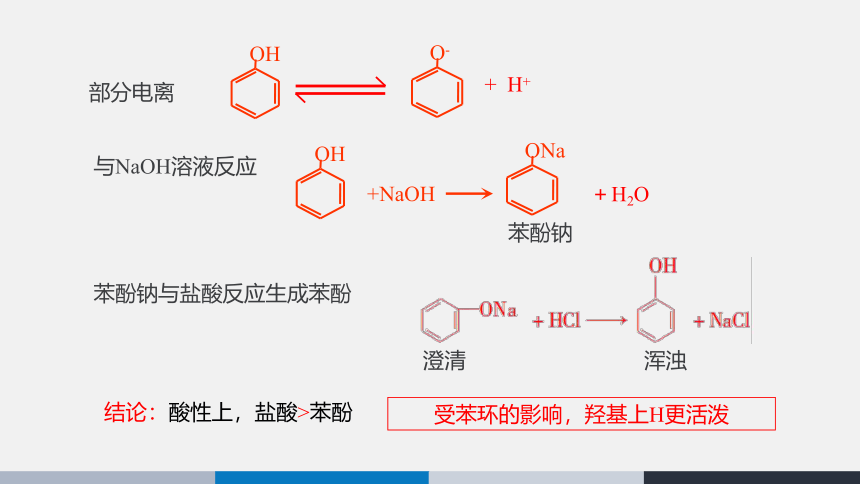
结论:酸性上,盐酸>苯酚
受苯环的影响,羟基上H更活泼
澄清
浑浊
OH
O-
+ H+
部分电离
+H2O
OH
ONa
+NaOH
与NaOH溶液反应
苯酚钠
苯酚钠与盐酸反应生成苯酚
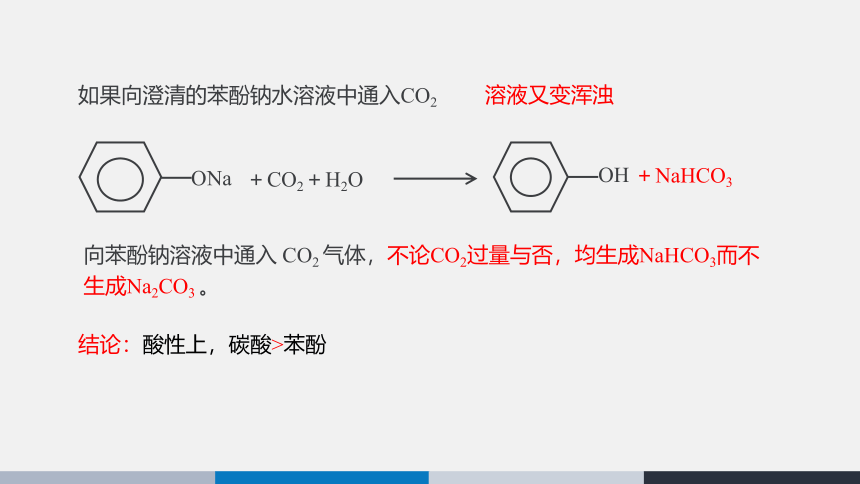
结论:酸性上,碳酸>苯酚
+CO2+H2O
+NaHCO3
OH
ONa
如果向澄清的苯酚钠水溶液中通入CO2
溶液又变浑浊
向苯酚钠溶液中通入 CO2 气体,不论CO2过量与否,均生成NaHCO3而不生成Na2CO3 。
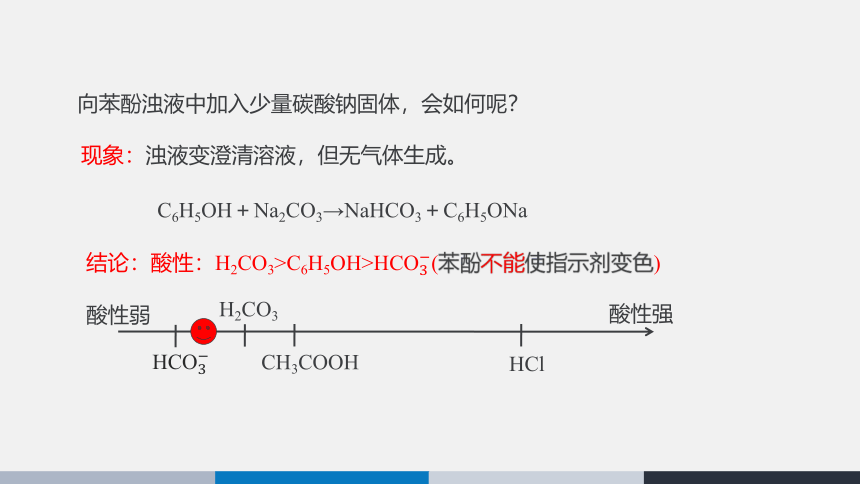
向苯酚浊液中加入少量碳酸钠固体,会如何呢?
现象:浊液变澄清溶液,但无气体生成。
C6H5OH+Na2CO3→NaHCO3+C6H5ONa
结论:酸性:H2CO3>C6H5OH>HCO3?(苯酚不能使指示剂变色)
?
H2CO3
CH3COOH
HCl
酸性强
酸性弱
HCO3?
?
C2H5OH
C6H5OH
酸性
NaOH
Na
原因
无
有
不反应
反应
反应温和
反应较剧烈
苯环对羟基的影响使得酚羟基的氢原子较为活泼
对比:乙醇和苯酚的化学性质
醇羟基与酚羟基的比较
代表物
乙醇
苯酚
是否具有酸性
与钠反应
与NaOH的反应
与Na2CO3的反应
与NaHCO3的反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}实验内容
向盛有少量苯酚稀溶液的试管里逐滴加入饱和溴水,边加边振荡,观察实验现象。
实验现象
实验原理
应用
现象:白色沉淀生成
2,4,6-三溴苯酚
此沉淀难溶于水,易溶于有机溶剂
+3Br2
+3HBr
(过量)
OH
OH
Br
Br
Br
现象:白色沉淀生成
(2)取代反应
苯酚的定性检验和定量测定
羟基对苯环的影响,使苯环上羟基邻、对位氢原子更活泼,易被取代
②可用于苯酚定性检验和定量测定,但不能用该反应来分离苯和苯酚
注:
①若溴水少量,则生成的三溴苯酚溶于苯酚,看不到沉淀;因此必须用过量的浓溴水或饱和溴水,但不需加热也不需加催化剂
苯酚也能像苯一样发生硝化、磺化、加成等反应。
+3H2
Ni
△
OH
OH
(环己醇)
+3HNO3
+3H2O
浓硫酸
OH
OH
NO2
NO2
O2N
(苦味酸)
△
类别
苯
苯酚
结构简式
溴化
反应
溴的状态
条件
产物
结论
原因
?Br
Br?
OH
Br
?OH
?Br
苯酚与溴的取代反应比苯易进行
酚羟基对苯环影响,使苯环上羟基邻、对位的氢原子的活性增强,易被取代
一元取代
三元取代
液溴
饱和溴水
FeBr3作催化剂
不需要催化剂
(1)由于苯环对羟基的影响,O一H极性变强,氢原子易电离而使苯酚表现弱酸性;醇羟基在水溶液中无法电离
(2)由于羟基对苯环的影响,苯环上处于羟基邻位和对位的氢原子的活性增强,从而使苯酚比苯更易与溴发生取代反应。
思考与讨论:
如何从分子内基团间相互作用的角度来解释下列事实:
(1)苯酚的酸性比乙醇的强。
(2)苯和苯酚发生溴代反应的条件和产物有很大的不同。
(3)显色反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}实验现象
结论
应用
溶液呈紫色
苯酚能与FeCl3反应,使溶液显紫色
用FeCl3溶液可以检验苯酚的存在
检验酚羟基存在的方法:
(1)与饱和溴水反应产生白色沉淀。
(2)滴加氯化铁溶液会显紫色。
紫色溶液
苯酚与FeCl3溶液作用显紫色,利用此性质也可以检验苯酚的存在。酚类物质一般都可以与FeCl3作用显色,可用于检验其存在。
a. 苯酚在空气中被O2氧化呈粉红色
b. 苯酚能使酸性KMnO4溶液褪色
c. 苯酚可以燃烧
(4)氧化反应
咬过的苹果或香蕉等水果,暴露在空气中
一段时间后,可以看到断面处变为棕色,
这种颜色的变化是由于酚类化合物被氧化
所致的。在氧气的作用下,水果中的酶将
酚转化为醌,因此显棕色。水果中含有多
种酚类物质,它们是形成水果口感、酸味以及颜色的一个重要来源,许多酚类物质具有重要的营养和保健功能。断面的棕色可以作为水果中含有酚类物质的一个标志,同时也说明酚进入人体后可以起到阻止有害氧化反应发生的作用。
化学与生活
类别
脂肪醇
芳香醇
酚
实例
CH3CH2OH
?
?
官能团
醇羟基(—OH)
酚羟基(—OH)
结构特点
—OH与链烃基相连
—OH与苯环侧链上的碳原子相连
—OH与苯环直接相连
化学性质
共性
(1)与钠反应 (2)取代反应 (3)氧化反应
—
加成反应(苯环的加成)
异性
(1)酯化反应
(2)消去反应(部分不能)
(1)弱酸性
(2)显色反应
脂肪醇、芳香醇和酚的比较
(1)醇与酚所含的官能团都为—OH,但醇—OH与饱和碳原子相连,酚—OH与苯环直接相连,决定两者化学性质有不同之处。
(2)醇和酚都能与金属钠反应放出H2,但由于苯环的存在,使苯酚中O—H易断裂,呈现弱酸性,能与NaOH反应生成 ,醇与NaOH不反应。
(3)由于苯环的存在,C—O不易断裂,但醇中的—OH能参与反应,醇能发生消去反应,酚不发生消去反应。醇中的—OH可被—X取代,而酚不能。
醇与酚性质对比的注意点
类别
苯
甲苯
苯酚
氧化反应
不被酸性KMnO4溶液氧化
可被酸性KMnO4溶液氧化
常温下在空气中部分被O2氧化,呈粉红色
取代反应
溴的状态
液溴
液溴
饱和溴水
条件
催化剂
催化剂
无催化剂
产物
?
甲苯的邻、对
两种一溴代物
?
苯、甲苯、苯酚的比较
类别
苯
甲苯
苯酚
取代反应
特点
苯酚与溴的取代反应比苯、甲苯易进行
原因
酚羟基对苯环的影响使苯环在羟基的邻、对位上的氢原子变得活泼,易被取代
与H2加成
条件
催化剂、加热
结论
都含苯环,故都可发生加成反应
酚的应用与危害
应用:苯酚是一种重要的化工原料,广泛用于制造酚醛树脂、染料、医药、农药等。
危害:含酚类物质的废水对生物具有毒害作用,会对水体造成严重污染。
来源:化工厂和炼焦厂的废水中常含有酚类物质,在排放前必须经过处理。
苯酚的用途
酚醛树脂
合成纤维
合成香料
医药
消毒剂
染料
农药
防腐剂
学习小结
1.下列关于苯酚的叙述,正确的是( )
A.热的苯酚浓溶液,冷却时不会形成浊液
B.苯酚可以和饱和溴水发生取代反应
C.苯酚既难溶于水也难溶于NaOH溶液
D.苯酚的酸性比碳酸强,比醋酸弱
B
当堂检测
2.三百多年前,著名化学家波义耳发现了铁盐与没食子酸(结构简式如图所
示 )的显色反应,并由此发明了蓝黑墨水。与制造蓝黑墨水相关的基团可能是( )
A.苯环 B.羧基
C.羧基中的羟基 D.酚羟基
D
3.下列关于苯酚的叙述中,不正确的是( )
A.其浓溶液如果不慎沾在皮肤上,应立即用酒精擦洗
B.其水溶液显强酸性,俗称石炭酸
C.超过65 ℃可以与水以任意比互溶
D.纯净的苯酚是无色晶体,在空气中易被氧化而呈粉红色
B
4.关于 的说法中,不正确的是( )
A.都能与金属钠反应放出氢气
B.三者互为同系物
C.都能使酸性KMnO4溶液褪色
D.都能在一定条件下发生取代反应
B
5.漆酚是我国特产漆的主要成分,结构如下所示,苯环侧链烃基为链状结构,则下列说法错误的是 ( )
A.能与FeCl3溶液发生显色反应
B.能使酸性KMnO4溶液褪色
C.能与NaHCO3溶液反应放出CO2
D.1 mol漆酚与足量浓溴水反应最多消耗5 mol Br2
C
本节内容结束
第二课时 酚
第三章 烃的衍生物
浓度很低的某些酚类溶液(与水的比例通常在 1:20 ~1:40),可以用来消毒杀菌。
在19世纪初,医院的设备很差,那时缺少麻醉药和消毒剂,许多病人死于手术后的伤口感染中。在英国的爱丁堡有一家医院,一名叫李斯特的的外科医生,发现在化工厂附近的污水沟里,沟水清澈,浮在水面上的草根很少腐烂。原来,就是从化工厂流出的石炭酸(苯酚)混杂在沟水里,石炭酸是化工厂提炼煤焦油时排出的“废弃物”。李斯特用石炭酸对手术器械、纱布等一系列用品进行了消毒,病人手术后伤口化脓、感染的现象立即减少了,死亡率大大下降。由此,爱丁堡医院手术伤口感染率一度成为全世界外科医院中最低的。这一发现使苯酚成为一种强有力的外科消毒剂,李斯特也因此被誉为“外科消毒之父”。同时使苯酚首次声名远扬。
是谁使苯酚声名远扬?
“外科消毒之父”-
约瑟夫·李斯特
了解酚典型代表物的组成、结构特点及性质。
能列举事实说明有机分子中集团之间存在相互影响。
学习目标
HO
OH
OH
OH
OCH3
CH2
葡萄酚
丁香酚
一、酚的组成与结构
酚——羟基与苯环上的碳原子直接相连的化合物
酚——官能团为羟基(—OH)
学习探究
二、苯酚的组成、结构与性质
1.组成与结构
苯酚是一元酚,是酚类化合物最简单的,其官能团为羟基(—OH)。
名称
苯酚,俗称石灰酸
分子式
C6H6O
官能团
—OH
结构特点
羟基与苯环直接相连
2.物理性质
(1)纯净的苯酚是无色晶体,有特殊气味,放置时间较长的苯酚,因部分被空气中的O2氧化而呈粉红色,所以保存时要密封。
(2)苯酚室温下在水中的溶解度为9.2 g,当温度高于65 ℃时能与水混溶,苯酚易溶于有机溶剂。熔点为43℃
(3)苯酚有毒,对皮肤有腐蚀性,如不慎沾到皮肤上,应立即用乙醇冲洗,再用水冲洗。
医院常用的“来苏水”消毒剂便是苯酚钠盐的稀溶液。
思考:常温下将苯酚溶于水,会有什么现象?加热苯酚和水的混合物,会发生什么现象?再冷却该混合物至室温,会发生什么现象?
苯酚乳浊液
加热
溶解度增大
苯酚澄清溶液
冷却
溶解度下降
苯酚乳浊液
3.化学性质
(1)酸性——弱酸性,俗称石炭酸
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}实验内容
实验现象
(1)向盛有少量苯酚晶体的试管中加入2 mL蒸馏水,振荡试管
(2)向试管中逐滴加入5% NaOH溶液并振荡试管
(3)再向试管中加入稀盐酸
溶液变混浊
溶液变澄清
溶液重新变混浊
加入氢氧化钠溶液
加入稀盐酸
苯酚能与碱反应,体现酸性。因此,苯酚俗称石炭酸。
但是不能使酸碱指示剂变色
结论:酸性上,盐酸>苯酚
受苯环的影响,羟基上H更活泼
澄清
浑浊
OH
O-
+ H+
部分电离
+H2O
OH
ONa
+NaOH
与NaOH溶液反应
苯酚钠
苯酚钠与盐酸反应生成苯酚
结论:酸性上,碳酸>苯酚
+CO2+H2O
+NaHCO3
OH
ONa
如果向澄清的苯酚钠水溶液中通入CO2
溶液又变浑浊
向苯酚钠溶液中通入 CO2 气体,不论CO2过量与否,均生成NaHCO3而不生成Na2CO3 。
向苯酚浊液中加入少量碳酸钠固体,会如何呢?
现象:浊液变澄清溶液,但无气体生成。
C6H5OH+Na2CO3→NaHCO3+C6H5ONa
结论:酸性:H2CO3>C6H5OH>HCO3?(苯酚不能使指示剂变色)
?
H2CO3
CH3COOH
HCl
酸性强
酸性弱
HCO3?
?
C2H5OH
C6H5OH
酸性
NaOH
Na
原因
无
有
不反应
反应
反应温和
反应较剧烈
苯环对羟基的影响使得酚羟基的氢原子较为活泼
对比:乙醇和苯酚的化学性质
醇羟基与酚羟基的比较
代表物
乙醇
苯酚
是否具有酸性
与钠反应
与NaOH的反应
与Na2CO3的反应
与NaHCO3的反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}实验内容
向盛有少量苯酚稀溶液的试管里逐滴加入饱和溴水,边加边振荡,观察实验现象。
实验现象
实验原理
应用
现象:白色沉淀生成
2,4,6-三溴苯酚
此沉淀难溶于水,易溶于有机溶剂
+3Br2
+3HBr
(过量)
OH
OH
Br
Br
Br
现象:白色沉淀生成
(2)取代反应
苯酚的定性检验和定量测定
羟基对苯环的影响,使苯环上羟基邻、对位氢原子更活泼,易被取代
②可用于苯酚定性检验和定量测定,但不能用该反应来分离苯和苯酚
注:
①若溴水少量,则生成的三溴苯酚溶于苯酚,看不到沉淀;因此必须用过量的浓溴水或饱和溴水,但不需加热也不需加催化剂
苯酚也能像苯一样发生硝化、磺化、加成等反应。
+3H2
Ni
△
OH
OH
(环己醇)
+3HNO3
+3H2O
浓硫酸
OH
OH
NO2
NO2
O2N
(苦味酸)
△
类别
苯
苯酚
结构简式
溴化
反应
溴的状态
条件
产物
结论
原因
?Br
Br?
OH
Br
?OH
?Br
苯酚与溴的取代反应比苯易进行
酚羟基对苯环影响,使苯环上羟基邻、对位的氢原子的活性增强,易被取代
一元取代
三元取代
液溴
饱和溴水
FeBr3作催化剂
不需要催化剂
(1)由于苯环对羟基的影响,O一H极性变强,氢原子易电离而使苯酚表现弱酸性;醇羟基在水溶液中无法电离
(2)由于羟基对苯环的影响,苯环上处于羟基邻位和对位的氢原子的活性增强,从而使苯酚比苯更易与溴发生取代反应。
思考与讨论:
如何从分子内基团间相互作用的角度来解释下列事实:
(1)苯酚的酸性比乙醇的强。
(2)苯和苯酚发生溴代反应的条件和产物有很大的不同。
(3)显色反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}实验现象
结论
应用
溶液呈紫色
苯酚能与FeCl3反应,使溶液显紫色
用FeCl3溶液可以检验苯酚的存在
检验酚羟基存在的方法:
(1)与饱和溴水反应产生白色沉淀。
(2)滴加氯化铁溶液会显紫色。
紫色溶液
苯酚与FeCl3溶液作用显紫色,利用此性质也可以检验苯酚的存在。酚类物质一般都可以与FeCl3作用显色,可用于检验其存在。
a. 苯酚在空气中被O2氧化呈粉红色
b. 苯酚能使酸性KMnO4溶液褪色
c. 苯酚可以燃烧
(4)氧化反应
咬过的苹果或香蕉等水果,暴露在空气中
一段时间后,可以看到断面处变为棕色,
这种颜色的变化是由于酚类化合物被氧化
所致的。在氧气的作用下,水果中的酶将
酚转化为醌,因此显棕色。水果中含有多
种酚类物质,它们是形成水果口感、酸味以及颜色的一个重要来源,许多酚类物质具有重要的营养和保健功能。断面的棕色可以作为水果中含有酚类物质的一个标志,同时也说明酚进入人体后可以起到阻止有害氧化反应发生的作用。
化学与生活
类别
脂肪醇
芳香醇
酚
实例
CH3CH2OH
?
?
官能团
醇羟基(—OH)
酚羟基(—OH)
结构特点
—OH与链烃基相连
—OH与苯环侧链上的碳原子相连
—OH与苯环直接相连
化学性质
共性
(1)与钠反应 (2)取代反应 (3)氧化反应
—
加成反应(苯环的加成)
异性
(1)酯化反应
(2)消去反应(部分不能)
(1)弱酸性
(2)显色反应
脂肪醇、芳香醇和酚的比较
(1)醇与酚所含的官能团都为—OH,但醇—OH与饱和碳原子相连,酚—OH与苯环直接相连,决定两者化学性质有不同之处。
(2)醇和酚都能与金属钠反应放出H2,但由于苯环的存在,使苯酚中O—H易断裂,呈现弱酸性,能与NaOH反应生成 ,醇与NaOH不反应。
(3)由于苯环的存在,C—O不易断裂,但醇中的—OH能参与反应,醇能发生消去反应,酚不发生消去反应。醇中的—OH可被—X取代,而酚不能。
醇与酚性质对比的注意点
类别
苯
甲苯
苯酚
氧化反应
不被酸性KMnO4溶液氧化
可被酸性KMnO4溶液氧化
常温下在空气中部分被O2氧化,呈粉红色
取代反应
溴的状态
液溴
液溴
饱和溴水
条件
催化剂
催化剂
无催化剂
产物
?
甲苯的邻、对
两种一溴代物
?
苯、甲苯、苯酚的比较
类别
苯
甲苯
苯酚
取代反应
特点
苯酚与溴的取代反应比苯、甲苯易进行
原因
酚羟基对苯环的影响使苯环在羟基的邻、对位上的氢原子变得活泼,易被取代
与H2加成
条件
催化剂、加热
结论
都含苯环,故都可发生加成反应
酚的应用与危害
应用:苯酚是一种重要的化工原料,广泛用于制造酚醛树脂、染料、医药、农药等。
危害:含酚类物质的废水对生物具有毒害作用,会对水体造成严重污染。
来源:化工厂和炼焦厂的废水中常含有酚类物质,在排放前必须经过处理。
苯酚的用途
酚醛树脂
合成纤维
合成香料
医药
消毒剂
染料
农药
防腐剂
学习小结
1.下列关于苯酚的叙述,正确的是( )
A.热的苯酚浓溶液,冷却时不会形成浊液
B.苯酚可以和饱和溴水发生取代反应
C.苯酚既难溶于水也难溶于NaOH溶液
D.苯酚的酸性比碳酸强,比醋酸弱
B
当堂检测
2.三百多年前,著名化学家波义耳发现了铁盐与没食子酸(结构简式如图所
示 )的显色反应,并由此发明了蓝黑墨水。与制造蓝黑墨水相关的基团可能是( )
A.苯环 B.羧基
C.羧基中的羟基 D.酚羟基
D
3.下列关于苯酚的叙述中,不正确的是( )
A.其浓溶液如果不慎沾在皮肤上,应立即用酒精擦洗
B.其水溶液显强酸性,俗称石炭酸
C.超过65 ℃可以与水以任意比互溶
D.纯净的苯酚是无色晶体,在空气中易被氧化而呈粉红色
B
4.关于 的说法中,不正确的是( )
A.都能与金属钠反应放出氢气
B.三者互为同系物
C.都能使酸性KMnO4溶液褪色
D.都能在一定条件下发生取代反应
B
5.漆酚是我国特产漆的主要成分,结构如下所示,苯环侧链烃基为链状结构,则下列说法错误的是 ( )
A.能与FeCl3溶液发生显色反应
B.能使酸性KMnO4溶液褪色
C.能与NaHCO3溶液反应放出CO2
D.1 mol漆酚与足量浓溴水反应最多消耗5 mol Br2
C
本节内容结束
