2.3 原子的结构(第二课时)课件(共25张PPT)2022-2023学年九年级上册鲁教版化学
文档属性
| 名称 | 2.3 原子的结构(第二课时)课件(共25张PPT)2022-2023学年九年级上册鲁教版化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-17 00:00:00 | ||
图片预览






文档简介
(共25张PPT)
第三节 原子的结构
(第二课时)
第二单元 探秘水世界
PART
01
PART
02
知道什么是相对原子质量,能说出相对原子质量和实际质量的关系,能根据相对原子质量的概念进行简单计算。
知道原子和离子之间可以相互转化,初步认识核外电子在化学反应中的作用。
学习目标
PART
03
认识到用一种新的标准——碳12原子质量的1/12来衡量原子质量的大小,会使得衡量结果更接近常规的数据范围,这是一种重要的科学方法。
从微观角度来看,化学反应的实质是分子破裂为原子,原子重新组成新的分子。化学变化前后分子的种类一定改变,而原子的种类、数目不变。
原子是化学变化中的最小粒子
原子能不能再分呢?原子是由什么构成的呢?
如何把核外电子层排布形象地表示出来?
1.核外电子的分层排布
电子层数:1、2、3、4、5、6、7
电子能量:
离核远近:
能量越低,离核越近;能量越高,离核越远。
一、原子中的电子
低 高
近 远
一个氧原子的原子核内有8个质子和8个中子。核外有8个电子,其中有2个电子能量相近都较低,另外6个电子能量相近且能量稍高。这些电子都同时绕原子核高速运动。
根据刚才的理解,请你把氧原子的结构以最简洁的方式画出来。
资料介绍:
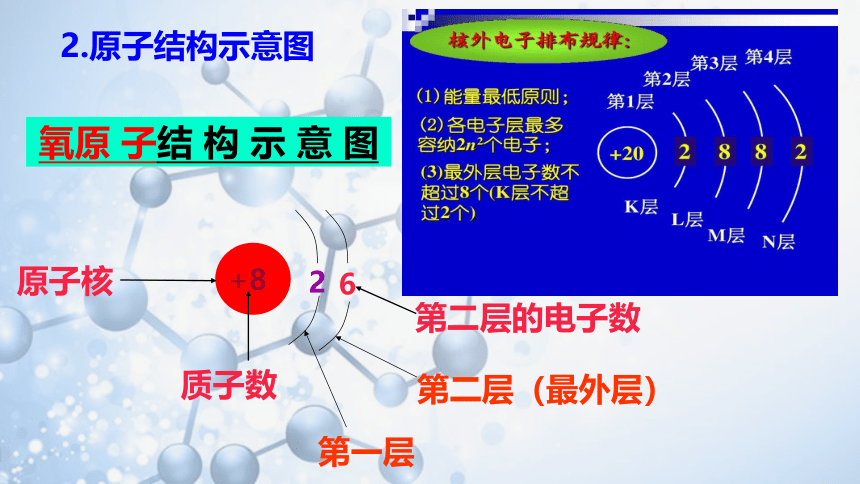
2
+8
6
原子核
质子数
第二层的电子数
2.原子结构示意图
氧原 子结 构 示 意 图
第一层
第二层(最外层)
3.电子与原子性质的关系
电子不仅决定原子的体积,也决定原子在化学
反应中的表现。
原 子 最外 层 电 子 数 原子 结 构 变 化 趋 势 化学
性 质
稀 有 气 体
金 属
非 金属
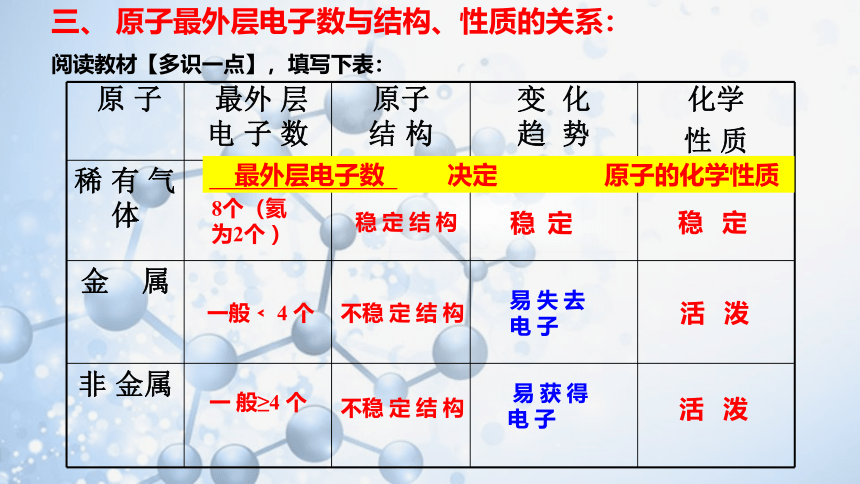
8个(氦 为2个 )
稳 定
稳 定
一般﹤ 4 个
不稳 定 结 构
易 失 去 电 子
活 泼
一 般≥4 个
易 获 得 电 子
活 泼
三、 原子最外层电子数与结构、性质的关系:
阅读教材【多识一点】,填写下表:
最外层电子数 决定 原子的化学性质
不稳 定 结 构
稳 定 结 构
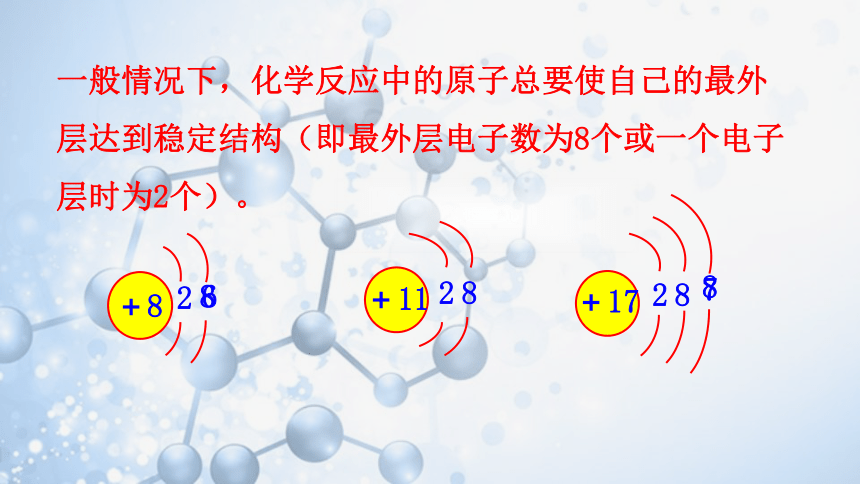
一般情况下,化学反应中的原子总要使自己的最外层达到稳定结构(即最外层电子数为8个或一个电子层时为2个)。
+11
2
8
+17
2
8
+8
2
8
8
6
7
4.离子
(1)离子的形成
原子失去电子后变成带正电
荷的阳离子,原子得到电子
后变成带负电荷的阴离子。
在化学反应中,原子核是不变的,发生改变的只是核外电子。
因得失电子而带电荷的原子(或原子团)叫离子。
氯化钠的形成过程
e-
Na
Cl
阳离子(带正电荷)如:Na+ 钠离子
阴离子(带负电荷)如:Cl- 氯离子
(2)离子的分类
(3)离子符号的表示
Mg2+
Cl
Na+
O2-
镁离子
氯离子
钠离子
氧离子
离子符号右上角的数字表示离子所带的电荷数,正负号表示离子所带电荷的电性。
-
Mg2+
每个镁离子带2个单位的正电荷
表示2个镁离子(镁离子的个数)
(4)离子符号的意义
2
构成物质的基本粒子——分子、原子、离子有何异同?它们之间有什么关系
【交流共享】
1.674×10-27
1.993×10-26
2.657×10-26
9.288×10-26
氢
碳
氧
铁
1个原子的质量/kg
原子种类
几种原子的质量
二、 原子质量的计量
问题:原子的质量如此小,无论书写、记忆还是使用都极不方便。原子的质量又该怎样衡量呢?
以一个碳12原子的实际质量(约1.993×10-26 kg)的1/12作为标准, 其他原子的质量跟它的比值, 就是这种原子的相对原子质量。
2.计算公式
1.相对原子质量
注意:相对原子质量是一个比值,不是原子的实际质量,单位一般不写。
氧原子的相对原子质量
碳12原子的质量×1/12
氧原子的质量
2.657×10﹣26kg
1.993×10﹣26kg×1/12
=
≈ 16
=
已知:氧原子的质量= 2.657×10﹣26kg
碳12原子的质量=1.993×10﹣26kg
计算氧的相对原子质量:
3.相对原子质量与原子的质量区别
(1)原子的质量是原子的实际存在的物质的多少,是实际质量或称为真实质量。
(2)相对原子质量是以C原子质量的1/12为标准来表示物质质量多少的相对质量。原子质量的单位是kg,相对原子质量的单位是1.原子的质量主要集中在原子核上。
(3)构成原子的三种粒子中,1个质子和1个中子的质量跟相对原子质量的标准(即一个碳12原子质量的1/12)相比,均约等于1,电子的质量很小,可以忽略不计,故原子的质量主要集中在质子和中子(即原子核)上。
相对原子质量≈质子数+中子数。
典型例题
知识点一:离子
【典例】(2022贵港)下列结构示意图所表示的微粒中,在化学反应中容易得到电子的是( )
A B C D
B
知识点二:相对原子质量
【典例2】已知某氧原子的相对原子质量为16,某硫原子的相对原子质量为32。如果该氧原子的质量为m,则该硫原子的质量为 ( )
A.32m B.2m
C.m D.不能确定
B
课堂达标
1. (2022济南)下图所示为某粒子的结构示意图。下列相关说法中,不合理的是( )
该粒子原子核内有11个质子
该粒子在化学反应中易失去电子
C. 该粒子呈电中性
D. 该粒子属于非金属元素
D
2. (2022湘西)硒是人体所需的微量元素,湘西地区土壤中硒的含量较高。据图回答:
(1)硒元素的相对原子质量是 ;
(2)图D表示的微粒在化学反应中容易 (填“得到”或“失去”)电子;
(3)A、B、C、D中表示金属元素的是 (填序号)。
78.96
得到
B
3. (2022锦州)根据以下几种粒子的结构示意图,回答下列问题:
(1)具有相对稳定结构的粒子是_________(填字母序号,下同)。
(2)具有相似化学性质的原子是___________。
(3)D粒子在化学反应中容易___________(填“失去”或“得到”)电子。
AB
CE
失去
课堂小结
1.原子在化学反应中的表现主要是由原子的最外层电子数决定的。
2.原子得到或失去电子后转变为离子。离子也是构成物质的一种微粒。
一、原子中的电子
二、相对原子质量
相对原子质量 =
某种原子的质量
碳12原子质量×1/12
2.相对原子质量 (近似值)≈ 质子数 + 中子数
1.概念:以碳12原子质量的1/12为标准,其他原子的质量跟它相比较所得到的比,作为这种原子的相对原子质量。
第三节 原子的结构
(第二课时)
第二单元 探秘水世界
PART
01
PART
02
知道什么是相对原子质量,能说出相对原子质量和实际质量的关系,能根据相对原子质量的概念进行简单计算。
知道原子和离子之间可以相互转化,初步认识核外电子在化学反应中的作用。
学习目标
PART
03
认识到用一种新的标准——碳12原子质量的1/12来衡量原子质量的大小,会使得衡量结果更接近常规的数据范围,这是一种重要的科学方法。
从微观角度来看,化学反应的实质是分子破裂为原子,原子重新组成新的分子。化学变化前后分子的种类一定改变,而原子的种类、数目不变。
原子是化学变化中的最小粒子
原子能不能再分呢?原子是由什么构成的呢?
如何把核外电子层排布形象地表示出来?
1.核外电子的分层排布
电子层数:1、2、3、4、5、6、7
电子能量:
离核远近:
能量越低,离核越近;能量越高,离核越远。
一、原子中的电子
低 高
近 远
一个氧原子的原子核内有8个质子和8个中子。核外有8个电子,其中有2个电子能量相近都较低,另外6个电子能量相近且能量稍高。这些电子都同时绕原子核高速运动。
根据刚才的理解,请你把氧原子的结构以最简洁的方式画出来。
资料介绍:
2
+8
6
原子核
质子数
第二层的电子数
2.原子结构示意图
氧原 子结 构 示 意 图
第一层
第二层(最外层)
3.电子与原子性质的关系
电子不仅决定原子的体积,也决定原子在化学
反应中的表现。
原 子 最外 层 电 子 数 原子 结 构 变 化 趋 势 化学
性 质
稀 有 气 体
金 属
非 金属
8个(氦 为2个 )
稳 定
稳 定
一般﹤ 4 个
不稳 定 结 构
易 失 去 电 子
活 泼
一 般≥4 个
易 获 得 电 子
活 泼
三、 原子最外层电子数与结构、性质的关系:
阅读教材【多识一点】,填写下表:
最外层电子数 决定 原子的化学性质
不稳 定 结 构
稳 定 结 构
一般情况下,化学反应中的原子总要使自己的最外层达到稳定结构(即最外层电子数为8个或一个电子层时为2个)。
+11
2
8
+17
2
8
+8
2
8
8
6
7
4.离子
(1)离子的形成
原子失去电子后变成带正电
荷的阳离子,原子得到电子
后变成带负电荷的阴离子。
在化学反应中,原子核是不变的,发生改变的只是核外电子。
因得失电子而带电荷的原子(或原子团)叫离子。
氯化钠的形成过程
e-
Na
Cl
阳离子(带正电荷)如:Na+ 钠离子
阴离子(带负电荷)如:Cl- 氯离子
(2)离子的分类
(3)离子符号的表示
Mg2+
Cl
Na+
O2-
镁离子
氯离子
钠离子
氧离子
离子符号右上角的数字表示离子所带的电荷数,正负号表示离子所带电荷的电性。
-
Mg2+
每个镁离子带2个单位的正电荷
表示2个镁离子(镁离子的个数)
(4)离子符号的意义
2
构成物质的基本粒子——分子、原子、离子有何异同?它们之间有什么关系
【交流共享】
1.674×10-27
1.993×10-26
2.657×10-26
9.288×10-26
氢
碳
氧
铁
1个原子的质量/kg
原子种类
几种原子的质量
二、 原子质量的计量
问题:原子的质量如此小,无论书写、记忆还是使用都极不方便。原子的质量又该怎样衡量呢?
以一个碳12原子的实际质量(约1.993×10-26 kg)的1/12作为标准, 其他原子的质量跟它的比值, 就是这种原子的相对原子质量。
2.计算公式
1.相对原子质量
注意:相对原子质量是一个比值,不是原子的实际质量,单位一般不写。
氧原子的相对原子质量
碳12原子的质量×1/12
氧原子的质量
2.657×10﹣26kg
1.993×10﹣26kg×1/12
=
≈ 16
=
已知:氧原子的质量= 2.657×10﹣26kg
碳12原子的质量=1.993×10﹣26kg
计算氧的相对原子质量:
3.相对原子质量与原子的质量区别
(1)原子的质量是原子的实际存在的物质的多少,是实际质量或称为真实质量。
(2)相对原子质量是以C原子质量的1/12为标准来表示物质质量多少的相对质量。原子质量的单位是kg,相对原子质量的单位是1.原子的质量主要集中在原子核上。
(3)构成原子的三种粒子中,1个质子和1个中子的质量跟相对原子质量的标准(即一个碳12原子质量的1/12)相比,均约等于1,电子的质量很小,可以忽略不计,故原子的质量主要集中在质子和中子(即原子核)上。
相对原子质量≈质子数+中子数。
典型例题
知识点一:离子
【典例】(2022贵港)下列结构示意图所表示的微粒中,在化学反应中容易得到电子的是( )
A B C D
B
知识点二:相对原子质量
【典例2】已知某氧原子的相对原子质量为16,某硫原子的相对原子质量为32。如果该氧原子的质量为m,则该硫原子的质量为 ( )
A.32m B.2m
C.m D.不能确定
B
课堂达标
1. (2022济南)下图所示为某粒子的结构示意图。下列相关说法中,不合理的是( )
该粒子原子核内有11个质子
该粒子在化学反应中易失去电子
C. 该粒子呈电中性
D. 该粒子属于非金属元素
D
2. (2022湘西)硒是人体所需的微量元素,湘西地区土壤中硒的含量较高。据图回答:
(1)硒元素的相对原子质量是 ;
(2)图D表示的微粒在化学反应中容易 (填“得到”或“失去”)电子;
(3)A、B、C、D中表示金属元素的是 (填序号)。
78.96
得到
B
3. (2022锦州)根据以下几种粒子的结构示意图,回答下列问题:
(1)具有相对稳定结构的粒子是_________(填字母序号,下同)。
(2)具有相似化学性质的原子是___________。
(3)D粒子在化学反应中容易___________(填“失去”或“得到”)电子。
AB
CE
失去
课堂小结
1.原子在化学反应中的表现主要是由原子的最外层电子数决定的。
2.原子得到或失去电子后转变为离子。离子也是构成物质的一种微粒。
一、原子中的电子
二、相对原子质量
相对原子质量 =
某种原子的质量
碳12原子质量×1/12
2.相对原子质量 (近似值)≈ 质子数 + 中子数
1.概念:以碳12原子质量的1/12为标准,其他原子的质量跟它相比较所得到的比,作为这种原子的相对原子质量。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
