10.2酸和碱的中和反应课件(共28张PPT)---2022-2023学年九年级化学人教版下册
文档属性
| 名称 | 10.2酸和碱的中和反应课件(共28张PPT)---2022-2023学年九年级化学人教版下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-17 00:00:00 | ||
图片预览





文档简介
(共28张PPT)
第十单元 酸和碱
酸和碱的中和反应
课堂导入
蜜蜂蛰伤
蚊子叮咬
蚊虫叮咬之时,在蚊子的口器中分泌出一种有机酸(蚁酸),在家庭中可使用浓肥皂水涂抹,可迅速止痒。
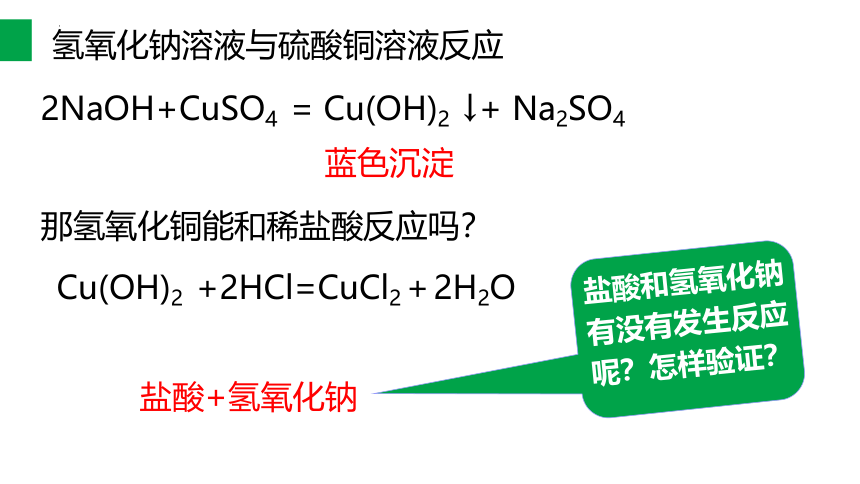
盐酸+氢氧化钠
盐酸和氢氧化钠有没有发生反应呢?怎样验证?
氢氧化钠溶液与硫酸铜溶液反应
蓝色沉淀
2NaOH+CuSO4 = Cu(OH)2 ↓+ Na2SO4
那氢氧化铜能和稀盐酸反应吗?
Cu(OH)2 +2HCl=CuCl2+2H2O
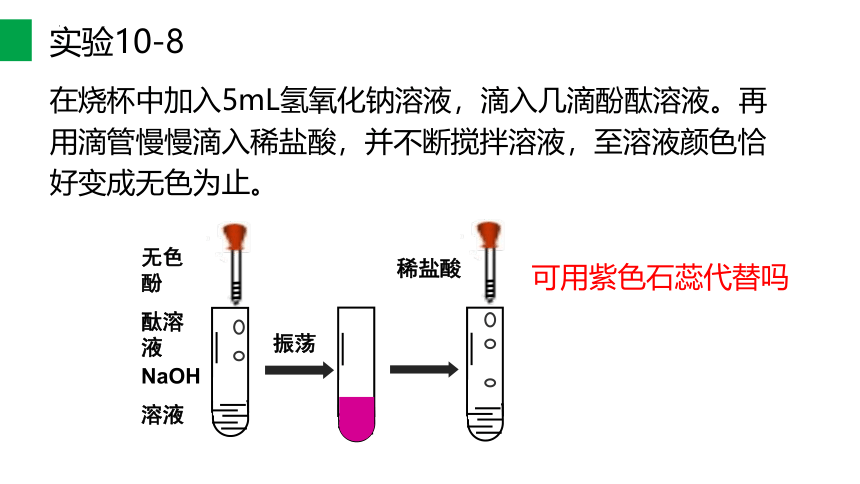
在烧杯中加入5mL氢氧化钠溶液,滴入几滴酚酞溶液。再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
NaOH
溶液
无色酚
酞溶液
稀盐酸
振荡
实验10-8
可用紫色石蕊代替吗
1.酚酞的作用:
起指示作用,判断反应有无发生
2.什么时候酸和碱恰好完全反应?
NaOH溶液中滴加酚酞后溶液显红色,随着滴加HCl,颜色逐渐消失至无色。
溶液刚好由红色变为无色
现象:
注意:
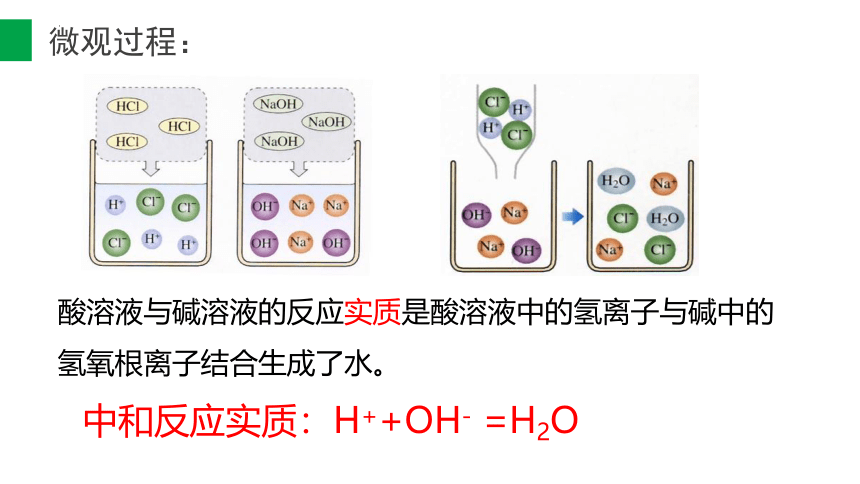
微观过程:
酸溶液与碱溶液的反应实质是酸溶液中的氢离子与碱中的氢氧根离子结合生成了水。
中和反应实质:H++OH- =H2O
①H2SO4 (硫酸)和NaOH(氢氧化钠)反应
②盐酸和熟石灰反应的化学方程式吗?
H2SO4 + 2NaOH == Na2SO4 + 2H2O
2HCl + Ca(OH)2 == CaCl2 +2 H2O
结合刚才所学到的知识,尝试写出以下方程式
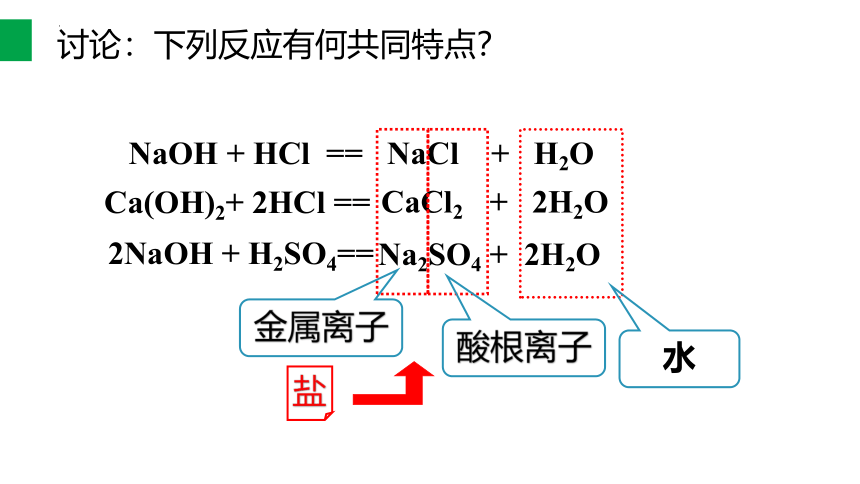
讨论:下列反应有何共同特点?
NaOH + HCl == NaCl + H2O
Ca(OH)2+ 2HCl ==
CaCl2 + 2H2O
2NaOH + H2SO4==
Na2SO4 + 2H2O
酸根离子
盐
水
金属离子
一.中和反应
1.概念:酸跟碱作用生成盐和水的反应。
2.实质:
H+ + OH – = H2O
问:有盐和水生成的反应都是中和反应吗?
碱
酸
盐
水
+
+
酸中的H+和碱中的OH – 结合生成水。
注意:
①中和反应生成盐和水,但生成盐和水的反应不一定
是中和反应。
②中和反应都是放热反应。(活泼金属与酸反应也放热)
3.盐:由金属离子(或铵根离子)和酸根离子构成
的化合物
例如:NaCl、Na2CO3、CaCO3、KMnO4、CuSO4 、Fe(NO3)3 、NaHCO3、NH4NO3
常见酸根:
CO32-(碳酸根离子)、SO42-(硫酸根离子)、NO3- (硝酸根离子) Cl-(氯离子)、HCO3-(碳酸氢根离子)
二、中和反应的应用
1.农业上,用熟石灰改良酸性土壤;
2.工厂中,可用熟石灰中和酸性废水;
3.医疗上,可用碱性药物中和过多的胃酸;
4.生活中,蚊虫叮咬后可用碱性溶液来缓解痛痒。
橘子、柠檬哪个更酸呢?
如何表示物质酸性的强弱呢
思考:
浓度为1%的盐酸,和浓度为10%的盐酸哪个酸性更强?
你能用什么方法区分两种溶液呢?
紫色石蕊溶液可以吗?
三.溶液酸碱度的表示方法—pH
1.表示方法:常用pH表示, pH的范围通常在0~14
之间。
碱性增强
酸性增强
中性
2.PH与溶液酸碱性的关系:
⑴ pH 7,溶液显中性 。
⑶ pH 7,溶液显碱性,pH越大,碱性越强。
=
>
如NaCl、Na2SO4等溶液
如HCl、H2SO4等溶液
⑵ pH 7,溶液显酸性, pH越小,酸性越强。
如 Ca(OH)2 、NaOH
<
、Na2CO3、NaHCO3等溶液
注意:pH表示溶液酸碱性的强弱程度,但不能确定是酸的溶液或碱的溶液。 如Na2CO3、NaHCO3显碱性,但是属于盐。
3.pH的测定方法:
在白瓷板或玻璃片上放一小片pH 试纸,用干净的玻璃棒蘸取被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较,读出被测液的pH 。
①不能直接把pH试纸浸入待测溶液中,以免污染试剂。
②不能先用水将pH试纸润湿,再进行测试,因为用水润湿后
的pH试纸会将待测溶液稀释,从而导致误差;
注意:
③实验室使用的pH试纸是一般是广泛pH试纸,测出的pH值
是1~14的整数;
更精确的pH测试仪器——pH计
下图是几种生活中常见物质,试着说一说它们的酸碱性。
4.溶液的酸碱度有重要意义:
①化工生产中许多反应必须在一定pH溶液里才能进行;
②在农业生产中,农作物一般适宜在pH为7或接近7土壤中生长;
③测定雨水的pH,可以了解空气的污染情况
[注:正常雨水的pH约为5.6,酸雨的pH小于5.6]
④测定人体内或排出的液体的pH,可以了解人体的健康状况。
①加碱: pH增大至=或>7
若pH<7
②加水: pH增大至≈7
①加酸: pH减小到=或<7
②加水: pH减小至≈7
补充:调节溶液pH的方法
若pH>7
酸的稀释:
碱的稀释:
典型例题
C
1.在通常情况下,某实验小组借助pH传感器探究稀盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示pH曲线。下列有关该实验的说法中正确的是( )
A.该实验是将氢氧化钠溶液滴入稀盐酸中B.a点溶液能使紫色石蕊试液变红C.b点时表示稀盐酸和氢氧化钠恰好完全反应D.c点时,溶液中的溶质只有氯化钠
A.从a到b过程中,烧杯中溶液的pH逐渐减小
B.b点表示氢氧化钠和盐酸恰好完全反应
C.c点表示所得溶液中溶质只有NaCl
D.稀盐酸与氢氧化钠溶液发生的反应是放热反应
C
2·将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸质量增加而发生变化,如图所示.有关叙述中错误的是( )
感谢各位的聆听
第十单元 酸和碱
酸和碱的中和反应
课堂导入
蜜蜂蛰伤
蚊子叮咬
蚊虫叮咬之时,在蚊子的口器中分泌出一种有机酸(蚁酸),在家庭中可使用浓肥皂水涂抹,可迅速止痒。
盐酸+氢氧化钠
盐酸和氢氧化钠有没有发生反应呢?怎样验证?
氢氧化钠溶液与硫酸铜溶液反应
蓝色沉淀
2NaOH+CuSO4 = Cu(OH)2 ↓+ Na2SO4
那氢氧化铜能和稀盐酸反应吗?
Cu(OH)2 +2HCl=CuCl2+2H2O
在烧杯中加入5mL氢氧化钠溶液,滴入几滴酚酞溶液。再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
NaOH
溶液
无色酚
酞溶液
稀盐酸
振荡
实验10-8
可用紫色石蕊代替吗
1.酚酞的作用:
起指示作用,判断反应有无发生
2.什么时候酸和碱恰好完全反应?
NaOH溶液中滴加酚酞后溶液显红色,随着滴加HCl,颜色逐渐消失至无色。
溶液刚好由红色变为无色
现象:
注意:
微观过程:
酸溶液与碱溶液的反应实质是酸溶液中的氢离子与碱中的氢氧根离子结合生成了水。
中和反应实质:H++OH- =H2O
①H2SO4 (硫酸)和NaOH(氢氧化钠)反应
②盐酸和熟石灰反应的化学方程式吗?
H2SO4 + 2NaOH == Na2SO4 + 2H2O
2HCl + Ca(OH)2 == CaCl2 +2 H2O
结合刚才所学到的知识,尝试写出以下方程式
讨论:下列反应有何共同特点?
NaOH + HCl == NaCl + H2O
Ca(OH)2+ 2HCl ==
CaCl2 + 2H2O
2NaOH + H2SO4==
Na2SO4 + 2H2O
酸根离子
盐
水
金属离子
一.中和反应
1.概念:酸跟碱作用生成盐和水的反应。
2.实质:
H+ + OH – = H2O
问:有盐和水生成的反应都是中和反应吗?
碱
酸
盐
水
+
+
酸中的H+和碱中的OH – 结合生成水。
注意:
①中和反应生成盐和水,但生成盐和水的反应不一定
是中和反应。
②中和反应都是放热反应。(活泼金属与酸反应也放热)
3.盐:由金属离子(或铵根离子)和酸根离子构成
的化合物
例如:NaCl、Na2CO3、CaCO3、KMnO4、CuSO4 、Fe(NO3)3 、NaHCO3、NH4NO3
常见酸根:
CO32-(碳酸根离子)、SO42-(硫酸根离子)、NO3- (硝酸根离子) Cl-(氯离子)、HCO3-(碳酸氢根离子)
二、中和反应的应用
1.农业上,用熟石灰改良酸性土壤;
2.工厂中,可用熟石灰中和酸性废水;
3.医疗上,可用碱性药物中和过多的胃酸;
4.生活中,蚊虫叮咬后可用碱性溶液来缓解痛痒。
橘子、柠檬哪个更酸呢?
如何表示物质酸性的强弱呢
思考:
浓度为1%的盐酸,和浓度为10%的盐酸哪个酸性更强?
你能用什么方法区分两种溶液呢?
紫色石蕊溶液可以吗?
三.溶液酸碱度的表示方法—pH
1.表示方法:常用pH表示, pH的范围通常在0~14
之间。
碱性增强
酸性增强
中性
2.PH与溶液酸碱性的关系:
⑴ pH 7,溶液显中性 。
⑶ pH 7,溶液显碱性,pH越大,碱性越强。
=
>
如NaCl、Na2SO4等溶液
如HCl、H2SO4等溶液
⑵ pH 7,溶液显酸性, pH越小,酸性越强。
如 Ca(OH)2 、NaOH
<
、Na2CO3、NaHCO3等溶液
注意:pH表示溶液酸碱性的强弱程度,但不能确定是酸的溶液或碱的溶液。 如Na2CO3、NaHCO3显碱性,但是属于盐。
3.pH的测定方法:
在白瓷板或玻璃片上放一小片pH 试纸,用干净的玻璃棒蘸取被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较,读出被测液的pH 。
①不能直接把pH试纸浸入待测溶液中,以免污染试剂。
②不能先用水将pH试纸润湿,再进行测试,因为用水润湿后
的pH试纸会将待测溶液稀释,从而导致误差;
注意:
③实验室使用的pH试纸是一般是广泛pH试纸,测出的pH值
是1~14的整数;
更精确的pH测试仪器——pH计
下图是几种生活中常见物质,试着说一说它们的酸碱性。
4.溶液的酸碱度有重要意义:
①化工生产中许多反应必须在一定pH溶液里才能进行;
②在农业生产中,农作物一般适宜在pH为7或接近7土壤中生长;
③测定雨水的pH,可以了解空气的污染情况
[注:正常雨水的pH约为5.6,酸雨的pH小于5.6]
④测定人体内或排出的液体的pH,可以了解人体的健康状况。
①加碱: pH增大至=或>7
若pH<7
②加水: pH增大至≈7
①加酸: pH减小到=或<7
②加水: pH减小至≈7
补充:调节溶液pH的方法
若pH>7
酸的稀释:
碱的稀释:
典型例题
C
1.在通常情况下,某实验小组借助pH传感器探究稀盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示pH曲线。下列有关该实验的说法中正确的是( )
A.该实验是将氢氧化钠溶液滴入稀盐酸中B.a点溶液能使紫色石蕊试液变红C.b点时表示稀盐酸和氢氧化钠恰好完全反应D.c点时,溶液中的溶质只有氯化钠
A.从a到b过程中,烧杯中溶液的pH逐渐减小
B.b点表示氢氧化钠和盐酸恰好完全反应
C.c点表示所得溶液中溶质只有NaCl
D.稀盐酸与氢氧化钠溶液发生的反应是放热反应
C
2·将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸质量增加而发生变化,如图所示.有关叙述中错误的是( )
感谢各位的聆听
同课章节目录
