泸州太平中学中学2014届九年级化学下册 8.3 金属资源的利用和保护(第1课时)学案(无答案)新人教版
文档属性
| 名称 | 泸州太平中学中学2014届九年级化学下册 8.3 金属资源的利用和保护(第1课时)学案(无答案)新人教版 |
|
|
| 格式 | zip | ||
| 文件大小 | 46.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-03-24 00:00:00 | ||
图片预览

文档简介
8.3. 金属资源的利用和保护(第1课时)学案
学习目标
知识与技能: 1、 了解从矿石中将铁还原出来的方法。(重点)
2、会根据方程式对含有杂质的反应物或生成物进行有关的计算。
过程与方法:通过观察一氧化碳与氧化铁反应实验,提高学生分析问题的能力
情感态度与价值观:认识一些矿石,增加热爱自然的热情。
【当堂训练】
1、下列物质中不能由金属与盐酸直接反应制得的是( )A.氯化镁 B.氯化锌 C.氯化铁 D.氯化铝
2、炼铁选用的铁矿石不仅要求含铁量高,而且要“有害元素”少。今有铁矿石:黄铁矿(FeS2)、菱铁矿(FeCO3) 、赤铁矿(Fe2O3)、褐铁矿(2Fe2O3·3H2O)、磁铁矿(Fe3O4),你认为不适宜炼铁的矿石应是( )。
A.黄铁矿 B.菱铁矿 C.赤铁矿 D. 磁铁矿
3、“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅,铝制易拉罐、
铜导线,可归为同一类回收,它们属于 ( )
A.金属或合金 B.氧化物 C.矿石 D.有机物
4、铁是一种应用广泛的金属,下列关于铁的说法中,正确的是( )
A.铁丝在氧气中燃烧生成氧化铁 B.铁在干燥的空气中容易生锈
C.铁是地壳中含量最多的金属元素 D.用铁锅炒菜可使食物中增加微量铁元素
5、盐酸与生铁反应,当生铁反应完毕后,烧杯里留有少量黑色物质,其主要物质为( )
A.氧化铁 B.四氧化三铁 C.碳 D.铁粉6.下列关于生铁和钢的描述中,正确的是( )A.生铁和钢都是混合物,其主要成份都是碳
B.生铁硬而有韧性,既可以铸又可煅C.生铁与钢的性能由很大的差别,主要是由于生铁和钢中的含碳量不同D.钢是用铁矿石和焦炭作原料炼制而成的7、.如图所示为炼铁实验装置,按下列要求进行回答:
(1)写出有标号的仪器名称:
①______________②_____________
(2)A装置中观察到的现象是:_________________________________________
B装置中观察到的现象是:______________________
装置C处气体燃烧时产生______________色火焰。
(3)写出B、C两部分所发生反应的化学方程式:
B部分:__________________________________________
C部分:__________________________________________
8、安徽省铜陵市是中国著名的“铜都”,铜矿蕴藏丰富,炼铜历史悠久。
该地产的一种矿石叫辉铜矿,主要成分为硫化亚铜(Cu2S),其中铜的化合价是
铜元素与硫元素的质量比是 。
(2)当地还产一种矿石叫孔雀石,成分为Cu2(OH)2CO3,加热时生成三种氧化物。该反应的化学方程式为 ,反应类型是 。
(3)反应中生成的黑色氧化物在一定的条件下能被还原,生成红色固体,在该反应中可加入的还原剂有 、 等。
9、冶炼20.0 t含杂质的质量分数为3.00%的生铁,需要含氧化铁质量分数为75%的赤铁矿石的质量是多
金属资源的存在形式及常见的矿石
学以致用:黄金是一种贵重的金属。在人类漫长的历史中,素有“沙里淘金”、“真金不怕火炼”之说。下列关于黄金的说法中不正确的是( )
A.黄金在自然界中以单质的形式存在 B.黄金的化学性质非常稳定
C.黄金是贵重金属,是因为它非常稀少 D.黄金属于合金
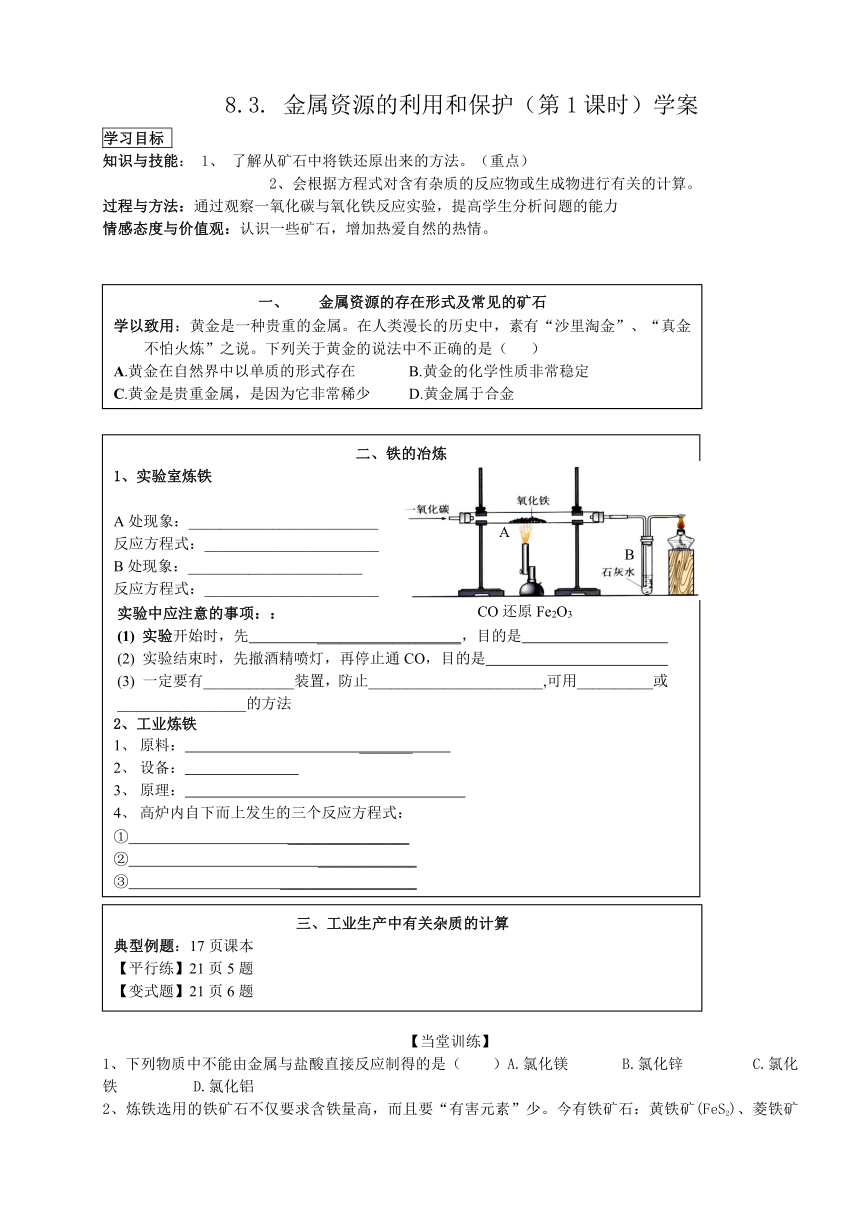
二、铁的冶炼
1、实验室炼铁
A处现象:_________________________
反应方程式:_______________________
B处现象:_______________________
反应方程式:_______________________
CO还原Fe2O3
2、工业炼铁
原料: _______
设备:
原理:
高炉内自下而上发生的三个反应方程式:
① ________________
② _____________
③ __________________
A
B
实验中应注意的事项::
(1) 实验开始时,先 ___________________,目的是
(2) 实验结束时,先撤酒精喷灯,再停止通CO,目的是
(3) 一定要有____________装置,防止_______________________,可用__________或_________________的方法
三、工业生产中有关杂质的计算
典型例题:17页课本
【平行练】21页5题
【变式题】21页6题
学习目标
知识与技能: 1、 了解从矿石中将铁还原出来的方法。(重点)
2、会根据方程式对含有杂质的反应物或生成物进行有关的计算。
过程与方法:通过观察一氧化碳与氧化铁反应实验,提高学生分析问题的能力
情感态度与价值观:认识一些矿石,增加热爱自然的热情。
【当堂训练】
1、下列物质中不能由金属与盐酸直接反应制得的是( )A.氯化镁 B.氯化锌 C.氯化铁 D.氯化铝
2、炼铁选用的铁矿石不仅要求含铁量高,而且要“有害元素”少。今有铁矿石:黄铁矿(FeS2)、菱铁矿(FeCO3) 、赤铁矿(Fe2O3)、褐铁矿(2Fe2O3·3H2O)、磁铁矿(Fe3O4),你认为不适宜炼铁的矿石应是( )。
A.黄铁矿 B.菱铁矿 C.赤铁矿 D. 磁铁矿
3、“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅,铝制易拉罐、
铜导线,可归为同一类回收,它们属于 ( )
A.金属或合金 B.氧化物 C.矿石 D.有机物
4、铁是一种应用广泛的金属,下列关于铁的说法中,正确的是( )
A.铁丝在氧气中燃烧生成氧化铁 B.铁在干燥的空气中容易生锈
C.铁是地壳中含量最多的金属元素 D.用铁锅炒菜可使食物中增加微量铁元素
5、盐酸与生铁反应,当生铁反应完毕后,烧杯里留有少量黑色物质,其主要物质为( )
A.氧化铁 B.四氧化三铁 C.碳 D.铁粉6.下列关于生铁和钢的描述中,正确的是( )A.生铁和钢都是混合物,其主要成份都是碳
B.生铁硬而有韧性,既可以铸又可煅C.生铁与钢的性能由很大的差别,主要是由于生铁和钢中的含碳量不同D.钢是用铁矿石和焦炭作原料炼制而成的7、.如图所示为炼铁实验装置,按下列要求进行回答:
(1)写出有标号的仪器名称:
①______________②_____________
(2)A装置中观察到的现象是:_________________________________________
B装置中观察到的现象是:______________________
装置C处气体燃烧时产生______________色火焰。
(3)写出B、C两部分所发生反应的化学方程式:
B部分:__________________________________________
C部分:__________________________________________
8、安徽省铜陵市是中国著名的“铜都”,铜矿蕴藏丰富,炼铜历史悠久。
该地产的一种矿石叫辉铜矿,主要成分为硫化亚铜(Cu2S),其中铜的化合价是
铜元素与硫元素的质量比是 。
(2)当地还产一种矿石叫孔雀石,成分为Cu2(OH)2CO3,加热时生成三种氧化物。该反应的化学方程式为 ,反应类型是 。
(3)反应中生成的黑色氧化物在一定的条件下能被还原,生成红色固体,在该反应中可加入的还原剂有 、 等。
9、冶炼20.0 t含杂质的质量分数为3.00%的生铁,需要含氧化铁质量分数为75%的赤铁矿石的质量是多
金属资源的存在形式及常见的矿石
学以致用:黄金是一种贵重的金属。在人类漫长的历史中,素有“沙里淘金”、“真金不怕火炼”之说。下列关于黄金的说法中不正确的是( )
A.黄金在自然界中以单质的形式存在 B.黄金的化学性质非常稳定
C.黄金是贵重金属,是因为它非常稀少 D.黄金属于合金
二、铁的冶炼
1、实验室炼铁
A处现象:_________________________
反应方程式:_______________________
B处现象:_______________________
反应方程式:_______________________
CO还原Fe2O3
2、工业炼铁
原料: _______
设备:
原理:
高炉内自下而上发生的三个反应方程式:
① ________________
② _____________
③ __________________
A
B
实验中应注意的事项::
(1) 实验开始时,先 ___________________,目的是
(2) 实验结束时,先撤酒精喷灯,再停止通CO,目的是
(3) 一定要有____________装置,防止_______________________,可用__________或_________________的方法
三、工业生产中有关杂质的计算
典型例题:17页课本
【平行练】21页5题
【变式题】21页6题
同课章节目录
