第一节 性质活泼的氧气-实验室制取氧气的装置和操作(18张ppt)
文档属性
| 名称 | 第一节 性质活泼的氧气-实验室制取氧气的装置和操作(18张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 604.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-03-25 00:00:00 | ||
图片预览





文档简介
课件18张PPT。第一节 性质活泼的氧气实验室制取氧气的装置和操作知识回顾1.工业上获得氧气是以 为原料,根据氧气和氮气的 的不同而分离出氧气的。从变化过程看,该变化是 (填物理变化或化学变化)。
2.物质由元素组成。用KMnO4、氯酸钾(KClO3 ) 、H2O2三种物质都可制得氧气,是因为这三种物质的组成中都含有液态空气沸点物理变化氧元素知识回顾原理一:用高锰酸钾作原料知识回顾
原理二:用双氧水和二氧化锰制取氧气催化剂:在化学反应中能增大其他物质的
反应速率,而本身的质量和化学
性质在反应前后都没有发生变化
的物质叫做催化剂
催化剂在化学反应中所起的作用叫催化作用实
验
装
置实
验
药
品实
验
步
骤实
验
原
理注
意
事
项实
验
目
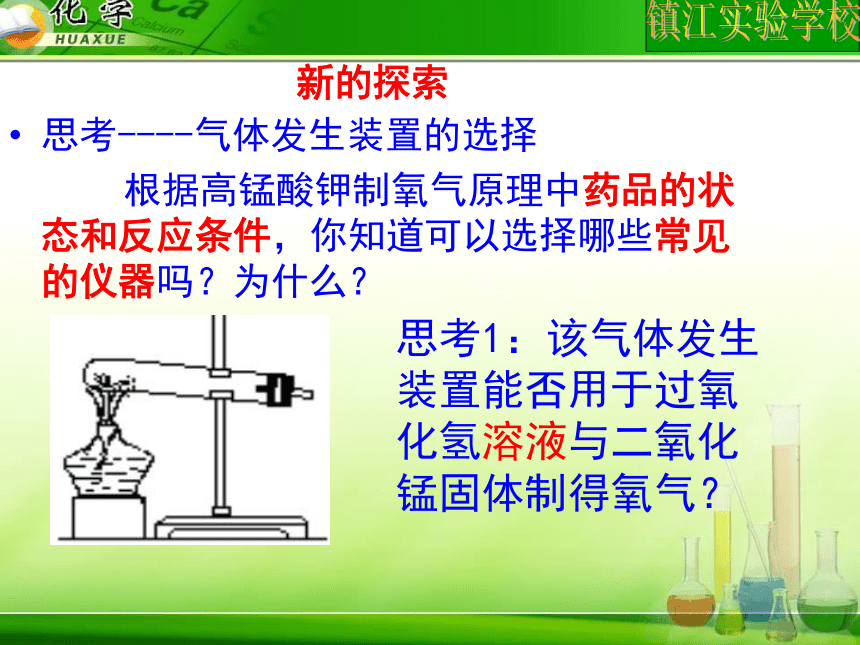
的实验室制取气体探究步骤新的探索思考----气体发生装置的选择
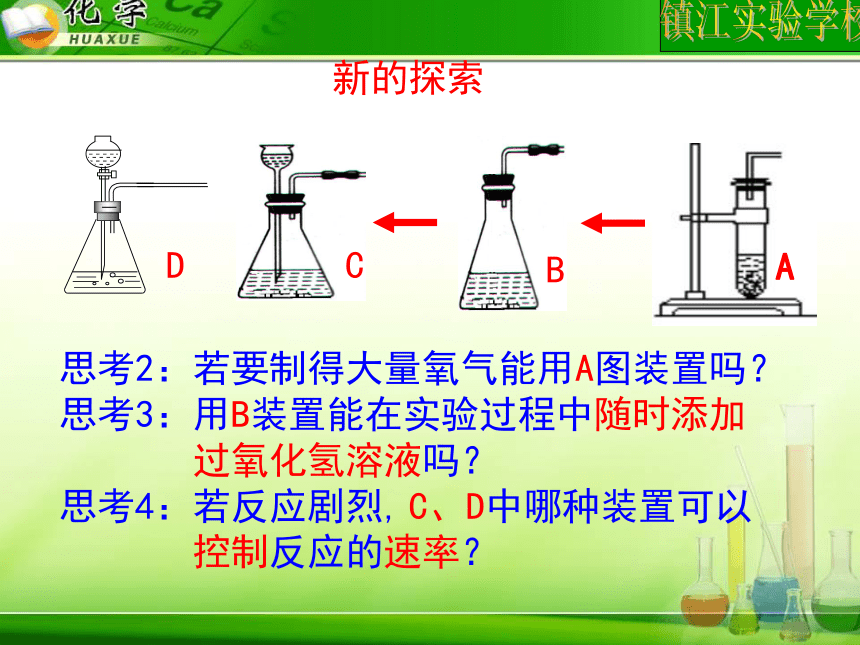
根据高锰酸钾制氧气原理中药品的状态和反应条件,你知道可以选择哪些常见的仪器吗?为什么?思考1:该气体发生装置能否用于过氧化氢溶液与二氧化锰固体制得氧气?新的探索思考2:若要制得大量氧气能用A图装置吗?
思考3:用B装置能在实验过程中随时添加
过氧化氢溶液吗?
思考4:若反应剧烈, C、D中哪种装置可以
控制反应的速率?A实验室制取气体的发生装置 1.常见类型:
2.选择:
依据反应物的状态、反应发生的条件
实验室制取气体的收集装置密度比空气大,不与空气中成份反应。气体性质密度比空气小,不与空气中成份反应。不易或难溶解于水,不与水
反应。实验室制取氧气装置图加热高锰酸钾制取氧气实验室制取氧气装置图双氧水与二氧化锰制氧气建议操作步骤(用排水法收集)1 、查(连接装置,检查装置气密性)
2 、装(装药品在试管中,管口放一团棉花,塞紧单孔塞)
3 、定(固定试管在铁架台上)(同时准备好收 集氧气的集气瓶等)
4 、点(点燃酒精灯加热药品,注意先均匀加热)
5 、收(收集气体)
6 、离(导管撤离出水槽)
7 、熄(灭酒精灯)
建议操作步骤(用排水法收集)1.组装仪器;
2.检查装置气密性;
3.加药品(先向锥形瓶中加二氧化锰粉末,再向分液漏斗中加过氧化氢溶液);
4.打开分液漏斗活塞,待气泡连续冒出时开始收集;
5.当瓶口有气泡冒出时,说明收集满了。水下盖好玻璃片,取出正放。动手试试吧比一比:看谁最先集满一瓶氧气
氧气的检验:用带火星的木条伸入瓶中,
观察是否复燃。
氧气的验满:用带火星的木条放在瓶口,
观察是否复燃。
想一想:你在实验中有什么疑问吗?
高锰酸钾制取氧气的注意事项:1、为什么试管口要放一团棉花?
2、为什么试管口要向下略微倾斜?
3、为什么要先将导管移出水面后再停
止加热?
…讨论:氧气收集法的比较不易或难溶于水,
不与水反应。密度比空气大,不
与空气成份反应较难判断气体是否已经集满
收集到较纯的氧
气,易判断集满不如排空
气法方便操作较为简单,
得到氧气干燥。讨论:两种制法的比较高锰
酸钾双氧
水和
二氧
化锰反应物
状态反应
条件两种方法的优劣点 固体固体 +
液体加热无需加
热,接
触即迅
速反应耗能,不易控制反应的速率,不够安全简单。操作简单、安全,产物水无污染,二氧化锰可以重复利用,可控制反应的速率。
通过本节课的学习我明白了。。。
2.物质由元素组成。用KMnO4、氯酸钾(KClO3 ) 、H2O2三种物质都可制得氧气,是因为这三种物质的组成中都含有液态空气沸点物理变化氧元素知识回顾原理一:用高锰酸钾作原料知识回顾
原理二:用双氧水和二氧化锰制取氧气催化剂:在化学反应中能增大其他物质的
反应速率,而本身的质量和化学
性质在反应前后都没有发生变化
的物质叫做催化剂
催化剂在化学反应中所起的作用叫催化作用实
验
装
置实
验
药
品实
验
步
骤实
验
原
理注
意
事
项实
验
目
的实验室制取气体探究步骤新的探索思考----气体发生装置的选择
根据高锰酸钾制氧气原理中药品的状态和反应条件,你知道可以选择哪些常见的仪器吗?为什么?思考1:该气体发生装置能否用于过氧化氢溶液与二氧化锰固体制得氧气?新的探索思考2:若要制得大量氧气能用A图装置吗?
思考3:用B装置能在实验过程中随时添加
过氧化氢溶液吗?
思考4:若反应剧烈, C、D中哪种装置可以
控制反应的速率?A实验室制取气体的发生装置 1.常见类型:
2.选择:
依据反应物的状态、反应发生的条件
实验室制取气体的收集装置密度比空气大,不与空气中成份反应。气体性质密度比空气小,不与空气中成份反应。不易或难溶解于水,不与水
反应。实验室制取氧气装置图加热高锰酸钾制取氧气实验室制取氧气装置图双氧水与二氧化锰制氧气建议操作步骤(用排水法收集)1 、查(连接装置,检查装置气密性)
2 、装(装药品在试管中,管口放一团棉花,塞紧单孔塞)
3 、定(固定试管在铁架台上)(同时准备好收 集氧气的集气瓶等)
4 、点(点燃酒精灯加热药品,注意先均匀加热)
5 、收(收集气体)
6 、离(导管撤离出水槽)
7 、熄(灭酒精灯)
建议操作步骤(用排水法收集)1.组装仪器;
2.检查装置气密性;
3.加药品(先向锥形瓶中加二氧化锰粉末,再向分液漏斗中加过氧化氢溶液);
4.打开分液漏斗活塞,待气泡连续冒出时开始收集;
5.当瓶口有气泡冒出时,说明收集满了。水下盖好玻璃片,取出正放。动手试试吧比一比:看谁最先集满一瓶氧气
氧气的检验:用带火星的木条伸入瓶中,
观察是否复燃。
氧气的验满:用带火星的木条放在瓶口,
观察是否复燃。
想一想:你在实验中有什么疑问吗?
高锰酸钾制取氧气的注意事项:1、为什么试管口要放一团棉花?
2、为什么试管口要向下略微倾斜?
3、为什么要先将导管移出水面后再停
止加热?
…讨论:氧气收集法的比较不易或难溶于水,
不与水反应。密度比空气大,不
与空气成份反应较难判断气体是否已经集满
收集到较纯的氧
气,易判断集满不如排空
气法方便操作较为简单,
得到氧气干燥。讨论:两种制法的比较高锰
酸钾双氧
水和
二氧
化锰反应物
状态反应
条件两种方法的优劣点 固体固体 +
液体加热无需加
热,接
触即迅
速反应耗能,不易控制反应的速率,不够安全简单。操作简单、安全,产物水无污染,二氧化锰可以重复利用,可控制反应的速率。
通过本节课的学习我明白了。。。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
