10.1常见的酸和碱(第1课时常见的酸)课件(31页)
文档属性
| 名称 | 10.1常见的酸和碱(第1课时常见的酸)课件(31页) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-19 00:00:00 | ||
图片预览










文档简介
(共31张PPT)
课题1 常见的酸和碱
常见的酸(1)
资料卡片:“酸”“碱”的由来
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等。
“酸”一词从有酸味的酒而来。最早,在制酒的时候,
有时把比较珍贵的酒放在窖中保存,在微生物的作用下,产生了酸。
P50
你知道在生活中还哪些物质含有酸?
HCl、H2SO4、HNO3、H2CO3等。
实验室中的酸
你知道在生活中还哪些物质含有碱?
实验室中的碱
Ca(OH)2、Cu(OH)2 、 NaOH等
NaOH溶液
Cu(OH)2沉淀
Ca(OH)2溶液
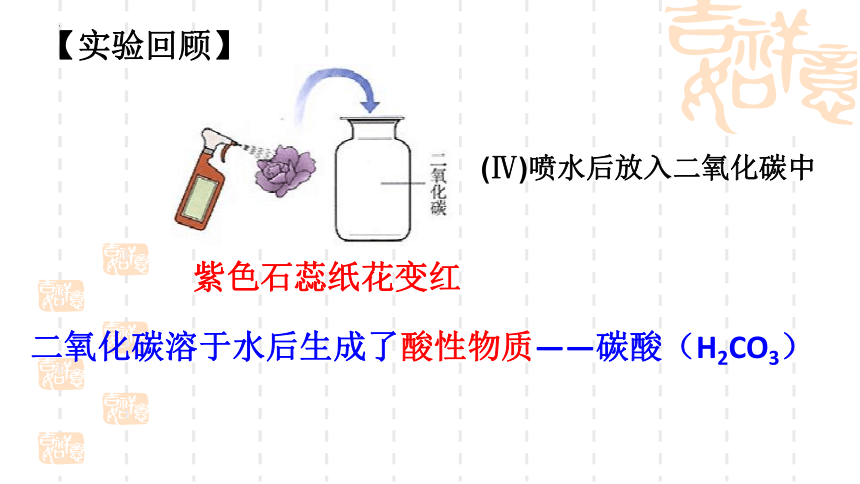
(Ⅳ)喷水后放入二氧化碳中
【实验回顾】
紫色石蕊纸花变红
二氧化碳溶于水后生成了酸性物质——碳酸(H2CO3)
一、酸、碱与指示剂作用
1、酸碱指示剂(指示剂)
(2)最常用的指示剂:
紫色石蕊溶液
无色酚酞溶液
(1)定义:遇到酸和碱时能发生特定的颜色变化的物质。
P50
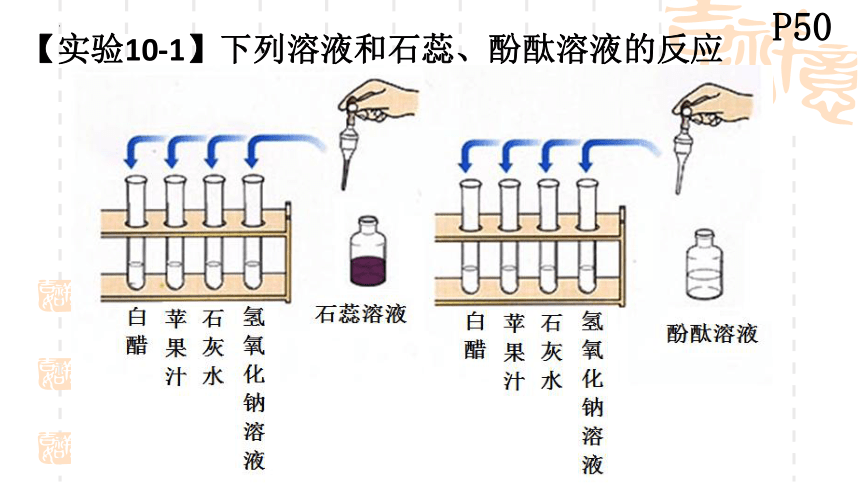
【实验10-1】下列溶液和石蕊、酚酞溶液的反应
P50
变红色
变蓝色
变红色
变蓝色
不变色
变红色
不变色
变红色
加入紫色石蕊溶液后的颜色变化 加入无色酚酞溶液后的颜色变化 溶液分类
(酸或碱)
蒸馏水
食醋
盐酸
石灰水
氢氧化钠溶液
酸
碱
酸
碱
实验10-1
紫色
不变色
中性物质
P51
1.紫色石蕊溶液遇酸变 ,遇碱变 。
2.无色酚酞溶液遇酸变 ,遇碱变 。
红
蓝
不变色
【结论】
红
检验酸碱溶液的操作步骤:
① 取样
② 滴加指示剂
③ 观察现象
④ 得出结论
例:如何鉴别两瓶无色液体:
稀盐酸和氢氧化钠溶液。
变红
变蓝
变红
紫色石蕊溶液
遇酸溶液
遇碱溶液
遇酸溶液
遇碱溶液
无色酚酞溶液
不变色
A
B
随堂练习
紫罗兰
罗伯特·波义耳Robert Boyle
沾上浓盐酸的紫罗兰
浓盐酸
酸碱指示剂
启发
制备
酸碱指示剂的来历
P51
2、自制酸碱指示剂
P51
使色素更好地溶解
探究:
紫色
紫色
红色
红色
红色
红色
红色
红色
红色
绿色
草绿色
草绿色
蓝色
蓝色
黄色
能
作对照
随堂练习
浓硫酸和浓盐酸的物理性质
(1)观察浓硫酸和浓盐酸的状态、颜色
注意:闻气体的方法
实验10-2
(2)打开瓶塞,观察发生的现象;并闻气味。
P52
--扇闻法
探究一:浓盐酸和浓硫酸的物理性质
颜色、状态
打开瓶口的现象
气味
密度(与水比较)
其它
硫酸(H2SO4)
盐酸(HCl)
无色、液态
无色、油状、粘稠、液态
无剌激性气味
有剌激性气味
大
大
无现象
瓶口有白雾
有吸水性
有挥发性
P52
是由于挥发出来的氯化氢气体与空气中的水蒸气结合,又形成盐酸小液滴。
拓展:
雾的产生原理:
液态小液滴悬浮于空气中形成的。
烟的产生原理:
固态小颗粒悬浮于空气中形成的。
P52
B
随堂练习
无色
讨论:
盐酸、硫酸有哪些主要用途?
P52
用途
盐酸 重要的化工产品。用于金属表面除锈、制造药物(如盐酸麻黄素、氯化锌)等;人体胃液中含有盐酸,可帮助消化。
用途
硫酸 重要的化工原料。用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等。
浓硫酸有吸水性,在实验室中常用它做干燥剂。
浓硫酸的特性
吸水性
(干燥剂:O2、H2、N2、HCl、CO2、CO)
( NH3不行)
用来干燥不能与其反应的酸性或中性气体
“长进短出”
讨论:
敞放久置于空气中的浓硫酸和浓盐酸,各成分怎样变化?
性质 溶质质量 溶剂质量 溶液质量 溶质质量分数
浓盐酸
浓硫酸
减少
不变
减少
减少
不变
增加
增加
减少
吸水性
挥发性
点拨:
变小
物理
密封
B
随堂练习
白雾
课堂小结
酸碱
指示剂
无色酚酞溶液
紫色石蕊溶液
酸溶液:变红
碱溶液:变蓝
酸溶液:不变色
碱溶液:变红
常见的酸
用途:除锈、制造药物
性质:刺激性气味,挥发性
盐酸
硫酸
用途:化工原料、干燥剂
性质:吸水性
C
B
A
紫
不断运动的
bde
课题1 常见的酸和碱
常见的酸(1)
资料卡片:“酸”“碱”的由来
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等。
“酸”一词从有酸味的酒而来。最早,在制酒的时候,
有时把比较珍贵的酒放在窖中保存,在微生物的作用下,产生了酸。
P50
你知道在生活中还哪些物质含有酸?
HCl、H2SO4、HNO3、H2CO3等。
实验室中的酸
你知道在生活中还哪些物质含有碱?
实验室中的碱
Ca(OH)2、Cu(OH)2 、 NaOH等
NaOH溶液
Cu(OH)2沉淀
Ca(OH)2溶液
(Ⅳ)喷水后放入二氧化碳中
【实验回顾】
紫色石蕊纸花变红
二氧化碳溶于水后生成了酸性物质——碳酸(H2CO3)
一、酸、碱与指示剂作用
1、酸碱指示剂(指示剂)
(2)最常用的指示剂:
紫色石蕊溶液
无色酚酞溶液
(1)定义:遇到酸和碱时能发生特定的颜色变化的物质。
P50
【实验10-1】下列溶液和石蕊、酚酞溶液的反应
P50
变红色
变蓝色
变红色
变蓝色
不变色
变红色
不变色
变红色
加入紫色石蕊溶液后的颜色变化 加入无色酚酞溶液后的颜色变化 溶液分类
(酸或碱)
蒸馏水
食醋
盐酸
石灰水
氢氧化钠溶液
酸
碱
酸
碱
实验10-1
紫色
不变色
中性物质
P51
1.紫色石蕊溶液遇酸变 ,遇碱变 。
2.无色酚酞溶液遇酸变 ,遇碱变 。
红
蓝
不变色
【结论】
红
检验酸碱溶液的操作步骤:
① 取样
② 滴加指示剂
③ 观察现象
④ 得出结论
例:如何鉴别两瓶无色液体:
稀盐酸和氢氧化钠溶液。
变红
变蓝
变红
紫色石蕊溶液
遇酸溶液
遇碱溶液
遇酸溶液
遇碱溶液
无色酚酞溶液
不变色
A
B
随堂练习
紫罗兰
罗伯特·波义耳Robert Boyle
沾上浓盐酸的紫罗兰
浓盐酸
酸碱指示剂
启发
制备
酸碱指示剂的来历
P51
2、自制酸碱指示剂
P51
使色素更好地溶解
探究:
紫色
紫色
红色
红色
红色
红色
红色
红色
红色
绿色
草绿色
草绿色
蓝色
蓝色
黄色
能
作对照
随堂练习
浓硫酸和浓盐酸的物理性质
(1)观察浓硫酸和浓盐酸的状态、颜色
注意:闻气体的方法
实验10-2
(2)打开瓶塞,观察发生的现象;并闻气味。
P52
--扇闻法
探究一:浓盐酸和浓硫酸的物理性质
颜色、状态
打开瓶口的现象
气味
密度(与水比较)
其它
硫酸(H2SO4)
盐酸(HCl)
无色、液态
无色、油状、粘稠、液态
无剌激性气味
有剌激性气味
大
大
无现象
瓶口有白雾
有吸水性
有挥发性
P52
是由于挥发出来的氯化氢气体与空气中的水蒸气结合,又形成盐酸小液滴。
拓展:
雾的产生原理:
液态小液滴悬浮于空气中形成的。
烟的产生原理:
固态小颗粒悬浮于空气中形成的。
P52
B
随堂练习
无色
讨论:
盐酸、硫酸有哪些主要用途?
P52
用途
盐酸 重要的化工产品。用于金属表面除锈、制造药物(如盐酸麻黄素、氯化锌)等;人体胃液中含有盐酸,可帮助消化。
用途
硫酸 重要的化工原料。用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等。
浓硫酸有吸水性,在实验室中常用它做干燥剂。
浓硫酸的特性
吸水性
(干燥剂:O2、H2、N2、HCl、CO2、CO)
( NH3不行)
用来干燥不能与其反应的酸性或中性气体
“长进短出”
讨论:
敞放久置于空气中的浓硫酸和浓盐酸,各成分怎样变化?
性质 溶质质量 溶剂质量 溶液质量 溶质质量分数
浓盐酸
浓硫酸
减少
不变
减少
减少
不变
增加
增加
减少
吸水性
挥发性
点拨:
变小
物理
密封
B
随堂练习
白雾
课堂小结
酸碱
指示剂
无色酚酞溶液
紫色石蕊溶液
酸溶液:变红
碱溶液:变蓝
酸溶液:不变色
碱溶液:变红
常见的酸
用途:除锈、制造药物
性质:刺激性气味,挥发性
盐酸
硫酸
用途:化工原料、干燥剂
性质:吸水性
C
B
A
紫
不断运动的
bde
同课章节目录
