10.2酸和碱的中和反应课件(37页)
图片预览








文档简介
(共37张PPT)
第十单元 酸和碱
课题2 酸和碱的中和反应
认知与了解
1.根据实验能判断酸和碱发生的化学反应。
2.能正确写出中和反应的化学方程式。
3.能举例说出中和反应在实际中的应用。
学习目标
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
走进生活
如果碱液沾到皮肤上 ,应用大量的水进行冲洗,然后涂上硼酸,为什么
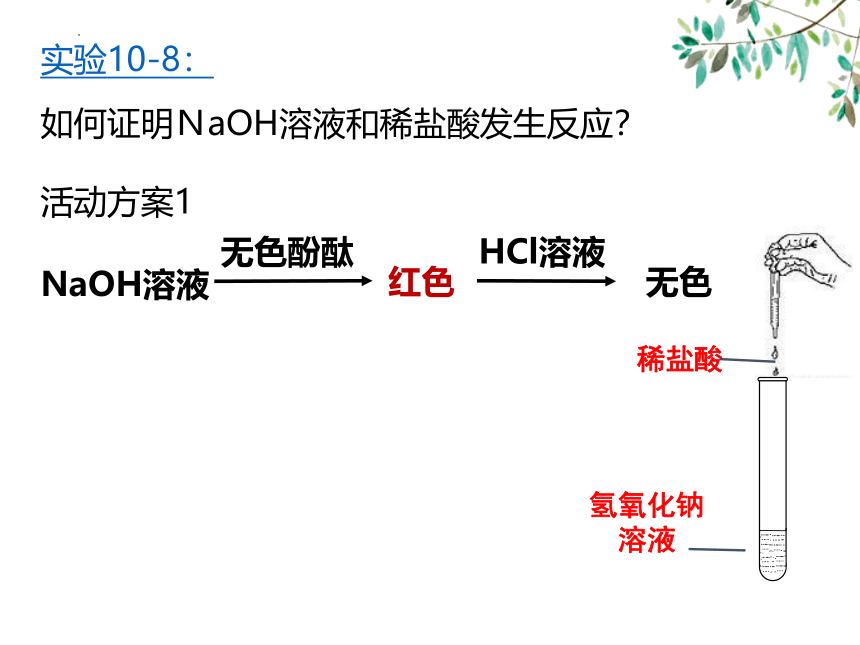
实验10-8:
如何证明NaOH溶液和稀盐酸发生反应?
稀盐酸
氢氧化钠溶液
NaOH溶液
无色酚酞
无色
HCl溶液
红色
活动方案1
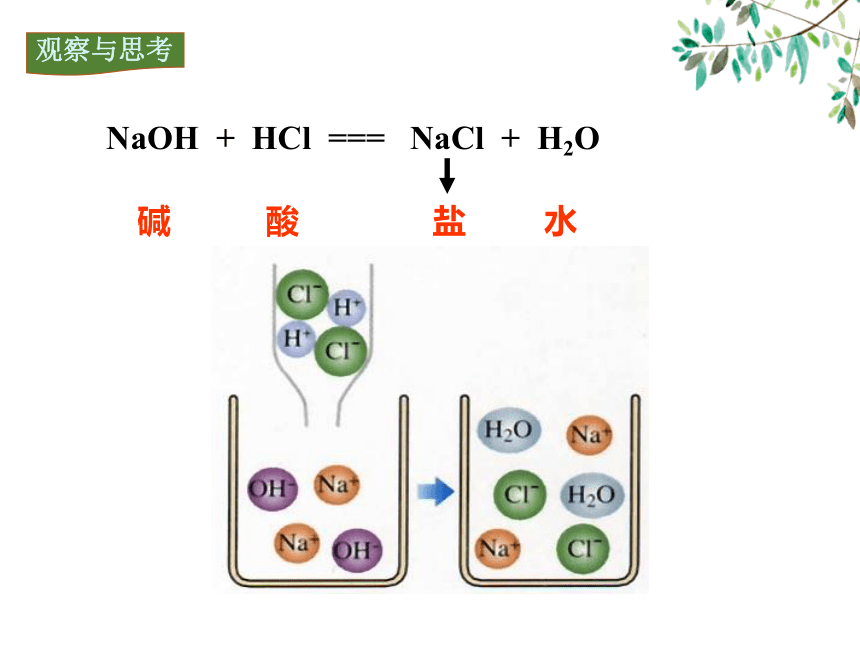
观察与思考
NaOH + HCl === NaCl + H2O
碱
酸
水
盐
CaCl2 + 2 H2O
NaOH+ H2SO4===
Ca(OH)2+ HCl ===
2
2
Na2SO4 + 2H2O
中和反应:酸和碱作用生成盐和水的反应
碱 + 酸 → 盐 + 水
由金属离子和酸根离子构成的化合物。
盐:
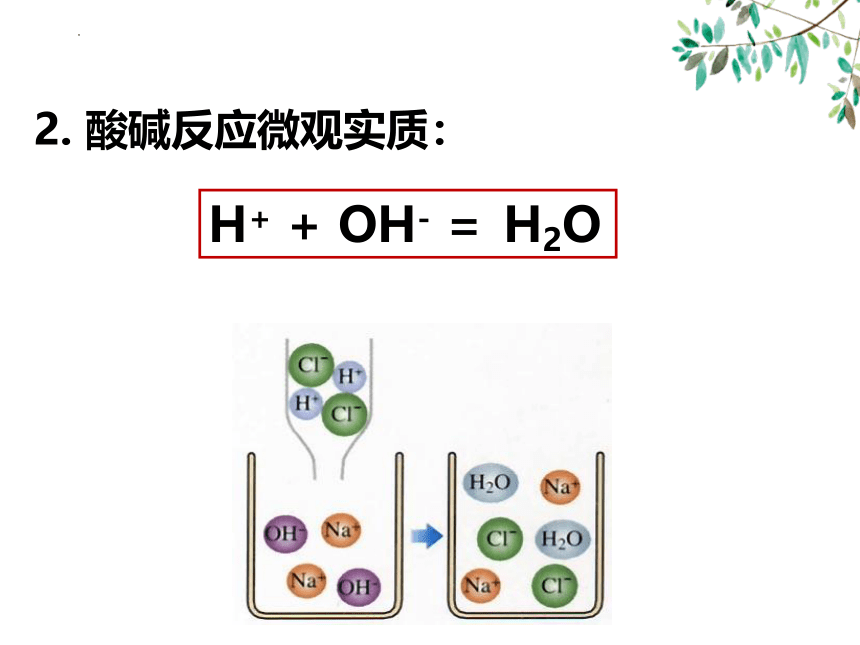
2. 酸碱反应微观实质:
H+ + OH- = H2O
巩固与练习
写出下列中和反应的化学方程式
Ca(OH)2 + H2SO4===
KOH + H2SO4 ===
Al(OH)3 + HCl ===
课堂与应用
1.下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2↑
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D CO2 + 2NaOH == Na2CO3 + H2O
C
中和反应在实际中的应用
二
1.改变土壤的酸碱性
熟石灰
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
改良时能否用NaOH?
碱性太强,价格太贵
思考与练习
2.处理工厂的废水
用熟石灰处理
方法1:可用熟石灰进行中和处理。
方法2:在废硫酸中加入废铁(硫酸亚铁可用来做动物的食品添加剂。)
2.处理工厂的废水
思考与练习
3.用于医药
Al(OH)3 + 3HCl === AlCl3 + 3H2O
你能写出中和胃酸的化学方程式吗?
一、酸碱指示剂
黄蜂蛰伤
蚊
虫叮咬
被蚊虫叮咬后,叮咬处很快会肿成大包,这是因为蚊虫能在人的皮肤内分泌出蚁酸,从而使皮肤肿痛。怎么办
思考与练习
被蚊虫叮咬可涂一些碱性物质如肥皂水、牙膏减轻痛痒
被黄蜂蜇到,毒液呈碱性,可涂食醋
思考讨论
探究—洗发剂和护发剂的酸碱性
健康的头发
受损伤的头发
工业废水的处理
酸和碱的中和反应
应用
改良酸性或碱性土壤
医药应用
中和反应:酸+碱 盐+水
学完本课你应该知道
练习与应用
1.下列应用与中和反应原理无关的是( )
A.服用含Al(OH)3的药物,治疗胃酸过多症
B.用稀硫酸除去铁钉表面的铁锈
C.用NaOH溶液洗涤石油产品中的残余硫酸
D.用熟石灰改良酸性土壤
B
课题2 第2课时
溶液酸碱度的表示方法——PH
知识技能
学习目标
1.能说出溶液酸碱性与pH的关系。
2.学会使用pH试纸测定溶液pH的方法。
3.能判断溶液pH图像的变化情况。
思考讨论
溶液的酸碱性:
表示溶液是酸性还是碱性的。(酸碱指示剂)
溶液的酸碱度:
表示溶液酸碱性的强弱程度。
思考讨论
pH试纸
1.测定pH最简便的方法:使用pH试纸
标准比色卡
pH的范围通常在0~14之间
思考讨论
溶液的酸碱度的表示方法
—pH
中性
酸性增强
碱性增强
PH < 7,溶液显酸性,pH越小酸性越强
PH = 7,溶液显中性
PH > 7,溶液显碱性,pH越大碱性越强
知识延伸
酸性溶液指酸溶液以及某些显酸性的盐溶液
如: 酸溶液:稀盐酸、稀硫酸
盐溶液:NH4Cl、CuSO4、NH4NO3 的溶液
碱性溶液指碱溶液以及某些显碱性的盐溶液
如: 碱溶液:NaOH、 Ca(OH)2
盐溶液:Na2CO3、NaHCO3、K2CO3的溶液
中性溶液主要指大部分的盐溶液
如: NaCl、 CaCl2、Na2SO4的溶液
酸溶液一定是酸性溶液,酸性溶液不一定是酸溶液;
碱溶液一定是碱性溶液,碱性溶液不一定是碱溶液。
思考讨论
指示剂 酸性溶液中的 颜色变化 中性溶液 中的颜色 碱性溶液中的
颜色变化
石蕊试液
酚酞试液
无 色
无 色
变红色
变蓝色
变红色
紫 色
酸溶液
酸性溶液
PH < 7
PH > 7
碱溶液
碱性溶液
思考讨论
实验10-9
2. 测定方法:
将pH试纸放在玻璃片上,用玻璃棒蘸取待测液,滴在pH试纸上,显色后与标准比色卡比较,读数。
注意:(1)pH值只能为整数,不能为小数。
(2)不能测浓硫酸、固体或气体的pH
(3)不能伸入到溶液中。(会污染原试剂)
(4)不能润湿pH试纸。(会改变酸碱度)
课堂练习
3.某同学用pH试纸测定溶液的酸碱度,下列操作或结论正确的是( )
A.用pH试纸直接蘸取待测溶液
B.先用水润湿pH试纸再测定溶液的酸碱度
C.用pH试纸测得石灰水的pH=5
D.用pH试纸测得盐酸的pH=1
D
思考讨论
日常生活中一些常见物质的PH
思考讨论
1.生活中一些常见物质的pH如图所示,下列四种物质中酸碱性与众不同的是( )
A.肥皂水 B.牙膏 C.西瓜汁 D.玉米粥
C
思考讨论
pH计
3. 测定pH的精确方法——
拓展延伸
人们通常把pH小于5.6的雨水称为酸雨。
大多数农作物适宜在接近中性的土壤中生长,酸性太强或碱性太强的土壤都不适宜农作物的生长。
思考分析
⑴酸性溶液的pH升高
7
酸中加水
酸中加碱
pH
思考讨论
⑵碱性溶液的pH降低
7
碱中加酸
碱中加水
pH
课堂练习
NaOH+HCl=NaCl+H2O
5.在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图13所示。
(1)该反应的化学方程式为:
。
(2)该实验操作是将
滴加到另一种溶液中。
(3)当加入溶液的质量为a g时,所得溶液中的溶
质为(写化学式) 。
(4)当加入溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈 色。
氢氧化钠溶液
HCl、NaCl
红
归纳总结
了解溶液的酸碱度有重要意义:
1. 化工生产中许多反应必须在一定PH溶液里才能进行;
2. 在农业生产中,农作物一般适宜在PH为7或接近7的土壤中生长;
3. 测定雨水的PH,可以了解空气的污染情况(正常雨水的PH约为 5.6,酸雨的PH小于5.6);
4. 测定人体内液体的PH,了解人体健康状况。
课堂练习
2. 以下物质遇到水形成的溶液中,pH值大于7的是( )
A.二氧化碳 B.氯化氢 C.氧化钙 D.氯化钠
C
D
1.某同学帮助校园绿化工人做花圃土壤分析,结果发现其pH小于7,为改良土壤应选择的物质是( )
A.氯化钾 B.烧碱
C.硝酸铵 D.熟石灰
课堂小结
pH与溶液酸碱性的关系
溶液酸碱度的表示法
|
pH
pH的测定——pH试纸的正确使用
pH应用
2.测定pH最简单的方法是使用_____________。测定时,用______________蘸取待测液,滴在_____________上,然后再与________________对照,得出该溶液的pH。
pH试纸
玻璃棒
pH试纸
标准比色卡
第十单元 酸和碱
课题2 酸和碱的中和反应
认知与了解
1.根据实验能判断酸和碱发生的化学反应。
2.能正确写出中和反应的化学方程式。
3.能举例说出中和反应在实际中的应用。
学习目标
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
走进生活
如果碱液沾到皮肤上 ,应用大量的水进行冲洗,然后涂上硼酸,为什么
实验10-8:
如何证明NaOH溶液和稀盐酸发生反应?
稀盐酸
氢氧化钠溶液
NaOH溶液
无色酚酞
无色
HCl溶液
红色
活动方案1
观察与思考
NaOH + HCl === NaCl + H2O
碱
酸
水
盐
CaCl2 + 2 H2O
NaOH+ H2SO4===
Ca(OH)2+ HCl ===
2
2
Na2SO4 + 2H2O
中和反应:酸和碱作用生成盐和水的反应
碱 + 酸 → 盐 + 水
由金属离子和酸根离子构成的化合物。
盐:
2. 酸碱反应微观实质:
H+ + OH- = H2O
巩固与练习
写出下列中和反应的化学方程式
Ca(OH)2 + H2SO4===
KOH + H2SO4 ===
Al(OH)3 + HCl ===
课堂与应用
1.下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2↑
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D CO2 + 2NaOH == Na2CO3 + H2O
C
中和反应在实际中的应用
二
1.改变土壤的酸碱性
熟石灰
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
改良时能否用NaOH?
碱性太强,价格太贵
思考与练习
2.处理工厂的废水
用熟石灰处理
方法1:可用熟石灰进行中和处理。
方法2:在废硫酸中加入废铁(硫酸亚铁可用来做动物的食品添加剂。)
2.处理工厂的废水
思考与练习
3.用于医药
Al(OH)3 + 3HCl === AlCl3 + 3H2O
你能写出中和胃酸的化学方程式吗?
一、酸碱指示剂
黄蜂蛰伤
蚊
虫叮咬
被蚊虫叮咬后,叮咬处很快会肿成大包,这是因为蚊虫能在人的皮肤内分泌出蚁酸,从而使皮肤肿痛。怎么办
思考与练习
被蚊虫叮咬可涂一些碱性物质如肥皂水、牙膏减轻痛痒
被黄蜂蜇到,毒液呈碱性,可涂食醋
思考讨论
探究—洗发剂和护发剂的酸碱性
健康的头发
受损伤的头发
工业废水的处理
酸和碱的中和反应
应用
改良酸性或碱性土壤
医药应用
中和反应:酸+碱 盐+水
学完本课你应该知道
练习与应用
1.下列应用与中和反应原理无关的是( )
A.服用含Al(OH)3的药物,治疗胃酸过多症
B.用稀硫酸除去铁钉表面的铁锈
C.用NaOH溶液洗涤石油产品中的残余硫酸
D.用熟石灰改良酸性土壤
B
课题2 第2课时
溶液酸碱度的表示方法——PH
知识技能
学习目标
1.能说出溶液酸碱性与pH的关系。
2.学会使用pH试纸测定溶液pH的方法。
3.能判断溶液pH图像的变化情况。
思考讨论
溶液的酸碱性:
表示溶液是酸性还是碱性的。(酸碱指示剂)
溶液的酸碱度:
表示溶液酸碱性的强弱程度。
思考讨论
pH试纸
1.测定pH最简便的方法:使用pH试纸
标准比色卡
pH的范围通常在0~14之间
思考讨论
溶液的酸碱度的表示方法
—pH
中性
酸性增强
碱性增强
PH < 7,溶液显酸性,pH越小酸性越强
PH = 7,溶液显中性
PH > 7,溶液显碱性,pH越大碱性越强
知识延伸
酸性溶液指酸溶液以及某些显酸性的盐溶液
如: 酸溶液:稀盐酸、稀硫酸
盐溶液:NH4Cl、CuSO4、NH4NO3 的溶液
碱性溶液指碱溶液以及某些显碱性的盐溶液
如: 碱溶液:NaOH、 Ca(OH)2
盐溶液:Na2CO3、NaHCO3、K2CO3的溶液
中性溶液主要指大部分的盐溶液
如: NaCl、 CaCl2、Na2SO4的溶液
酸溶液一定是酸性溶液,酸性溶液不一定是酸溶液;
碱溶液一定是碱性溶液,碱性溶液不一定是碱溶液。
思考讨论
指示剂 酸性溶液中的 颜色变化 中性溶液 中的颜色 碱性溶液中的
颜色变化
石蕊试液
酚酞试液
无 色
无 色
变红色
变蓝色
变红色
紫 色
酸溶液
酸性溶液
PH < 7
PH > 7
碱溶液
碱性溶液
思考讨论
实验10-9
2. 测定方法:
将pH试纸放在玻璃片上,用玻璃棒蘸取待测液,滴在pH试纸上,显色后与标准比色卡比较,读数。
注意:(1)pH值只能为整数,不能为小数。
(2)不能测浓硫酸、固体或气体的pH
(3)不能伸入到溶液中。(会污染原试剂)
(4)不能润湿pH试纸。(会改变酸碱度)
课堂练习
3.某同学用pH试纸测定溶液的酸碱度,下列操作或结论正确的是( )
A.用pH试纸直接蘸取待测溶液
B.先用水润湿pH试纸再测定溶液的酸碱度
C.用pH试纸测得石灰水的pH=5
D.用pH试纸测得盐酸的pH=1
D
思考讨论
日常生活中一些常见物质的PH
思考讨论
1.生活中一些常见物质的pH如图所示,下列四种物质中酸碱性与众不同的是( )
A.肥皂水 B.牙膏 C.西瓜汁 D.玉米粥
C
思考讨论
pH计
3. 测定pH的精确方法——
拓展延伸
人们通常把pH小于5.6的雨水称为酸雨。
大多数农作物适宜在接近中性的土壤中生长,酸性太强或碱性太强的土壤都不适宜农作物的生长。
思考分析
⑴酸性溶液的pH升高
7
酸中加水
酸中加碱
pH
思考讨论
⑵碱性溶液的pH降低
7
碱中加酸
碱中加水
pH
课堂练习
NaOH+HCl=NaCl+H2O
5.在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图13所示。
(1)该反应的化学方程式为:
。
(2)该实验操作是将
滴加到另一种溶液中。
(3)当加入溶液的质量为a g时,所得溶液中的溶
质为(写化学式) 。
(4)当加入溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈 色。
氢氧化钠溶液
HCl、NaCl
红
归纳总结
了解溶液的酸碱度有重要意义:
1. 化工生产中许多反应必须在一定PH溶液里才能进行;
2. 在农业生产中,农作物一般适宜在PH为7或接近7的土壤中生长;
3. 测定雨水的PH,可以了解空气的污染情况(正常雨水的PH约为 5.6,酸雨的PH小于5.6);
4. 测定人体内液体的PH,了解人体健康状况。
课堂练习
2. 以下物质遇到水形成的溶液中,pH值大于7的是( )
A.二氧化碳 B.氯化氢 C.氧化钙 D.氯化钠
C
D
1.某同学帮助校园绿化工人做花圃土壤分析,结果发现其pH小于7,为改良土壤应选择的物质是( )
A.氯化钾 B.烧碱
C.硝酸铵 D.熟石灰
课堂小结
pH与溶液酸碱性的关系
溶液酸碱度的表示法
|
pH
pH的测定——pH试纸的正确使用
pH应用
2.测定pH最简单的方法是使用_____________。测定时,用______________蘸取待测液,滴在_____________上,然后再与________________对照,得出该溶液的pH。
pH试纸
玻璃棒
pH试纸
标准比色卡
同课章节目录
