2022-2023学年九年级化学人教版下册8.2金属的化学性质培优卷(含解析)
文档属性
| 名称 | 2022-2023学年九年级化学人教版下册8.2金属的化学性质培优卷(含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 100.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-19 00:00:00 | ||
图片预览


文档简介
金属的化学性质培优卷
一、单选题
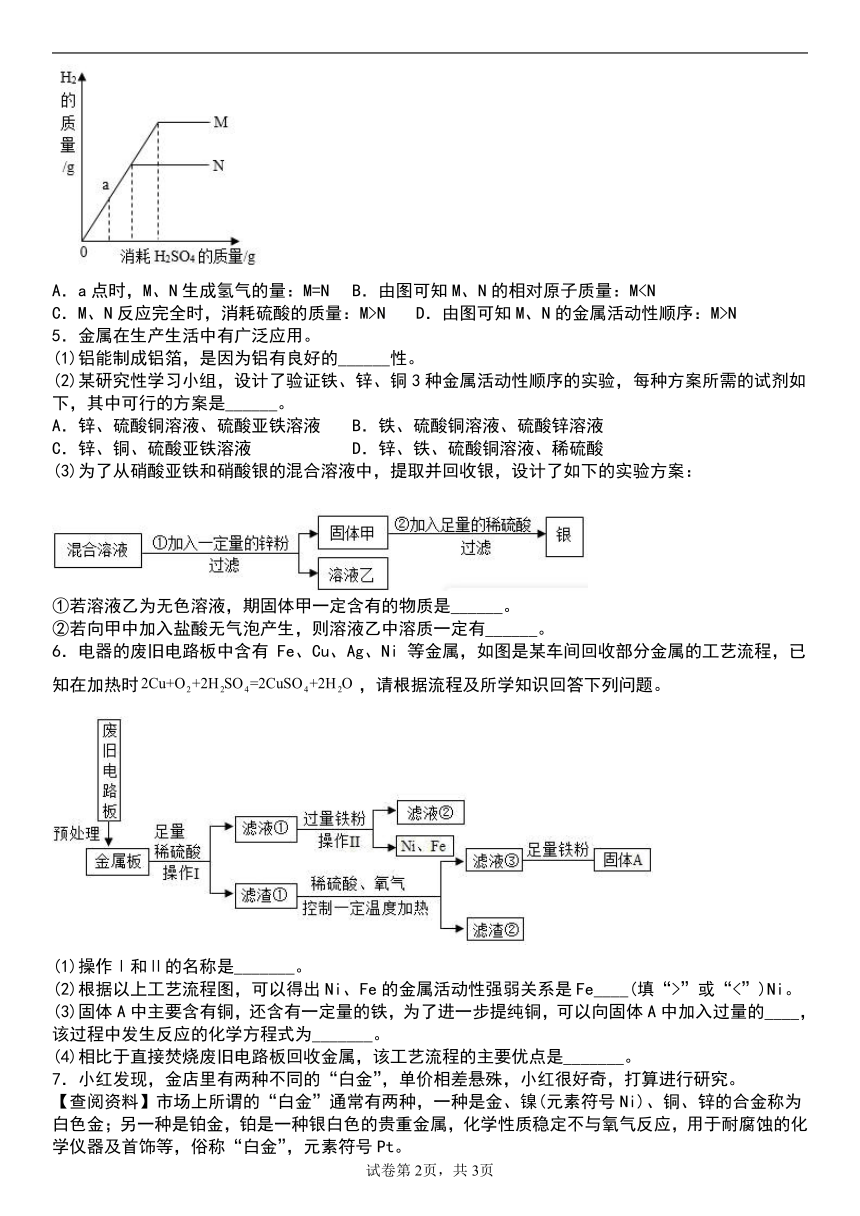
1.向等质量的镁粉和铁粉中分别逐滴加入同浓度的稀盐酸至过量,酸溶液的质量与生成盐的质量如下图所示,请根据题干和图像信息判断,下列说法正确的是( )
①镁粉消耗稀盐酸的质量多
②参加反应的稀盐酸的质量相等
③金属铁比金属镁相对原子质量大
④铁粉与稀盐酸反应比镁粉快
A.①③ B.①④ C.②③ D.③④
2.等质量、等浓度的稀硫酸分别与足量的镁、铁两种金属反应,下列图像能正确表示产生氢气质量与反应时间之间关系的是( )
A.B.C. D.
3.相同质量的镁、铁、锌三种金属,分别与足量的、相同质量分数的稀硫酸充分反应,生成氢气质量与反应时间关系见如图,分析图像判断,下面说法正确的是( )
A.金属锌反应速率最大
B.金属锌的活动性最强
C.金属镁生成氢气质量最多
D.金属铁消耗稀硫酸质量最多
4.向等质量的金属M、N中逐滴加入稀硫酸至过量(已知M、N在化合物中的化合价都是+2价),反应产生的氢气与消耗酸的关系如图。结合图像判断,下列说法错误的是( )
A.a点时,M、N生成氢气的量:M=N B.由图可知M、N的相对原子质量:MC.M、N反应完全时,消耗硫酸的质量:M>N D.由图可知M、N的金属活动性顺序:M>N
5.金属在生产生活中有广泛应用。
(1)铝能制成铝箔,是因为铝有良好的______性。
(2)某研究性学习小组,设计了验证铁、锌、铜3种金属活动性顺序的实验,每种方案所需的试剂如下,其中可行的方案是______。
A.锌、硫酸铜溶液、硫酸亚铁溶液 B.铁、硫酸铜溶液、硫酸锌溶液
C.锌、铜、硫酸亚铁溶液 D.锌、铁、硫酸铜溶液、稀硫酸
(3)为了从硝酸亚铁和硝酸银的混合溶液中,提取并回收银,设计了如下的实验方案:
①若溶液乙为无色溶液,期固体甲一定含有的物质是______。
②若向甲中加入盐酸无气泡产生,则溶液乙中溶质一定有______。
6.电器的废旧电路板中含有 Fe、Cu、Ag、Ni 等金属,如图是某车间回收部分金属的工艺流程,已知在加热时,请根据流程及所学知识回答下列问题。
(1)操作Ⅰ和Ⅱ的名称是_______。
(2)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱关系是Fe____(填“>”或“<”)Ni。
(3)固体A中主要含有铜,还含有一定量的铁,为了进一步提纯铜,可以向固体A中加入过量的____,该过程中发生反应的化学方程式为_______。
(4)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是_______。
7.小红发现,金店里有两种不同的“白金”,单价相差悬殊,小红很好奇,打算进行研究。
【查阅资料】市场上所谓的“白金”通常有两种,一种是金、镍(元素符号Ni)、铜、锌的合金称为白色金;另一种是铂金,铂是一种银白色的贵重金属,化学性质稳定不与氧气反应,用于耐腐蚀的化学仪器及首饰等,俗称“白金”,元素符号Pt。
【探究活动】小红结合化学课上学习的金属活动性顺序,和兴趣小组的同学一起展开探究活动。
任务一:鉴别两种白金
(1)小红设计实验一:将这种白金放在石棉网上用酒精灯加热,观察到金属表面___________。则这种白金为“白色金”。
(2)小红设计实验二:将这种白金放入__________________中,观察到金属表面冒气泡,则这种白金为“白色金”。
(3)小红设计实验三:将白色金属放入硝酸银溶液中,观察到金属表面有银白色物质附着,则这种白金为“白色金”,写出一个反应的化学方程式__________________。
任务二:探究Zn、Ni、Cu的金属活动性顺序。
【作出假设】假设①Zn>Ni>Cu; 假设②Zn>Cu>Ni; 假设③______。
(4)假设③是___________。
【查阅资料】镍能与稀盐酸或稀硫酸酸反应,NiCl2、NiSO4、Ni(NO3)2都可溶于水。
【设计实验】同温下,取大小、形状相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察记录现象。
金属 Ni Zn Cu
与盐酸反应的现象 气体产生缓慢 金属逐渐溶解 气体产生激烈 金属迅速溶解 无明显现象
【得出结论】
(5)原假设中正确的是__________________(填序号)。
【拓展应用】
(6)根据上述实验结论,选择下列药品的组合也能验证出Zn、Ni、Cu的金属活动性顺序的是_______(填字母)。A.Zn、Cu、Ni(NO3)2溶液 B.Ni、ZnSO4溶液、CuSO4溶液
C.Zn、Ni(NO3)2溶液、Cu(NO3)2溶液 D.Zn、Ni、Cu(NO3)2溶液
试卷第1页,共3页
参考答案:
1.A
【详解】①图像横坐标为消耗酸溶液的质量,由图可知,镁粉消耗稀盐酸的质量多,正确;
②由①分析可知,参加反应的稀盐酸的质量不相等,错误;
③铁、镁和稀盐酸反应都生成+2价盐,由图可知,镁粉消耗稀盐酸的质量多,生成氢气质量大;化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;故金属铁比金属镁相对原子质量大,正确;
④该图像没有时间轴,不能体现铁粉与稀盐酸反应比镁粉快,错误。
故选A。
2.B
【详解】在金属活动性顺序中,Mg>Fe,则镁的反应速率快,铁的反应速率较慢,即镁的斜线比铁的斜线陡;等质量、等浓度的稀硫酸分别与足量的镁、铁两种金属反应,说明酸全部参加反应,则生成氢气的质量最终是相同的,故选B。
3.C
【分析】三种金属的活动性由强到弱是镁>锌>铁,质量相同的三种金属与足量酸反应理论上产生氢气由多到少是镁>铁>锌。
【详解】A、图中可以看到,金属镁与酸反应产生氢气的质量上升是最快的,所以金属镁反应速率最大,A错误,不符合题意;
B、镁反应速率最大,金属活动性最强,B错误,不符合题意;
C、图中可知,金属镁产生氢气的质量最高,生成的氢气质量最多,C正确,符合题意;
D、产生的氢气中氢元素全部来自于稀硫酸,产生的氢气越多,消耗的稀硫酸质量越多,镁应该是消耗稀硫酸质量最多的金属,D错误,不符合题意。
故选:C。
【点睛】将常见几种金属的金属活动性和产生氢气的能力熟练掌握,有利于解决这类问题。
4.D
【详解】A、由图可知,a点时,M、N生成氢气的量:M=N,不符合题意;
B、生成氢气的质量=金属质量×化合价/相对原子质量,金属质量相同,化合价相同,生成氢气的质量:M>N,故M、N的相对原子质量:MC、由图可知,M、N反应完全时,生成氢气的质量为:M>N,生成氢气中的氢元素完全来自于硫酸,故消耗硫酸的质量:M>N,不符合题意;
D、该图无法比较两种金属与酸反应速率的快慢,无法得出两种金属的活动性顺序,符合题意。
故选D。
5.(1)延展
(2)BCD
(3) 银、铁 硝酸锌、硝酸亚铁
【详解】(1)铝能制成铝箔,是因为铝有良好的延展性。
(2)A、锌与硫酸亚铁反应可验证锌的活动性比铁强,锌跟硫酸铜反应可验证锌的活动性比铜强,无法比较铁和铜的活泼性,选项错误;
B、铁与硫酸铜反应,可验证铁的活动性比铜强;铁与硫酸锌不反应,可知铁的活动性比锌弱,选项正确;
C、锌与硫酸亚铁反应,可验证锌的活动性比铁强;铜与硫酸亚铁不反应,可知铜的活动性比铁弱,选项正确;
D、锌、铁与硫酸铜溶液反应,可知锌的活动性最强;锌、铁与稀硫酸溶液反应,锌的反应速率更快,可知锌比铁活泼,选项正确。
故选BCD。
(3)①在金属活动性顺序中,锌>铁>银,加入的锌粉能与硝酸银反应生成银,能与硝酸亚铁反应生成铁,生成的铁能与硝酸银反应生成银和硝酸亚铁,加入的锌粉首先与硝酸银反应,若溶液乙为无色溶液,说明硝酸亚铁已全部参加反应,故固体甲一定有银和铁,锌有可能剩余。
②若向甲中加入盐酸无气泡产生,说明固体甲不含锌、铁,锌粉能与硝酸银反应生成硝酸锌,溶液中一定含有硝酸锌、硝酸亚铁,可能含有未反应的硝酸银。
6.(1)过滤
(2)>
(3) 稀盐酸(合理即可)
(4)环保
【详解】(1)由流程图可知,操作Ⅰ和Ⅱ是将固体和液体分离,则操作Ⅰ和Ⅱ的名称是过滤。
(2)金属板中加入足量稀硫酸,过滤得到滤液①,向滤液①中加入过量铁粉,过滤得到镍和铁,说明滤液①中含有硫酸镍,铁和硫酸镍反应生成镍,则根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱关系是Fe>Ni。
(3)固体A中主要含有铜,还含有一定量的铁,为了进一步提纯铜,需要将铁反应,形成溶液,然后过滤得到铜,铁和稀盐酸反应生成氯化亚铁和铜,故可以向固体A中加入过量的稀盐酸(合理即可),该过程中发生反应的化学方程式为。
(4)由流程图可知,整个过程产生污染物较少,可以避免焚烧产生的污染性气体等,则相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是环保。
7.(1)变黑
(2)稀硫酸或稀盐酸
(3)或
(4)Ni>Zn>Cu
(5)①
(6)AB
【详解】(1)铜丝加热生成黑色的氧化铜,则可观察到金属表面变黑。
(2)锌能与硫酸反应生成硫酸锌和氢气,则可将这种白金放入硫酸中,若观察到金属表面冒气泡,则这种白金为“白色金”。
(3)锌能与硝酸银反应生成银和硝酸锌,反应的化学方程式为,铜能与硝酸银反应生成银和硝酸铜,反应的化学方程式为。
(4)已知锌的活动性比铜前,结合前面假设,可知假设③为Ni>Zn>Cu。
(5)Zn、Ni能与盐酸反应,且锌反应较快,Cu不能与盐酸反应,则说明金属活动性顺序:Zn>Ni>Cu,则假设①成立。
(6)A、锌能与Ni(NO3)2反应,铜不能反应,则说明金属活动性Zn>Ni>Cu,该选项符合题意;
B、Ni不能与ZnSO4反应,但能与CuSO4反应,则说明金属活动性Zn>Ni>Cu,该选项符合题意;
C、Zn与Ni(NO3)2、Cu(NO3)2均能反应,则说明Zn的金属活动性最强,但没有比较Ni和Cu的金属活动性顺序,该选项不符合题意;
D、Zn、Ni均能与Cu(NO3)2反应,则说明Cu的活动性最弱,但没有比较Zn和Ni的金属活动性顺序,该选项不符合题意。
故选AB。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.向等质量的镁粉和铁粉中分别逐滴加入同浓度的稀盐酸至过量,酸溶液的质量与生成盐的质量如下图所示,请根据题干和图像信息判断,下列说法正确的是( )
①镁粉消耗稀盐酸的质量多
②参加反应的稀盐酸的质量相等
③金属铁比金属镁相对原子质量大
④铁粉与稀盐酸反应比镁粉快
A.①③ B.①④ C.②③ D.③④
2.等质量、等浓度的稀硫酸分别与足量的镁、铁两种金属反应,下列图像能正确表示产生氢气质量与反应时间之间关系的是( )
A.B.C. D.
3.相同质量的镁、铁、锌三种金属,分别与足量的、相同质量分数的稀硫酸充分反应,生成氢气质量与反应时间关系见如图,分析图像判断,下面说法正确的是( )
A.金属锌反应速率最大
B.金属锌的活动性最强
C.金属镁生成氢气质量最多
D.金属铁消耗稀硫酸质量最多
4.向等质量的金属M、N中逐滴加入稀硫酸至过量(已知M、N在化合物中的化合价都是+2价),反应产生的氢气与消耗酸的关系如图。结合图像判断,下列说法错误的是( )
A.a点时,M、N生成氢气的量:M=N B.由图可知M、N的相对原子质量:M
5.金属在生产生活中有广泛应用。
(1)铝能制成铝箔,是因为铝有良好的______性。
(2)某研究性学习小组,设计了验证铁、锌、铜3种金属活动性顺序的实验,每种方案所需的试剂如下,其中可行的方案是______。
A.锌、硫酸铜溶液、硫酸亚铁溶液 B.铁、硫酸铜溶液、硫酸锌溶液
C.锌、铜、硫酸亚铁溶液 D.锌、铁、硫酸铜溶液、稀硫酸
(3)为了从硝酸亚铁和硝酸银的混合溶液中,提取并回收银,设计了如下的实验方案:
①若溶液乙为无色溶液,期固体甲一定含有的物质是______。
②若向甲中加入盐酸无气泡产生,则溶液乙中溶质一定有______。
6.电器的废旧电路板中含有 Fe、Cu、Ag、Ni 等金属,如图是某车间回收部分金属的工艺流程,已知在加热时,请根据流程及所学知识回答下列问题。
(1)操作Ⅰ和Ⅱ的名称是_______。
(2)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱关系是Fe____(填“>”或“<”)Ni。
(3)固体A中主要含有铜,还含有一定量的铁,为了进一步提纯铜,可以向固体A中加入过量的____,该过程中发生反应的化学方程式为_______。
(4)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是_______。
7.小红发现,金店里有两种不同的“白金”,单价相差悬殊,小红很好奇,打算进行研究。
【查阅资料】市场上所谓的“白金”通常有两种,一种是金、镍(元素符号Ni)、铜、锌的合金称为白色金;另一种是铂金,铂是一种银白色的贵重金属,化学性质稳定不与氧气反应,用于耐腐蚀的化学仪器及首饰等,俗称“白金”,元素符号Pt。
【探究活动】小红结合化学课上学习的金属活动性顺序,和兴趣小组的同学一起展开探究活动。
任务一:鉴别两种白金
(1)小红设计实验一:将这种白金放在石棉网上用酒精灯加热,观察到金属表面___________。则这种白金为“白色金”。
(2)小红设计实验二:将这种白金放入__________________中,观察到金属表面冒气泡,则这种白金为“白色金”。
(3)小红设计实验三:将白色金属放入硝酸银溶液中,观察到金属表面有银白色物质附着,则这种白金为“白色金”,写出一个反应的化学方程式__________________。
任务二:探究Zn、Ni、Cu的金属活动性顺序。
【作出假设】假设①Zn>Ni>Cu; 假设②Zn>Cu>Ni; 假设③______。
(4)假设③是___________。
【查阅资料】镍能与稀盐酸或稀硫酸酸反应,NiCl2、NiSO4、Ni(NO3)2都可溶于水。
【设计实验】同温下,取大小、形状相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察记录现象。
金属 Ni Zn Cu
与盐酸反应的现象 气体产生缓慢 金属逐渐溶解 气体产生激烈 金属迅速溶解 无明显现象
【得出结论】
(5)原假设中正确的是__________________(填序号)。
【拓展应用】
(6)根据上述实验结论,选择下列药品的组合也能验证出Zn、Ni、Cu的金属活动性顺序的是_______(填字母)。A.Zn、Cu、Ni(NO3)2溶液 B.Ni、ZnSO4溶液、CuSO4溶液
C.Zn、Ni(NO3)2溶液、Cu(NO3)2溶液 D.Zn、Ni、Cu(NO3)2溶液
试卷第1页,共3页
参考答案:
1.A
【详解】①图像横坐标为消耗酸溶液的质量,由图可知,镁粉消耗稀盐酸的质量多,正确;
②由①分析可知,参加反应的稀盐酸的质量不相等,错误;
③铁、镁和稀盐酸反应都生成+2价盐,由图可知,镁粉消耗稀盐酸的质量多,生成氢气质量大;化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;故金属铁比金属镁相对原子质量大,正确;
④该图像没有时间轴,不能体现铁粉与稀盐酸反应比镁粉快,错误。
故选A。
2.B
【详解】在金属活动性顺序中,Mg>Fe,则镁的反应速率快,铁的反应速率较慢,即镁的斜线比铁的斜线陡;等质量、等浓度的稀硫酸分别与足量的镁、铁两种金属反应,说明酸全部参加反应,则生成氢气的质量最终是相同的,故选B。
3.C
【分析】三种金属的活动性由强到弱是镁>锌>铁,质量相同的三种金属与足量酸反应理论上产生氢气由多到少是镁>铁>锌。
【详解】A、图中可以看到,金属镁与酸反应产生氢气的质量上升是最快的,所以金属镁反应速率最大,A错误,不符合题意;
B、镁反应速率最大,金属活动性最强,B错误,不符合题意;
C、图中可知,金属镁产生氢气的质量最高,生成的氢气质量最多,C正确,符合题意;
D、产生的氢气中氢元素全部来自于稀硫酸,产生的氢气越多,消耗的稀硫酸质量越多,镁应该是消耗稀硫酸质量最多的金属,D错误,不符合题意。
故选:C。
【点睛】将常见几种金属的金属活动性和产生氢气的能力熟练掌握,有利于解决这类问题。
4.D
【详解】A、由图可知,a点时,M、N生成氢气的量:M=N,不符合题意;
B、生成氢气的质量=金属质量×化合价/相对原子质量,金属质量相同,化合价相同,生成氢气的质量:M>N,故M、N的相对原子质量:M
D、该图无法比较两种金属与酸反应速率的快慢,无法得出两种金属的活动性顺序,符合题意。
故选D。
5.(1)延展
(2)BCD
(3) 银、铁 硝酸锌、硝酸亚铁
【详解】(1)铝能制成铝箔,是因为铝有良好的延展性。
(2)A、锌与硫酸亚铁反应可验证锌的活动性比铁强,锌跟硫酸铜反应可验证锌的活动性比铜强,无法比较铁和铜的活泼性,选项错误;
B、铁与硫酸铜反应,可验证铁的活动性比铜强;铁与硫酸锌不反应,可知铁的活动性比锌弱,选项正确;
C、锌与硫酸亚铁反应,可验证锌的活动性比铁强;铜与硫酸亚铁不反应,可知铜的活动性比铁弱,选项正确;
D、锌、铁与硫酸铜溶液反应,可知锌的活动性最强;锌、铁与稀硫酸溶液反应,锌的反应速率更快,可知锌比铁活泼,选项正确。
故选BCD。
(3)①在金属活动性顺序中,锌>铁>银,加入的锌粉能与硝酸银反应生成银,能与硝酸亚铁反应生成铁,生成的铁能与硝酸银反应生成银和硝酸亚铁,加入的锌粉首先与硝酸银反应,若溶液乙为无色溶液,说明硝酸亚铁已全部参加反应,故固体甲一定有银和铁,锌有可能剩余。
②若向甲中加入盐酸无气泡产生,说明固体甲不含锌、铁,锌粉能与硝酸银反应生成硝酸锌,溶液中一定含有硝酸锌、硝酸亚铁,可能含有未反应的硝酸银。
6.(1)过滤
(2)>
(3) 稀盐酸(合理即可)
(4)环保
【详解】(1)由流程图可知,操作Ⅰ和Ⅱ是将固体和液体分离,则操作Ⅰ和Ⅱ的名称是过滤。
(2)金属板中加入足量稀硫酸,过滤得到滤液①,向滤液①中加入过量铁粉,过滤得到镍和铁,说明滤液①中含有硫酸镍,铁和硫酸镍反应生成镍,则根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱关系是Fe>Ni。
(3)固体A中主要含有铜,还含有一定量的铁,为了进一步提纯铜,需要将铁反应,形成溶液,然后过滤得到铜,铁和稀盐酸反应生成氯化亚铁和铜,故可以向固体A中加入过量的稀盐酸(合理即可),该过程中发生反应的化学方程式为。
(4)由流程图可知,整个过程产生污染物较少,可以避免焚烧产生的污染性气体等,则相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是环保。
7.(1)变黑
(2)稀硫酸或稀盐酸
(3)或
(4)Ni>Zn>Cu
(5)①
(6)AB
【详解】(1)铜丝加热生成黑色的氧化铜,则可观察到金属表面变黑。
(2)锌能与硫酸反应生成硫酸锌和氢气,则可将这种白金放入硫酸中,若观察到金属表面冒气泡,则这种白金为“白色金”。
(3)锌能与硝酸银反应生成银和硝酸锌,反应的化学方程式为,铜能与硝酸银反应生成银和硝酸铜,反应的化学方程式为。
(4)已知锌的活动性比铜前,结合前面假设,可知假设③为Ni>Zn>Cu。
(5)Zn、Ni能与盐酸反应,且锌反应较快,Cu不能与盐酸反应,则说明金属活动性顺序:Zn>Ni>Cu,则假设①成立。
(6)A、锌能与Ni(NO3)2反应,铜不能反应,则说明金属活动性Zn>Ni>Cu,该选项符合题意;
B、Ni不能与ZnSO4反应,但能与CuSO4反应,则说明金属活动性Zn>Ni>Cu,该选项符合题意;
C、Zn与Ni(NO3)2、Cu(NO3)2均能反应,则说明Zn的金属活动性最强,但没有比较Ni和Cu的金属活动性顺序,该选项不符合题意;
D、Zn、Ni均能与Cu(NO3)2反应,则说明Cu的活动性最弱,但没有比较Zn和Ni的金属活动性顺序,该选项不符合题意。
故选AB。
答案第1页,共2页
答案第1页,共2页
同课章节目录
