人教版(2019)必修第二册 第五章 化工生产中的重要非金属元素 专题复习(共25张PPT)
文档属性
| 名称 | 人教版(2019)必修第二册 第五章 化工生产中的重要非金属元素 专题复习(共25张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 6.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-21 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
第五章 专题复习
高一年级 化学
第五章 化工生产中的重要非金属元素
整理与提升
从物质类别和元素价态的视角研究硫和氮等元素及其化合物的性质和用途,可以深化对物质间转化关系的认识。工业上利用这些转化关系,通过控制条件等方法,遵循生态文明思想,可以获得相应的化工产品,实现环境保护与资源利用的和谐统一。
知
识
体
系
构
建
知
识
体
系
构
建
天津市春季学期中小学精品课程资源
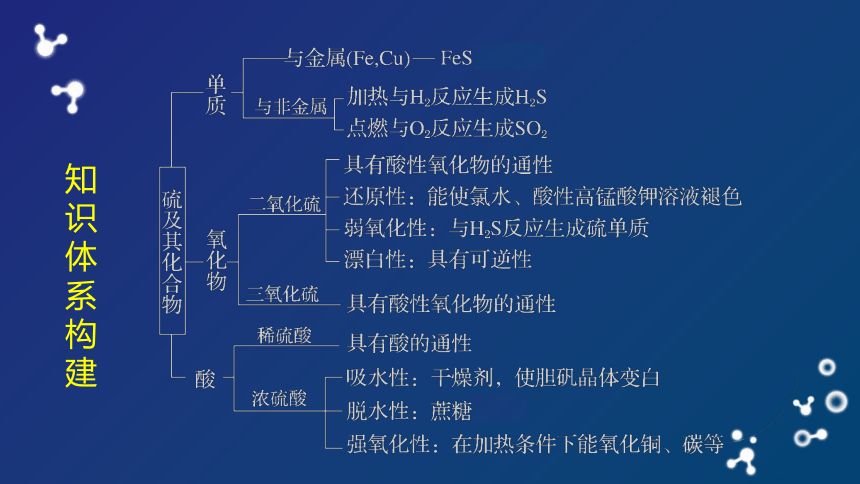
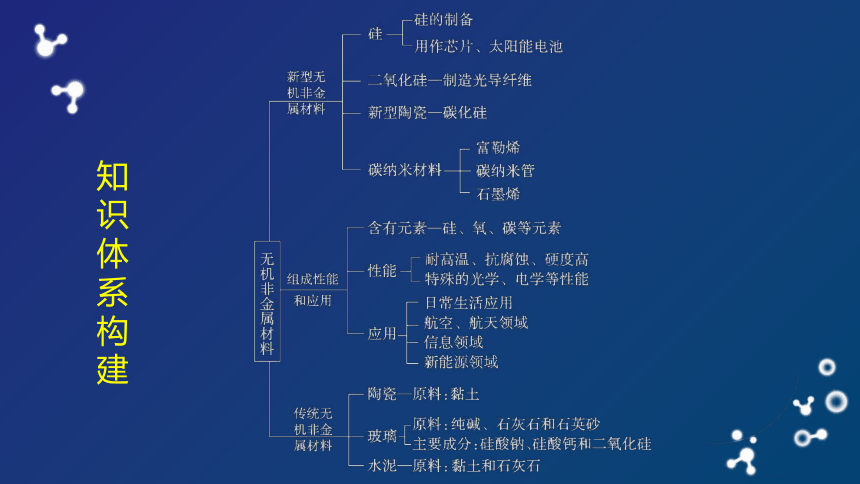
知
识
体
系
构
建
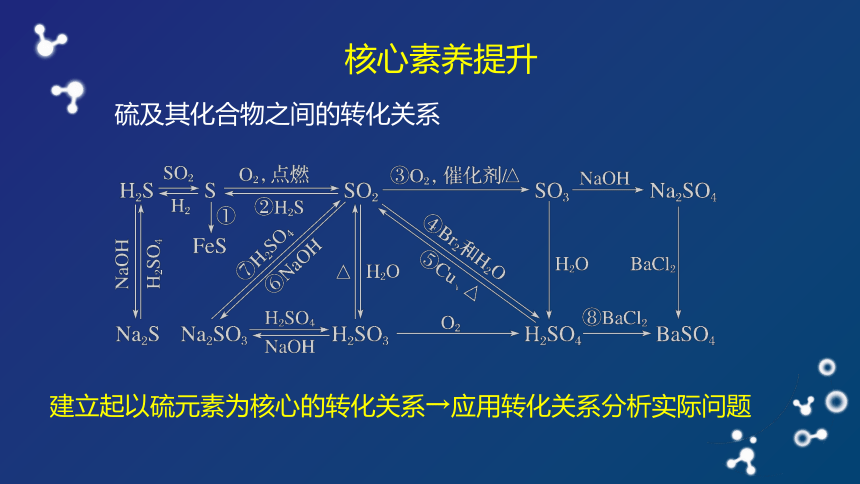
硫及其化合物之间的转化关系
核心素养提升
建立起以硫元素为核心的转化关系→应用转化关系分析实际问题
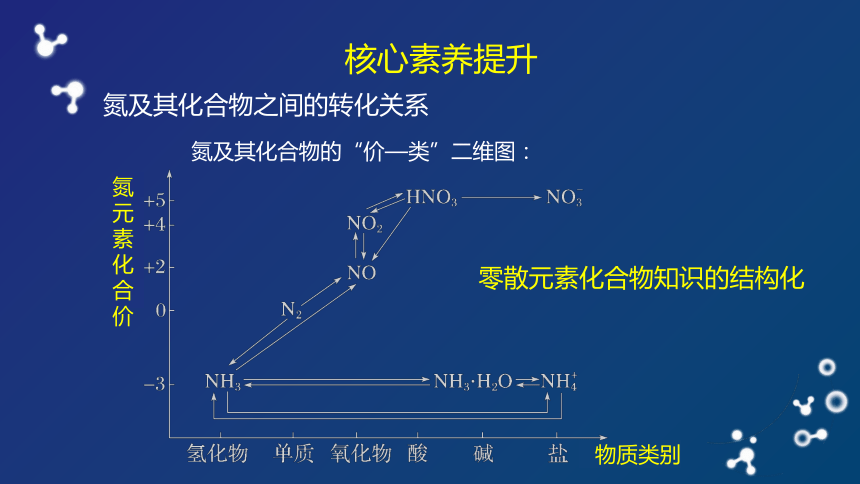
氮及其化合物之间的转化关系
核心素养提升
零散元素化合物知识的结构化
氮及其化合物的“价—类”二维图:
氮
元
素
化
合
价
物质类别
非金属及其化合物对环境的影响
核心素养提升
通过本章学习,充分认识某些化学过程对人类健康和社会发展带来的双重影响。
既了解硫、氮及其化合物和无机非金属材料对人类社会发展的贡献:
如:无机非金属材料在生活、生产、科技(航空、航天、信息、新能源等领域)有着广泛的应用;二氧化硫常用作漂白剂;工业上合成氨用于制造氮肥和生产硝酸;硫酸和硝酸都是重要的化工原料等。
非金属及其化合物对环境的影响
通过本章学习,充分认识某些化学过程对人类健康和社会发展带来的双重影响。
又熟知硫、氮及其化合物对环境的影响:
工业生产和日常生活中大量使用化石燃料产生的二氧化硫、氮氧化物都是大气污染物,都能形成酸雨,严重威胁自然生态环境和人类生存环境,氮氧化物还是形成光化学烟雾、雾霾的重要原因;
工业废水、生活污水、农业上过量使用氮肥、水产养殖使用饵料等,造成水体污染,使水体富营养化。
一、二氧化硫和二氧化碳的重要性质及应用
1.性质比较
SO2 CO2
相同点 常温下是气体,密度大于空气,酸性氧化物 不同点 易溶于水(1体积水 可溶约40体积SO2) 微溶于水
有还原性 无还原性
能使品红溶液褪色 不能使品红溶液褪色
酸性:H2SO3>H2CO3 应用 (除杂) CO2中混有少量SO2,将气体通入饱和NaHCO3溶液中洗气 2. SO2和CO2的鉴别方法
(1)用品红溶液,使品红溶液褪色的是SO2,不能使品红溶液褪色的是CO2。
(2)用氢硫酸,出现浑浊的是SO2,无明显现象的是CO2。
化学方程式为:2H2S+SO2 = 2H2O+3S↓。
(3)用酸性高锰酸钾溶液,使溶液紫色褪去的是SO2,无明显现象的是CO2。
化学方程式为:2KMnO4+5SO2+2H2O = K2SO4+2MnSO4+2H2SO4。
(4)用溴水,使橙色褪去的是SO2,无明显现象的是CO2。
化学方程式为:Br2+2H2O+SO2 = 2HBr+H2SO4。
(5)用硝酸钡溶液,产生白色沉淀的是SO2,无明显现象的是CO2。
3.CO2和SO2混合气体中存在CO2的检验方法
例 : 下列溶液中:
①澄清石灰水; ②H2S溶液; ③酸性KMnO4溶液;
④溴水; ⑤Ba(NO3)2溶液; ⑥品红溶液;
⑦湿润的蓝色石蕊试纸。
不能区别SO2和CO2气体的是( )
A.①⑦ B.①⑤⑦
C.②③④⑤⑥ D.①⑤
A
练习与应用
例 : 用如图所示装置设计一个实验,验证浓硫酸与木炭粉在加热条件下反应产生的各种产物。
这些装置的连接顺序(按产物气流从左到右的方向)是________→________→________→________(填装置的序号)。
④ ② ① ③
复习与提高
二、常见非金属及其化合物的特殊性质和转化关系
1.非金属及其化合物的特殊性质
(1) SO2具有漂白性、较强的还原性,可被卤素、酸性KMnO4溶液等氧化。
(2) 浓硫酸具有三大特性:吸水性、脱水性、强氧化性。
(3) NH3的水溶液呈碱性。
(4) 稀硝酸、浓硝酸都具有强氧化性。
(5) SiO2与氢氟酸、氢氧化钠溶液均能反应,但其不是两性氧化物。
2.非金属及其化合物的特征转化
符合此条件的常见A物质有NH3、 N2、 H2S、S、CH4、C等,如:
例 .元素化合物的知识在社会生产、生活、环境中都有很大的应用。A、B、C、D、E均为中学化学常见的纯净物,A是单质。它们之间有如下的转化关系:
(1)若B是一种碱性气体,D是一种红棕色气体,据此回答下列问题:
①C、D两种化合物能引起的环境问题是________。
A.光化学烟雾 B.能源短缺 C.酸雨 D.温室效应
②C是大气污染物之一。目前,有一种治理方法是在400 ℃左右、有催化剂存在的情况下,用B把C还原为A和水,则该反应的化学方程式是__________________。
③实验室制取B的化学方程式是___________________________。
复习与提高
例 .元素化合物的知识在社会生产、生活、环境中都有很大的应用。A、B、C、D、E均为中学化学常见的纯净物,A是单质。它们之间有如下的转化关系:
(2)若B是一种臭鸡蛋气味的气体,A是一种淡黄色的固体单质,
E是工业生产中一种重要的化合物,据此回答下列问题:
①B和C可以发生反应生成A,写出该反应的化学方程式:_________________。
②金属铜投入E的稀溶液中不发生反应,但再加入H2O2溶液后铜开始溶解,溶液逐渐变为蓝色,写出该反应的离子方程式:__________________________。
复习与提高
三、常见气体的制备、净化、收集及尾气处理
1.气体的发生装置
(1) 加热固体药品制取气体(图①),如制取氨。
(2) 固体与液体反应不加热制取气体(图②),如制取二氧化碳。
(3) 固体与液体或液体与液体反应加热制取气体(图③),如制取氯气。
2.气体的净化干燥装置
结合气体杂质的性质:
如果想用液体试剂来除杂就选用图A装置
如果想用固体试剂来除杂就选用图B、C装置。
3.气体的收集装置
排空气法 排液(水)法
气体收集装置的选择要根据气体的水溶性、是否与氧气反应及气体的密度。
一般有排空气法、排液(水)法,也可将气体直接装入贮气袋中。
4. 尾气处理装置
对于有毒或对空气有污染的气体,要进行尾气处理。
结合气体的性质可以选择用:
吸收剂吸收(图A)、燃烧(图B)或装袋集中处理(图C)的方法。
例 .如图装置可用于制取并收集表格中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
选项 气体 a b c
A NO2 浓硝酸 铜片 NaOH溶液
B SO2 浓硫酸 Cu 酸性KMnO4溶液
C NH3 浓氨水 生石灰 碱石灰
D CO2 稀硝酸 CaCO3 浓硫酸
D
复习与提高
课后作业
2. 每位同学根据自己所学
制作本章知识的个性化思维导图
1. 教材P27~28 复习与提高 1~10题
谢 谢
第五章 专题复习
高一年级 化学
第五章 化工生产中的重要非金属元素
整理与提升
从物质类别和元素价态的视角研究硫和氮等元素及其化合物的性质和用途,可以深化对物质间转化关系的认识。工业上利用这些转化关系,通过控制条件等方法,遵循生态文明思想,可以获得相应的化工产品,实现环境保护与资源利用的和谐统一。
知
识
体
系
构
建
知
识
体
系
构
建
天津市春季学期中小学精品课程资源
知
识
体
系
构
建
硫及其化合物之间的转化关系
核心素养提升
建立起以硫元素为核心的转化关系→应用转化关系分析实际问题
氮及其化合物之间的转化关系
核心素养提升
零散元素化合物知识的结构化
氮及其化合物的“价—类”二维图:
氮
元
素
化
合
价
物质类别
非金属及其化合物对环境的影响
核心素养提升
通过本章学习,充分认识某些化学过程对人类健康和社会发展带来的双重影响。
既了解硫、氮及其化合物和无机非金属材料对人类社会发展的贡献:
如:无机非金属材料在生活、生产、科技(航空、航天、信息、新能源等领域)有着广泛的应用;二氧化硫常用作漂白剂;工业上合成氨用于制造氮肥和生产硝酸;硫酸和硝酸都是重要的化工原料等。
非金属及其化合物对环境的影响
通过本章学习,充分认识某些化学过程对人类健康和社会发展带来的双重影响。
又熟知硫、氮及其化合物对环境的影响:
工业生产和日常生活中大量使用化石燃料产生的二氧化硫、氮氧化物都是大气污染物,都能形成酸雨,严重威胁自然生态环境和人类生存环境,氮氧化物还是形成光化学烟雾、雾霾的重要原因;
工业废水、生活污水、农业上过量使用氮肥、水产养殖使用饵料等,造成水体污染,使水体富营养化。
一、二氧化硫和二氧化碳的重要性质及应用
1.性质比较
SO2 CO2
相同点 常温下是气体,密度大于空气,酸性氧化物 不同点 易溶于水(1体积水 可溶约40体积SO2) 微溶于水
有还原性 无还原性
能使品红溶液褪色 不能使品红溶液褪色
酸性:H2SO3>H2CO3 应用 (除杂) CO2中混有少量SO2,将气体通入饱和NaHCO3溶液中洗气 2. SO2和CO2的鉴别方法
(1)用品红溶液,使品红溶液褪色的是SO2,不能使品红溶液褪色的是CO2。
(2)用氢硫酸,出现浑浊的是SO2,无明显现象的是CO2。
化学方程式为:2H2S+SO2 = 2H2O+3S↓。
(3)用酸性高锰酸钾溶液,使溶液紫色褪去的是SO2,无明显现象的是CO2。
化学方程式为:2KMnO4+5SO2+2H2O = K2SO4+2MnSO4+2H2SO4。
(4)用溴水,使橙色褪去的是SO2,无明显现象的是CO2。
化学方程式为:Br2+2H2O+SO2 = 2HBr+H2SO4。
(5)用硝酸钡溶液,产生白色沉淀的是SO2,无明显现象的是CO2。
3.CO2和SO2混合气体中存在CO2的检验方法
例 : 下列溶液中:
①澄清石灰水; ②H2S溶液; ③酸性KMnO4溶液;
④溴水; ⑤Ba(NO3)2溶液; ⑥品红溶液;
⑦湿润的蓝色石蕊试纸。
不能区别SO2和CO2气体的是( )
A.①⑦ B.①⑤⑦
C.②③④⑤⑥ D.①⑤
A
练习与应用
例 : 用如图所示装置设计一个实验,验证浓硫酸与木炭粉在加热条件下反应产生的各种产物。
这些装置的连接顺序(按产物气流从左到右的方向)是________→________→________→________(填装置的序号)。
④ ② ① ③
复习与提高
二、常见非金属及其化合物的特殊性质和转化关系
1.非金属及其化合物的特殊性质
(1) SO2具有漂白性、较强的还原性,可被卤素、酸性KMnO4溶液等氧化。
(2) 浓硫酸具有三大特性:吸水性、脱水性、强氧化性。
(3) NH3的水溶液呈碱性。
(4) 稀硝酸、浓硝酸都具有强氧化性。
(5) SiO2与氢氟酸、氢氧化钠溶液均能反应,但其不是两性氧化物。
2.非金属及其化合物的特征转化
符合此条件的常见A物质有NH3、 N2、 H2S、S、CH4、C等,如:
例 .元素化合物的知识在社会生产、生活、环境中都有很大的应用。A、B、C、D、E均为中学化学常见的纯净物,A是单质。它们之间有如下的转化关系:
(1)若B是一种碱性气体,D是一种红棕色气体,据此回答下列问题:
①C、D两种化合物能引起的环境问题是________。
A.光化学烟雾 B.能源短缺 C.酸雨 D.温室效应
②C是大气污染物之一。目前,有一种治理方法是在400 ℃左右、有催化剂存在的情况下,用B把C还原为A和水,则该反应的化学方程式是__________________。
③实验室制取B的化学方程式是___________________________。
复习与提高
例 .元素化合物的知识在社会生产、生活、环境中都有很大的应用。A、B、C、D、E均为中学化学常见的纯净物,A是单质。它们之间有如下的转化关系:
(2)若B是一种臭鸡蛋气味的气体,A是一种淡黄色的固体单质,
E是工业生产中一种重要的化合物,据此回答下列问题:
①B和C可以发生反应生成A,写出该反应的化学方程式:_________________。
②金属铜投入E的稀溶液中不发生反应,但再加入H2O2溶液后铜开始溶解,溶液逐渐变为蓝色,写出该反应的离子方程式:__________________________。
复习与提高
三、常见气体的制备、净化、收集及尾气处理
1.气体的发生装置
(1) 加热固体药品制取气体(图①),如制取氨。
(2) 固体与液体反应不加热制取气体(图②),如制取二氧化碳。
(3) 固体与液体或液体与液体反应加热制取气体(图③),如制取氯气。
2.气体的净化干燥装置
结合气体杂质的性质:
如果想用液体试剂来除杂就选用图A装置
如果想用固体试剂来除杂就选用图B、C装置。
3.气体的收集装置
排空气法 排液(水)法
气体收集装置的选择要根据气体的水溶性、是否与氧气反应及气体的密度。
一般有排空气法、排液(水)法,也可将气体直接装入贮气袋中。
4. 尾气处理装置
对于有毒或对空气有污染的气体,要进行尾气处理。
结合气体的性质可以选择用:
吸收剂吸收(图A)、燃烧(图B)或装袋集中处理(图C)的方法。
例 .如图装置可用于制取并收集表格中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
选项 气体 a b c
A NO2 浓硝酸 铜片 NaOH溶液
B SO2 浓硫酸 Cu 酸性KMnO4溶液
C NH3 浓氨水 生石灰 碱石灰
D CO2 稀硝酸 CaCO3 浓硫酸
D
复习与提高
课后作业
2. 每位同学根据自己所学
制作本章知识的个性化思维导图
1. 教材P27~28 复习与提高 1~10题
谢 谢
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
