5.2氮及其化合物 课件 (共17张PPT) 2022-2023学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 5.2氮及其化合物 课件 (共17张PPT) 2022-2023学年高一下学期化学人教版(2019)必修第二册 |  | |
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-21 15:45:34 | ||
图片预览



文档简介
(共17张PPT)
氮及其重要化合物
1、氮气及其氧化物
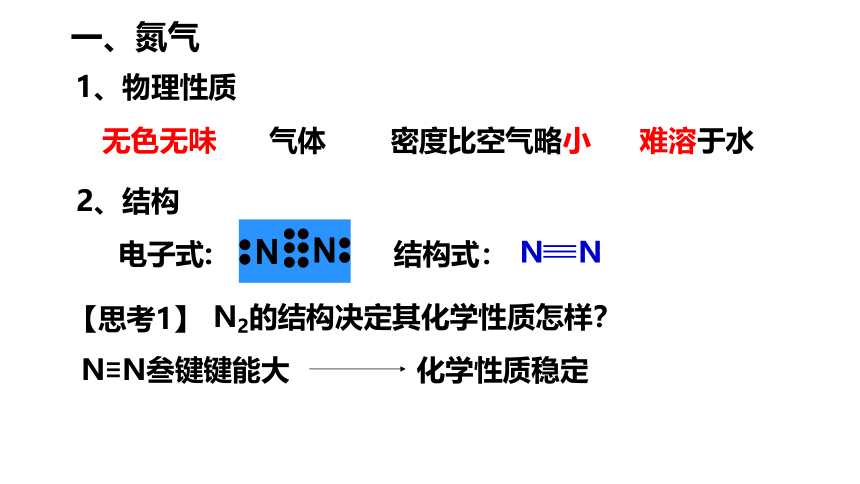
一、氮气
1、物理性质
无色无味
气体
密度比空气略小
难溶于水
2、结构
电子式:
结构式:
N N
N≡N叁键键能大
N2的结构决定其化学性质怎样?
化学性质稳定
【思考1】
3、化学性质
常温下稳定
用作保护气
高温或放电等条件下也能与氢气、氧气和活泼金属反应
(1)氧化性
N2+3H2 2NH3
高温、高压
催化剂
N2+3Mg Mg3N2
点燃
人工固氮
工业合成氨、制硝酸
(2)还原性
N2+O2 2NO
放电
自然固氮
N2 化合态氮
根瘤菌
氮的固定:
将游离态的氮转变为化合态的氮
空气
降温加压
液态
蒸发
N2
O2
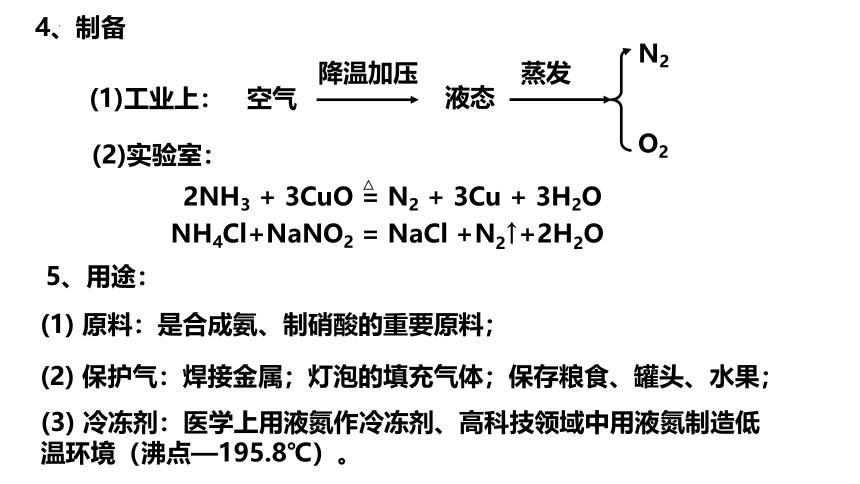
4、制备
(1)工业上:
(2)实验室:
NH4Cl+NaNO2 = NaCl +N2↑+2H2O
2NH3 + 3CuO = N2 + 3Cu + 3H2O
△
5、用途:
(1) 原料:是合成氨、制硝酸的重要原料;
(2) 保护气:焊接金属;灯泡的填充气体;保存粮食、罐头、水果;
(3) 冷冻剂:医学上用液氮作冷冻剂、高科技领域中用液氮制造低温环境(沸点—195.8℃)。
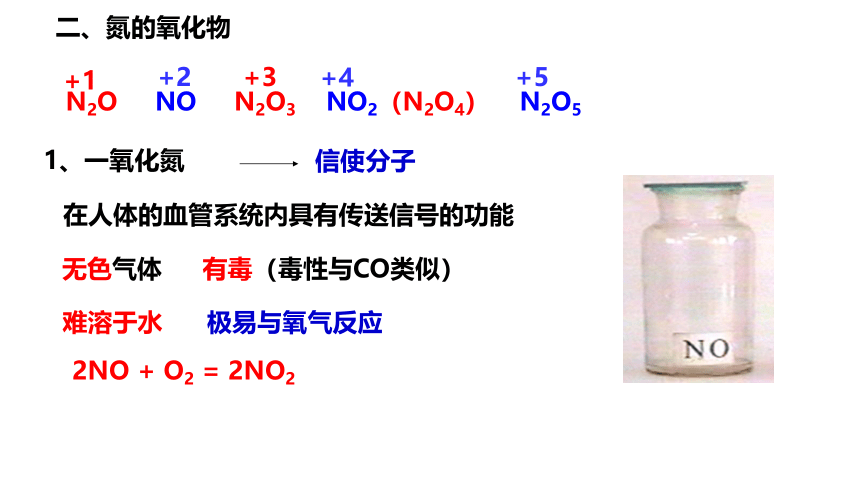
二、氮的氧化物
N2O NO N2O3 NO2(N2O4) N2O5
1、一氧化氮
2NO + O2 = 2NO2
+1
+2
+3
+4
+5
无色气体
有毒(毒性与CO类似)
难溶于水
极易与氧气反应
信使分子
在人体的血管系统内具有传送信号的功能
2、二氧化氮
3NO2 + H2O = 2HNO3 + NO
NO2是一种强氧化剂,能将I-、SO2、H2S等氧化:
2KI+4NO2=2KNO3+I2+2NO
SO2+NO2=NO+SO3
H2S+NO2=S+NO+H2O
2NO2 N2O4
红棕色
有刺激性气味
有毒气体
易液化
密度比空气大
易溶于水
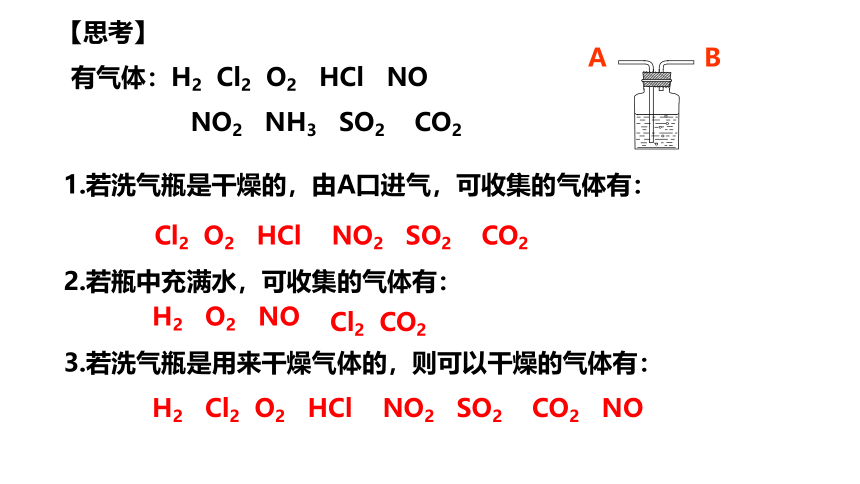
1.若洗气瓶是干燥的,由A口进气,可收集的气体有:
有气体:H2 Cl2 O2 HCl NO
NO2 NH3 SO2 CO2
A B
Cl2 O2 HCl NO2 SO2 CO2
H2 O2 NO
【思考】
2.若瓶中充满水,可收集的气体有:
3.若洗气瓶是用来干燥气体的,则可以干燥的气体有:
H2 Cl2 O2 HCl NO2 SO2 CO2 NO
Cl2 CO2
【2011年全国理综】在实验室欲制取适量NO气体。
①下图中最适合完成该实验的简易装置是________(填序号);
高考链接
②根据所选的装置完成下表(不需要的可不填):
应加入的物质 所起的作用
A
B
C
D
铜片和稀硝酸
发生NO气体
水
排水收集NO气体
接收B中排出的水
Ⅰ
[江苏]利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
(3)该工艺需控制NO和NO2物质的量之比接近1∶1。若n(NO) ∶n(NO2)>1∶1,则会导致 ;若n(NO) ∶n(NO2)<1∶1,则会导致 。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式 。
尾气中NO含量升高
Ca(NO3)2含量升高
3NO2-+2H+=NO3-+2NO↑+H2O
4NO + 3O2 + 2H2O = 4HNO3
4NO2 + O2 + 2H2O = 4HNO3
3NO2 + H2O = 2HNO3 + NO
2NO+O2=2NO2
2NO2 N2O4
氮氧化物的重要反应
NO2 + NO + 2NaOH = 2NaNO2+H2O
2NO2 + 2NaOH = NaNO3+NaNO2+H2O
高温可逆,常温几乎不可逆
2HNO3(浓)+ NO = 3NO2 + H2O
【北京】某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。(问题:实验开始前应打开弹簧夹通入某种气体,其目的是?为完成该探究实验,请写出②~⑥各试剂的名称或化学式)
高考链接
【思考】
如何鉴别都为红棕色的溴蒸气和二氧化氮
二氧化氮和溴蒸气的鉴别
NO2和溴蒸气在性质上的相似之处:
A.均有氧化性 B.溶于水后溶液呈酸性 C.能与碱溶液反应
NO2和溴蒸气在性质上的差异之处:
A.通入水中,NO2溶于水发生反应后溶液无色而溴蒸气溶于水溶液呈橙色
B.通入AgNO3溶液,有淡黄色沉淀生成的为溴蒸气
C.通入CCl4有机溶剂中, 溶于CCl4而且CCl4溶液呈橙红色的为Br2(气)
D.将盛有溴蒸气和NO2气体试管放入冷水中冷却,气体颜色变浅的为NO2
鉴别两者不能用淀粉KI试纸、碱溶液等
不能将NO2和Br2蒸气区分开来的是( )
A.水
B.CCl4
C.湿润的KI淀粉试纸
D.AgNO3溶液
C
试一试:
NOx的主要来源:
三、氮的氧化物对大气的污染
NOx的危害:
①形成酸雨
②形成光化学烟雾
③破坏臭氧层(形成臭氧空洞)
汽车尾气、氮肥的生产、金属的冶炼
四、混合气体(NO、NO2、O2)被水吸收的计算
4NO+3O2+2H2O= 4HNO3
4NO2+O2+2H2O= 4HNO3
练习:一支容积为12 mL的试管内充满O2和NO2的混合气体,将试管倒置于水中,充分反应后若无气体剩余,原混合气体中NO2和O2的体积各为多少?
氮及其重要化合物
1、氮气及其氧化物
一、氮气
1、物理性质
无色无味
气体
密度比空气略小
难溶于水
2、结构
电子式:
结构式:
N N
N≡N叁键键能大
N2的结构决定其化学性质怎样?
化学性质稳定
【思考1】
3、化学性质
常温下稳定
用作保护气
高温或放电等条件下也能与氢气、氧气和活泼金属反应
(1)氧化性
N2+3H2 2NH3
高温、高压
催化剂
N2+3Mg Mg3N2
点燃
人工固氮
工业合成氨、制硝酸
(2)还原性
N2+O2 2NO
放电
自然固氮
N2 化合态氮
根瘤菌
氮的固定:
将游离态的氮转变为化合态的氮
空气
降温加压
液态
蒸发
N2
O2
4、制备
(1)工业上:
(2)实验室:
NH4Cl+NaNO2 = NaCl +N2↑+2H2O
2NH3 + 3CuO = N2 + 3Cu + 3H2O
△
5、用途:
(1) 原料:是合成氨、制硝酸的重要原料;
(2) 保护气:焊接金属;灯泡的填充气体;保存粮食、罐头、水果;
(3) 冷冻剂:医学上用液氮作冷冻剂、高科技领域中用液氮制造低温环境(沸点—195.8℃)。
二、氮的氧化物
N2O NO N2O3 NO2(N2O4) N2O5
1、一氧化氮
2NO + O2 = 2NO2
+1
+2
+3
+4
+5
无色气体
有毒(毒性与CO类似)
难溶于水
极易与氧气反应
信使分子
在人体的血管系统内具有传送信号的功能
2、二氧化氮
3NO2 + H2O = 2HNO3 + NO
NO2是一种强氧化剂,能将I-、SO2、H2S等氧化:
2KI+4NO2=2KNO3+I2+2NO
SO2+NO2=NO+SO3
H2S+NO2=S+NO+H2O
2NO2 N2O4
红棕色
有刺激性气味
有毒气体
易液化
密度比空气大
易溶于水
1.若洗气瓶是干燥的,由A口进气,可收集的气体有:
有气体:H2 Cl2 O2 HCl NO
NO2 NH3 SO2 CO2
A B
Cl2 O2 HCl NO2 SO2 CO2
H2 O2 NO
【思考】
2.若瓶中充满水,可收集的气体有:
3.若洗气瓶是用来干燥气体的,则可以干燥的气体有:
H2 Cl2 O2 HCl NO2 SO2 CO2 NO
Cl2 CO2
【2011年全国理综】在实验室欲制取适量NO气体。
①下图中最适合完成该实验的简易装置是________(填序号);
高考链接
②根据所选的装置完成下表(不需要的可不填):
应加入的物质 所起的作用
A
B
C
D
铜片和稀硝酸
发生NO气体
水
排水收集NO气体
接收B中排出的水
Ⅰ
[江苏]利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
(3)该工艺需控制NO和NO2物质的量之比接近1∶1。若n(NO) ∶n(NO2)>1∶1,则会导致 ;若n(NO) ∶n(NO2)<1∶1,则会导致 。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式 。
尾气中NO含量升高
Ca(NO3)2含量升高
3NO2-+2H+=NO3-+2NO↑+H2O
4NO + 3O2 + 2H2O = 4HNO3
4NO2 + O2 + 2H2O = 4HNO3
3NO2 + H2O = 2HNO3 + NO
2NO+O2=2NO2
2NO2 N2O4
氮氧化物的重要反应
NO2 + NO + 2NaOH = 2NaNO2+H2O
2NO2 + 2NaOH = NaNO3+NaNO2+H2O
高温可逆,常温几乎不可逆
2HNO3(浓)+ NO = 3NO2 + H2O
【北京】某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。(问题:实验开始前应打开弹簧夹通入某种气体,其目的是?为完成该探究实验,请写出②~⑥各试剂的名称或化学式)
高考链接
【思考】
如何鉴别都为红棕色的溴蒸气和二氧化氮
二氧化氮和溴蒸气的鉴别
NO2和溴蒸气在性质上的相似之处:
A.均有氧化性 B.溶于水后溶液呈酸性 C.能与碱溶液反应
NO2和溴蒸气在性质上的差异之处:
A.通入水中,NO2溶于水发生反应后溶液无色而溴蒸气溶于水溶液呈橙色
B.通入AgNO3溶液,有淡黄色沉淀生成的为溴蒸气
C.通入CCl4有机溶剂中, 溶于CCl4而且CCl4溶液呈橙红色的为Br2(气)
D.将盛有溴蒸气和NO2气体试管放入冷水中冷却,气体颜色变浅的为NO2
鉴别两者不能用淀粉KI试纸、碱溶液等
不能将NO2和Br2蒸气区分开来的是( )
A.水
B.CCl4
C.湿润的KI淀粉试纸
D.AgNO3溶液
C
试一试:
NOx的主要来源:
三、氮的氧化物对大气的污染
NOx的危害:
①形成酸雨
②形成光化学烟雾
③破坏臭氧层(形成臭氧空洞)
汽车尾气、氮肥的生产、金属的冶炼
四、混合气体(NO、NO2、O2)被水吸收的计算
4NO+3O2+2H2O= 4HNO3
4NO2+O2+2H2O= 4HNO3
练习:一支容积为12 mL的试管内充满O2和NO2的混合气体,将试管倒置于水中,充分反应后若无气体剩余,原混合气体中NO2和O2的体积各为多少?
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
