3.5.2 合成任务二 官能团的引入消除转化和保护-(共30张PPT)高二化学(人教版2019选择性必修3)
文档属性
| 名称 | 3.5.2 合成任务二 官能团的引入消除转化和保护-(共30张PPT)高二化学(人教版2019选择性必修3) |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-21 00:00:00 | ||
图片预览







文档简介
(共30张PPT)
走进奇妙的化学世界
选择性必修3
第三章 烃的衍生物
第五节 有机合成
你知道吗
从远古时代起,人类长期依靠自然界的资源生存。在实践中,人类逐渐学会了对自然资源进行加工和转化,从生物体中获得有机化合物。然而,自然资源是有限的,天然有机物的性能并不能满足人们的全部需要。19世纪20年代,德国化学家维勒合成了尿素,开创了人工合成有机物的新时代。此后,人们陆续合成了多种天然有机物,还合成了大量自然界并不存在的新的有机物,以满足生产、生活和科学研究对物质性能的特殊需要。有机合成帮助人们发现和制备了-一系列药物、香料、染料、催化剂、添加剂等,有力地推动了材料科学和生命科学的发展。
有机合成的主要任务
有机合成使用相对简单易得的原料,通过有机化学反应构建骨架和引入官能团,由此合成出具有特定结构和性质的目标分子。
化学与生活
“水立方”是我国第一个采用ETFE(乙烯—四氟乙烯共聚物)膜材料作为立面维护体系的建筑。
学习
目标
第2课时
官能团的引入 消除 转化和保护
PART
01
PART
02
认识有机合成的关键是碳骨架的构建和官能团的转化,掌握官能团的引入和转化的一些技巧。
从不同角度对有机化合物的转化关系进行分析和推断,能根据有机化合物的官能团的转化等分析有机合成的合理性。
学习任务:官能团的引入 消除 转化和保护
一、官能团的引入
1.引入碳碳双键
(1)醇或卤代烃的消去反应
CH3CH2OH
CH2=CH2↑+H2O
CH3CH2Br+NaOH CH2=CH2↑+NaBr+H2O
乙醇
△
(2)炔烃的不完全加成反应
CH≡CH+HCl
CH2=CHCl
2.引入碳氧双键
a.醇的催化氧化引入碳氧双键。例如:
2RCH2OH+O2
催化剂
△
2RCHO+2H2O
2RCH(OH)R'+O2
催化剂
△
2R—C—R+2H2O
O
b.某些烯烃被酸性高锰酸钾溶液氧化的反应:
例如:
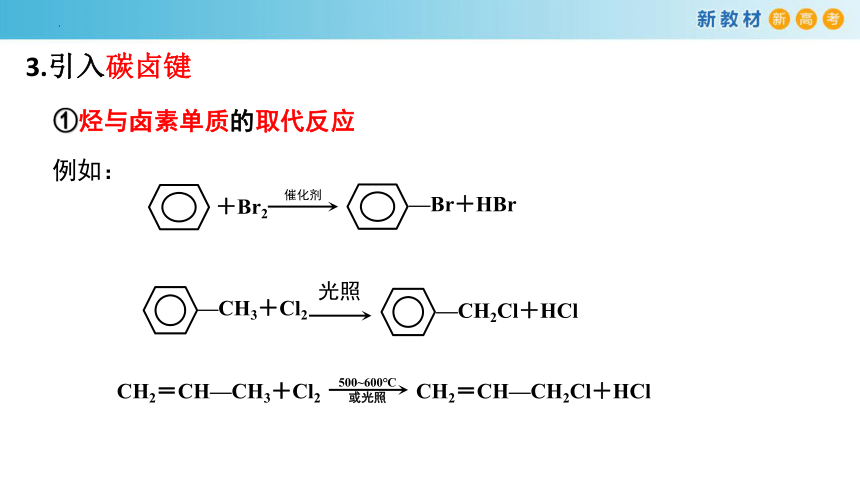
+Br2
催化剂
—Br+HBr
—CH3+Cl2
光照
—CH2Cl+HCl
CH2=CH—CH3+Cl2
500~600℃
或光照
CH2=CH—CH2Cl+HCl
①烃与卤素单质的取代反应
3.引入碳卤键
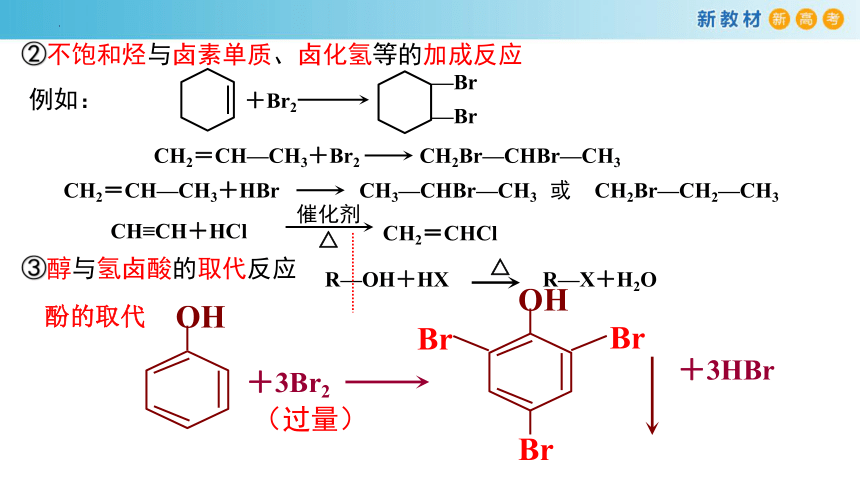
+Br2
—Br
—Br
CH2=CH—CH3+Br2
CH2Br—CHBr—CH3
CH2=CH—CH3+HBr
CH3—CHBr—CH3
CH2Br—CH2—CH3
或
CH≡CH+HCl
催化剂
△
CH2=CHCl
△
R—OH+HX
R—X+H2O
②不饱和烃与卤素单质、卤化氢等的加成反应
例如:
③醇与氢卤酸的取代反应
酚的取代
+3Br2
+3HBr
(过量)
OH
OH
Br
Br
Br
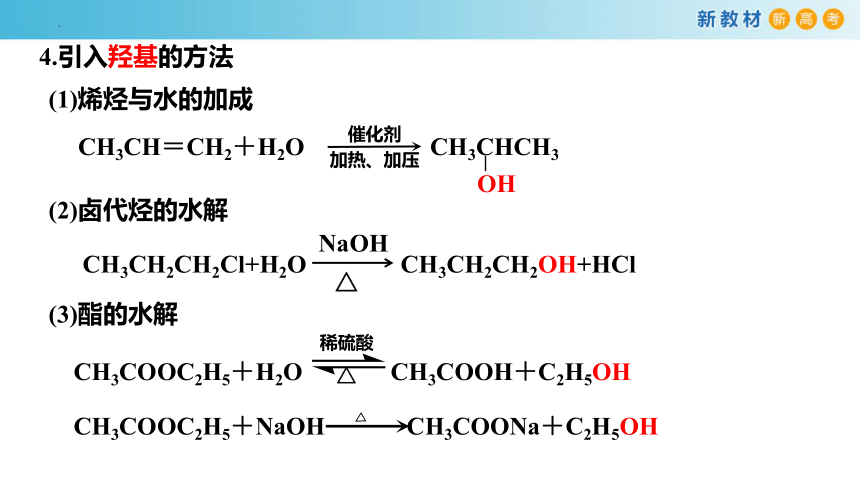
4.引入羟基的方法
(1)烯烃与水的加成
(2)卤代烃的水解
CH3CH2CH2Cl+H2O CH3CH2CH2OH+HCl
NaOH
△
(3)酯的水解
CH3COOC2H5+NaOH CH3COONa+C2H5OH
△
CH3COOC2H5+H2O CH3COOH+C2H5OH
稀硫酸
△
CH3CH=CH2+H2O CH3CHCH3
催化剂
加热、加压
OH
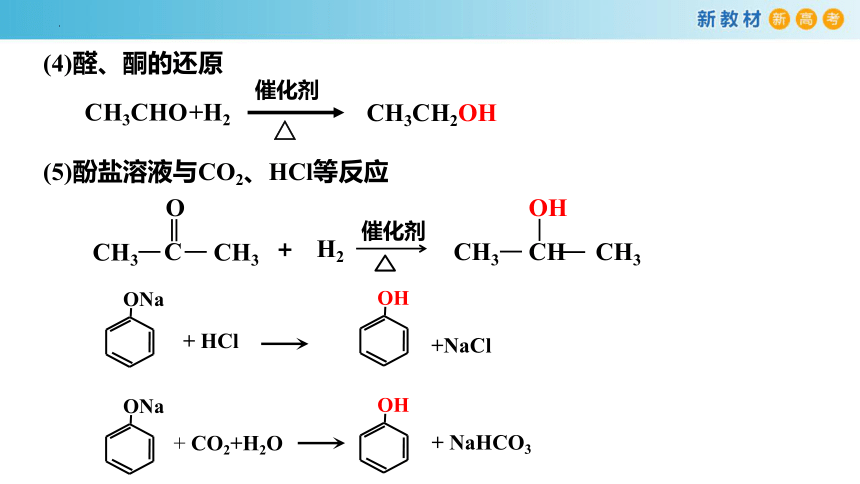
(4)醛、酮的还原
催化剂
CH3CH2OH
CH3CHO
+H2
O
C
CH3
CH3
+
H2
催化剂
OH
CH
CH3
CH3
(5)酚盐溶液与CO2、HCl等反应
+NaCl
OH
+ HCl
ONa
+ NaHCO3
OH
+ CO2+H2O
ONa
△
5.引入羧基的方法
(1)醛的氧化反应
(2)酯、酰胺的水解反应
2CH3CHO+O2
2CH3COOH
CH3COOC2H5+H2O CH3COOH+C2H5OH
稀硫酸
△
催化剂
(3)伯醇被酸性高锰酸钾溶液氧化的反应
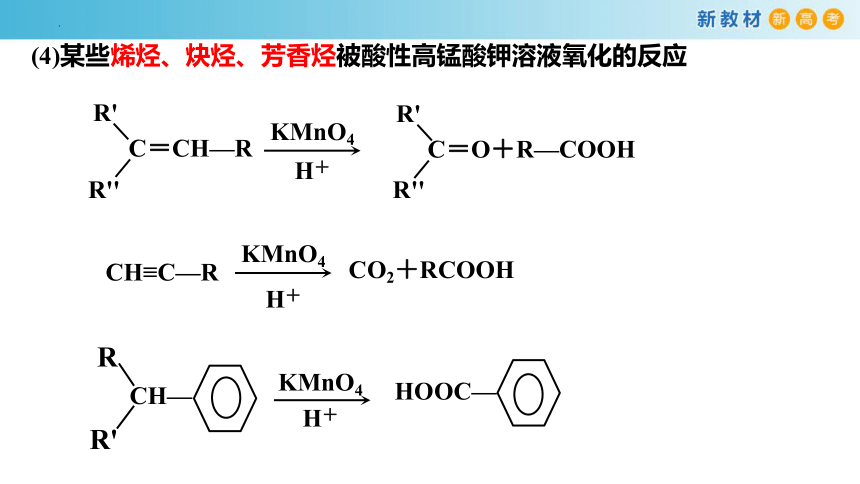
(4)某些烯烃、炔烃、芳香烃被酸性高锰酸钾溶液氧化的反应
CH≡C—R
KMnO4
H+
CO2+RCOOH
CH—
R
R'
KMnO4
H+
HOOC—
C=CH—R
R'
R''
KMnO4
H+
C=O+R—COOH
R'
R''
有机合成的主要任务二: 官能团引入
官能团 引入方法(举例)
碳碳双键 卤代烃的消去或醇的消去或炔烃的不完全加成
碳卤键 醇、酚的取代或烯烃、炔烃的加成或
烷烃、苯及苯的同系物的取代
羟基 烯烃与水的加成或卤代烃的水解或醛的还原或酯的水解
醛基 醇的催化氧化或烯烃的氧化
羧基 醇的氧化或醛的氧化或酯的水解
酯基
酯化反应
二、官能团的消除
加成反应
1.消除不饱和键
2.消除羟基
取代、消去、酯化、氧化
3.消除醛基、酮羰基
加成、氧化
4.消除碳卤键
消去、水解
5.消除酯基、酰胺基
水解
烷烃
烯烃
炔烃
卤代烃
醛
羧酸
酯
醇
加成(+ H2O)
消去(- H2O)
+ H2
+ H2
X2 、HX 加成
X2 /HX 加成
消去(-HX)
+X2
+ HX
+ H2O
氧化
还原
氧化
酯化
水解
水解
酯化
官能团种类变化:
1.利用衍变关系进行转化
三、官能团的转化
2.通过消去、加成(控制试剂)、水解反应使官能团数目增加或减少
CH3CH2OH CH2=CH2
消去
-H2O
加成
+Cl2
CH2—CH2
Cl
Cl
水解
CH2—CH2
OH
OH
官能团数目变化:
CH2CH2Br
CH2=CH2
CH2Br-CH2Br
3.通过消去、加成(控制试剂)使官能团位置改变
CH3CH2CH2Cl
CH3—CH—CH3
Cl
CH3CH=CH2
加成(+ HCl)
消去(-HCl)
官能团位置变化:
官能团的转化体现在烃及其衍生物的相互转化关系中:
规律总结
醇
醛
羧酸
[O]
H2
[O]
四、官能团的保护
含有多个官能团的有机物在进行反应时,非目标官能团也可能受到影响。此时需要将该官能团保护起来,先将其转化为不受该反应影响的其他官能团,反应后再转化复原。
因酚羟基易被氧化,故在加入氧化剂之前将-OH先转化为-ONa(或-OCH3),待其他基氧化后,再酸化使其转化为-OH,其过程表示为
OCH3
COOH
OH
COOH
CH3I
KMnO4/H+
H+
OCH3
CH3
OH
CH3
1.酚羟基的保护
2.醇羟基的保护
可先将羟基转化为醚键,使醇转化为在一般反应条件下比较稳定的醚。待相关合成反应结束后,再在一定条件下脱除起保护作用的基团(保护基),恢复羟基。
用甲苯合成对羟基苯甲酸乙酯的路线如下,其中③的目的是 。
【课堂练习3】
保护酚羟基
碳碳双键易加成,易被O3、H2O2、酸性高锰酸钾等氧化,在氧化其他基团前,可以利用其与HCl等的加成反应将其保护起来,待氧化后再利用消去反应将其转变为碳碳双键。
3.碳碳双键的保护
C=C
+HX
—C—C—
X
H
NaOH/醇
△
C=C
C=C
+H2O
—C—C—
OH
H
浓硫酸
△
C=C
4.醛基的保护
醛基可被弱氧化剂氧化,为避免在反应过程中受到影响,对其保护和恢复过程为
问:设计A、B两步的目的是什么?
防止碳碳双键被氧化
以HOCH2-CH=CH-CH2OH为原料合成HOOC-CH=CH-COOH的路线为
HOCH2-CH=CH-CH2OH
HOCH2-CHCl-CH2-CH2OH
HOOC-CHCl-CH2-COOH
HOOC-CH=CH-COOH
A
B
C
【课堂练习4】
6.氨基(-NH2)的保护
胺基易被O2、O3、H2O2等氧化
CH3
浓硝酸
浓硫酸,加热
CH3
NO2
KMnO4/H+
COOH
NO2
Fe/HCl
COOH
NH2
NH2
COOH
NO2
COOH
Cu/Ag
加热
CH2=CHCH2OH
CH2=CHCHO
催化氧化
CH2=CH-COOH
CH2=CH-CH2-OH
CH2=CH-COOH
KMnO4
方案1:
方案2:
方案3:
1.下列用 制取 的方案中可行的是( )
CH2=CH-CH2-OH
CH2=CH-COOH
方案2:
方案3:
CH2=CHCH2OH
KMnO4
HCl
CH3CHClCH2OH
CH3CHClCOOH
H+
CH2=CHCOONa
CH2=CH-COOH
NaOH/醇
-HCl
2.(1)将 直接氧化能
得到 吗?若不能,如何得到?
(2)由 怎样转变为
有机合成
课堂小结
有机合成的
概念:
任务:碳架构建与
过程:
官能团转化
种类变化
数目变化
位置变化
消去、加成
引入与保护
走进奇妙的化学世界
选择性必修3
第三章 烃的衍生物
第五节 有机合成
你知道吗
从远古时代起,人类长期依靠自然界的资源生存。在实践中,人类逐渐学会了对自然资源进行加工和转化,从生物体中获得有机化合物。然而,自然资源是有限的,天然有机物的性能并不能满足人们的全部需要。19世纪20年代,德国化学家维勒合成了尿素,开创了人工合成有机物的新时代。此后,人们陆续合成了多种天然有机物,还合成了大量自然界并不存在的新的有机物,以满足生产、生活和科学研究对物质性能的特殊需要。有机合成帮助人们发现和制备了-一系列药物、香料、染料、催化剂、添加剂等,有力地推动了材料科学和生命科学的发展。
有机合成的主要任务
有机合成使用相对简单易得的原料,通过有机化学反应构建骨架和引入官能团,由此合成出具有特定结构和性质的目标分子。
化学与生活
“水立方”是我国第一个采用ETFE(乙烯—四氟乙烯共聚物)膜材料作为立面维护体系的建筑。
学习
目标
第2课时
官能团的引入 消除 转化和保护
PART
01
PART
02
认识有机合成的关键是碳骨架的构建和官能团的转化,掌握官能团的引入和转化的一些技巧。
从不同角度对有机化合物的转化关系进行分析和推断,能根据有机化合物的官能团的转化等分析有机合成的合理性。
学习任务:官能团的引入 消除 转化和保护
一、官能团的引入
1.引入碳碳双键
(1)醇或卤代烃的消去反应
CH3CH2OH
CH2=CH2↑+H2O
CH3CH2Br+NaOH CH2=CH2↑+NaBr+H2O
乙醇
△
(2)炔烃的不完全加成反应
CH≡CH+HCl
CH2=CHCl
2.引入碳氧双键
a.醇的催化氧化引入碳氧双键。例如:
2RCH2OH+O2
催化剂
△
2RCHO+2H2O
2RCH(OH)R'+O2
催化剂
△
2R—C—R+2H2O
O
b.某些烯烃被酸性高锰酸钾溶液氧化的反应:
例如:
+Br2
催化剂
—Br+HBr
—CH3+Cl2
光照
—CH2Cl+HCl
CH2=CH—CH3+Cl2
500~600℃
或光照
CH2=CH—CH2Cl+HCl
①烃与卤素单质的取代反应
3.引入碳卤键
+Br2
—Br
—Br
CH2=CH—CH3+Br2
CH2Br—CHBr—CH3
CH2=CH—CH3+HBr
CH3—CHBr—CH3
CH2Br—CH2—CH3
或
CH≡CH+HCl
催化剂
△
CH2=CHCl
△
R—OH+HX
R—X+H2O
②不饱和烃与卤素单质、卤化氢等的加成反应
例如:
③醇与氢卤酸的取代反应
酚的取代
+3Br2
+3HBr
(过量)
OH
OH
Br
Br
Br
4.引入羟基的方法
(1)烯烃与水的加成
(2)卤代烃的水解
CH3CH2CH2Cl+H2O CH3CH2CH2OH+HCl
NaOH
△
(3)酯的水解
CH3COOC2H5+NaOH CH3COONa+C2H5OH
△
CH3COOC2H5+H2O CH3COOH+C2H5OH
稀硫酸
△
CH3CH=CH2+H2O CH3CHCH3
催化剂
加热、加压
OH
(4)醛、酮的还原
催化剂
CH3CH2OH
CH3CHO
+H2
O
C
CH3
CH3
+
H2
催化剂
OH
CH
CH3
CH3
(5)酚盐溶液与CO2、HCl等反应
+NaCl
OH
+ HCl
ONa
+ NaHCO3
OH
+ CO2+H2O
ONa
△
5.引入羧基的方法
(1)醛的氧化反应
(2)酯、酰胺的水解反应
2CH3CHO+O2
2CH3COOH
CH3COOC2H5+H2O CH3COOH+C2H5OH
稀硫酸
△
催化剂
(3)伯醇被酸性高锰酸钾溶液氧化的反应
(4)某些烯烃、炔烃、芳香烃被酸性高锰酸钾溶液氧化的反应
CH≡C—R
KMnO4
H+
CO2+RCOOH
CH—
R
R'
KMnO4
H+
HOOC—
C=CH—R
R'
R''
KMnO4
H+
C=O+R—COOH
R'
R''
有机合成的主要任务二: 官能团引入
官能团 引入方法(举例)
碳碳双键 卤代烃的消去或醇的消去或炔烃的不完全加成
碳卤键 醇、酚的取代或烯烃、炔烃的加成或
烷烃、苯及苯的同系物的取代
羟基 烯烃与水的加成或卤代烃的水解或醛的还原或酯的水解
醛基 醇的催化氧化或烯烃的氧化
羧基 醇的氧化或醛的氧化或酯的水解
酯基
酯化反应
二、官能团的消除
加成反应
1.消除不饱和键
2.消除羟基
取代、消去、酯化、氧化
3.消除醛基、酮羰基
加成、氧化
4.消除碳卤键
消去、水解
5.消除酯基、酰胺基
水解
烷烃
烯烃
炔烃
卤代烃
醛
羧酸
酯
醇
加成(+ H2O)
消去(- H2O)
+ H2
+ H2
X2 、HX 加成
X2 /HX 加成
消去(-HX)
+X2
+ HX
+ H2O
氧化
还原
氧化
酯化
水解
水解
酯化
官能团种类变化:
1.利用衍变关系进行转化
三、官能团的转化
2.通过消去、加成(控制试剂)、水解反应使官能团数目增加或减少
CH3CH2OH CH2=CH2
消去
-H2O
加成
+Cl2
CH2—CH2
Cl
Cl
水解
CH2—CH2
OH
OH
官能团数目变化:
CH2CH2Br
CH2=CH2
CH2Br-CH2Br
3.通过消去、加成(控制试剂)使官能团位置改变
CH3CH2CH2Cl
CH3—CH—CH3
Cl
CH3CH=CH2
加成(+ HCl)
消去(-HCl)
官能团位置变化:
官能团的转化体现在烃及其衍生物的相互转化关系中:
规律总结
醇
醛
羧酸
[O]
H2
[O]
四、官能团的保护
含有多个官能团的有机物在进行反应时,非目标官能团也可能受到影响。此时需要将该官能团保护起来,先将其转化为不受该反应影响的其他官能团,反应后再转化复原。
因酚羟基易被氧化,故在加入氧化剂之前将-OH先转化为-ONa(或-OCH3),待其他基氧化后,再酸化使其转化为-OH,其过程表示为
OCH3
COOH
OH
COOH
CH3I
KMnO4/H+
H+
OCH3
CH3
OH
CH3
1.酚羟基的保护
2.醇羟基的保护
可先将羟基转化为醚键,使醇转化为在一般反应条件下比较稳定的醚。待相关合成反应结束后,再在一定条件下脱除起保护作用的基团(保护基),恢复羟基。
用甲苯合成对羟基苯甲酸乙酯的路线如下,其中③的目的是 。
【课堂练习3】
保护酚羟基
碳碳双键易加成,易被O3、H2O2、酸性高锰酸钾等氧化,在氧化其他基团前,可以利用其与HCl等的加成反应将其保护起来,待氧化后再利用消去反应将其转变为碳碳双键。
3.碳碳双键的保护
C=C
+HX
—C—C—
X
H
NaOH/醇
△
C=C
C=C
+H2O
—C—C—
OH
H
浓硫酸
△
C=C
4.醛基的保护
醛基可被弱氧化剂氧化,为避免在反应过程中受到影响,对其保护和恢复过程为
问:设计A、B两步的目的是什么?
防止碳碳双键被氧化
以HOCH2-CH=CH-CH2OH为原料合成HOOC-CH=CH-COOH的路线为
HOCH2-CH=CH-CH2OH
HOCH2-CHCl-CH2-CH2OH
HOOC-CHCl-CH2-COOH
HOOC-CH=CH-COOH
A
B
C
【课堂练习4】
6.氨基(-NH2)的保护
胺基易被O2、O3、H2O2等氧化
CH3
浓硝酸
浓硫酸,加热
CH3
NO2
KMnO4/H+
COOH
NO2
Fe/HCl
COOH
NH2
NH2
COOH
NO2
COOH
Cu/Ag
加热
CH2=CHCH2OH
CH2=CHCHO
催化氧化
CH2=CH-COOH
CH2=CH-CH2-OH
CH2=CH-COOH
KMnO4
方案1:
方案2:
方案3:
1.下列用 制取 的方案中可行的是( )
CH2=CH-CH2-OH
CH2=CH-COOH
方案2:
方案3:
CH2=CHCH2OH
KMnO4
HCl
CH3CHClCH2OH
CH3CHClCOOH
H+
CH2=CHCOONa
CH2=CH-COOH
NaOH/醇
-HCl
2.(1)将 直接氧化能
得到 吗?若不能,如何得到?
(2)由 怎样转变为
有机合成
课堂小结
有机合成的
概念:
任务:碳架构建与
过程:
官能团转化
种类变化
数目变化
位置变化
消去、加成
引入与保护
