人教版(2019)必修 第二册第八章化学与可持续发展专题复习(共48张PPT)
文档属性
| 名称 | 人教版(2019)必修 第二册第八章化学与可持续发展专题复习(共48张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-22 10:33:59 | ||
图片预览



文档简介
(共48张PPT)
第八章 专题复习
高一年级 化学
环节二
化学品的合理使用
自然资源的开发利用
环境保护与绿色化学
化学与可持续发展
专题一、自然资源的开发利用
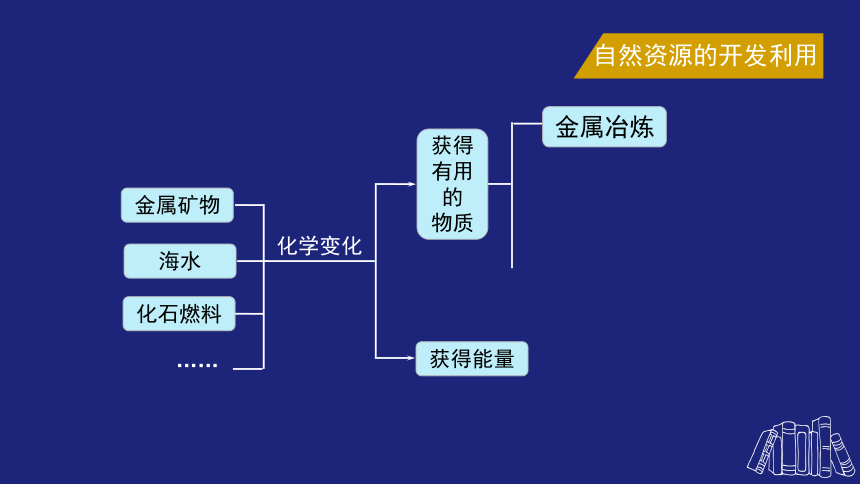
金属矿物
海水
化石燃料
……
化学变化
获得能量
获得有用的
物质
金属冶炼
自然资源的开发利用
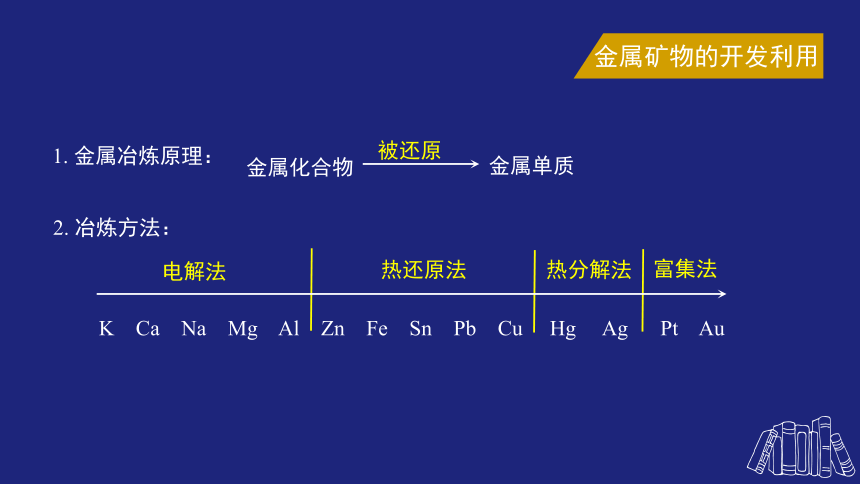
1. 金属冶炼原理:
金属矿物的开发利用
被还原
金属化合物
金属单质
2. 冶炼方法:
K Ca Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
电解法
热还原法
热分解法
富集法
例如:
热分解法:汞:2HgO 2Hg+O2 ↑
银:2Ag2O 4Ag+O2 ↑
热还原法:铜:2CuO+C 2Cu+CO2 ↑
铁:2Fe2O3+3CO 4Fe+3CO2 Fe2O3+2Al Al2O3+2Fe (铝热反应)
电解法: 铝:2Al2O3(熔融) 4Al+3O2↑ (不能用AlCl3,AlCl3不是离子化合物)
镁:MgCl2(熔融) Mg+Cl2↑
钠:2NaCl (熔融) 2Na+Cl2 ↑
Δ
Δ
高温
高温
高温
电解
电解
电解
金属矿物的开发利用
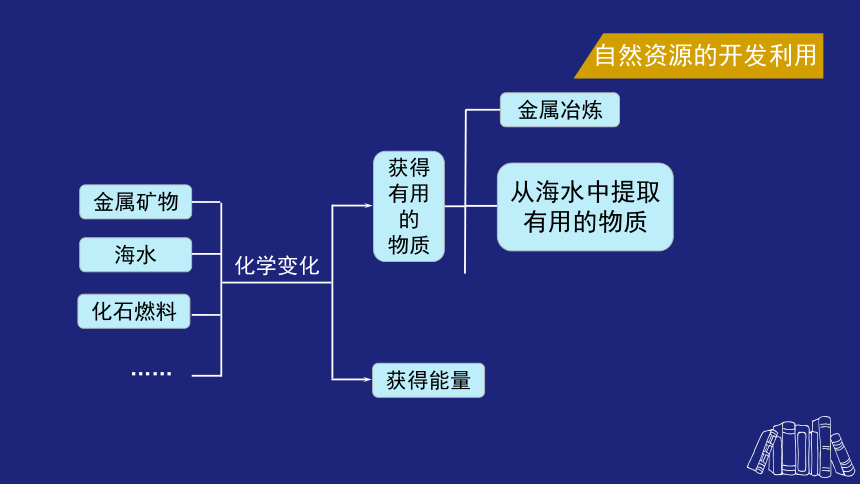
金属矿物
海水
化石燃料
……
化学变化
获得能量
获得有用的
物质
金属冶炼
从海水中提取有用的物质
自然资源的开发利用
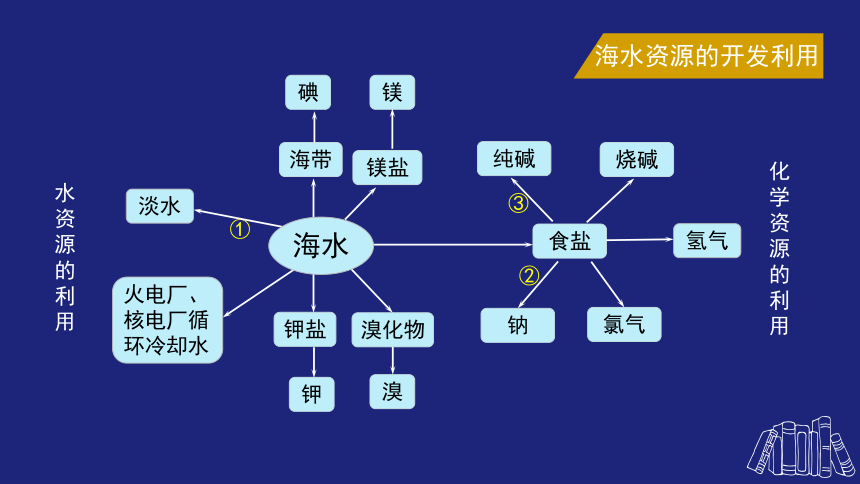
海水资源的开发利用
纯碱
碘
②
③
淡水
氢气
烧碱
钠
氯气
钾盐
溴化物
钾
溴
海带
镁盐
镁
食盐
①
火电厂、核电厂循环冷却水
海水
水资源的利用
化学资源的利用
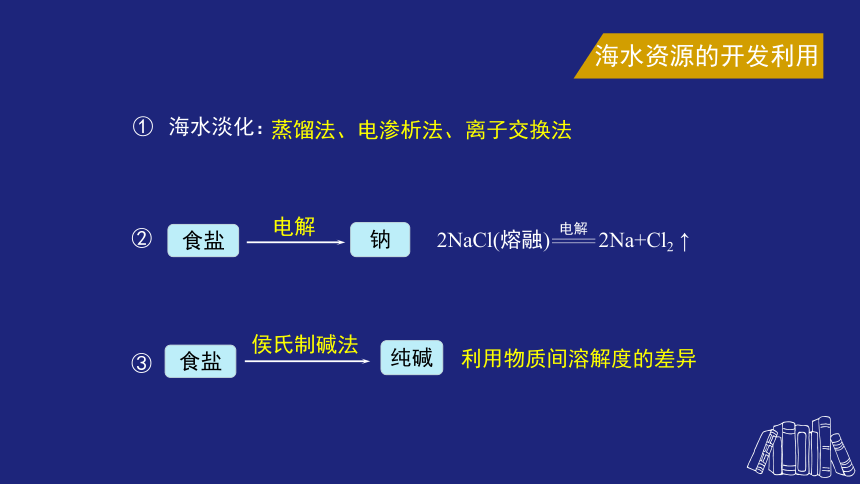
海水淡化:
蒸馏法、电渗析法、离子交换法
②
食盐
钠
电解
③
食盐
纯碱
利用物质间溶解度的差异
侯氏制碱法
2NaCl(熔融) 2Na+Cl2 ↑
电解
海水资源的开发利用
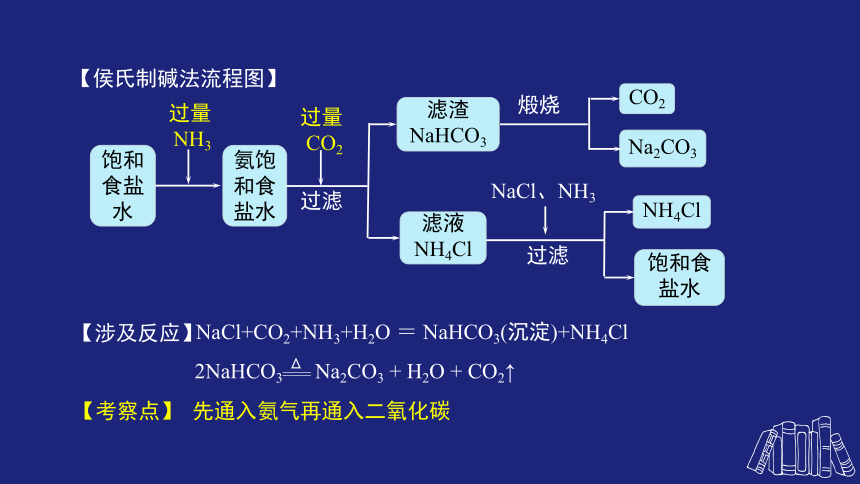
【侯氏制碱法流程图】
NaCl+CO2+NH3+H2O = NaHCO3(沉淀)+NH4Cl
【涉及反应】
【考察点】
先通入氨气再通入二氧化碳
饱和食盐水
过量
NH3
氨饱和食盐水
过量
CO2
过滤
滤渣
NaHCO3
Na2CO3
煅烧
CO2
滤液
NH4Cl
饱和食盐水
NH4Cl
NaCl、NH3
过滤
2NaHCO3 Na2CO3 + H2O + CO2↑
Δ
纯碱
②
③
淡水
氢气
烧碱
钠
氯气
钾盐
溴化物
钾
溴
食盐
①
火电厂、核电厂循环冷却水
海水
水资源的利用
化学资源的利用
④
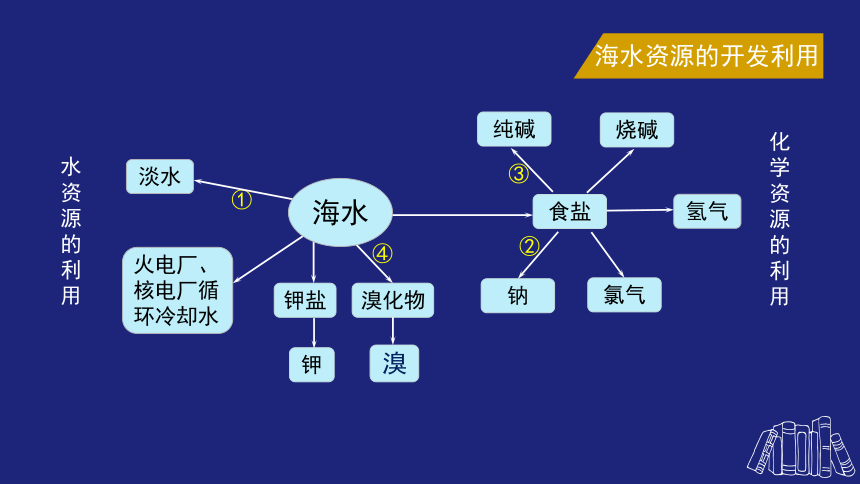
海水资源的开发利用
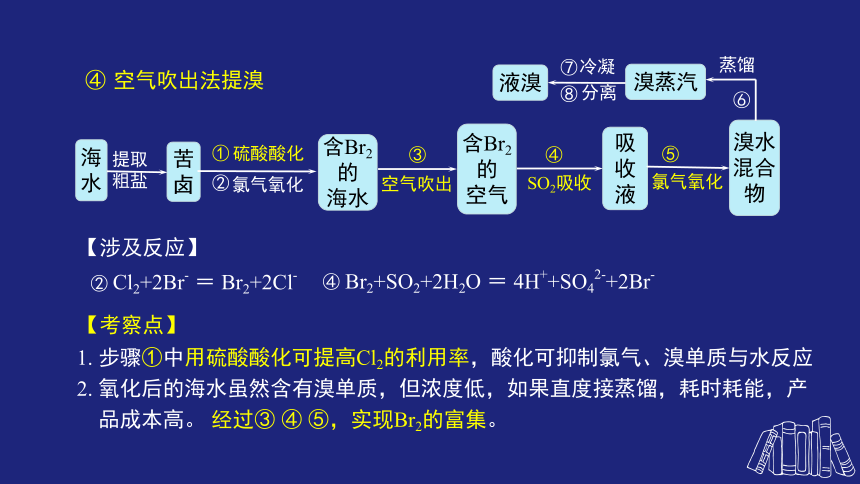
空气吹出法提溴
④
【涉及反应】
Cl2+2Br- = Br2+2Cl-
Br2+SO2+2H2O = 4H++SO42-+2Br-
②
④
【考察点】
1. 步骤①中用硫酸酸化可提高Cl2的利用率,酸化可抑制氯气、溴单质与水反应
2. 氧化后的海水虽然含有溴单质,但浓度低,如果直度接蒸馏,耗时耗能,产
品成本高。 经过③ ④ ⑤,实现Br2的富集。
海
水
提取
粗盐
苦
卤
硫酸酸化
溴蒸汽
含Br2的
空气
含Br2
的
海水
溴水
混合
物
吸收液
①
氯气氧化
②
空气吹出
③
SO2吸收
④
氯气氧化
⑤
蒸馏
⑥
冷凝
⑦
⑧
分离
液溴
纯碱
碘
②
③
淡水
氢气
烧碱
钠
氯气
钾盐
溴化物
钾
溴
海带
食盐
①
火电厂、核电厂循环冷却水
海水
水资源的利用
化学资源的利用
④
⑤
海水资源的开发利用
【涉及反应】
Cl2+2I- = I2+2Cl-
1. 灼烧海带需要用到的仪器有:坩埚、坩埚钳、泥三角、三脚架、酒精灯。
2. 氧化剂除可用氯气,还可以选择H2O2、酸性高锰酸钾溶液、新制氯水等,
这些氧化剂与I-发生氧化还原反应的离子方程式的配平需要熟练掌握。
3. 萃取剂的选择原则:ⅰ不与原溶液反应; ⅱ与原溶剂不互溶; ⅲ溶质
在萃取剂中的溶解度大于在原溶剂中的溶解度。
⑤ 海带提碘
【考察点】
海
带
灼烧
海带灰
浸泡
单质碘
含I-
的溶液
海带灰悬浊液
含I2的有机溶液
含I2
的溶液
过滤
适量氯气
萃取
蒸馏
氧化
纯碱
碘
②
③
淡水
氢气
烧碱
钠
氯气
钾盐
溴化物
钾
溴
海带
镁盐
镁
食盐
①
火电厂、核电厂循环冷却水
海水
水资源的利用
化学资源的利用
⑥
④
⑤
海水资源的开发利用
海水
提取
粗盐
苦卤
高温
煅烧
MgCl2
溶液
Mg(OH)2
Mg
无水MgCl2
盐酸
③
④
电解
贝壳CaCO3
【涉及反应】
Mg2++Ca(OH)2 = Mg(OH)2 +Ca2+
Mg(OH)2+2H+ = Mg2++2H2O
②
③
⑥ 海水制镁
一定
条件
CaO
H2O
石灰乳
①
②
⑤
MgCl2(熔融) Mg+Cl2↑
①
CaCO3 CaO+CO2↑
电解
高温
金属矿物
海水
化石燃料
……
化学变化
获得能量
获得有用的
物质
金属冶炼
从海水中提取有用的物质
……
化石燃料的综合利用
煤的
综合利用
天然气化工
自然资源的开发利用
石油炼制
化学变化
物理变化
化石燃料的综合利用
化石燃料 煤 石油 天然气
主要成分 有机物和少量无机物组成的复杂混合物,组成以碳元素为主 多种碳氢化合物组成的混合物,成分复杂 主要成分是甲烷,天然气的水合物又称为可燃冰
综合利用 煤的 干馏 煤的气化 煤的液化 分馏 裂化 裂解 催化重整
天然气化工
化学变化
变化过程 原理 产物
煤 干馏 使煤隔绝空气加强热,使其分解的过程 出炉煤气、煤焦油、焦炭
气化 把煤中的有机物转化为可燃性气体 氢气、一氧化碳等
液化 把煤转化为液体燃料的过程 液体燃料如甲醇、汽油等
石 油 分馏 利用石油中各组分沸点的不同进行分离 汽油、煤油、柴油、重油等
裂化 将大分子的重油断裂为小分子的轻质油 轻质油
裂解 深度的裂化 乙烯、丙烯、甲烷等气态烃
催化重整 石油中链状烃重新调整结构转化为环状烃 苯或甲苯等
化石燃料的综合利用
[例 题]工业上冶炼下列金属的化学反应原理不正确的是( )
A. 2NaCl (熔融) 2Na+Cl2 ↑
B. 2MgO 2Mg+O2 ↑
C. Fe2O3+3CO 2Fe+3CO2
D. 2HgO 2Hg+O2 ↑
B
电解
典型例题
高温
△
△
[例 题]在冶金工业上,均不能用常用还原剂制得的是 ( )
A. Na、Mg、Al、K B. Na、K、Fe、Zn
C. Zn、Fe、Cu、Ag D. Mg、Al、Zn、Fe
典型例题
A
[例 题] 下列变化不属于化学变化的是( )
① 煤的干馏 ② 煤的液化 ③ 煤的汽化 ④ 石油的分馏
⑤ 石油的催化裂化 ⑥ 石油的裂解 ⑦ 煤的开采 ⑧ 海水蒸馏
A. ①②③④⑧ B. ②④⑥⑤⑦ C. ④⑦⑧ D. ⑥⑧
典型例题
C
[解析]裂化汽油中含有不饱和烃,而直馏汽油是由石油直接分馏得到
的汽油不含不饱和烃,所以可选用直馏汽油萃取溴。故选 A。
[例 题]下列物质中能用于萃取溴水中溴的是 ( )
A. 直馏汽油 B. 裂化汽油
C. 酒精 D. 水
A
典型例题
[例 题] 石灰石是一种化工原料,如图,下列说法正确的是( )
A. 漂粉精是混合物,主要成分是氯化钙
B. 图示的制纯碱方法,要求先向饱和食盐水中通 NH3,然后再通 CO2
C. 纯碱属于碱,俗名苏打
D. 制取纯碱和漂粉精所涉及的反应都是非氧化还原反应
B
[解析] 2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O 漂粉精主要成分是次氯酸钙,
该反应属于氧化还原反应;纯碱碳酸钠属于盐类。故选 B。
石灰石
高温
CO2
NaHCO3
NaCl NH3
H2O
H2O
纯碱
漂粉精
Cl2
△
CaO
Ca(OH)2
[例 题] 从海带中提取碘的实验过程如下图所示
(1) 步骤①灼烧海带时会用到下列仪器中的( )
A. 烧杯 B. 坩埚 C. 表面皿 D. 泥三角 E. 酒精灯 F. 三脚架
(2) 步骤③和⑤的操作名称是 、 _
(3) 步骤④反应的离子方程式是____________________________
(4) 请设计实验,检验水溶液中是否含有碘单质_______________________
___________________________________________________
过滤
B D E F
萃取
2I-+2H++H2O2 = I2 +2H2O
加入几滴淀粉溶液,如果出现蓝色,则说明含有碘单质
取少量水溶液于试管中,
海带
①灼烧
海带灰
②浸泡
海带灰悬浊液
③
含I-溶液
④H2O2、稀硫酸
含I2溶液
⑤提取碘
I2的CCl4溶液
⑥
单质I2
专题二、化学品的合理使用
化学品的合理使用
合理用药
安全使用食品添加剂
农药
化肥
化肥、农药的合理施用
化学品的合理使用
土壤酸碱性、作物营养状况、化肥本身的性质
水体富营养化、影响土壤酸碱性、作物残留超标等
高效、低毒、低残留
化肥农药合理施用
新型农药的发展方向
合理施用化肥考虑因素
滥用化肥和农药的危害
化学品的合理使用
滥用药物危害严重
安全、有效、经济、适当等
合理用药
重要性
药物分类
原则
天然药物
合成药物
处方药
非处方药 OTC
化学品的合理使用
天然的和人工合成的
按照GB 2760-2014《食品安全国家标准 食品添加剂使用标准》的规定使用
食品添加剂
分类
定义
相关使用原则和规定
为改善食品品质和色、香、味,以及防腐、保鲜和加工工艺的需要而加入食品中的人工合成或天然的物质
化学品的合理使用
名称 主要作用 常用物质 代表物结构或成分
着色剂 改善食 品颜色 红曲红、β-胡萝卜素、姜黄、柠檬黄、靛蓝
增味剂 增加食品的鲜味 味精(谷氨酸钠)
膨松剂 使面团疏松、多孔 单一膨松剂、 复合膨松剂 NaHCO3 NH4HCO3
凝固剂 改善食 品形态 盐卤、 葡萄糖酸-δ-内酯 MgCl2 CaSO4
柠檬黄
常见食品添加剂
防腐剂 防止食品 腐败变质 苯甲酸、苯甲酸钠、亚硝酸钠、山梨酸、山梨酸钾
山梨酸钾
抗氧 化剂 防止食品被氧化变质 抗坏血酸(VC) VC
营养 强化剂 补充必要的营养成分 维生素、碳酸钙、硫酸亚铁、硫酸锌、碘酸钾 VB、VD、CaCO3、FeSO4、ZnSO4、KIO3
常见食品添加剂
典型例题
[例 题] 下列对化肥、农药的说法正确的是( )
A. 农药本身有毒,应该禁止施用农药
B. 化肥可以使农作物增产,应尽可能大量施用化肥
C. 硝酸铵(NH4NO3)可直接作化肥使用
D. 为了减少污染应根据作物、虫害和农药的特点合理施用农药
D
[例 题] 下列说法正确的是( )
A. 为了使火腿肠颜色更鲜艳,可多加一些亚硝酸钠
B. 碳酸氢钠类药物可以用于治疗胃溃疡患者胃酸过多
C. 药物可以治疗疾病,所有的药物都可以自行购买
D. 在规定范围内规范使用食品添加剂,对人体健康不会产生不良影响
D
[解析]使用食品添加剂应当符合相应质量标准,而不是越多越好。碳酸氢钠
与胃酸作用生成大量二氧化碳使胃内压强增大,胃溃疡患者易形成胃
穿孔。处方药需要凭医生的 处方才能从药房或药店获得。
典型例题
专题三、环境保护与绿色化学
工业三废
固体废物的处理应遵循无害化、减量化、资源化的原则,
达到减少环境污染和资源回收利用这两个重要目的。
废气
常用的污水处理方法包括物理法、化学法和生物法,
污水处理常用的化学方法有 、 、 等。
化石燃料的燃烧
工业生产过程产生的废气
工业废气携带的颗粒物
氧化还原法
废水
废渣
一定条件下
次生污染物
【雾霾、光化学烟雾、
酸雨(pH<5.6)等】
中和法
沉淀法
工业三废
利用化学原理和技术手段,减少或消除产品和应用中涉及
的有害化学物质, 。
绿色化学
绿色化学
常见原子利用率100%的反应有 、 、 。
核心
反应物原子全部转化为期望的最终产物,原子利用率100%。
原子经济性反应
加聚反应
从源头减少或消除污染
加成反应
化合反应
环境问题 主要污染物 主要危害
温室效应 主要是CO2,此外还包括甲烷等气体 全球气候变暖,破坏生态环境
酸雨 SO2、NOx 土壤酸化、水源污染、建筑物腐蚀
光化学烟雾 NOx、碳氢化合物 破坏人体呼吸系统,严重可导致死亡
臭氧层空洞 氟氯代烷、NOx 到达地面紫外线增多,危害环境和健康
赤潮和水华 含氮磷元素的营 养物质排入水体 水体富营养化,水中藻类疯长,
使水体浑浊、水质恶化
白色污染 废弃塑料制品 难降解、难回收,对土壤有极大危害
PM2.5 颗粒物 污染空气、形成雾霾,危害健康
常见环境污染问题
[例 题] 下列说法不正确的是( )
A. 重金属、农药和难降解的有机物等会造成水体污染
B. 装修材料中的甲醛、芳香烃及氡等会造成居室污染
C. 水体污染会造成地方性甲状腺肿
D. 推广垃圾分类存放、分类回收、分类处理
C
[解析] 地方性甲状腺肿是由于缺碘造成的,故选C。
典型例题
[例 题]下列有关环境问题的说法正确的是 ( )
A. 燃煤时加入适量石灰石可减少废气中 SO2 的含量
B. 臭氧体积分数超过 10-4 % 的空气有利于人体健康
C. pH 在 5. 6 ~7. 0 之间的降水通常称为酸雨
D. 制备CuSO4采用:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O 符合绿色化学理念
A
[解析] 按照绿色化学的理念,制备硫酸铜,应采用 2Cu+O2 2CuO;
CuO+H2SO4 = CuSO4+H2O。
△
典型例题
△
课后作业
运用所学知识设计实验,检验市售加碘食盐中的碘酸钾。
提示:(1) 5I- +IO3- +6H+ = 3I2+3H2O
(2) 5SO32- +2IO3- + 2H+ = 5SO42-+ I2 +H2O
(3) 碘单质与淀粉作用显蓝色
(4) 市售碘盐中的碘元素以可溶性盐的形式存在
完成教材P124 复习与提高的第1、7、8、9题
拓展题
必做题
环节二
化学品的合理使用
自然资源的开发利用
环境保护与绿色化学
化学与可持续发展
同学们,再见!
[例 题]已知MgO、MgCl2的熔点分别为2800℃、604℃,将MgO、MgCl2加热
熔融后通电电解,都可得到金属镁。海水中含有MgCl2,工业上从海水
中提取镁,正确的方法是 ( )
A. 海水 Mg(OH)2 Mg
B. 海水 MgCl2溶液 MgCl2熔融 Mg
C. 海水 Mg(OH)2 MgO Mg
D. 海水 Mg(OH)2 MgCl2溶液 MgCl2熔融 Mg
D
典型例题
NaOH
电解
HCl
石灰乳
灼烧
电解
电解
石灰乳
HCl
电解
[例 题] 从海水中提取食盐和溴的过程如下
(1)请列举海水淡化的三种方法___________________________________
(2)母液在进行第Ⅰ步氯气氧化前需 ,为了______________________
(3)步骤Ⅱ中将Br2还原为Br-,其目的为_______________
(4)步骤Ⅱ反应的离子方程式为 _______________________________由此反应
可知,除环境保护外,工业生产中应解决的主要问题___________________
蒸馏法、 电渗析法、 离子交换法
强酸对设备的严重腐蚀
富集溴元素
酸化
Br2+SO2+H2O = 4H++SO42-+2Br-
抑制氯气和溴单质与水反应
淡水
①通入适
量氯气
②蒸馏
①通入空
气吹出Br2
②用SO2水
溶液吸收
海水
淡化
NaCl
母液
Cl2
低浓
度Br2溶液
含HBr等物质的溶液
工业溴
Ⅰ
Ⅱ
Ⅲ
[例 题]下列做法不符合绿色化学理念的是( )
A.推广使用秸秆发酵制沼气的技术
B.推广使用新能源公交车
C.发展太阳能、风能等新能源
D.焚烧废弃塑料
典型例题
D
[例 题] 下列说法正确的是( )
A. 为了使火腿肠颜色更鲜艳,可多加一些亚硝酸钠
B. 为了使婴幼儿对食品有兴趣,可以在食品中多加一些着色剂
C. 药物可以治疗疾病,所有的药物都可以自行购买
D. 在规定范围内规范使用食品添加剂,对人体健康不会产生不良影响
D
[解析]使用食品添加剂应当符合相应质量标准,而不是越多越好,在规定范
围内使用,不会产生不良影响。处方药需要凭医生的处方才能从药房
或药店获得。
典型例题
[例 题]分类(填序号)
① 谷氨酸钠 ② 葡萄糖酸-δ-内酯 ③ 乳酸钙 ④ 氢氧化铝 ⑤ 亚硝酸钠
⑥ 山梨酸钾 ⑦ 小苏打 ⑧ β-胡萝卜素 ⑨ 硫酸亚铁 ⑩ 碘酸钾
(1)着色剂________;(2)增味剂________;
(3)膨松剂________;(4)凝固剂________;
(5)防腐剂________;(6)营养强化剂________ ;
(7)用于胃溃疡患者治疗胃酸的药物________。
⑧
①
典型例题
⑦
⑤⑥
②
③⑨⑩
④
第八章 专题复习
高一年级 化学
环节二
化学品的合理使用
自然资源的开发利用
环境保护与绿色化学
化学与可持续发展
专题一、自然资源的开发利用
金属矿物
海水
化石燃料
……
化学变化
获得能量
获得有用的
物质
金属冶炼
自然资源的开发利用
1. 金属冶炼原理:
金属矿物的开发利用
被还原
金属化合物
金属单质
2. 冶炼方法:
K Ca Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
电解法
热还原法
热分解法
富集法
例如:
热分解法:汞:2HgO 2Hg+O2 ↑
银:2Ag2O 4Ag+O2 ↑
热还原法:铜:2CuO+C 2Cu+CO2 ↑
铁:2Fe2O3+3CO 4Fe+3CO2 Fe2O3+2Al Al2O3+2Fe (铝热反应)
电解法: 铝:2Al2O3(熔融) 4Al+3O2↑ (不能用AlCl3,AlCl3不是离子化合物)
镁:MgCl2(熔融) Mg+Cl2↑
钠:2NaCl (熔融) 2Na+Cl2 ↑
Δ
Δ
高温
高温
高温
电解
电解
电解
金属矿物的开发利用
金属矿物
海水
化石燃料
……
化学变化
获得能量
获得有用的
物质
金属冶炼
从海水中提取有用的物质
自然资源的开发利用
海水资源的开发利用
纯碱
碘
②
③
淡水
氢气
烧碱
钠
氯气
钾盐
溴化物
钾
溴
海带
镁盐
镁
食盐
①
火电厂、核电厂循环冷却水
海水
水资源的利用
化学资源的利用
海水淡化:
蒸馏法、电渗析法、离子交换法
②
食盐
钠
电解
③
食盐
纯碱
利用物质间溶解度的差异
侯氏制碱法
2NaCl(熔融) 2Na+Cl2 ↑
电解
海水资源的开发利用
【侯氏制碱法流程图】
NaCl+CO2+NH3+H2O = NaHCO3(沉淀)+NH4Cl
【涉及反应】
【考察点】
先通入氨气再通入二氧化碳
饱和食盐水
过量
NH3
氨饱和食盐水
过量
CO2
过滤
滤渣
NaHCO3
Na2CO3
煅烧
CO2
滤液
NH4Cl
饱和食盐水
NH4Cl
NaCl、NH3
过滤
2NaHCO3 Na2CO3 + H2O + CO2↑
Δ
纯碱
②
③
淡水
氢气
烧碱
钠
氯气
钾盐
溴化物
钾
溴
食盐
①
火电厂、核电厂循环冷却水
海水
水资源的利用
化学资源的利用
④
海水资源的开发利用
空气吹出法提溴
④
【涉及反应】
Cl2+2Br- = Br2+2Cl-
Br2+SO2+2H2O = 4H++SO42-+2Br-
②
④
【考察点】
1. 步骤①中用硫酸酸化可提高Cl2的利用率,酸化可抑制氯气、溴单质与水反应
2. 氧化后的海水虽然含有溴单质,但浓度低,如果直度接蒸馏,耗时耗能,产
品成本高。 经过③ ④ ⑤,实现Br2的富集。
海
水
提取
粗盐
苦
卤
硫酸酸化
溴蒸汽
含Br2的
空气
含Br2
的
海水
溴水
混合
物
吸收液
①
氯气氧化
②
空气吹出
③
SO2吸收
④
氯气氧化
⑤
蒸馏
⑥
冷凝
⑦
⑧
分离
液溴
纯碱
碘
②
③
淡水
氢气
烧碱
钠
氯气
钾盐
溴化物
钾
溴
海带
食盐
①
火电厂、核电厂循环冷却水
海水
水资源的利用
化学资源的利用
④
⑤
海水资源的开发利用
【涉及反应】
Cl2+2I- = I2+2Cl-
1. 灼烧海带需要用到的仪器有:坩埚、坩埚钳、泥三角、三脚架、酒精灯。
2. 氧化剂除可用氯气,还可以选择H2O2、酸性高锰酸钾溶液、新制氯水等,
这些氧化剂与I-发生氧化还原反应的离子方程式的配平需要熟练掌握。
3. 萃取剂的选择原则:ⅰ不与原溶液反应; ⅱ与原溶剂不互溶; ⅲ溶质
在萃取剂中的溶解度大于在原溶剂中的溶解度。
⑤ 海带提碘
【考察点】
海
带
灼烧
海带灰
浸泡
单质碘
含I-
的溶液
海带灰悬浊液
含I2的有机溶液
含I2
的溶液
过滤
适量氯气
萃取
蒸馏
氧化
纯碱
碘
②
③
淡水
氢气
烧碱
钠
氯气
钾盐
溴化物
钾
溴
海带
镁盐
镁
食盐
①
火电厂、核电厂循环冷却水
海水
水资源的利用
化学资源的利用
⑥
④
⑤
海水资源的开发利用
海水
提取
粗盐
苦卤
高温
煅烧
MgCl2
溶液
Mg(OH)2
Mg
无水MgCl2
盐酸
③
④
电解
贝壳CaCO3
【涉及反应】
Mg2++Ca(OH)2 = Mg(OH)2 +Ca2+
Mg(OH)2+2H+ = Mg2++2H2O
②
③
⑥ 海水制镁
一定
条件
CaO
H2O
石灰乳
①
②
⑤
MgCl2(熔融) Mg+Cl2↑
①
CaCO3 CaO+CO2↑
电解
高温
金属矿物
海水
化石燃料
……
化学变化
获得能量
获得有用的
物质
金属冶炼
从海水中提取有用的物质
……
化石燃料的综合利用
煤的
综合利用
天然气化工
自然资源的开发利用
石油炼制
化学变化
物理变化
化石燃料的综合利用
化石燃料 煤 石油 天然气
主要成分 有机物和少量无机物组成的复杂混合物,组成以碳元素为主 多种碳氢化合物组成的混合物,成分复杂 主要成分是甲烷,天然气的水合物又称为可燃冰
综合利用 煤的 干馏 煤的气化 煤的液化 分馏 裂化 裂解 催化重整
天然气化工
化学变化
变化过程 原理 产物
煤 干馏 使煤隔绝空气加强热,使其分解的过程 出炉煤气、煤焦油、焦炭
气化 把煤中的有机物转化为可燃性气体 氢气、一氧化碳等
液化 把煤转化为液体燃料的过程 液体燃料如甲醇、汽油等
石 油 分馏 利用石油中各组分沸点的不同进行分离 汽油、煤油、柴油、重油等
裂化 将大分子的重油断裂为小分子的轻质油 轻质油
裂解 深度的裂化 乙烯、丙烯、甲烷等气态烃
催化重整 石油中链状烃重新调整结构转化为环状烃 苯或甲苯等
化石燃料的综合利用
[例 题]工业上冶炼下列金属的化学反应原理不正确的是( )
A. 2NaCl (熔融) 2Na+Cl2 ↑
B. 2MgO 2Mg+O2 ↑
C. Fe2O3+3CO 2Fe+3CO2
D. 2HgO 2Hg+O2 ↑
B
电解
典型例题
高温
△
△
[例 题]在冶金工业上,均不能用常用还原剂制得的是 ( )
A. Na、Mg、Al、K B. Na、K、Fe、Zn
C. Zn、Fe、Cu、Ag D. Mg、Al、Zn、Fe
典型例题
A
[例 题] 下列变化不属于化学变化的是( )
① 煤的干馏 ② 煤的液化 ③ 煤的汽化 ④ 石油的分馏
⑤ 石油的催化裂化 ⑥ 石油的裂解 ⑦ 煤的开采 ⑧ 海水蒸馏
A. ①②③④⑧ B. ②④⑥⑤⑦ C. ④⑦⑧ D. ⑥⑧
典型例题
C
[解析]裂化汽油中含有不饱和烃,而直馏汽油是由石油直接分馏得到
的汽油不含不饱和烃,所以可选用直馏汽油萃取溴。故选 A。
[例 题]下列物质中能用于萃取溴水中溴的是 ( )
A. 直馏汽油 B. 裂化汽油
C. 酒精 D. 水
A
典型例题
[例 题] 石灰石是一种化工原料,如图,下列说法正确的是( )
A. 漂粉精是混合物,主要成分是氯化钙
B. 图示的制纯碱方法,要求先向饱和食盐水中通 NH3,然后再通 CO2
C. 纯碱属于碱,俗名苏打
D. 制取纯碱和漂粉精所涉及的反应都是非氧化还原反应
B
[解析] 2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O 漂粉精主要成分是次氯酸钙,
该反应属于氧化还原反应;纯碱碳酸钠属于盐类。故选 B。
石灰石
高温
CO2
NaHCO3
NaCl NH3
H2O
H2O
纯碱
漂粉精
Cl2
△
CaO
Ca(OH)2
[例 题] 从海带中提取碘的实验过程如下图所示
(1) 步骤①灼烧海带时会用到下列仪器中的( )
A. 烧杯 B. 坩埚 C. 表面皿 D. 泥三角 E. 酒精灯 F. 三脚架
(2) 步骤③和⑤的操作名称是 、 _
(3) 步骤④反应的离子方程式是____________________________
(4) 请设计实验,检验水溶液中是否含有碘单质_______________________
___________________________________________________
过滤
B D E F
萃取
2I-+2H++H2O2 = I2 +2H2O
加入几滴淀粉溶液,如果出现蓝色,则说明含有碘单质
取少量水溶液于试管中,
海带
①灼烧
海带灰
②浸泡
海带灰悬浊液
③
含I-溶液
④H2O2、稀硫酸
含I2溶液
⑤提取碘
I2的CCl4溶液
⑥
单质I2
专题二、化学品的合理使用
化学品的合理使用
合理用药
安全使用食品添加剂
农药
化肥
化肥、农药的合理施用
化学品的合理使用
土壤酸碱性、作物营养状况、化肥本身的性质
水体富营养化、影响土壤酸碱性、作物残留超标等
高效、低毒、低残留
化肥农药合理施用
新型农药的发展方向
合理施用化肥考虑因素
滥用化肥和农药的危害
化学品的合理使用
滥用药物危害严重
安全、有效、经济、适当等
合理用药
重要性
药物分类
原则
天然药物
合成药物
处方药
非处方药 OTC
化学品的合理使用
天然的和人工合成的
按照GB 2760-2014《食品安全国家标准 食品添加剂使用标准》的规定使用
食品添加剂
分类
定义
相关使用原则和规定
为改善食品品质和色、香、味,以及防腐、保鲜和加工工艺的需要而加入食品中的人工合成或天然的物质
化学品的合理使用
名称 主要作用 常用物质 代表物结构或成分
着色剂 改善食 品颜色 红曲红、β-胡萝卜素、姜黄、柠檬黄、靛蓝
增味剂 增加食品的鲜味 味精(谷氨酸钠)
膨松剂 使面团疏松、多孔 单一膨松剂、 复合膨松剂 NaHCO3 NH4HCO3
凝固剂 改善食 品形态 盐卤、 葡萄糖酸-δ-内酯 MgCl2 CaSO4
柠檬黄
常见食品添加剂
防腐剂 防止食品 腐败变质 苯甲酸、苯甲酸钠、亚硝酸钠、山梨酸、山梨酸钾
山梨酸钾
抗氧 化剂 防止食品被氧化变质 抗坏血酸(VC) VC
营养 强化剂 补充必要的营养成分 维生素、碳酸钙、硫酸亚铁、硫酸锌、碘酸钾 VB、VD、CaCO3、FeSO4、ZnSO4、KIO3
常见食品添加剂
典型例题
[例 题] 下列对化肥、农药的说法正确的是( )
A. 农药本身有毒,应该禁止施用农药
B. 化肥可以使农作物增产,应尽可能大量施用化肥
C. 硝酸铵(NH4NO3)可直接作化肥使用
D. 为了减少污染应根据作物、虫害和农药的特点合理施用农药
D
[例 题] 下列说法正确的是( )
A. 为了使火腿肠颜色更鲜艳,可多加一些亚硝酸钠
B. 碳酸氢钠类药物可以用于治疗胃溃疡患者胃酸过多
C. 药物可以治疗疾病,所有的药物都可以自行购买
D. 在规定范围内规范使用食品添加剂,对人体健康不会产生不良影响
D
[解析]使用食品添加剂应当符合相应质量标准,而不是越多越好。碳酸氢钠
与胃酸作用生成大量二氧化碳使胃内压强增大,胃溃疡患者易形成胃
穿孔。处方药需要凭医生的 处方才能从药房或药店获得。
典型例题
专题三、环境保护与绿色化学
工业三废
固体废物的处理应遵循无害化、减量化、资源化的原则,
达到减少环境污染和资源回收利用这两个重要目的。
废气
常用的污水处理方法包括物理法、化学法和生物法,
污水处理常用的化学方法有 、 、 等。
化石燃料的燃烧
工业生产过程产生的废气
工业废气携带的颗粒物
氧化还原法
废水
废渣
一定条件下
次生污染物
【雾霾、光化学烟雾、
酸雨(pH<5.6)等】
中和法
沉淀法
工业三废
利用化学原理和技术手段,减少或消除产品和应用中涉及
的有害化学物质, 。
绿色化学
绿色化学
常见原子利用率100%的反应有 、 、 。
核心
反应物原子全部转化为期望的最终产物,原子利用率100%。
原子经济性反应
加聚反应
从源头减少或消除污染
加成反应
化合反应
环境问题 主要污染物 主要危害
温室效应 主要是CO2,此外还包括甲烷等气体 全球气候变暖,破坏生态环境
酸雨 SO2、NOx 土壤酸化、水源污染、建筑物腐蚀
光化学烟雾 NOx、碳氢化合物 破坏人体呼吸系统,严重可导致死亡
臭氧层空洞 氟氯代烷、NOx 到达地面紫外线增多,危害环境和健康
赤潮和水华 含氮磷元素的营 养物质排入水体 水体富营养化,水中藻类疯长,
使水体浑浊、水质恶化
白色污染 废弃塑料制品 难降解、难回收,对土壤有极大危害
PM2.5 颗粒物 污染空气、形成雾霾,危害健康
常见环境污染问题
[例 题] 下列说法不正确的是( )
A. 重金属、农药和难降解的有机物等会造成水体污染
B. 装修材料中的甲醛、芳香烃及氡等会造成居室污染
C. 水体污染会造成地方性甲状腺肿
D. 推广垃圾分类存放、分类回收、分类处理
C
[解析] 地方性甲状腺肿是由于缺碘造成的,故选C。
典型例题
[例 题]下列有关环境问题的说法正确的是 ( )
A. 燃煤时加入适量石灰石可减少废气中 SO2 的含量
B. 臭氧体积分数超过 10-4 % 的空气有利于人体健康
C. pH 在 5. 6 ~7. 0 之间的降水通常称为酸雨
D. 制备CuSO4采用:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O 符合绿色化学理念
A
[解析] 按照绿色化学的理念,制备硫酸铜,应采用 2Cu+O2 2CuO;
CuO+H2SO4 = CuSO4+H2O。
△
典型例题
△
课后作业
运用所学知识设计实验,检验市售加碘食盐中的碘酸钾。
提示:(1) 5I- +IO3- +6H+ = 3I2+3H2O
(2) 5SO32- +2IO3- + 2H+ = 5SO42-+ I2 +H2O
(3) 碘单质与淀粉作用显蓝色
(4) 市售碘盐中的碘元素以可溶性盐的形式存在
完成教材P124 复习与提高的第1、7、8、9题
拓展题
必做题
环节二
化学品的合理使用
自然资源的开发利用
环境保护与绿色化学
化学与可持续发展
同学们,再见!
[例 题]已知MgO、MgCl2的熔点分别为2800℃、604℃,将MgO、MgCl2加热
熔融后通电电解,都可得到金属镁。海水中含有MgCl2,工业上从海水
中提取镁,正确的方法是 ( )
A. 海水 Mg(OH)2 Mg
B. 海水 MgCl2溶液 MgCl2熔融 Mg
C. 海水 Mg(OH)2 MgO Mg
D. 海水 Mg(OH)2 MgCl2溶液 MgCl2熔融 Mg
D
典型例题
NaOH
电解
HCl
石灰乳
灼烧
电解
电解
石灰乳
HCl
电解
[例 题] 从海水中提取食盐和溴的过程如下
(1)请列举海水淡化的三种方法___________________________________
(2)母液在进行第Ⅰ步氯气氧化前需 ,为了______________________
(3)步骤Ⅱ中将Br2还原为Br-,其目的为_______________
(4)步骤Ⅱ反应的离子方程式为 _______________________________由此反应
可知,除环境保护外,工业生产中应解决的主要问题___________________
蒸馏法、 电渗析法、 离子交换法
强酸对设备的严重腐蚀
富集溴元素
酸化
Br2+SO2+H2O = 4H++SO42-+2Br-
抑制氯气和溴单质与水反应
淡水
①通入适
量氯气
②蒸馏
①通入空
气吹出Br2
②用SO2水
溶液吸收
海水
淡化
NaCl
母液
Cl2
低浓
度Br2溶液
含HBr等物质的溶液
工业溴
Ⅰ
Ⅱ
Ⅲ
[例 题]下列做法不符合绿色化学理念的是( )
A.推广使用秸秆发酵制沼气的技术
B.推广使用新能源公交车
C.发展太阳能、风能等新能源
D.焚烧废弃塑料
典型例题
D
[例 题] 下列说法正确的是( )
A. 为了使火腿肠颜色更鲜艳,可多加一些亚硝酸钠
B. 为了使婴幼儿对食品有兴趣,可以在食品中多加一些着色剂
C. 药物可以治疗疾病,所有的药物都可以自行购买
D. 在规定范围内规范使用食品添加剂,对人体健康不会产生不良影响
D
[解析]使用食品添加剂应当符合相应质量标准,而不是越多越好,在规定范
围内使用,不会产生不良影响。处方药需要凭医生的处方才能从药房
或药店获得。
典型例题
[例 题]分类(填序号)
① 谷氨酸钠 ② 葡萄糖酸-δ-内酯 ③ 乳酸钙 ④ 氢氧化铝 ⑤ 亚硝酸钠
⑥ 山梨酸钾 ⑦ 小苏打 ⑧ β-胡萝卜素 ⑨ 硫酸亚铁 ⑩ 碘酸钾
(1)着色剂________;(2)增味剂________;
(3)膨松剂________;(4)凝固剂________;
(5)防腐剂________;(6)营养强化剂________ ;
(7)用于胃溃疡患者治疗胃酸的药物________。
⑧
①
典型例题
⑦
⑤⑥
②
③⑨⑩
④
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
