8.1《自然资源的开发利用》(第1课时)课件(共28张PPT)
文档属性
| 名称 | 8.1《自然资源的开发利用》(第1课时)课件(共28张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-22 00:00:00 | ||
图片预览







文档简介
(共28张PPT)
第八章
化学与可持续发展
第一节
选择性必修一
1st
自然资源的开发利用 第一课时
第八章 化学与可持续发展
学习目标
认识金属矿物的开发和利用
2. 认识海水资源的开发和利用
导入
我们的身边离不开自然资源,无论是汽车、飞机、轮船还是我们身上的衣服、鞋子、帽子,以及我们的食物,都是从自然界中得到的,那么这些资源都是怎么进入我们的生活的,我们就简单的来了解一下吧。
一、金属矿物的开发利用
1、金属元素的存在
绝大多数金属以化合物的形式存在于自然界。 少数不活泼金属(如金和铂)以游离态存在。 在地壳中,含量最高的金属元素是铝,其次是铁。
把金属从矿石中提炼出来,这个过程就叫金属的冶炼。
铝矿
铁矿
金矿石
朱砂
一、金属矿物的开发利用
用还原的方法使金属化合物中金属离子得到电子变成金属原子
氧化还原反应
2、金属冶炼原理
(化合态)M n+
得电子
M(游离态)
(被还原)
( 1 )冶炼金属的原理:
( 2 )冶炼金属的实质:
金属活动顺序与金属冶炼
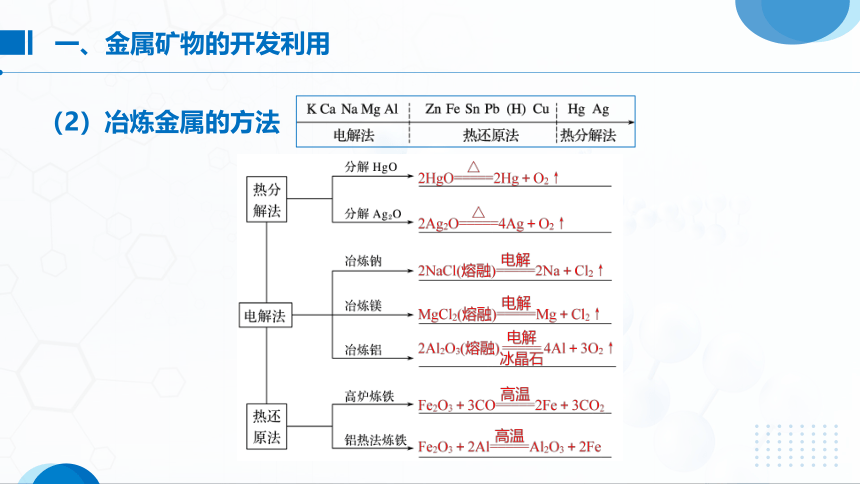
金属的活动顺序 K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属原子失电子能力 强 → 弱 金属离子得电子能力 弱 → 强 主要冶炼方法 电解法 热还原法 热分解法
(1)步骤
一、金属矿物的开发利用
2、金属冶炼过程
①矿石的富集
②冶炼
③精炼
一、金属矿物的开发利用
(2)冶炼金属的方法
一、金属矿物的开发利用
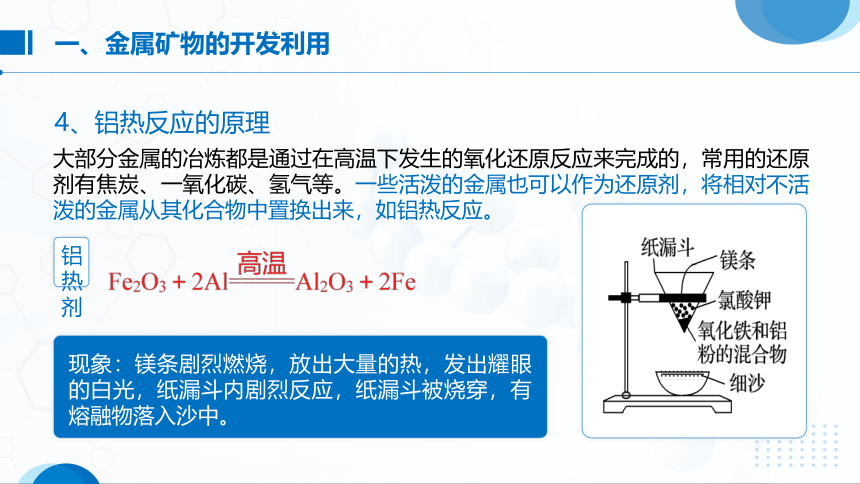
4、铝热反应的原理
大部分金属的冶炼都是通过在高温下发生的氧化还原反应来完成的,常用的还原剂有焦炭、一氧化碳、氢气等。一些活泼的金属也可以作为还原剂,将相对不活泼的金属从其化合物中置换出来,如铝热反应。
现象:镁条剧烈燃烧,放出大量的热,发出耀眼的白光,纸漏斗内剧烈反应,纸漏斗被烧穿,有熔融物落入沙中。
铝
热
剂
一、金属矿物的开发利用
【思考与交流】
(1)铝热反应需要高温条件,是否还需要持续加热?
铝热反应为放热反应,放出的热可以维持反应继续进行,因此不需要持续加热。
(2)实验中,镁条、氯酸钾的作用是什么?
引发反应的操作是什么?
镁条是引燃剂,氯酸钾为助燃剂,点燃镁条,促使氯酸钾分解,释放出氧气,使镁条更剧烈燃烧,单位时间内放出更多热量,从而引发Al和Fe2O3发生反应。
(3)蒸发皿中铺少量细沙的作用是什么?
一是防止蒸发皿炸裂,二是防止生成的熔融物溅出。
一、金属矿物的开发利用
铝热反应的原理可以应用在生产上,如用于焊接钢轨等。在冶金工业上也常用这一反应原理,使铝与金属氧化物反应,冶炼钒、铬、锰等等高熔点金属。
大多数金属矿石里含有杂质,如石英、石灰等,因此在冶炼金属时首先需要富集矿石。
在富集好的矿石中利用不同方法将金属还原出来,最后进行提纯。
一、金属矿物的开发利用
5、炼钢炼铁
黄铜矿
菱铁矿
铜铅锌矿
一、金属矿物的开发利用
热还原法
Fe2O3+3CO == 2Fe+3CO2
炼铁炉剖面图
出渣口
热风口
环炉热风管
热风管
炉体支架
耐火砖层
炉身外壳
大料钟
大料斗
炉煤气管
小料钟
小料斗
炼铁炉
炉缸
炉腹
炉腰
炉身
炉喉
~200°C
~500°C
~800°C
~1400°C
~1800°C
900~1000°C
出铁口
料钟调控阀
一、金属矿物的开发利用
炼铁的高炉(反应原理)
在金属活动性顺序中,钾、钠、钙等几种金属的还原性很强,这些金属都很容易失去电子,因此不能用一般的方法和还原剂使其从化合物中还原出来,只能用通电分解其熔融盐或氧化物的方法来冶炼。
一、金属矿物的开发利用
电解法
①提高金属矿物利用率 ③防止金属腐蚀
②开发环保高效金属冶炼方法 ④加强金属回收再利用
(1)合理开发利用金属资源
①节约矿物资源 ②节约能源 ③减少环境污染
(2)金属的回收和资源保护
回收金属的实例
①废旧钢铁用于炼钢 ②废铁屑用于制铁盐 ③定影液用于回收银
一、金属矿物的开发利用
7、合理开发利用金属资源
一、金属矿物的开发利用
【思考与讨论】
计算表明,生产1mol铝消耗的电能至少为1.8x106J,回收铝质饮料罐得到铝与从铝土矿制铝相比,前者的能耗仅为后者的3%-5%。通过对上述数据的分析和比较,结合图8-1和图8-2,你想到了什么?请将你的想法与同学交流。
积极开展废弃金属的回收利用,是实现我国金属工业持续发展的重要途径,不仅可以在相当程度上解决国内金属矿山原料不足的问题,而且有助于保护自然资源,减少金属生产和消费过程中对生态环境的影响和破坏。可以大大缓解社会和经济发展对矿产资源不断增长的需求,明显降低金属生产过程中的煤炭,电力等能源消耗,减少环境污染,实现有金属工业的可持续发展,创造节约性社会。
二、海水资源的开发利用
约占地球表面积的71%
水的储量约为1.3×109亿吨,约占地球总水量的97%
含有很多种常量元素和微量元素。
1、海水资源的广阔性
与岩石、大气和生物的相互作用,
溶解和悬浮着大量的无机物和有机物,
H、O两种元素,加上Cl、Na、K、Mg、Ca、S、C、F、B、Br、Sr等11种元素超过总量的99%,
其他为微量元素,总计含有80多种元素。
2、海水资源的多样性
二、海水资源的开发利用
元素种类很多,总储量很大,
元素的富集程度很低。
例如,海水中金元素的总储量约为5×107t,
而1t海水中的含量仅有4×10-6g。
3、海水资源的分散性
海水的淡化
直接利用海水的循环冷却
4、海水中水资源利用的项目
二、海水资源的开发利用
(1)途径
5、海水的淡化
①提取淡水 ②从海水中把盐分离
(2)海水淡化的方法及其特点
主要有蒸馏法、电渗析法、离子交换法等。
蒸馏法的历史最久,技术和工艺也比较完善,但成本较高。
二、海水资源的开发利用
6、海水的综合利用
氯气
纯碱
钠
氢气
烧碱
食盐
火电厂、核电厂的循环冷却水
镁盐
溴化物
钾盐
淡水
食盐
镁
溴
钾
二、海水资源的开发利用
【思考与讨论】海水提溴:
空气吹出法
海水
浓缩酸化
通入氯气
海水
Cl-、Br2
通入空气水蒸气(吹入)
通入SO2
反应后富集溴
HBr、
SO4
2-
Br2蒸汽
通入水蒸气和Cl2,蒸馏
冷凝器溴单质
反应离子方程式:
二、海水资源的开发利用
提溴步骤:
氧化;富集;提取
2Br-+ Cl2 = Br2 +2Cl-
2H2O +Br2 + SO2 = 4H++SO4 2- +2Br-
2Br-+Cl2= Br2+2Cl-
置换反应得到的 Br2 的浓度很低,难以收集,用空气吹出 Br2 后用 SO2 吸收,使溴得到富集。
二、海水资源的开发利用
(1)海水淡化同化工生产结合 (2)同能源技术结合
6、海水综合利用的重要方向
①从海水中制得的氯化钠除食用外,还用作工业原料,
②生产烧碱、纯碱、金属钠以及氯气、盐酸、漂白粉等含氯化工产品。
③从海水中制取镁、钾、溴及其化工产品,是在传统制盐工业上的发展。
④从海水中获得其他物质和能量具有广阔的前景。
铀和重水--核能开发中的重要原料,
从海水中提取铀和重水对一个国家来说具有战略意义。
⑤化学在开发海洋药物方面也将发挥越来越大的作用。
⑦潮汐能、波浪能等也是越来越受到重视和开发的新型能源。
【课堂练习】
1. 铝能用于冶炼难熔的金属(如Cr、V、Mn等),这不是因为( )
A. 铝具有还原性
B. 铝具有导电性
C. 铝较Cr、V、Mn等价格便宜
D. 冶炼反应放出大量的热
B
【课堂练习】
2.冶炼金属一般有下列四种方法:①焦炭法 ②水煤气(或氢气或一氧化碳)法 ③活泼金属置换法 ④电解法。四种方法在工业上均有应用。古代有(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜;现代有(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁,对它们的冶炼方法的分析不正确的是( )
A.(Ⅰ)用① B.(Ⅱ)用②
C.(Ⅲ)用③ D.(Ⅳ)用④
B
向奋斗在一线的老师致敬
课堂小结
感谢您的观看
选择性必修一
THS
第八章
化学与可持续发展
第一节
选择性必修一
1st
自然资源的开发利用 第一课时
第八章 化学与可持续发展
学习目标
认识金属矿物的开发和利用
2. 认识海水资源的开发和利用
导入
我们的身边离不开自然资源,无论是汽车、飞机、轮船还是我们身上的衣服、鞋子、帽子,以及我们的食物,都是从自然界中得到的,那么这些资源都是怎么进入我们的生活的,我们就简单的来了解一下吧。
一、金属矿物的开发利用
1、金属元素的存在
绝大多数金属以化合物的形式存在于自然界。 少数不活泼金属(如金和铂)以游离态存在。 在地壳中,含量最高的金属元素是铝,其次是铁。
把金属从矿石中提炼出来,这个过程就叫金属的冶炼。
铝矿
铁矿
金矿石
朱砂
一、金属矿物的开发利用
用还原的方法使金属化合物中金属离子得到电子变成金属原子
氧化还原反应
2、金属冶炼原理
(化合态)M n+
得电子
M(游离态)
(被还原)
( 1 )冶炼金属的原理:
( 2 )冶炼金属的实质:
金属活动顺序与金属冶炼
金属的活动顺序 K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属原子失电子能力 强 → 弱 金属离子得电子能力 弱 → 强 主要冶炼方法 电解法 热还原法 热分解法
(1)步骤
一、金属矿物的开发利用
2、金属冶炼过程
①矿石的富集
②冶炼
③精炼
一、金属矿物的开发利用
(2)冶炼金属的方法
一、金属矿物的开发利用
4、铝热反应的原理
大部分金属的冶炼都是通过在高温下发生的氧化还原反应来完成的,常用的还原剂有焦炭、一氧化碳、氢气等。一些活泼的金属也可以作为还原剂,将相对不活泼的金属从其化合物中置换出来,如铝热反应。
现象:镁条剧烈燃烧,放出大量的热,发出耀眼的白光,纸漏斗内剧烈反应,纸漏斗被烧穿,有熔融物落入沙中。
铝
热
剂
一、金属矿物的开发利用
【思考与交流】
(1)铝热反应需要高温条件,是否还需要持续加热?
铝热反应为放热反应,放出的热可以维持反应继续进行,因此不需要持续加热。
(2)实验中,镁条、氯酸钾的作用是什么?
引发反应的操作是什么?
镁条是引燃剂,氯酸钾为助燃剂,点燃镁条,促使氯酸钾分解,释放出氧气,使镁条更剧烈燃烧,单位时间内放出更多热量,从而引发Al和Fe2O3发生反应。
(3)蒸发皿中铺少量细沙的作用是什么?
一是防止蒸发皿炸裂,二是防止生成的熔融物溅出。
一、金属矿物的开发利用
铝热反应的原理可以应用在生产上,如用于焊接钢轨等。在冶金工业上也常用这一反应原理,使铝与金属氧化物反应,冶炼钒、铬、锰等等高熔点金属。
大多数金属矿石里含有杂质,如石英、石灰等,因此在冶炼金属时首先需要富集矿石。
在富集好的矿石中利用不同方法将金属还原出来,最后进行提纯。
一、金属矿物的开发利用
5、炼钢炼铁
黄铜矿
菱铁矿
铜铅锌矿
一、金属矿物的开发利用
热还原法
Fe2O3+3CO == 2Fe+3CO2
炼铁炉剖面图
出渣口
热风口
环炉热风管
热风管
炉体支架
耐火砖层
炉身外壳
大料钟
大料斗
炉煤气管
小料钟
小料斗
炼铁炉
炉缸
炉腹
炉腰
炉身
炉喉
~200°C
~500°C
~800°C
~1400°C
~1800°C
900~1000°C
出铁口
料钟调控阀
一、金属矿物的开发利用
炼铁的高炉(反应原理)
在金属活动性顺序中,钾、钠、钙等几种金属的还原性很强,这些金属都很容易失去电子,因此不能用一般的方法和还原剂使其从化合物中还原出来,只能用通电分解其熔融盐或氧化物的方法来冶炼。
一、金属矿物的开发利用
电解法
①提高金属矿物利用率 ③防止金属腐蚀
②开发环保高效金属冶炼方法 ④加强金属回收再利用
(1)合理开发利用金属资源
①节约矿物资源 ②节约能源 ③减少环境污染
(2)金属的回收和资源保护
回收金属的实例
①废旧钢铁用于炼钢 ②废铁屑用于制铁盐 ③定影液用于回收银
一、金属矿物的开发利用
7、合理开发利用金属资源
一、金属矿物的开发利用
【思考与讨论】
计算表明,生产1mol铝消耗的电能至少为1.8x106J,回收铝质饮料罐得到铝与从铝土矿制铝相比,前者的能耗仅为后者的3%-5%。通过对上述数据的分析和比较,结合图8-1和图8-2,你想到了什么?请将你的想法与同学交流。
积极开展废弃金属的回收利用,是实现我国金属工业持续发展的重要途径,不仅可以在相当程度上解决国内金属矿山原料不足的问题,而且有助于保护自然资源,减少金属生产和消费过程中对生态环境的影响和破坏。可以大大缓解社会和经济发展对矿产资源不断增长的需求,明显降低金属生产过程中的煤炭,电力等能源消耗,减少环境污染,实现有金属工业的可持续发展,创造节约性社会。
二、海水资源的开发利用
约占地球表面积的71%
水的储量约为1.3×109亿吨,约占地球总水量的97%
含有很多种常量元素和微量元素。
1、海水资源的广阔性
与岩石、大气和生物的相互作用,
溶解和悬浮着大量的无机物和有机物,
H、O两种元素,加上Cl、Na、K、Mg、Ca、S、C、F、B、Br、Sr等11种元素超过总量的99%,
其他为微量元素,总计含有80多种元素。
2、海水资源的多样性
二、海水资源的开发利用
元素种类很多,总储量很大,
元素的富集程度很低。
例如,海水中金元素的总储量约为5×107t,
而1t海水中的含量仅有4×10-6g。
3、海水资源的分散性
海水的淡化
直接利用海水的循环冷却
4、海水中水资源利用的项目
二、海水资源的开发利用
(1)途径
5、海水的淡化
①提取淡水 ②从海水中把盐分离
(2)海水淡化的方法及其特点
主要有蒸馏法、电渗析法、离子交换法等。
蒸馏法的历史最久,技术和工艺也比较完善,但成本较高。
二、海水资源的开发利用
6、海水的综合利用
氯气
纯碱
钠
氢气
烧碱
食盐
火电厂、核电厂的循环冷却水
镁盐
溴化物
钾盐
淡水
食盐
镁
溴
钾
二、海水资源的开发利用
【思考与讨论】海水提溴:
空气吹出法
海水
浓缩酸化
通入氯气
海水
Cl-、Br2
通入空气水蒸气(吹入)
通入SO2
反应后富集溴
HBr、
SO4
2-
Br2蒸汽
通入水蒸气和Cl2,蒸馏
冷凝器溴单质
反应离子方程式:
二、海水资源的开发利用
提溴步骤:
氧化;富集;提取
2Br-+ Cl2 = Br2 +2Cl-
2H2O +Br2 + SO2 = 4H++SO4 2- +2Br-
2Br-+Cl2= Br2+2Cl-
置换反应得到的 Br2 的浓度很低,难以收集,用空气吹出 Br2 后用 SO2 吸收,使溴得到富集。
二、海水资源的开发利用
(1)海水淡化同化工生产结合 (2)同能源技术结合
6、海水综合利用的重要方向
①从海水中制得的氯化钠除食用外,还用作工业原料,
②生产烧碱、纯碱、金属钠以及氯气、盐酸、漂白粉等含氯化工产品。
③从海水中制取镁、钾、溴及其化工产品,是在传统制盐工业上的发展。
④从海水中获得其他物质和能量具有广阔的前景。
铀和重水--核能开发中的重要原料,
从海水中提取铀和重水对一个国家来说具有战略意义。
⑤化学在开发海洋药物方面也将发挥越来越大的作用。
⑦潮汐能、波浪能等也是越来越受到重视和开发的新型能源。
【课堂练习】
1. 铝能用于冶炼难熔的金属(如Cr、V、Mn等),这不是因为( )
A. 铝具有还原性
B. 铝具有导电性
C. 铝较Cr、V、Mn等价格便宜
D. 冶炼反应放出大量的热
B
【课堂练习】
2.冶炼金属一般有下列四种方法:①焦炭法 ②水煤气(或氢气或一氧化碳)法 ③活泼金属置换法 ④电解法。四种方法在工业上均有应用。古代有(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜;现代有(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁,对它们的冶炼方法的分析不正确的是( )
A.(Ⅰ)用① B.(Ⅱ)用②
C.(Ⅲ)用③ D.(Ⅳ)用④
B
向奋斗在一线的老师致敬
课堂小结
感谢您的观看
选择性必修一
THS
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
