1.2研究有机化合物的一般方法——2022-2023学年高二化学人教版(2019)选择性必修3同步课时训练(含答案)
文档属性
| 名称 | 1.2研究有机化合物的一般方法——2022-2023学年高二化学人教版(2019)选择性必修3同步课时训练(含答案) | 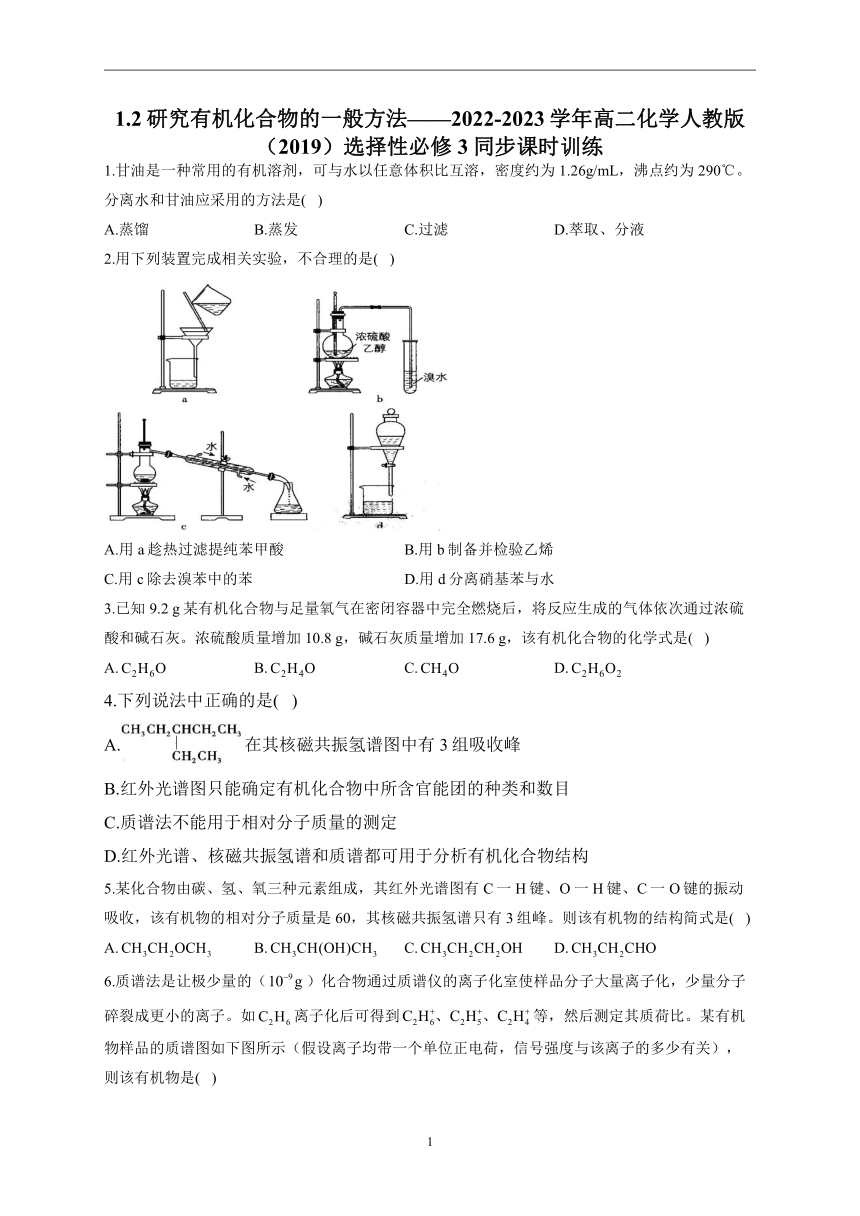 | |
| 格式 | docx | ||
| 文件大小 | 277.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-23 18:26:09 | ||
图片预览


文档简介
1.2研究有机化合物的一般方法——2022-2023学年高二化学人教版(2019)选择性必修3同步课时训练
1.甘油是一种常用的有机溶剂,可与水以任意体积比互溶,密度约为1.26g/mL,沸点约为290℃。分离水和甘油应采用的方法是( )
A.蒸馏 B.蒸发 C.过滤 D.萃取、分液
2.用下列装置完成相关实验,不合理的是( )
A.用a趁热过滤提纯苯甲酸 B.用b制备并检验乙烯
C.用c除去溴苯中的苯 D.用d分离硝基苯与水
3.已知9.2 g某有机化合物与足量氧气在密闭容器中完全燃烧后,将反应生成的气体依次通过浓硫酸和碱石灰。浓硫酸质量增加10.8 g,碱石灰质量增加17.6 g,该有机化合物的化学式是( )
A. B. C. D.
4.下列说法中正确的是( )
A.在其核磁共振氢谱图中有3组吸收峰
B.红外光谱图只能确定有机化合物中所含官能团的种类和数目
C.质谱法不能用于相对分子质量的测定
D.红外光谱、核磁共振氢谱和质谱都可用于分析有机化合物结构
5.某化合物由碳、氢、氧三种元素组成,其红外光谱图有C一H键、O一H键、C一O键的振动吸收,该有机物的相对分子质量是60,其核磁共振氢谱只有3组峰。则该有机物的结构简式是( )
A. B. C. D.
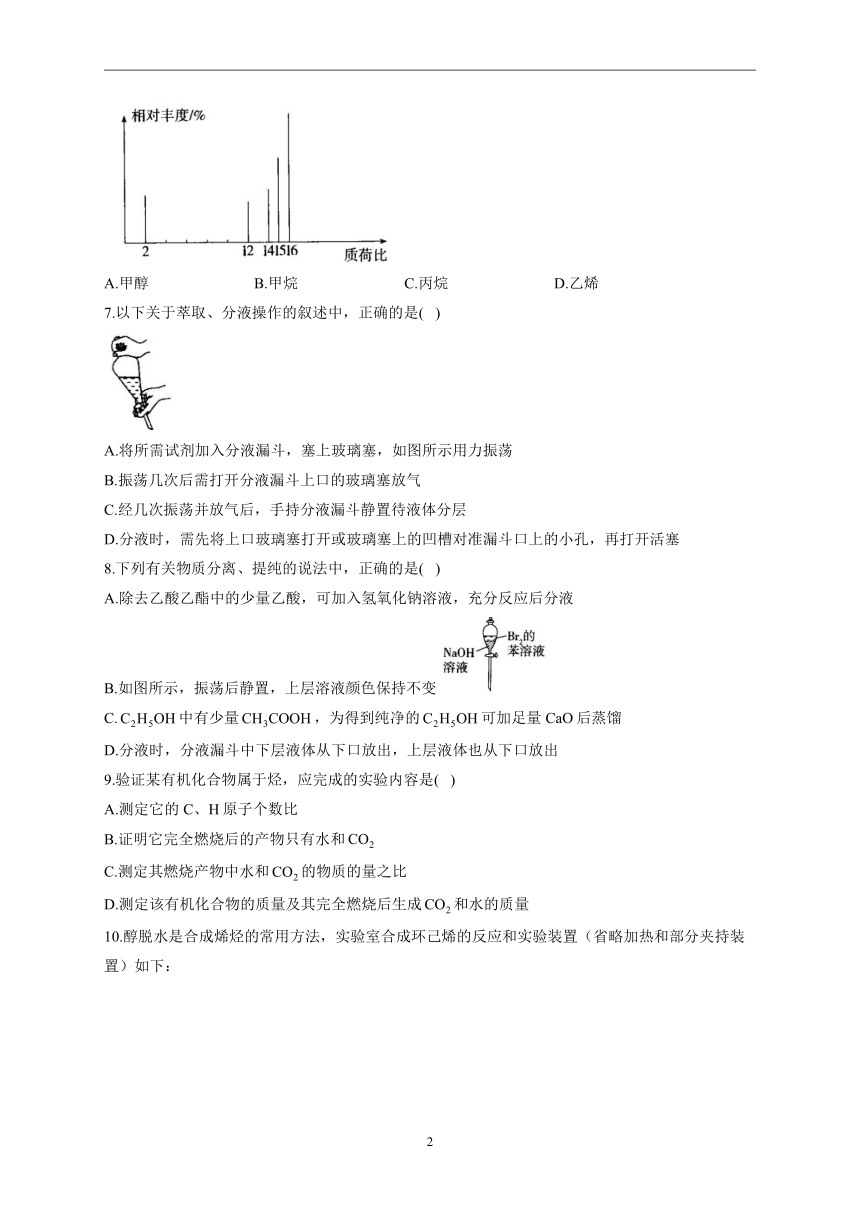
6.质谱法是让极少量的()化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如离子化后可得到等,然后测定其质荷比。某有机物样品的质谱图如下图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物是( )
A.甲醇 B.甲烷 C.丙烷 D.乙烯
7.以下关于萃取、分液操作的叙述中,正确的是( )
A.将所需试剂加入分液漏斗,塞上玻璃塞,如图所示用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开活塞
8.下列有关物质分离、提纯的说法中,正确的是( )
A.除去乙酸乙酯中的少量乙酸,可加入氢氧化钠溶液,充分反应后分液
B.如图所示,振荡后静置,上层溶液颜色保持不变
C.中有少量,为得到纯净的可加足量CaO后蒸馏
D.分液时,分液漏斗中下层液体从下口放出,上层液体也从下口放出
9.验证某有机化合物属于烃,应完成的实验内容是( )
A.测定它的C、H原子个数比
B.证明它完全燃烧后的产物只有水和
C.测定其燃烧产物中水和的物质的量之比
D.测定该有机化合物的质量及其完全燃烧后生成和水的质量
10.醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置(省略加热和部分夹持装置)如下:
可能用到的有关数据如下:
相对分子质量 沸点/℃ 密度/ 溶解性
环己醇 100 161 0.9618 微溶于水
环己烯 82 83 0.8102 难溶于水
合成反应:
在a中加入20g环己醇和少量碎瓷片,在搅动下慢慢加入1mL浓;b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离、提纯:
反应得到的粗产物倒入分液漏斗中,分别用少量5%的碳酸钠溶液和蒸馏水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到10g纯净环己烯。
回答下列问题:
(1)装置b的名称是_______。
(2)加入碎瓷片的作用是_______;如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是_______(填字母)。
A.立即补加
B.冷却后补加
C.继续加热
D.重新配料
(3)分液漏斗在使用前须清洗干净并_______,在本实验分离过程中,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(4)分离、提纯过程中加入无水氯化钙的目的是_______。
11.两种有机化合物A和B可以互溶,有关性质如下:
相对密度(20℃ ) 熔点 沸点 溶解性
A 0.7893 -117.3°C 78.5°C 与水以任意比混溶
B 0.7137 -116.6°C 34.5°C 不溶于水
(1)若要除去A和B的混合物中少量的B,采用______(填序号)方法即可得到A。
a.重结晶 b.蒸馏 c.萃取 d.加水充分振荡,分液
(2)将有机化合物A置于氧气流中充分燃烧,实验测得:生成5.4 g和8.8 g ,消耗氧气6.72 L(标准状况下),则该物质的最简式为________,若要确定其分子式,_____________(填“是”或“否”)需有其他条件。已知有机化合物A的核磁共振氢谱、质谱如图所示,则A的结构简式为________。
(3)若质谱图显示B的相对分子质量为74,红外光谱如图所示,则B的结构简式为________,其官能团的名称为_______。
(4)准确称取一定质量的A和B的混合物,在足量氧气中充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增重19.8 g和35.2 g。计算混合物中A和B的物质的量之比为______。
答案以及解析
1.答案:A
解析:甘油和水以任意体积比互溶,不能用过滤、蒸发、萃取、分液的方法分离,二者沸点相差较大,可用蒸馏的方法分离。
2.答案:B
解析:用a趁热过滤提纯苯甲酸,图示过滤装置满足“一贴、二低、三靠”的要求,且用玻璃棒引流,合理,故A不符合题意;利用乙醇在浓硫酸、加热的条件下制取的乙烯中会混有等杂质,能与溴水反应而使其褪色,对乙烯的检验产生干扰,且b中没有收集、除杂装置,导管直接插入溴水中会产生倒吸,不合理,故B符合题意;溴苯与苯的沸点相差较大,可以通过蒸馏将两者分离,且c中温度计的水银球放在蒸馏烧瓶的支管口处,冷凝水下口进、上口出,合理,故C不符合题意;硝基苯不溶于水,且密度比水大,因此可通过分液的方法将硝基苯与水分离开,硝基苯从下端放出,合理,故D不符合题意。
3.答案:A
解析:将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增加的10.8 g为生成水的质量,碱石灰增加的17.6 g为生成二氧化碳的质量。生成水的物质的量为,氢原子的物质的量为0.6 mol×2=1.2 mol;生成二氧化碳的物质的量为,碳原子的物质的量为0.4 mol;9.2 g该有机化合物分子中含有氧原子的物质的量为。1 mol该有机化合物分子中含有C、H、O原子的物质的量之比为0.4 mol:1.2 mol:0.2 mol=2:6:1,该有机化合物的最简式为,由于氢原子已经饱和,故该有机化合物分子式为, A正确。
4.答案:AD
解析:在其核磁共振氢谱图中有3组吸收峰,故A正确;红外光谱图只能确定有机化合物中所含官能团的种类,无法确定其数目,故B错误;通过质谱法可以测定有机化合物的相对分子质量,故C错误;红外光谱仪用于测定有机化合物的化学键、官能团种类,核磁共振仪可测定有机化合物分子中氢原子的种类,质谱仪用于测定有机化合物的相对分子质量,所以红外光谱、核磁共振氢谱、质谱都可用于分析有机化合物结构,故D正确。
5.答案:B
解析:相对分子质量为60,但分子中不含O一H键,有3种氢原子,A错误;相对分子质量为60,分子中含有C一H键、O一H键、C一O键,只有3种氢原子,B正确;相对分子质量为60,含有C一H键、O一H键、C一O键,有4种氢原子,C错误;相对分子质量为58,不含O一H键、C一O键,有3种氢原子,D错误。
6.答案:B
解析:由有机物样品的质谱图可知,该有机物微粒质荷比最大值为16,则该有机物的相对分子质量为16,甲醇、甲烷、丙烷、乙烯的相对分子质量分别为32、16、44、28,则该有机物为甲烷。
7.答案:D
解析:一只手压住玻璃塞,一只手握住活塞,把分液漏斗倒转过来振荡,A错误;振荡几次后打开活塞放气,不需打开分液漏斗上口的玻璃塞放气,B错误;将分液漏斗放在铁架台上静置待液体分层,C错误;分液时将分液漏斗上的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔,再打开活塞,待下层液体流尽时,关闭活塞,从上口倒出上层液体,D正确。
8.答案:C
解析:乙酸乙酯在氢氧化钠溶液中能水解,故A错;与NaOH溶液反应,上层溶液颜色会变浅或变为无色,故B错;乙酸与氧化钙反应生成高沸点的盐,乙醇不能与CaO反应,然后蒸馏得到乙醇,故C正确;分液时下层液体从下口放出,上层液体从上口倒出,故D错。
9.答案:D
解析:烃只含C、H两种元素。只测定它的C、H原子个数比,不能确定是否含有O原子,不能验证该有机化合物属于烃,故A错误;烃和烃的含氧衍生物的燃烧产物都是,则只证明该有机化合物完全燃烧后产物只有,不能验证该有机化合物属于烃,故B错误;只测定其燃烧产物中的物质的量之比,只能测出它的C、H原子个数比,不能确定是否含有O原子,不能验证该有机化合物属于烃,故C错误;测定该有机化合物的质量及其完全燃烧后生成的质量,若有机化合物的质量与中C、H元素的质量之和相等,则能验证该有杋化合物属于烃,故D正确。
10.答案:(1)直形冷凝管
(2)防止暴沸;B
(3)检漏;上口倒出
(4)干燥环已烯
解析:(1)由题图可知装置b的名称是直形冷凝管。
(2)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加碎瓷片,应冷却后补加。
(3)分液漏斗在使用前应清洗干净并检查是否漏水。产物中环己烯难溶于水且密度比水的小,静置后在上层,无机相在下层,下层液体从下口放出,上层液体从上口倒出。
(4)加入无水氯化钙的目的是干燥环己烯。
11.答案:(1)b
(2);否;
(3);醚键
(4)2:1
解析:(1)由表格数据可知,A易溶于水,B不溶于水,但A、B互溶,二者沸点差异较大,故除去A和B混合物中的少量B可采用的方法是蒸馏,b符合题意。
(2)由题意可知,,,,则有机化合物中含有氧原子的物质的量是0.3 mol+0.4 mol-,1 mol该有机化合物中,所以该物质的最简式为,由于分子中碳、氢原子的个数比是1:3,已经达到饱和,所以确定其分子式,不需要其他条件,即最简式就是分子式。分子式为,核磁共振氢谱表明其分子中有3种化学环境的氢原子,则A的结构简式为。
(3)B的相对分子质量为74,根据红外光谱图,B中存在对称的甲基、亚甲基和COC,根据对称性,B的结构简式为。
(4)A和B的化学式分别为,设的物质的量分别是mol、mol,则
2 3
4 5
,,解得=0.2,=0.1,即A和B的物质的量之比2:1。
2
1.甘油是一种常用的有机溶剂,可与水以任意体积比互溶,密度约为1.26g/mL,沸点约为290℃。分离水和甘油应采用的方法是( )
A.蒸馏 B.蒸发 C.过滤 D.萃取、分液
2.用下列装置完成相关实验,不合理的是( )
A.用a趁热过滤提纯苯甲酸 B.用b制备并检验乙烯
C.用c除去溴苯中的苯 D.用d分离硝基苯与水
3.已知9.2 g某有机化合物与足量氧气在密闭容器中完全燃烧后,将反应生成的气体依次通过浓硫酸和碱石灰。浓硫酸质量增加10.8 g,碱石灰质量增加17.6 g,该有机化合物的化学式是( )
A. B. C. D.
4.下列说法中正确的是( )
A.在其核磁共振氢谱图中有3组吸收峰
B.红外光谱图只能确定有机化合物中所含官能团的种类和数目
C.质谱法不能用于相对分子质量的测定
D.红外光谱、核磁共振氢谱和质谱都可用于分析有机化合物结构
5.某化合物由碳、氢、氧三种元素组成,其红外光谱图有C一H键、O一H键、C一O键的振动吸收,该有机物的相对分子质量是60,其核磁共振氢谱只有3组峰。则该有机物的结构简式是( )
A. B. C. D.
6.质谱法是让极少量的()化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如离子化后可得到等,然后测定其质荷比。某有机物样品的质谱图如下图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物是( )
A.甲醇 B.甲烷 C.丙烷 D.乙烯
7.以下关于萃取、分液操作的叙述中,正确的是( )
A.将所需试剂加入分液漏斗,塞上玻璃塞,如图所示用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开活塞
8.下列有关物质分离、提纯的说法中,正确的是( )
A.除去乙酸乙酯中的少量乙酸,可加入氢氧化钠溶液,充分反应后分液
B.如图所示,振荡后静置,上层溶液颜色保持不变
C.中有少量,为得到纯净的可加足量CaO后蒸馏
D.分液时,分液漏斗中下层液体从下口放出,上层液体也从下口放出
9.验证某有机化合物属于烃,应完成的实验内容是( )
A.测定它的C、H原子个数比
B.证明它完全燃烧后的产物只有水和
C.测定其燃烧产物中水和的物质的量之比
D.测定该有机化合物的质量及其完全燃烧后生成和水的质量
10.醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置(省略加热和部分夹持装置)如下:
可能用到的有关数据如下:
相对分子质量 沸点/℃ 密度/ 溶解性
环己醇 100 161 0.9618 微溶于水
环己烯 82 83 0.8102 难溶于水
合成反应:
在a中加入20g环己醇和少量碎瓷片,在搅动下慢慢加入1mL浓;b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离、提纯:
反应得到的粗产物倒入分液漏斗中,分别用少量5%的碳酸钠溶液和蒸馏水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到10g纯净环己烯。
回答下列问题:
(1)装置b的名称是_______。
(2)加入碎瓷片的作用是_______;如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是_______(填字母)。
A.立即补加
B.冷却后补加
C.继续加热
D.重新配料
(3)分液漏斗在使用前须清洗干净并_______,在本实验分离过程中,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(4)分离、提纯过程中加入无水氯化钙的目的是_______。
11.两种有机化合物A和B可以互溶,有关性质如下:
相对密度(20℃ ) 熔点 沸点 溶解性
A 0.7893 -117.3°C 78.5°C 与水以任意比混溶
B 0.7137 -116.6°C 34.5°C 不溶于水
(1)若要除去A和B的混合物中少量的B,采用______(填序号)方法即可得到A。
a.重结晶 b.蒸馏 c.萃取 d.加水充分振荡,分液
(2)将有机化合物A置于氧气流中充分燃烧,实验测得:生成5.4 g和8.8 g ,消耗氧气6.72 L(标准状况下),则该物质的最简式为________,若要确定其分子式,_____________(填“是”或“否”)需有其他条件。已知有机化合物A的核磁共振氢谱、质谱如图所示,则A的结构简式为________。
(3)若质谱图显示B的相对分子质量为74,红外光谱如图所示,则B的结构简式为________,其官能团的名称为_______。
(4)准确称取一定质量的A和B的混合物,在足量氧气中充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增重19.8 g和35.2 g。计算混合物中A和B的物质的量之比为______。
答案以及解析
1.答案:A
解析:甘油和水以任意体积比互溶,不能用过滤、蒸发、萃取、分液的方法分离,二者沸点相差较大,可用蒸馏的方法分离。
2.答案:B
解析:用a趁热过滤提纯苯甲酸,图示过滤装置满足“一贴、二低、三靠”的要求,且用玻璃棒引流,合理,故A不符合题意;利用乙醇在浓硫酸、加热的条件下制取的乙烯中会混有等杂质,能与溴水反应而使其褪色,对乙烯的检验产生干扰,且b中没有收集、除杂装置,导管直接插入溴水中会产生倒吸,不合理,故B符合题意;溴苯与苯的沸点相差较大,可以通过蒸馏将两者分离,且c中温度计的水银球放在蒸馏烧瓶的支管口处,冷凝水下口进、上口出,合理,故C不符合题意;硝基苯不溶于水,且密度比水大,因此可通过分液的方法将硝基苯与水分离开,硝基苯从下端放出,合理,故D不符合题意。
3.答案:A
解析:将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增加的10.8 g为生成水的质量,碱石灰增加的17.6 g为生成二氧化碳的质量。生成水的物质的量为,氢原子的物质的量为0.6 mol×2=1.2 mol;生成二氧化碳的物质的量为,碳原子的物质的量为0.4 mol;9.2 g该有机化合物分子中含有氧原子的物质的量为。1 mol该有机化合物分子中含有C、H、O原子的物质的量之比为0.4 mol:1.2 mol:0.2 mol=2:6:1,该有机化合物的最简式为,由于氢原子已经饱和,故该有机化合物分子式为, A正确。
4.答案:AD
解析:在其核磁共振氢谱图中有3组吸收峰,故A正确;红外光谱图只能确定有机化合物中所含官能团的种类,无法确定其数目,故B错误;通过质谱法可以测定有机化合物的相对分子质量,故C错误;红外光谱仪用于测定有机化合物的化学键、官能团种类,核磁共振仪可测定有机化合物分子中氢原子的种类,质谱仪用于测定有机化合物的相对分子质量,所以红外光谱、核磁共振氢谱、质谱都可用于分析有机化合物结构,故D正确。
5.答案:B
解析:相对分子质量为60,但分子中不含O一H键,有3种氢原子,A错误;相对分子质量为60,分子中含有C一H键、O一H键、C一O键,只有3种氢原子,B正确;相对分子质量为60,含有C一H键、O一H键、C一O键,有4种氢原子,C错误;相对分子质量为58,不含O一H键、C一O键,有3种氢原子,D错误。
6.答案:B
解析:由有机物样品的质谱图可知,该有机物微粒质荷比最大值为16,则该有机物的相对分子质量为16,甲醇、甲烷、丙烷、乙烯的相对分子质量分别为32、16、44、28,则该有机物为甲烷。
7.答案:D
解析:一只手压住玻璃塞,一只手握住活塞,把分液漏斗倒转过来振荡,A错误;振荡几次后打开活塞放气,不需打开分液漏斗上口的玻璃塞放气,B错误;将分液漏斗放在铁架台上静置待液体分层,C错误;分液时将分液漏斗上的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔,再打开活塞,待下层液体流尽时,关闭活塞,从上口倒出上层液体,D正确。
8.答案:C
解析:乙酸乙酯在氢氧化钠溶液中能水解,故A错;与NaOH溶液反应,上层溶液颜色会变浅或变为无色,故B错;乙酸与氧化钙反应生成高沸点的盐,乙醇不能与CaO反应,然后蒸馏得到乙醇,故C正确;分液时下层液体从下口放出,上层液体从上口倒出,故D错。
9.答案:D
解析:烃只含C、H两种元素。只测定它的C、H原子个数比,不能确定是否含有O原子,不能验证该有机化合物属于烃,故A错误;烃和烃的含氧衍生物的燃烧产物都是,则只证明该有机化合物完全燃烧后产物只有,不能验证该有机化合物属于烃,故B错误;只测定其燃烧产物中的物质的量之比,只能测出它的C、H原子个数比,不能确定是否含有O原子,不能验证该有机化合物属于烃,故C错误;测定该有机化合物的质量及其完全燃烧后生成的质量,若有机化合物的质量与中C、H元素的质量之和相等,则能验证该有杋化合物属于烃,故D正确。
10.答案:(1)直形冷凝管
(2)防止暴沸;B
(3)检漏;上口倒出
(4)干燥环已烯
解析:(1)由题图可知装置b的名称是直形冷凝管。
(2)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加碎瓷片,应冷却后补加。
(3)分液漏斗在使用前应清洗干净并检查是否漏水。产物中环己烯难溶于水且密度比水的小,静置后在上层,无机相在下层,下层液体从下口放出,上层液体从上口倒出。
(4)加入无水氯化钙的目的是干燥环己烯。
11.答案:(1)b
(2);否;
(3);醚键
(4)2:1
解析:(1)由表格数据可知,A易溶于水,B不溶于水,但A、B互溶,二者沸点差异较大,故除去A和B混合物中的少量B可采用的方法是蒸馏,b符合题意。
(2)由题意可知,,,,则有机化合物中含有氧原子的物质的量是0.3 mol+0.4 mol-,1 mol该有机化合物中,所以该物质的最简式为,由于分子中碳、氢原子的个数比是1:3,已经达到饱和,所以确定其分子式,不需要其他条件,即最简式就是分子式。分子式为,核磁共振氢谱表明其分子中有3种化学环境的氢原子,则A的结构简式为。
(3)B的相对分子质量为74,根据红外光谱图,B中存在对称的甲基、亚甲基和COC,根据对称性,B的结构简式为。
(4)A和B的化学式分别为,设的物质的量分别是mol、mol,则
2 3
4 5
,,解得=0.2,=0.1,即A和B的物质的量之比2:1。
2
