8.2.2 金属的化学性质(2)【教学课件24页】-2022-2023学年九年级化学下册同步备课系列(人教版)
文档属性
| 名称 | 8.2.2 金属的化学性质(2)【教学课件24页】-2022-2023学年九年级化学下册同步备课系列(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 8.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-22 00:00:00 | ||
图片预览







文档简介
(共24张PPT)
第八单元 金属和金属材料
课题2 金属的化学性质
第2课时
金属的活动性顺序
2
金属与金属化合物溶液反应
1
本节重点
本节难点
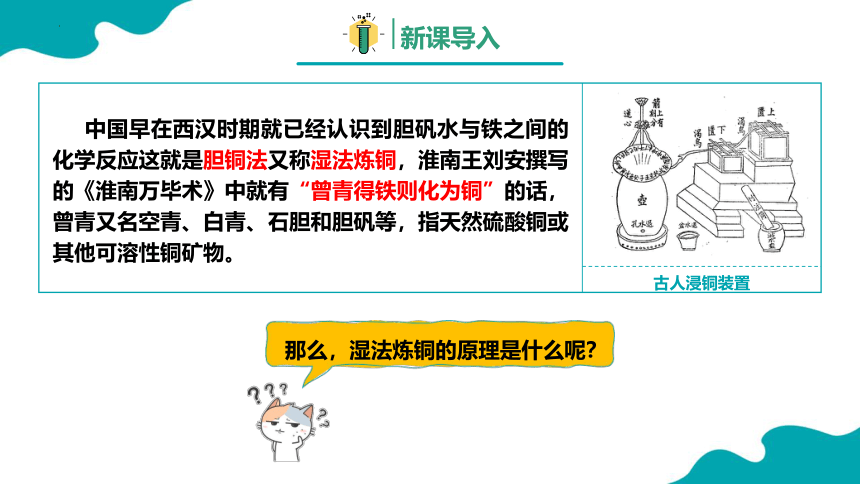
那么,湿法炼铜的原理是什么呢?
中国早在西汉时期就已经认识到胆矾水与铁之间的化学反应这就是胆铜法又称湿法炼铜,淮南王刘安撰写的《淮南万毕术》中就有“曾青得铁则化为铜”的话,曾青又名空青、白青、石胆和胆矾等,指天然硫酸铜或其他可溶性铜矿物。
古人浸铜装置
实验探究
探究:金属与金属盐溶液的反应
金属与金属盐溶液的反应
探究一
把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,过一会儿取出,观察,有什么现象发生?
探究二
把一根洁净的铜丝浸入硝酸银溶液中,过一会儿取出,观察,有什么现象发生?
探究三
把另一根洁净的铜丝浸入硫酸铝溶液中,过一会儿取出,观察,有什么现象发生?
实验 现象 结论(化学方程式) 活动性
铝丝浸入硫酸铜溶液中
铜丝浸入硝酸银溶液中
铜丝浸入硫酸铝溶液中
铝表面附有红色固体,溶液由蓝色变无色
不反应
无现象
铜表面附有银白色固体,溶液由无色变蓝色
___>___
Cu
Al
___>___
Ag
Cu
___>___
Cu
Al
2Al+3CuSO4 Al2(SO4)3 + 3Cu
铝丝浸入硫酸铜溶液中
铜丝浸入硝酸银溶液中
金属与金属盐溶液的反应
Cu +2AgNO3 Cu(NO3)2+2Ag
金属的活动性顺序:铝 > 铜 > 银
活动性强的金属能将活动性弱的金属从其化合物溶液中置换出来
结论
金属与金属盐溶液的反应
实验结论
注意:Fe2+的化合溶液呈_____色, Fe3+的化合物溶液呈_____色,Cu2+的化合物溶液呈_____色
浅绿
黄
蓝
【例1】(陕西省西安市经开区第一学校2022-2023学年九年级上学期期末化学试题)某文化衫图案上:你的美(Mg)偷走我的心(Zn)能发生
是由于镁的( )
A.延展性好 B.导电性好 C.导热性好 D.金属活动性比锌强
【详解】你的美(Mg)偷走我的心(Zn)能发生,是由于镁的金属活动性比锌强,能和硫酸锌反应生成硫酸镁和锌,反应的化学方程式为:Mg+ZnSO4=MgSO4+Zn。
故选D。
D
金属活动性由强逐渐减弱
钾 钙 钠 镁 铝 锌 铁 锡 铅 (氢) 铜 汞 银 铂 金
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
人们经过了许多类似上述实验的探究过程,进行了认真的去伪存真、由表及里的分析,归纳和总结出了常见金属在溶液中的活动性顺序:
金属活动性顺序表
金属活动顺序表的口诀:嫁给那美女,身体细纤轻,统共一百斤
金属活动性顺序表
应用一:判断金属活动性
金属活动性顺序表——应用
规律一
在金属活动性顺序里,金属的位置越靠前,它的活动性越强
Na>Mg> Fe >Cu
例题:Na、Fe、Mg、Cu四种金属,其活动性由强到弱的顺序?
金属活动性顺序表
应用二:金属是否能与酸反应
金属活动性顺序表——应用
规律二
在金属活动性顺序里,氢前面的金属能置换出盐酸、稀硫酸中的氢。
例题:
①Al、Mg、Sn、Pb、Ag五种金属,不能与酸反应的是?
②已知Ni和Fe的性质相似,Ni是否能与盐酸反应,其方程式是?
Ag
能与盐酸反应,Ni + 2HCl NiCl2 + H2↑
例题:
①向硝酸铜溶液中分别加入铁粉和银粉,其化学方程式?
②已知Ni和Fe的性质相似,向硝酸银溶液中加入镍粉,是否会反应,其化学方程式是?
金属活动性顺序表
应用三:金属与金属化合物溶液反应
金属活动性顺序表——应用
规律三
在金属活动性顺序里,前面的金属能把位于后面的金属从其化合物溶液 里置换出来
钾钙钠除外
Fe + Cu(NO3)2 Cu + Fe(NO3)2 银和硝酸铜不反应
会发生反应,Ni + 2AgNO3 Ni(NO3)2 + 2Ag
中国早在西汉时期就已经认识到胆矾水与铁之间的化学反应这就是胆铜法又称湿法炼铜,淮南王刘安撰写的《淮南万毕术》中就有“曾青得铁则化为铜”的话,曾青又名空青、白青、石胆和胆矾等,指天然硫酸铜或其他可溶性铜矿物。
古人浸铜装置
湿法炼铜的原理:
Fe+CuSO FeSO +Cu
最不活泼的金属——铱
元素符号Ir,原子序数77,原子量192.22,元素名来源于拉丁文,原意是“彩虹”。
铱的化学性质很稳定。是最耐腐蚀的金属,铱对酸的化学稳定性极高,不溶于酸,只有海绵状的铱才会缓慢地溶于热王水中,如果是致密状态的铱,即使是沸腾的王水,也不能腐蚀。
1.(重庆市綦江区2022-2023学年九年级上学期期末化学试题)《天工开物》记载“烧铁器浮于胆矾水中,即成铜色也”。下列说法正确的是( )
A.“铜色”指蓝色
B.“铁器”适宜盛放“胆矾水”
C.“即成铜色也”发生了置换反应
D.“成铜色”后“胆矾水”质量增加
,56份质量的铁生成64份质量的铜,
C
【详解】A、“铜色”指红色,故A不正确;
B、胆矾水是硫酸铜溶液,铁和硫酸铜反应,“铁器”不宜盛放“胆矾水”,故B不正确;
C、“即成铜色也”发生反应为铁和硫酸铜生成硫酸亚铁和铜,反应符合一种单质和一种化合物生成另一种单质和另一种化合物,属于置换反应,故C正确;
D、铁和硫酸铜反应的关系式为
“成铜色”后“胆根水”质量减少,故D不正确。故选C。
2.(湖南省衡阳市2021-2022学年九年级下学期期末化学试题)下列物质不会发生化学反应的是( )
A.铁与稀盐酸
B.锌与硫酸铝
C.铁与硝酸银
D.镁与硫酸锌
【详解】A、铁在金属活动性顺序中,排在氢前,铁可以与稀盐酸反应生成氯化锌和氢气,故A不符合题意;
B、锌在金属活动性顺序中排在铝后,故锌不能与硫酸铝反应,故B符合题意;
C、铁在金属活动性顺序中排在银前,铁可以与硝酸银反应生成硝酸亚铁和银,故C不符合题意;
D、镁在金属活动性顺序中排在锌前,镁可以与硫酸锌反应生成硫酸镁和锌,故D不符合题意;
故选B。
B
【详解】铁、铜、镁、银四种金属的活动性由强到弱的顺序是镁、铁、铜、银,将一定质量的铁粉放入到足量的Cu(NO3)2、Mg(NO3)2和AgNO3混合溶液中,铁不能与硝酸镁反应,铁先与硝酸银反应生成硝酸亚铁和银,硝酸银完全反应后,剩余的铁再与硝酸铜反应生成硝酸亚铁和铜,充分反应后过滤,测得滤渣中只含有一种金属,则该金属是铁与硝酸银反应生成的银,故选C。
3.(2022-2023学年九年级化学下册同步备课系列)将一定质量的铁粉放入到足量的Cu(NO3)2、Mg(NO3)2和AgNO3混合溶液中,充分反应后过滤,测得滤渣中只含有一种金属,则该金属是( )
A.Fe
B.Cu
C.Ag
D.Mg
C
4.(广东省梅州市五华县2022-2023学年九年级上学期期末化学试题)用实验比较铜、锌、银的金属活动性,除三种金属外最好的方法是选用下列试剂中的( )
A.ZnSO4溶液 B.AgNO3溶液 C.CuSO4溶液 D.稀盐酸
【详解】A、铜、锌、银的三种金属单质都不能与ZnSO4溶液反应,因此,使用ZnSO4溶液不能完成比较铜、锌、银的金属活动性,故A不正确;
B、铜、锌都能与AgNO3溶液反应,说明了铜锌、的活动性大于银,但无法比较铜、锌的活动性强弱,故B不正确;
C、锌能与硫酸铜溶液反应置换出铜,说明锌比铜活泼,而银与硫酸铜溶液不反应,说明铜比银活泼,故用硫酸铜溶液能比较铜、锌、银的金属活动性,故C正确;
D、银、锌、铜的三种金属单质只有锌与稀盐酸反应,无法判断铜、银活动性强弱。因此,使用稀盐酸不能完成比较铜、铝、银的金属活动性,故D不正确;
故选:C。
C
【详解】在金属活动性顺序表中,氢前的金属能置换出酸中的氢,将金属锰(Mn)投入稀盐酸中,有气泡产生,可知Mn>H;将镁条插入硫酸锰溶液中,如果有锰析出可知Mg>Mn;又在金属活动顺序表中CuMn>Cu,故选A。
5.(备战2023年中考化学一轮复习考点微专题)将金属锰(Mn)投入稀盐酸中,有气泡产生。将镁条插入硫酸锰溶液中,如果有锰析出,则Mn、Mg、Cu的金属活泼性由强到弱的顺序是( )
A.Mg、Mn、Cu
B.Mn、Mg、Cu
C.Cu、Mg、Mn
D.Cu、Mn、Mg
A
6.(湖南省衡阳市2021-2022学年九年级下学期期末化学试题)为验证铝、铁、铜三种金属活动性强弱,小佳用三支试管,只取一次稀盐酸就达到了目的,实验流程如图所示:
(1)能证明铜的活动性较铁的弱的现象是
________________________________________________________________。
(2)D处试管中可观察到的现象为
_________________________________________________________。
铜中加入稀盐酸无明显现象,取上清液加入铁粉后有气泡产生
溶液由浅绿色变为无色,有黑色固体析出
(3)三种金属的活动性由强到弱的顺序为_______________。
铝、铁、铜
(4)实验室中要求所加铁粉过量,如果加入铁粉不足,为保证实验成功,应该注意的事项是___________________________。
铝粉要过量
6.(湖南省衡阳市2021-2022学年九年级下学期期末化学试题)为验证铝、铁、铜三种金属活动性强弱,小佳用三支试管,只取一次稀盐酸就达到了目的,实验流程如图所示:
(5)写出实验中发生的置换反应化学方程式
__________________________________________________________(写一个即可)。
Fe+2HCl=FeCl2+H2↑或2Al+3FeCl2=2AlCl3+3Fe
6.(湖南省衡阳市2021-2022学年九年级下学期期末化学试题)为验证铝、铁、铜三种金属活动性强弱,小佳用三支试管,只取一次稀盐酸就达到了目的,实验流程如图所示:
课题2
金属的化学性质
第2课时
金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
应用
越排在前面的金属,活泼性越强
位于氢前面的金属能置换出盐酸、稀硫酸中的氢
排在前面的金属能把排在后面的金属从它们化合物的溶液中置换出来(不包括K、Ca、Na)
THANKS
谢谢聆听
第八单元 金属和金属材料
课题2 金属的化学性质
第2课时
金属的活动性顺序
2
金属与金属化合物溶液反应
1
本节重点
本节难点
那么,湿法炼铜的原理是什么呢?
中国早在西汉时期就已经认识到胆矾水与铁之间的化学反应这就是胆铜法又称湿法炼铜,淮南王刘安撰写的《淮南万毕术》中就有“曾青得铁则化为铜”的话,曾青又名空青、白青、石胆和胆矾等,指天然硫酸铜或其他可溶性铜矿物。
古人浸铜装置
实验探究
探究:金属与金属盐溶液的反应
金属与金属盐溶液的反应
探究一
把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,过一会儿取出,观察,有什么现象发生?
探究二
把一根洁净的铜丝浸入硝酸银溶液中,过一会儿取出,观察,有什么现象发生?
探究三
把另一根洁净的铜丝浸入硫酸铝溶液中,过一会儿取出,观察,有什么现象发生?
实验 现象 结论(化学方程式) 活动性
铝丝浸入硫酸铜溶液中
铜丝浸入硝酸银溶液中
铜丝浸入硫酸铝溶液中
铝表面附有红色固体,溶液由蓝色变无色
不反应
无现象
铜表面附有银白色固体,溶液由无色变蓝色
___>___
Cu
Al
___>___
Ag
Cu
___>___
Cu
Al
2Al+3CuSO4 Al2(SO4)3 + 3Cu
铝丝浸入硫酸铜溶液中
铜丝浸入硝酸银溶液中
金属与金属盐溶液的反应
Cu +2AgNO3 Cu(NO3)2+2Ag
金属的活动性顺序:铝 > 铜 > 银
活动性强的金属能将活动性弱的金属从其化合物溶液中置换出来
结论
金属与金属盐溶液的反应
实验结论
注意:Fe2+的化合溶液呈_____色, Fe3+的化合物溶液呈_____色,Cu2+的化合物溶液呈_____色
浅绿
黄
蓝
【例1】(陕西省西安市经开区第一学校2022-2023学年九年级上学期期末化学试题)某文化衫图案上:你的美(Mg)偷走我的心(Zn)能发生
是由于镁的( )
A.延展性好 B.导电性好 C.导热性好 D.金属活动性比锌强
【详解】你的美(Mg)偷走我的心(Zn)能发生,是由于镁的金属活动性比锌强,能和硫酸锌反应生成硫酸镁和锌,反应的化学方程式为:Mg+ZnSO4=MgSO4+Zn。
故选D。
D
金属活动性由强逐渐减弱
钾 钙 钠 镁 铝 锌 铁 锡 铅 (氢) 铜 汞 银 铂 金
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
人们经过了许多类似上述实验的探究过程,进行了认真的去伪存真、由表及里的分析,归纳和总结出了常见金属在溶液中的活动性顺序:
金属活动性顺序表
金属活动顺序表的口诀:嫁给那美女,身体细纤轻,统共一百斤
金属活动性顺序表
应用一:判断金属活动性
金属活动性顺序表——应用
规律一
在金属活动性顺序里,金属的位置越靠前,它的活动性越强
Na>Mg> Fe >Cu
例题:Na、Fe、Mg、Cu四种金属,其活动性由强到弱的顺序?
金属活动性顺序表
应用二:金属是否能与酸反应
金属活动性顺序表——应用
规律二
在金属活动性顺序里,氢前面的金属能置换出盐酸、稀硫酸中的氢。
例题:
①Al、Mg、Sn、Pb、Ag五种金属,不能与酸反应的是?
②已知Ni和Fe的性质相似,Ni是否能与盐酸反应,其方程式是?
Ag
能与盐酸反应,Ni + 2HCl NiCl2 + H2↑
例题:
①向硝酸铜溶液中分别加入铁粉和银粉,其化学方程式?
②已知Ni和Fe的性质相似,向硝酸银溶液中加入镍粉,是否会反应,其化学方程式是?
金属活动性顺序表
应用三:金属与金属化合物溶液反应
金属活动性顺序表——应用
规律三
在金属活动性顺序里,前面的金属能把位于后面的金属从其化合物溶液 里置换出来
钾钙钠除外
Fe + Cu(NO3)2 Cu + Fe(NO3)2 银和硝酸铜不反应
会发生反应,Ni + 2AgNO3 Ni(NO3)2 + 2Ag
中国早在西汉时期就已经认识到胆矾水与铁之间的化学反应这就是胆铜法又称湿法炼铜,淮南王刘安撰写的《淮南万毕术》中就有“曾青得铁则化为铜”的话,曾青又名空青、白青、石胆和胆矾等,指天然硫酸铜或其他可溶性铜矿物。
古人浸铜装置
湿法炼铜的原理:
Fe+CuSO FeSO +Cu
最不活泼的金属——铱
元素符号Ir,原子序数77,原子量192.22,元素名来源于拉丁文,原意是“彩虹”。
铱的化学性质很稳定。是最耐腐蚀的金属,铱对酸的化学稳定性极高,不溶于酸,只有海绵状的铱才会缓慢地溶于热王水中,如果是致密状态的铱,即使是沸腾的王水,也不能腐蚀。
1.(重庆市綦江区2022-2023学年九年级上学期期末化学试题)《天工开物》记载“烧铁器浮于胆矾水中,即成铜色也”。下列说法正确的是( )
A.“铜色”指蓝色
B.“铁器”适宜盛放“胆矾水”
C.“即成铜色也”发生了置换反应
D.“成铜色”后“胆矾水”质量增加
,56份质量的铁生成64份质量的铜,
C
【详解】A、“铜色”指红色,故A不正确;
B、胆矾水是硫酸铜溶液,铁和硫酸铜反应,“铁器”不宜盛放“胆矾水”,故B不正确;
C、“即成铜色也”发生反应为铁和硫酸铜生成硫酸亚铁和铜,反应符合一种单质和一种化合物生成另一种单质和另一种化合物,属于置换反应,故C正确;
D、铁和硫酸铜反应的关系式为
“成铜色”后“胆根水”质量减少,故D不正确。故选C。
2.(湖南省衡阳市2021-2022学年九年级下学期期末化学试题)下列物质不会发生化学反应的是( )
A.铁与稀盐酸
B.锌与硫酸铝
C.铁与硝酸银
D.镁与硫酸锌
【详解】A、铁在金属活动性顺序中,排在氢前,铁可以与稀盐酸反应生成氯化锌和氢气,故A不符合题意;
B、锌在金属活动性顺序中排在铝后,故锌不能与硫酸铝反应,故B符合题意;
C、铁在金属活动性顺序中排在银前,铁可以与硝酸银反应生成硝酸亚铁和银,故C不符合题意;
D、镁在金属活动性顺序中排在锌前,镁可以与硫酸锌反应生成硫酸镁和锌,故D不符合题意;
故选B。
B
【详解】铁、铜、镁、银四种金属的活动性由强到弱的顺序是镁、铁、铜、银,将一定质量的铁粉放入到足量的Cu(NO3)2、Mg(NO3)2和AgNO3混合溶液中,铁不能与硝酸镁反应,铁先与硝酸银反应生成硝酸亚铁和银,硝酸银完全反应后,剩余的铁再与硝酸铜反应生成硝酸亚铁和铜,充分反应后过滤,测得滤渣中只含有一种金属,则该金属是铁与硝酸银反应生成的银,故选C。
3.(2022-2023学年九年级化学下册同步备课系列)将一定质量的铁粉放入到足量的Cu(NO3)2、Mg(NO3)2和AgNO3混合溶液中,充分反应后过滤,测得滤渣中只含有一种金属,则该金属是( )
A.Fe
B.Cu
C.Ag
D.Mg
C
4.(广东省梅州市五华县2022-2023学年九年级上学期期末化学试题)用实验比较铜、锌、银的金属活动性,除三种金属外最好的方法是选用下列试剂中的( )
A.ZnSO4溶液 B.AgNO3溶液 C.CuSO4溶液 D.稀盐酸
【详解】A、铜、锌、银的三种金属单质都不能与ZnSO4溶液反应,因此,使用ZnSO4溶液不能完成比较铜、锌、银的金属活动性,故A不正确;
B、铜、锌都能与AgNO3溶液反应,说明了铜锌、的活动性大于银,但无法比较铜、锌的活动性强弱,故B不正确;
C、锌能与硫酸铜溶液反应置换出铜,说明锌比铜活泼,而银与硫酸铜溶液不反应,说明铜比银活泼,故用硫酸铜溶液能比较铜、锌、银的金属活动性,故C正确;
D、银、锌、铜的三种金属单质只有锌与稀盐酸反应,无法判断铜、银活动性强弱。因此,使用稀盐酸不能完成比较铜、铝、银的金属活动性,故D不正确;
故选:C。
C
【详解】在金属活动性顺序表中,氢前的金属能置换出酸中的氢,将金属锰(Mn)投入稀盐酸中,有气泡产生,可知Mn>H;将镁条插入硫酸锰溶液中,如果有锰析出可知Mg>Mn;又在金属活动顺序表中Cu
5.(备战2023年中考化学一轮复习考点微专题)将金属锰(Mn)投入稀盐酸中,有气泡产生。将镁条插入硫酸锰溶液中,如果有锰析出,则Mn、Mg、Cu的金属活泼性由强到弱的顺序是( )
A.Mg、Mn、Cu
B.Mn、Mg、Cu
C.Cu、Mg、Mn
D.Cu、Mn、Mg
A
6.(湖南省衡阳市2021-2022学年九年级下学期期末化学试题)为验证铝、铁、铜三种金属活动性强弱,小佳用三支试管,只取一次稀盐酸就达到了目的,实验流程如图所示:
(1)能证明铜的活动性较铁的弱的现象是
________________________________________________________________。
(2)D处试管中可观察到的现象为
_________________________________________________________。
铜中加入稀盐酸无明显现象,取上清液加入铁粉后有气泡产生
溶液由浅绿色变为无色,有黑色固体析出
(3)三种金属的活动性由强到弱的顺序为_______________。
铝、铁、铜
(4)实验室中要求所加铁粉过量,如果加入铁粉不足,为保证实验成功,应该注意的事项是___________________________。
铝粉要过量
6.(湖南省衡阳市2021-2022学年九年级下学期期末化学试题)为验证铝、铁、铜三种金属活动性强弱,小佳用三支试管,只取一次稀盐酸就达到了目的,实验流程如图所示:
(5)写出实验中发生的置换反应化学方程式
__________________________________________________________(写一个即可)。
Fe+2HCl=FeCl2+H2↑或2Al+3FeCl2=2AlCl3+3Fe
6.(湖南省衡阳市2021-2022学年九年级下学期期末化学试题)为验证铝、铁、铜三种金属活动性强弱,小佳用三支试管,只取一次稀盐酸就达到了目的,实验流程如图所示:
课题2
金属的化学性质
第2课时
金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
应用
越排在前面的金属,活泼性越强
位于氢前面的金属能置换出盐酸、稀硫酸中的氢
排在前面的金属能把排在后面的金属从它们化合物的溶液中置换出来(不包括K、Ca、Na)
THANKS
谢谢聆听
同课章节目录
