8.3.1 金属资源的利用与保护(1)【课件】(共30张PPT)(人教版)
文档属性
| 名称 | 8.3.1 金属资源的利用与保护(1)【课件】(共30张PPT)(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 19.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-23 00:00:00 | ||
图片预览











文档简介
(共30张PPT)
第八单元 金属和金属材料
课题3 金属资源的利用与保护
第1课时
本节重点
本节难点
1
金属资源在自然界的存在
2
铁的冶炼
3
有关含杂质物质的计算
炉火照天地,红星乱紫烟
诗句描述了铜官山脚下,冶铜工人在熊熊的炉火,火舌窜动中,炼铜的场景
那么,如何从金属矿石中得到我们想要的金属呢?
地球上的金属资源广泛存在于地壳和海洋中,除少数很不活泼的金属如金银等有单质形式存在外,其余都以化合物的形式存在。
以单质形式存在的金属
金 Au
银 Ag
铂 Pt
自然界中的几种矿石
以化合物形式存在 — 铁
赤铁矿Fe2O3
菱铁矿FeCO3
磁铁矿Fe3O4
黄铁矿FeS2
自然界中的几种矿石
以化合物形式存在 — 铜
黄铜矿CuFeS2
辉铜矿Cu2S
孔雀石Cu2(OH)2CO3
自然界中的几种矿石
以化合物形式存在 — 铝
铝土矿Al2O3
明矾石KAl(SO4)·12H2O
自然界中的几种矿石
人类最早使用的铁矿石——陨铁
铁的冶炼
大自然向人类提供了丰富的金属矿物资源,人类每年要提取数以亿吨计的金属,用于工农业生产和其他领域。其中,提取量最大的是铁。
平谷县出土的商铁刃铜钺
铁刃部分已锈蚀
现代炼铁
古代炼铁
铁的冶炼
为纪念1996年钢铁产量突破1亿吨而发行的邮票
铁的冶炼
铁的冶炼
怎样把铁矿石变成铁呢?
把铁元素从铁矿石中提炼出来
我们学过哪些能得到铁的化学方程式呢?
3C+2Fe2O3 4Fe+3CO2↑
高温
3CO+Fe2O3 2Fe+3CO2
高温
(工业炼铁的原理)
3CO+Fe2O3 2Fe+3CO2
高温
将矿石中的二氧化硅转变为炉渣
铁矿石、焦炭、石灰石
高炉气体
高炉气体
出铁口
进风口
O2
N2
热空气
生铁
进风口
出渣口
CO2+C 2CO
高温
C+O2 CO2
高温
CaCO3+SiO2 CaSiO3 + CO2↑
高温
炉渣
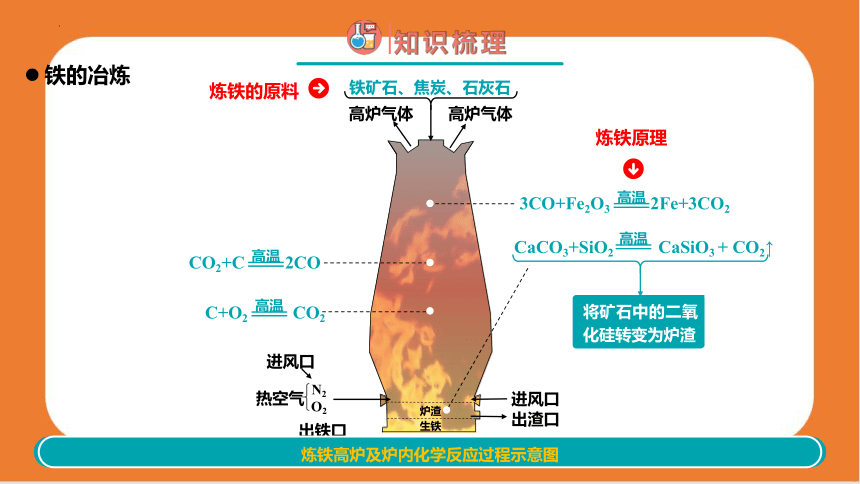
铁的冶炼
炼铁的原料
炼铁原理
炼铁高炉及炉内化学反应过程示意图
因为这两种矿石含铁量高(质量分数大),且含硫等“有害元素”少,冶炼时产生的污染小。
常见的铁矿石中理论上最适宜炼铁的两种矿石是什么?理由?
赤铁矿Fe2O3
磁铁矿Fe3O4
最适宜炼铁的两种矿石:
【例1】(2023秋·九年级课时练习)关于工业炼铁的说法正确的是( )
A.铁矿石用于炼铁是因为含有大量单质铁
B.焦炭的主要作用是不完全燃烧制取CO
C.在高炉中冶炼出来的是生铁,不是纯铁
D.高炉的尾气成分为CO,可以直接排放
D
【详解】A、铁矿石用于炼铁是因为含有大量铁的化合物,故 A 选项错误;
B、焦炭的主要作用是燃烧提供能量和不完全燃烧制取CO,用CO还原铁的化合物,故 B 选项错误;
C、在高炉中冶炼出来的是生铁,是含碳的铁合金,故 C选项正确;
D、一氧化碳有毒,不能直接排放,故D选项错误。
故选C。
红色粉末(氧化铁)逐渐变成黑色
澄清的石灰水逐渐变浑浊
尾气燃烧产生蓝色火焰
实验现象:
铁的冶炼
实验室用一氧化碳还原氧化铁的装置
化学方程式:
3CO+Fe2O3 2Fe+3CO2
高温
回顾实验,回答下面问题:
实验前为什么先通一氧化碳?
问题1:
如何处理尾气?
问题2:
分析工业炼铁的原理。
问题3:
分析原料产物是否为纯净物。
问题4:
答:为了排净装置中的空气,防止加热时发生爆炸。
答:利用一氧化碳的还原性,把铁从化合物中还原出来。
答:尾气中含有一氧化碳要点燃或收集再利用。
答:原料不是纯净物,矿石中含有杂质。
高炉炼铁和实验室炼铁有什么区别?其产物是纯铁吗?
Fe2O3+3CO 2Fe+3CO2
高温
两者的产物不同。工业炼铁得到的是生铁,实验室得到的是纯铁。
设备不同。工业炼铁设备是高炉,实验室用玻璃管。
对环境影响不同。高炉炼铁对环境影响大,实验室对环境影响小。
操作难易程度不同。高炉炼铁工艺复杂,实验室操作简单。
铁的冶炼
生铁
可经过吹氧冶炼等工序生产钢,含碳量降至0.03%~2%的铁合金
含有2%~4.3%的碳及少量磷和硫的铁合金
硬而脆,不利于加工
【例1】(2023秋·陕西咸阳·九年级统考期末)下列有关模拟工业炼铁的叙述不正确的是( )
D
A.赤铁矿的主要成分是Fe2O3
B.硬质玻璃管中红色固体变为黑色
C.用燃着的酒精灯可防止CO污染空气
D.实验时应先点燃酒精喷灯后再通CO
【详解】A、赤铁矿的主要成分是Fe2O3,故A正确;
B、一氧化碳和氧化铁高温生成铁和二氧化碳,硬质玻璃管中红色固体变为黑色,故B正确;
C、一氧化碳具有可燃性,用燃着的酒精灯可防止CO污染空气,故C正确;
D、为防止发生爆炸,实验时应先通CO后再点燃酒精喷灯,故D不正确。
故选D。
涉及杂质问题的计算
纯净物的质量 = 不纯物质的总质量×纯度
纯度= ×100%
纯净物的质量
不纯物质的总质量
在实际生产时,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题。
含杂质的计算一般做法如下:
第二步,依据化学方程式,根据已知纯物质的质量计算未知纯物质的质量;
第一步,将含杂质的物质质量转化成纯净物的质量;
第三步,将纯物质转化成杂质物质的质量。
不纯物质的质量=纯净物的质量 ÷纯度
【例1】(2023秋·河北邢台·九年级校考期末)某炼铁厂用赤铁矿石冶炼生铁。若要炼出1120t含铁90%的生铁,需要含氧化铁80%的赤铁矿石的质量是( )
A.1500 t B. 1440 t C. 1800 t D. 1980 t
【详解】设理论上需要含氧化铁80%的赤铁矿石的质量为x
x=1800t
故选C
C
热分解法:
适用于金属活动性弱的,在常见金属活动性顺序的右端区域
物理提取:
其密度很大,用多次淘洗法去掉矿粒,泥沙等杂质,便可得到
钾 钙 钠 镁 铝 锌 铁 锡 铅 (氢) 铜 汞 银 铂 金
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
热还原法:
适用于金属活动性比较强,在常见金属活动性顺序中居于中间区域(Zn~Cu)
电解法:
一般用于金属活动性顺序中铝及铝以前的金属冶炼
冶炼金属的方法
1.(2023春·九年级课时练习)下列物质中不是炼铁高炉中投放的基本原料的是( )
A.铁矿石 B.石灰石 C.焦炭 D.生铁
【详解】A、铁矿石是炼铁高炉中投入的基本原料,A不符合题意;
B、石灰石是炼铁高炉中投入的基本原料,作用是将二氧化硅转化成炉渣而除掉,B不符合题意;
C、焦炭是炼铁高炉中投入的基本原料,作用是通过热量,产生还原剂一氧化碳,C不符合题意;
D、生铁是高炉炼铁的产品,不是原料,D符合题意。
综上所述:选择D。
D
2.(2023春·重庆北碚·九年级西南大学附中校考开学考试)中国高铁是一张国家名片,工业中常利用赤铁矿来炼铁,下列说法中正确的是( )
A.地壳中含量最高的金属元素是铁元素
B.高炉炼铁得到的产品是纯铁
C.炼铁过程中,氧化铁体现了还原性
D.高炉炼铁时加入石灰石可将杂质二氧化硅转化为炉渣
【详解】A、地壳中含量前四位的元素(由高到低)为:O、Si、Al、Fe,则含量最高的金属元素是铝元素,故选项说法错误;
B、高炉炼铁得到的铁中含有杂质,属于混合物,不是纯铁,故选项说法错误;
C、工业中通过赤铁矿炼铁的原理为Fe2O3与CO在高温下反应产生Fe,CO将氧化铁还原为铁,体现了还原性,故选项说法错误;
D、石灰石的主要成分是碳酸钙,碳酸钙能与杂质二氧化硅结合生成炉渣CaSiO3,从而达到除杂的目的,故选项说法正确。
故选D。
D
3.(2023·广西柳州·统考一模)某混合气体中可能含有H2、CO和CO2中的一种或几种,为检验其成分,小明同学按照下图装置进行实验时观察到红棕色固体变黑,澄清石灰水变浑浊,由此可知混合气体的组成情况可能有( )
A.2种 B.3种 C.4种 D.5种
D
【详解】实验时观察到红棕色固体变黑,说明含有氢气或一氧化碳,澄清石灰水变浑浊,可能含有二氧化碳,混合气体的组成情况可能有:1.氢气、二氧化碳,2.氢气、一氧化碳,3.一氧化碳、二氧化碳,4.氢气、一氧化碳、二氧化碳,5.一氧化碳共5种情况,故选D。
4.(2023秋·河北石家庄·九年级石家庄市第四十二中学校考期末)下列有关金属材料的说法正确的是( )
A.铁矿石是一种铁合金 B.氧化铁属于金属材料
C.生铁的含碳量高于钢 D.自然界中的金属都以化合物的形式存在
【详解】A、铁矿石不是铁合金,故说法错误;
B、氧化铁是铁的氧化物,不是金属材料,故说法错误;
C、生铁和钢都是铁合金,其中含碳量较高的是生铁,故说法正确;
D、少数不活泼金属以单质形式存在,如金、银等,故说法错误。
故选C。
C
5.(2022秋·江苏徐州·九年级竞赛)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。”(注:炉甘石的主要成分是碳酸锌)火法炼锌主要发生的化学反应是 ,下列说法正确的是( )
A.X的化学式是CO2
B.“逐层用煤炭饼垫盛”是为了燃烧提供高温
C.反应前后固体的质量不变
D.“罐中炉甘石熔化成团”,团的主要成分是锌
【详解】A、由质量守恒定律:X的化学式为CO,故选项说法错误;
B、反应的原理是火法炼锌主要发生的化学反应方程式为:
,碳是反应物,逐层用煤炭饼垫盛,是为了使碳与碳酸锌充分反应,故选项说法错误;
C、反应后有气体生成,由质量守恒定律,反应前后固体的质量减少,故选项说法错误;
D、罐中炉甘石熔化成团,团的主要成分是生成的锌,故选项说法正确。
故选D。
D
6.(2020·山东青岛·校考一模)早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
(1)请写出工业炼铁的反应方程式:_______________________________。
(2)实验开始时要先通入CO,目的是
__________________________________________________________________。
排净装置内的空气,防止一氧化碳与空气混合加热爆炸
6.(2020·山东青岛·校考一模)早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
(3)实验中A装置的实验现象是:B装置可观察到的现象是____________________。右边导气管口放置点燃的酒精灯的目的是
__________________________________________。
澄清石灰水变浑浊
处理尾气,防止一氧化碳污染环境
6.(2020·山东青岛·校考一模)早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
(4)小刚通过实验测定样品中氧化铁的质量分数,他称取了25g样品,通入一氧化碳至反应结束后,称得B装置增加了13.2g,试根据B装置的变化数据,计算出样品中氧化铁的质量分数(写出计算过程)。
课题3
金属的利用与保护
第1课时
金属资源的概况
铁的冶炼
炼铁原理
工业炼铁设备:炼铁高炉
工业炼铁原料:铁矿石、焦炭、石灰石
含杂质物质的计算
单质
化合物
第八单元 金属和金属材料
课题3 金属资源的利用与保护
第1课时
本节重点
本节难点
1
金属资源在自然界的存在
2
铁的冶炼
3
有关含杂质物质的计算
炉火照天地,红星乱紫烟
诗句描述了铜官山脚下,冶铜工人在熊熊的炉火,火舌窜动中,炼铜的场景
那么,如何从金属矿石中得到我们想要的金属呢?
地球上的金属资源广泛存在于地壳和海洋中,除少数很不活泼的金属如金银等有单质形式存在外,其余都以化合物的形式存在。
以单质形式存在的金属
金 Au
银 Ag
铂 Pt
自然界中的几种矿石
以化合物形式存在 — 铁
赤铁矿Fe2O3
菱铁矿FeCO3
磁铁矿Fe3O4
黄铁矿FeS2
自然界中的几种矿石
以化合物形式存在 — 铜
黄铜矿CuFeS2
辉铜矿Cu2S
孔雀石Cu2(OH)2CO3
自然界中的几种矿石
以化合物形式存在 — 铝
铝土矿Al2O3
明矾石KAl(SO4)·12H2O
自然界中的几种矿石
人类最早使用的铁矿石——陨铁
铁的冶炼
大自然向人类提供了丰富的金属矿物资源,人类每年要提取数以亿吨计的金属,用于工农业生产和其他领域。其中,提取量最大的是铁。
平谷县出土的商铁刃铜钺
铁刃部分已锈蚀
现代炼铁
古代炼铁
铁的冶炼
为纪念1996年钢铁产量突破1亿吨而发行的邮票
铁的冶炼
铁的冶炼
怎样把铁矿石变成铁呢?
把铁元素从铁矿石中提炼出来
我们学过哪些能得到铁的化学方程式呢?
3C+2Fe2O3 4Fe+3CO2↑
高温
3CO+Fe2O3 2Fe+3CO2
高温
(工业炼铁的原理)
3CO+Fe2O3 2Fe+3CO2
高温
将矿石中的二氧化硅转变为炉渣
铁矿石、焦炭、石灰石
高炉气体
高炉气体
出铁口
进风口
O2
N2
热空气
生铁
进风口
出渣口
CO2+C 2CO
高温
C+O2 CO2
高温
CaCO3+SiO2 CaSiO3 + CO2↑
高温
炉渣
铁的冶炼
炼铁的原料
炼铁原理
炼铁高炉及炉内化学反应过程示意图
因为这两种矿石含铁量高(质量分数大),且含硫等“有害元素”少,冶炼时产生的污染小。
常见的铁矿石中理论上最适宜炼铁的两种矿石是什么?理由?
赤铁矿Fe2O3
磁铁矿Fe3O4
最适宜炼铁的两种矿石:
【例1】(2023秋·九年级课时练习)关于工业炼铁的说法正确的是( )
A.铁矿石用于炼铁是因为含有大量单质铁
B.焦炭的主要作用是不完全燃烧制取CO
C.在高炉中冶炼出来的是生铁,不是纯铁
D.高炉的尾气成分为CO,可以直接排放
D
【详解】A、铁矿石用于炼铁是因为含有大量铁的化合物,故 A 选项错误;
B、焦炭的主要作用是燃烧提供能量和不完全燃烧制取CO,用CO还原铁的化合物,故 B 选项错误;
C、在高炉中冶炼出来的是生铁,是含碳的铁合金,故 C选项正确;
D、一氧化碳有毒,不能直接排放,故D选项错误。
故选C。
红色粉末(氧化铁)逐渐变成黑色
澄清的石灰水逐渐变浑浊
尾气燃烧产生蓝色火焰
实验现象:
铁的冶炼
实验室用一氧化碳还原氧化铁的装置
化学方程式:
3CO+Fe2O3 2Fe+3CO2
高温
回顾实验,回答下面问题:
实验前为什么先通一氧化碳?
问题1:
如何处理尾气?
问题2:
分析工业炼铁的原理。
问题3:
分析原料产物是否为纯净物。
问题4:
答:为了排净装置中的空气,防止加热时发生爆炸。
答:利用一氧化碳的还原性,把铁从化合物中还原出来。
答:尾气中含有一氧化碳要点燃或收集再利用。
答:原料不是纯净物,矿石中含有杂质。
高炉炼铁和实验室炼铁有什么区别?其产物是纯铁吗?
Fe2O3+3CO 2Fe+3CO2
高温
两者的产物不同。工业炼铁得到的是生铁,实验室得到的是纯铁。
设备不同。工业炼铁设备是高炉,实验室用玻璃管。
对环境影响不同。高炉炼铁对环境影响大,实验室对环境影响小。
操作难易程度不同。高炉炼铁工艺复杂,实验室操作简单。
铁的冶炼
生铁
可经过吹氧冶炼等工序生产钢,含碳量降至0.03%~2%的铁合金
含有2%~4.3%的碳及少量磷和硫的铁合金
硬而脆,不利于加工
【例1】(2023秋·陕西咸阳·九年级统考期末)下列有关模拟工业炼铁的叙述不正确的是( )
D
A.赤铁矿的主要成分是Fe2O3
B.硬质玻璃管中红色固体变为黑色
C.用燃着的酒精灯可防止CO污染空气
D.实验时应先点燃酒精喷灯后再通CO
【详解】A、赤铁矿的主要成分是Fe2O3,故A正确;
B、一氧化碳和氧化铁高温生成铁和二氧化碳,硬质玻璃管中红色固体变为黑色,故B正确;
C、一氧化碳具有可燃性,用燃着的酒精灯可防止CO污染空气,故C正确;
D、为防止发生爆炸,实验时应先通CO后再点燃酒精喷灯,故D不正确。
故选D。
涉及杂质问题的计算
纯净物的质量 = 不纯物质的总质量×纯度
纯度= ×100%
纯净物的质量
不纯物质的总质量
在实际生产时,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题。
含杂质的计算一般做法如下:
第二步,依据化学方程式,根据已知纯物质的质量计算未知纯物质的质量;
第一步,将含杂质的物质质量转化成纯净物的质量;
第三步,将纯物质转化成杂质物质的质量。
不纯物质的质量=纯净物的质量 ÷纯度
【例1】(2023秋·河北邢台·九年级校考期末)某炼铁厂用赤铁矿石冶炼生铁。若要炼出1120t含铁90%的生铁,需要含氧化铁80%的赤铁矿石的质量是( )
A.1500 t B. 1440 t C. 1800 t D. 1980 t
【详解】设理论上需要含氧化铁80%的赤铁矿石的质量为x
x=1800t
故选C
C
热分解法:
适用于金属活动性弱的,在常见金属活动性顺序的右端区域
物理提取:
其密度很大,用多次淘洗法去掉矿粒,泥沙等杂质,便可得到
钾 钙 钠 镁 铝 锌 铁 锡 铅 (氢) 铜 汞 银 铂 金
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
热还原法:
适用于金属活动性比较强,在常见金属活动性顺序中居于中间区域(Zn~Cu)
电解法:
一般用于金属活动性顺序中铝及铝以前的金属冶炼
冶炼金属的方法
1.(2023春·九年级课时练习)下列物质中不是炼铁高炉中投放的基本原料的是( )
A.铁矿石 B.石灰石 C.焦炭 D.生铁
【详解】A、铁矿石是炼铁高炉中投入的基本原料,A不符合题意;
B、石灰石是炼铁高炉中投入的基本原料,作用是将二氧化硅转化成炉渣而除掉,B不符合题意;
C、焦炭是炼铁高炉中投入的基本原料,作用是通过热量,产生还原剂一氧化碳,C不符合题意;
D、生铁是高炉炼铁的产品,不是原料,D符合题意。
综上所述:选择D。
D
2.(2023春·重庆北碚·九年级西南大学附中校考开学考试)中国高铁是一张国家名片,工业中常利用赤铁矿来炼铁,下列说法中正确的是( )
A.地壳中含量最高的金属元素是铁元素
B.高炉炼铁得到的产品是纯铁
C.炼铁过程中,氧化铁体现了还原性
D.高炉炼铁时加入石灰石可将杂质二氧化硅转化为炉渣
【详解】A、地壳中含量前四位的元素(由高到低)为:O、Si、Al、Fe,则含量最高的金属元素是铝元素,故选项说法错误;
B、高炉炼铁得到的铁中含有杂质,属于混合物,不是纯铁,故选项说法错误;
C、工业中通过赤铁矿炼铁的原理为Fe2O3与CO在高温下反应产生Fe,CO将氧化铁还原为铁,体现了还原性,故选项说法错误;
D、石灰石的主要成分是碳酸钙,碳酸钙能与杂质二氧化硅结合生成炉渣CaSiO3,从而达到除杂的目的,故选项说法正确。
故选D。
D
3.(2023·广西柳州·统考一模)某混合气体中可能含有H2、CO和CO2中的一种或几种,为检验其成分,小明同学按照下图装置进行实验时观察到红棕色固体变黑,澄清石灰水变浑浊,由此可知混合气体的组成情况可能有( )
A.2种 B.3种 C.4种 D.5种
D
【详解】实验时观察到红棕色固体变黑,说明含有氢气或一氧化碳,澄清石灰水变浑浊,可能含有二氧化碳,混合气体的组成情况可能有:1.氢气、二氧化碳,2.氢气、一氧化碳,3.一氧化碳、二氧化碳,4.氢气、一氧化碳、二氧化碳,5.一氧化碳共5种情况,故选D。
4.(2023秋·河北石家庄·九年级石家庄市第四十二中学校考期末)下列有关金属材料的说法正确的是( )
A.铁矿石是一种铁合金 B.氧化铁属于金属材料
C.生铁的含碳量高于钢 D.自然界中的金属都以化合物的形式存在
【详解】A、铁矿石不是铁合金,故说法错误;
B、氧化铁是铁的氧化物,不是金属材料,故说法错误;
C、生铁和钢都是铁合金,其中含碳量较高的是生铁,故说法正确;
D、少数不活泼金属以单质形式存在,如金、银等,故说法错误。
故选C。
C
5.(2022秋·江苏徐州·九年级竞赛)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。”(注:炉甘石的主要成分是碳酸锌)火法炼锌主要发生的化学反应是 ,下列说法正确的是( )
A.X的化学式是CO2
B.“逐层用煤炭饼垫盛”是为了燃烧提供高温
C.反应前后固体的质量不变
D.“罐中炉甘石熔化成团”,团的主要成分是锌
【详解】A、由质量守恒定律:X的化学式为CO,故选项说法错误;
B、反应的原理是火法炼锌主要发生的化学反应方程式为:
,碳是反应物,逐层用煤炭饼垫盛,是为了使碳与碳酸锌充分反应,故选项说法错误;
C、反应后有气体生成,由质量守恒定律,反应前后固体的质量减少,故选项说法错误;
D、罐中炉甘石熔化成团,团的主要成分是生成的锌,故选项说法正确。
故选D。
D
6.(2020·山东青岛·校考一模)早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
(1)请写出工业炼铁的反应方程式:_______________________________。
(2)实验开始时要先通入CO,目的是
__________________________________________________________________。
排净装置内的空气,防止一氧化碳与空气混合加热爆炸
6.(2020·山东青岛·校考一模)早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
(3)实验中A装置的实验现象是:B装置可观察到的现象是____________________。右边导气管口放置点燃的酒精灯的目的是
__________________________________________。
澄清石灰水变浑浊
处理尾气,防止一氧化碳污染环境
6.(2020·山东青岛·校考一模)早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
(4)小刚通过实验测定样品中氧化铁的质量分数,他称取了25g样品,通入一氧化碳至反应结束后,称得B装置增加了13.2g,试根据B装置的变化数据,计算出样品中氧化铁的质量分数(写出计算过程)。
课题3
金属的利用与保护
第1课时
金属资源的概况
铁的冶炼
炼铁原理
工业炼铁设备:炼铁高炉
工业炼铁原料:铁矿石、焦炭、石灰石
含杂质物质的计算
单质
化合物
同课章节目录
