2022-2023学年人教版九年级化学下册 第九单元复习《溶液》导学案(WORD版,含答案 )
文档属性
| 名称 | 2022-2023学年人教版九年级化学下册 第九单元复习《溶液》导学案(WORD版,含答案 ) |

|
|
| 格式 | zip | ||
| 文件大小 | 202.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-23 00:00:00 | ||
图片预览

文档简介
第九单元复习
【课时目标】
1.认识溶解现象,知道溶液是由溶质和溶剂组成的;知道水是最重要的溶剂,酒精、汽油等也是常见的溶剂。
2.了解饱和溶液和溶解度的含义,初步学会绘制和查阅溶解度曲线。
3.认识溶质质量分数的含义,能进行溶质质量分数的简单计算,并能进行化学方程式与溶质质量分数的综合计算;初步学会配制一定溶质质量分数的溶液。
重点:1.溶液、饱和溶液和溶解度的概念,固体溶解度曲线的含义与应用;2.溶液中溶质的质量分数及计算。
难点:1.溶解度概念的认识,固体溶解度曲线的含义与应用;2.配制一定溶质质量分数溶液的方法及操作等。
【学习活动】
任务一 溶液的概念和性质
1.近几年来,各种网红饮品店星罗棋布,成为各类潮人新时尚。下列常见饮品中,属于溶液的是( )
A.珍珠奶茶 B.奶盖咖啡 C.果粒橙汁 D.“雪碧”饮料
2.溶液在生产生活中有着广泛的应用,下列溶液中溶剂不是水的是( )
A.碘酒 B.盐酸 C.氯化钠溶液 D.酒精溶液
3.溶液与人们的生活息息相关。下列有关溶液说法正确的是( )
A.溶质可以是固体,也可以是液体或气体
B.将汽油与水充分混合,得到的是溶液
C.将10%的某溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.某饱和溶液降温到t℃析出晶体后,得到的溶液是t℃时的不饱和溶液
【变式1】下列有关溶液、乳浊液的描述中正确的是( )
A.油污溶于汽油得到的混合物属于乳浊液
B.可用过滤的方法将溶液和乳浊液中的分散物质分离出来
C.植物油分散到水中形成的混合物不稳定,久置后会分层
D.用洗洁精清洗油脂得到的混合物属于溶液
任务二 饱和溶液和不饱和溶液
4.下列说法中正确的是( )
A.含溶质较多的溶液一定是饱和溶液
B.饱和溶液一定是浓溶液
C.不能再溶解溶质的溶液一定是饱和溶液
D.有固体溶质与溶液共存的溶液一定是该温度下该固体的饱和溶液
5.30℃时,往100 g硝酸钾溶液中加入10g硝酸钾晶体,充分搅拌后,尚有部分晶体未溶,稍加热后晶体全部溶解,试判断下列说法中正确的是( )
A.搅拌后及加热前一定是饱和溶液
B.搅拌后及加热前一定是不饱和溶液
C.加热后一定是饱和溶液
D.加热后一定是不饱和溶液
6.下列关于饱和溶液和结晶的说法正确的是( )
A.将稀盐酸在敞口容器中加热蒸干水分可得HCl晶体
B.将硝酸钾的热饱和溶液降低温度后可得硝酸钾晶体
C.NaCl的近饱和溶液可通过升高温度的方法得到饱和溶液
D.通过将CaO加入水中的方法可以得到CaO的饱和溶液
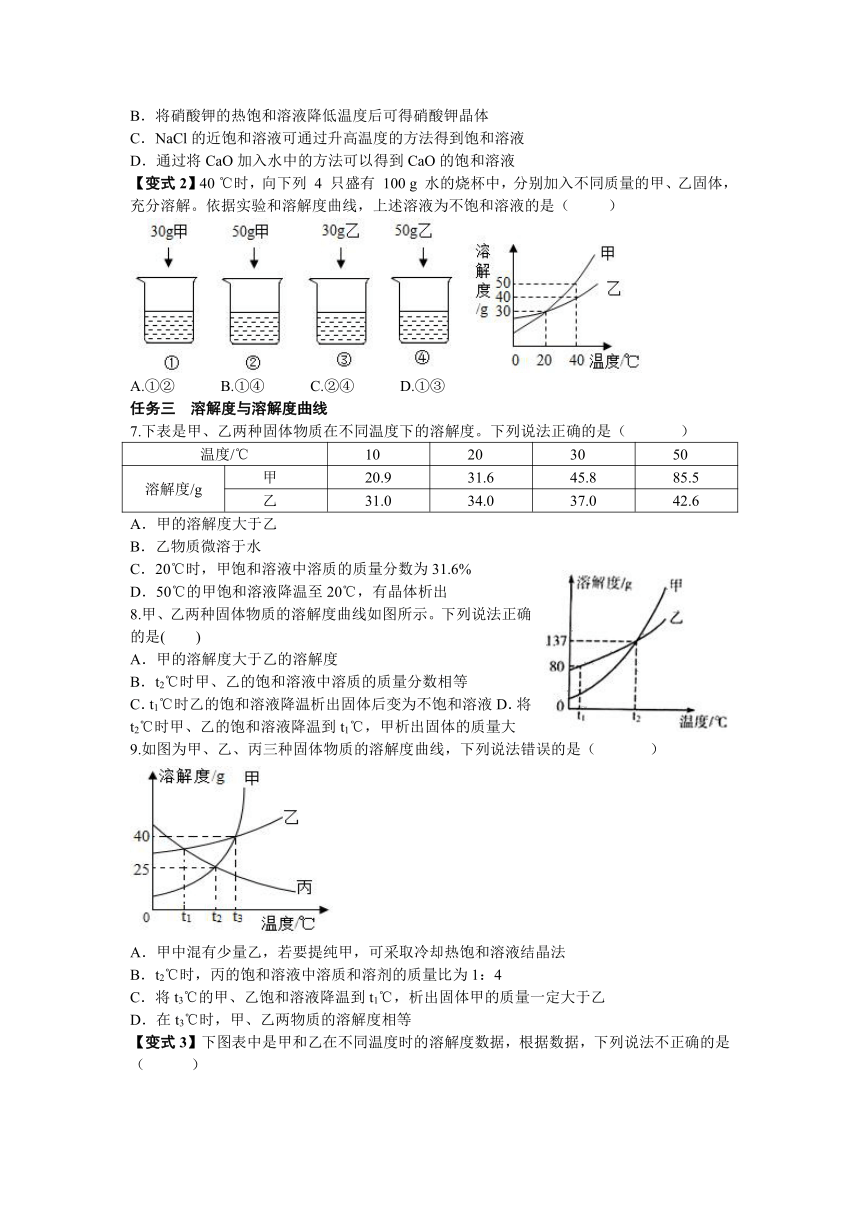
【变式2】40 ℃时,向下列 4 只盛有 100 g 水的烧杯中,分别加入不同质量的甲、乙固体,充分溶解。依据实验和溶解度曲线,上述溶液为不饱和溶液的是( )
A.①② B.①④ C.②④ D.①③
任务三 溶解度与溶解度曲线
7.下表是甲、乙两种固体物质在不同温度下的溶解度。下列说法正确的是( )
温度/℃ 10 20 30 50
溶解度/g 甲 20.9 31.6 45.8 85.5
乙 31.0 34.0 37.0 42.6
A.甲的溶解度大于乙
B.乙物质微溶于水
C.20℃时,甲饱和溶液中溶质的质量分数为31.6%
D.50℃的甲饱和溶液降温至20℃,有晶体析出
8.甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.t2℃时甲、乙的饱和溶液中溶质的质量分数相等
C.t1℃时乙的饱和溶液降温析出固体后变为不饱和溶液D.将t2℃时甲、乙的饱和溶液降温到t1℃,甲析出固体的质量大
9.如图为甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
A.甲中混有少量乙,若要提纯甲,可采取冷却热饱和溶液结晶法
B.t2℃时,丙的饱和溶液中溶质和溶剂的质量比为1:4
C.将t3℃的甲、乙饱和溶液降温到t1℃,析出固体甲的质量一定大于乙
D.在t3℃时,甲、乙两物质的溶解度相等
【变式3】下图表中是甲和乙在不同温度时的溶解度数据,根据数据,下列说法不正确的是( )
温度/℃ 10 30 50 70
溶解度/g 甲 33.3 41.4 50.4 55.2
乙 20.9 45.8 85.5 110
A.由上表可知,50℃时,甲的溶解度为50.4g
B.甲、乙溶解度受温度的影响较大的是乙
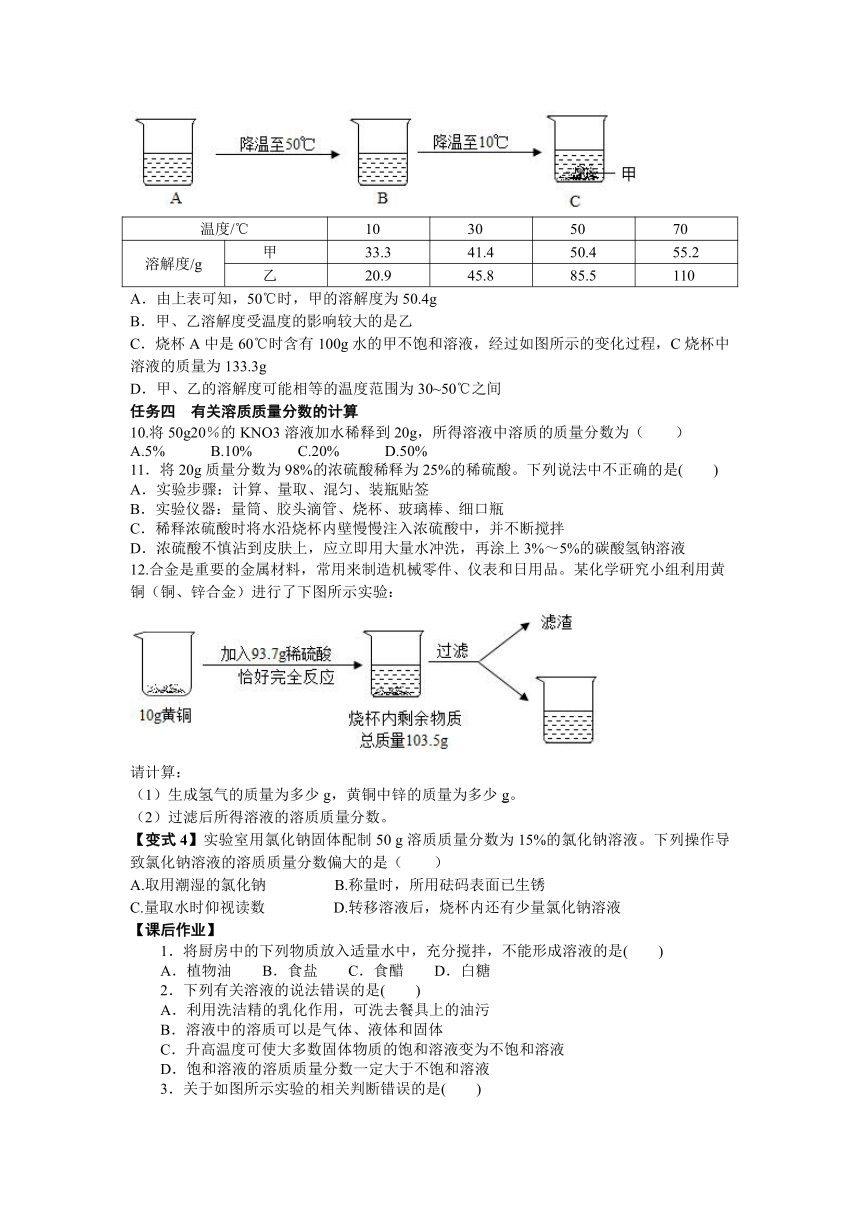
C.烧杯A中是60℃时含有100g水的甲不饱和溶液,经过如图所示的变化过程,C烧杯中溶液的质量为133.3g
D.甲、乙的溶解度可能相等的温度范围为30~50℃之间
任务四 有关溶质质量分数的计算
10.将50g20%的KNO3溶液加水稀释到20g,所得溶液中溶质的质量分数为( )
A.5% B.10% C.20% D.50%
11.将20g质量分数为98%的浓硫酸稀释为25%的稀硫酸。下列说法中不正确的是( )
A.实验步骤:计算、量取、混匀、装瓶贴签
B.实验仪器:量筒、胶头滴管、烧杯、玻璃棒、细口瓶
C.稀释浓硫酸时将水沿烧杯内壁慢慢注入浓硫酸中,并不断搅拌
D.浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
12.合金是重要的金属材料,常用来制造机械零件、仪表和日用品。某化学研究小组利用黄铜(铜、锌合金)进行了下图所示实验:
请计算:
(1)生成氢气的质量为多少g,黄铜中锌的质量为多少g。
(2)过滤后所得溶液的溶质质量分数。
【变式4】实验室用氯化钠固体配制50 g溶质质量分数为15%的氯化钠溶液。下列操作导致氯化钠溶液的溶质质量分数偏大的是( )
A.取用潮湿的氯化钠 B.称量时,所用砝码表面已生锈
C.量取水时仰视读数 D.转移溶液后,烧杯内还有少量氯化钠溶液
【课后作业】
1.将厨房中的下列物质放入适量水中,充分搅拌,不能形成溶液的是( )
A.植物油 B.食盐 C.食醋 D.白糖
2.下列有关溶液的说法错误的是( )
A.利用洗洁精的乳化作用,可洗去餐具上的油污
B.溶液中的溶质可以是气体、液体和固体
C.升高温度可使大多数固体物质的饱和溶液变为不饱和溶液
D.饱和溶液的溶质质量分数一定大于不饱和溶液
3.关于如图所示实验的相关判断错误的是( )
A.固体X可能是NaOH
B.固体X可能是NH4NO3
C.Ca(OH)2溶解度:①>②
D.Ca(OH)2质量分数:①=③
4.小明自制了一杯蔗糖水(无固体剩余),用于缓解运动后出现的低血糖症状,之后他结合下表蔗糖的溶解度数据,归纳出以下问题,其中正确的是( )
温度/℃ 0 10 20 40 60 80 100
溶解度/g 182 191 204 238 287 362 487
A.配制的蔗糖溶液下层比上层甜
B.降温,糖水中一定有晶体析出
C.20℃时,蔗糖饱和溶液质量一定为304g
D.升温,糖水中蔗糖的质量分数不变
5.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.甲和丙都属于易溶物质
B.溶解度大小关系:甲>乙>丙
C.等质量甲、乙两种物质的溶液从t2℃降到t1℃时,析出晶体最多的是甲
D.三种物质的饱和溶液从t2℃降到t1℃,所得溶液溶质质量分数:乙>甲>丙
6.将200g溶有物质M的溶液从95℃降低到10℃,不同温度时析出溶质M的质量如下表所示。下列说法正确的是( )
温度/℃ 95 90 80 30 10
析出M的质量/g 0 0 15 100 116
A.95℃时该溶液为饱和溶液
B.M的溶解度随温度的升高而减小
C.30℃时析出M后所得溶液中含100g水
D.从M的不饱和溶液中析出M可采用先蒸发溶剂、再冷却结晶的方法
7.现有编号为①、②、③的三个烧杯中均分别盛有100克水,20℃时向三个烧杯中分别加入36克、56克、76克的同种物质,充分溶解,实验结果如图所示,下列判断正确的是( )
A.①中所得溶液一定是不饱和溶液
B.②③中所得溶液溶质的质量分数相等
C.若②中溶液升温到30℃,溶液的质量一定不变
D.若③中溶液恒温蒸发,溶质的质量分数一定变大
8.甲、乙、丙三种固体物质的溶解度曲线如图1所示,请回答下列问题:
(1)t2℃时,甲物质的溶解度为________。
(2)t2℃时,将50g 甲物质放入50g水中充分溶解,所得溶液是________(填“饱和”或“不饱和”)溶液。
(3)将t2℃时的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液溶质质量分数由大到小的顺序为________。
(4)如图2,t1℃时,若向烧杯中加入足量的________(填字母)并使之充分溶解,在试管中可观察到有晶体析出。
A.氯化钠 B.氢氧化钠 C.硝酸铵
9.实验室按下图步骤配制100g质量分数为22%的蔗糖溶液。
回答下列问题:
(1)所需蔗糖的质量为___________。
(2)用规格为__________(填“50”、“100”或“500”)mL的量筒量取________mL蒸馏水倒入盛有蔗糖的烧杯中进行溶解。(水的密度约为1g/cm3)。
(3)溶解时玻璃棒的作用是_________。
(4)下列情况会导致所配溶液中溶质的质量分数偏高的是_________(填字母序号)。
A.蔗糖中混有少量杂质
B.称量时蔗糖和砝码位置放反了(使用了游码)
C.用于溶解蔗糖的烧杯洗净后残留有少量的水
D.用量筒量取水时,俯视读数
10.某兴趣小组对石灰石样品进行如下实验分析:取12g样品放入烧杯中,将100g稀盐酸分4次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
次数 1 2 3 4
加入稀盐酸的质量/g 25 25 25 25
剩余固体的质量/g 8 4 2 2
求:
(1)样品中碳酸钙的质量为________g。
(2)第4次加入稀盐酸后所得溶液中CaCl2的质量分数。(计算结果保留0.1%)。
【评价与反思】___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
参考答案
【学习活动】1.D 2.A 3.A 【变式1】C 4.D 5.A 6.B 【变式2】D 7.D 8.B 9.C 【变式3】D 10.A 11.C 12.(1)0.2 6.5 (2)16.1% 【变式4】B
【课后作业】1.A 2.D 3.B 4.D 5.D 6.D 7.B 8.(1)60g (2)饱和 (3)乙>甲>丙 (4)B 9.(1)22g (2)100 78 (3)搅拌,加速溶解 (4)D 10.(1)10 (2)10.5%
【课时目标】
1.认识溶解现象,知道溶液是由溶质和溶剂组成的;知道水是最重要的溶剂,酒精、汽油等也是常见的溶剂。
2.了解饱和溶液和溶解度的含义,初步学会绘制和查阅溶解度曲线。
3.认识溶质质量分数的含义,能进行溶质质量分数的简单计算,并能进行化学方程式与溶质质量分数的综合计算;初步学会配制一定溶质质量分数的溶液。
重点:1.溶液、饱和溶液和溶解度的概念,固体溶解度曲线的含义与应用;2.溶液中溶质的质量分数及计算。
难点:1.溶解度概念的认识,固体溶解度曲线的含义与应用;2.配制一定溶质质量分数溶液的方法及操作等。
【学习活动】
任务一 溶液的概念和性质
1.近几年来,各种网红饮品店星罗棋布,成为各类潮人新时尚。下列常见饮品中,属于溶液的是( )
A.珍珠奶茶 B.奶盖咖啡 C.果粒橙汁 D.“雪碧”饮料
2.溶液在生产生活中有着广泛的应用,下列溶液中溶剂不是水的是( )
A.碘酒 B.盐酸 C.氯化钠溶液 D.酒精溶液
3.溶液与人们的生活息息相关。下列有关溶液说法正确的是( )
A.溶质可以是固体,也可以是液体或气体
B.将汽油与水充分混合,得到的是溶液
C.将10%的某溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.某饱和溶液降温到t℃析出晶体后,得到的溶液是t℃时的不饱和溶液
【变式1】下列有关溶液、乳浊液的描述中正确的是( )
A.油污溶于汽油得到的混合物属于乳浊液
B.可用过滤的方法将溶液和乳浊液中的分散物质分离出来
C.植物油分散到水中形成的混合物不稳定,久置后会分层
D.用洗洁精清洗油脂得到的混合物属于溶液
任务二 饱和溶液和不饱和溶液
4.下列说法中正确的是( )
A.含溶质较多的溶液一定是饱和溶液
B.饱和溶液一定是浓溶液
C.不能再溶解溶质的溶液一定是饱和溶液
D.有固体溶质与溶液共存的溶液一定是该温度下该固体的饱和溶液
5.30℃时,往100 g硝酸钾溶液中加入10g硝酸钾晶体,充分搅拌后,尚有部分晶体未溶,稍加热后晶体全部溶解,试判断下列说法中正确的是( )
A.搅拌后及加热前一定是饱和溶液
B.搅拌后及加热前一定是不饱和溶液
C.加热后一定是饱和溶液
D.加热后一定是不饱和溶液
6.下列关于饱和溶液和结晶的说法正确的是( )
A.将稀盐酸在敞口容器中加热蒸干水分可得HCl晶体
B.将硝酸钾的热饱和溶液降低温度后可得硝酸钾晶体
C.NaCl的近饱和溶液可通过升高温度的方法得到饱和溶液
D.通过将CaO加入水中的方法可以得到CaO的饱和溶液
【变式2】40 ℃时,向下列 4 只盛有 100 g 水的烧杯中,分别加入不同质量的甲、乙固体,充分溶解。依据实验和溶解度曲线,上述溶液为不饱和溶液的是( )
A.①② B.①④ C.②④ D.①③
任务三 溶解度与溶解度曲线
7.下表是甲、乙两种固体物质在不同温度下的溶解度。下列说法正确的是( )
温度/℃ 10 20 30 50
溶解度/g 甲 20.9 31.6 45.8 85.5
乙 31.0 34.0 37.0 42.6
A.甲的溶解度大于乙
B.乙物质微溶于水
C.20℃时,甲饱和溶液中溶质的质量分数为31.6%
D.50℃的甲饱和溶液降温至20℃,有晶体析出
8.甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.t2℃时甲、乙的饱和溶液中溶质的质量分数相等
C.t1℃时乙的饱和溶液降温析出固体后变为不饱和溶液D.将t2℃时甲、乙的饱和溶液降温到t1℃,甲析出固体的质量大
9.如图为甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
A.甲中混有少量乙,若要提纯甲,可采取冷却热饱和溶液结晶法
B.t2℃时,丙的饱和溶液中溶质和溶剂的质量比为1:4
C.将t3℃的甲、乙饱和溶液降温到t1℃,析出固体甲的质量一定大于乙
D.在t3℃时,甲、乙两物质的溶解度相等
【变式3】下图表中是甲和乙在不同温度时的溶解度数据,根据数据,下列说法不正确的是( )
温度/℃ 10 30 50 70
溶解度/g 甲 33.3 41.4 50.4 55.2
乙 20.9 45.8 85.5 110
A.由上表可知,50℃时,甲的溶解度为50.4g
B.甲、乙溶解度受温度的影响较大的是乙
C.烧杯A中是60℃时含有100g水的甲不饱和溶液,经过如图所示的变化过程,C烧杯中溶液的质量为133.3g
D.甲、乙的溶解度可能相等的温度范围为30~50℃之间
任务四 有关溶质质量分数的计算
10.将50g20%的KNO3溶液加水稀释到20g,所得溶液中溶质的质量分数为( )
A.5% B.10% C.20% D.50%
11.将20g质量分数为98%的浓硫酸稀释为25%的稀硫酸。下列说法中不正确的是( )
A.实验步骤:计算、量取、混匀、装瓶贴签
B.实验仪器:量筒、胶头滴管、烧杯、玻璃棒、细口瓶
C.稀释浓硫酸时将水沿烧杯内壁慢慢注入浓硫酸中,并不断搅拌
D.浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
12.合金是重要的金属材料,常用来制造机械零件、仪表和日用品。某化学研究小组利用黄铜(铜、锌合金)进行了下图所示实验:
请计算:
(1)生成氢气的质量为多少g,黄铜中锌的质量为多少g。
(2)过滤后所得溶液的溶质质量分数。
【变式4】实验室用氯化钠固体配制50 g溶质质量分数为15%的氯化钠溶液。下列操作导致氯化钠溶液的溶质质量分数偏大的是( )
A.取用潮湿的氯化钠 B.称量时,所用砝码表面已生锈
C.量取水时仰视读数 D.转移溶液后,烧杯内还有少量氯化钠溶液
【课后作业】
1.将厨房中的下列物质放入适量水中,充分搅拌,不能形成溶液的是( )
A.植物油 B.食盐 C.食醋 D.白糖
2.下列有关溶液的说法错误的是( )
A.利用洗洁精的乳化作用,可洗去餐具上的油污
B.溶液中的溶质可以是气体、液体和固体
C.升高温度可使大多数固体物质的饱和溶液变为不饱和溶液
D.饱和溶液的溶质质量分数一定大于不饱和溶液
3.关于如图所示实验的相关判断错误的是( )
A.固体X可能是NaOH
B.固体X可能是NH4NO3
C.Ca(OH)2溶解度:①>②
D.Ca(OH)2质量分数:①=③
4.小明自制了一杯蔗糖水(无固体剩余),用于缓解运动后出现的低血糖症状,之后他结合下表蔗糖的溶解度数据,归纳出以下问题,其中正确的是( )
温度/℃ 0 10 20 40 60 80 100
溶解度/g 182 191 204 238 287 362 487
A.配制的蔗糖溶液下层比上层甜
B.降温,糖水中一定有晶体析出
C.20℃时,蔗糖饱和溶液质量一定为304g
D.升温,糖水中蔗糖的质量分数不变
5.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.甲和丙都属于易溶物质
B.溶解度大小关系:甲>乙>丙
C.等质量甲、乙两种物质的溶液从t2℃降到t1℃时,析出晶体最多的是甲
D.三种物质的饱和溶液从t2℃降到t1℃,所得溶液溶质质量分数:乙>甲>丙
6.将200g溶有物质M的溶液从95℃降低到10℃,不同温度时析出溶质M的质量如下表所示。下列说法正确的是( )
温度/℃ 95 90 80 30 10
析出M的质量/g 0 0 15 100 116
A.95℃时该溶液为饱和溶液
B.M的溶解度随温度的升高而减小
C.30℃时析出M后所得溶液中含100g水
D.从M的不饱和溶液中析出M可采用先蒸发溶剂、再冷却结晶的方法
7.现有编号为①、②、③的三个烧杯中均分别盛有100克水,20℃时向三个烧杯中分别加入36克、56克、76克的同种物质,充分溶解,实验结果如图所示,下列判断正确的是( )
A.①中所得溶液一定是不饱和溶液
B.②③中所得溶液溶质的质量分数相等
C.若②中溶液升温到30℃,溶液的质量一定不变
D.若③中溶液恒温蒸发,溶质的质量分数一定变大
8.甲、乙、丙三种固体物质的溶解度曲线如图1所示,请回答下列问题:
(1)t2℃时,甲物质的溶解度为________。
(2)t2℃时,将50g 甲物质放入50g水中充分溶解,所得溶液是________(填“饱和”或“不饱和”)溶液。
(3)将t2℃时的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液溶质质量分数由大到小的顺序为________。
(4)如图2,t1℃时,若向烧杯中加入足量的________(填字母)并使之充分溶解,在试管中可观察到有晶体析出。
A.氯化钠 B.氢氧化钠 C.硝酸铵
9.实验室按下图步骤配制100g质量分数为22%的蔗糖溶液。
回答下列问题:
(1)所需蔗糖的质量为___________。
(2)用规格为__________(填“50”、“100”或“500”)mL的量筒量取________mL蒸馏水倒入盛有蔗糖的烧杯中进行溶解。(水的密度约为1g/cm3)。
(3)溶解时玻璃棒的作用是_________。
(4)下列情况会导致所配溶液中溶质的质量分数偏高的是_________(填字母序号)。
A.蔗糖中混有少量杂质
B.称量时蔗糖和砝码位置放反了(使用了游码)
C.用于溶解蔗糖的烧杯洗净后残留有少量的水
D.用量筒量取水时,俯视读数
10.某兴趣小组对石灰石样品进行如下实验分析:取12g样品放入烧杯中,将100g稀盐酸分4次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
次数 1 2 3 4
加入稀盐酸的质量/g 25 25 25 25
剩余固体的质量/g 8 4 2 2
求:
(1)样品中碳酸钙的质量为________g。
(2)第4次加入稀盐酸后所得溶液中CaCl2的质量分数。(计算结果保留0.1%)。
【评价与反思】___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
参考答案
【学习活动】1.D 2.A 3.A 【变式1】C 4.D 5.A 6.B 【变式2】D 7.D 8.B 9.C 【变式3】D 10.A 11.C 12.(1)0.2 6.5 (2)16.1% 【变式4】B
【课后作业】1.A 2.D 3.B 4.D 5.D 6.D 7.B 8.(1)60g (2)饱和 (3)乙>甲>丙 (4)B 9.(1)22g (2)100 78 (3)搅拌,加速溶解 (4)D 10.(1)10 (2)10.5%
同课章节目录
