化学(科粤版)九下参考课件:8.3 酸和碱的反应(共21张PPT)
文档属性
| 名称 | 化学(科粤版)九下参考课件:8.3 酸和碱的反应(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-23 00:00:00 | ||
图片预览








文档简介
(共21张PPT)
第八章 常见的酸、碱、盐
8.3 酸和碱的反应
1.理解酸和碱具有通性的原因。
2.认识复分解反应,知道中和反应是复分解反应的一种特殊形式。
3.能从微观粒子的角度认识酸碱中和反应,了解中和反应的实际应用。
教学目标
目 录/
1.
酸和碱的组成
2.
中和反应
3.
中和反应的应用
PART 01
酸和碱的组成
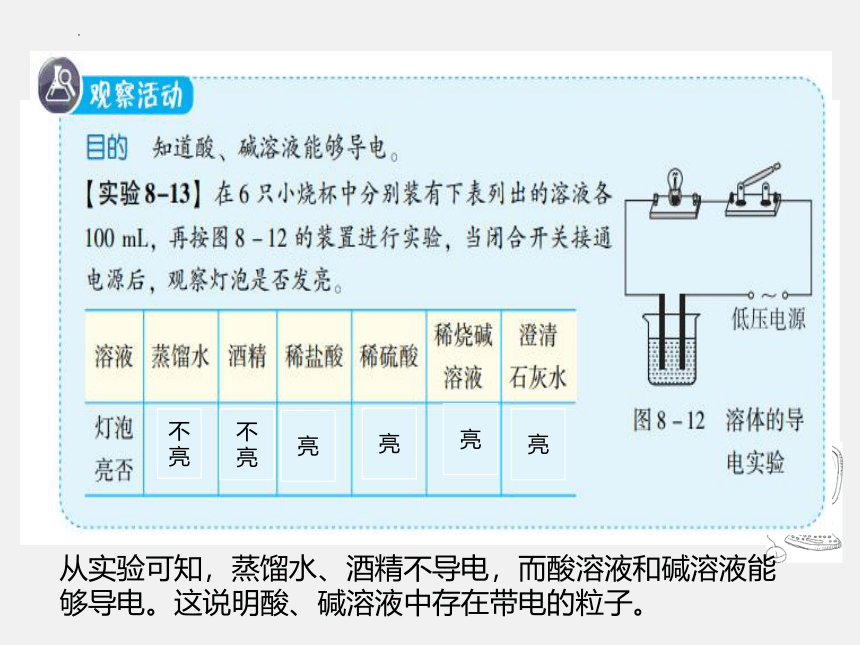
从实验可知,蒸馏水、酒精不导电,而酸溶液和碱溶液能够导电。这说明酸、碱溶液中存在带电的粒子。
不亮
不亮
亮
亮
亮
亮
分析---这些带电的粒子是什么
可见,酸溶液中的阳离子都是氢离子,对应的阴离子是各种酸的酸根离子。酸溶液中都含有氢离子,所以酸有相似的化学性质。碱溶液中的阴离子都是氢氧根离子,阳离子为金属离子。碱溶液中都含有氢氧根离子,所以碱有相似的化学性质。
PART 02
中和反应
编号 实验操作 实验现象
① 取3 mL稀氢氧化钠溶液于试管中,逐滴加入稀盐酸 无明显现象
② 取3 mL NaOH溶液于试管中,滴1、2滴酚酞溶液 溶液变红
③ 逐渐往NaOH溶液中滴稀盐酸,振荡 最初溶液颜色无明显变化,最后滴人一滴,溶液颜色突然消失
④ 向上述刚好褪色的溶液中再滴两滴NaOH溶液,振荡 溶液又变为红色
⑤ 再次滴入微量稀盐酸,振荡 溶液又变为无色
【结论】
NaOH 和HCI发生了化学反应,反应的化学方程式为:
NaOH+HCI=NaCI+HO,即酸和碱可以发生化学反应,生成盐和水。
酸跟碱生成盐和水的反应,叫作中和反应。
酸和碱的主要化学性质
概念解读-----复分解反应
链接教材P239讨论与交流
1.若用AB和CD分别表示两种化合物,如何表示复分解反应的通式
2.中和反应和复分解反应两者有什么关系 为什么
AB+CD=AC+BD
中和反应属于复分解反应,复分解反应包含中和反应。复分解反应是两种化合物互相交换成分生成另外两种化合物的反应;中和反应是酸跟碱生成盐和水的反应,故是复分解反应的一个特殊类型。金属氧化物和酸、酸和盐、碱和盐等的反应也是复分解反应。
链接教材P239讨论与交流
3.我们已经学习过化合、分解、置换、复分解等各种基本反应类型。
你能归纳出它们各自的特点,并准确判断某个具体化学反应属于什么基本反应类型吗 请举例说明。
化合反应 分解反应 置换反应 复分解反应
定义 由两种或两种以上的物质生成另一种物质的反应 一种物质生成两种或两种以上其他物质的反应 由一种单质与一种化合物反应,生成另一种单质与另一种化合物的反应 由两种化合物互相交换成分,生成另外两种化合物的反应
特点 多变一 一变多 单换单 双交换,价不变
PART 03
中和反应的应用
酸碱中和在日常的生产和生活中有广泛的应用。
①改良酸性或碱性的土壤:向放干的鱼塘底撒熟石灰中和鱼塘底泥中过多的有机酸;用熟石灰改良酸性土壤。
②废水处理:废水中的酸性物质(如硫酸、盐酸)要先用碱性物质(如烧碱、熟石灰)将其中和成中性后再排放,否则会造成水体污染。
③医药应用:蚂蚁、蚊虫叮咬后涂抹弱碱性的肥皂水、小苏打水等减轻疼痛;胃酸(主要是盐酸)过多的病人服用碱性的“胃舒平”[主要成分为Al(OH)3]或小苏打片(主要成分为NaHCO3)进行治疗。
④调节溶液的酸碱性:实验时经常需要将溶液的pH控制在某一特定范围内。当溶液的酸性或碱性太强或太弱时,可以加适当的碱或酸进行调节。
课堂练习
1.中和反应在生产和生活中有着广泛的应用。下列应用与中和反应原理一定无关的是( )A.服用含氢氧化铝的药物治疗胃酸过多症
B.用稀硫酸处理印染厂的碱性废水
C.在工业上,用盐酸来除铁锈
D.在蚊虫叮咬处涂抹稀氨水减轻痛痒
【解答】解:A.服用含氢氧化铝的药物治疗胃酸过多症,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。B.用稀硫酸处理印染厂的碱性废水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。C.在工业上,用盐酸来除铁锈,是铁锈的主要成分氧化铁与稀盐酸反应,该反应不是酸与碱反应生成盐和水的反应,不属于中和反应,故选项正确。D.在蚊虫叮咬处抹稀氨水以减轻瘙痒疼痛,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。故选:C。
2.某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是( )
A.向图中c点所示溶液中滴加无色酚酞,溶液不变色
B.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯
C.图中a点所示溶液中,含有的溶质是NaCl和NaOH
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应
【解答】解:A.c点溶液显碱性,向图中c点所示溶液中滴加无色酚酞,溶液变红色,该选项说法不正确;B.实验过程中,溶液pH由小于7逐渐升高至大于7,是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的烧杯中,该选项说法不正确;C.图中a点所示溶液中,含有的溶质是NaCl和HCl,该选项说法不正确;D.由a点到b点的pH变化过程证明酸和碱发生了中和反应,这是因为过程中溶液由显酸性变成显中性,该选项说法正确。故选:D。
3.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。由此分析下列说法正确的是( )
A.反应前后阴、阳离子的总数目不变 B.反应前后溶剂质量不变
C.反应后溶液呈中性
D.反应前后元素种类发生了变化
【解答】解:A.由二者恰好完全反应的微观示意图,可以看出,反应的实质是氢离子和氢氧根离子结合生成水分子,反应前后阴、阳离子的总数目减少,故选项说法错误。B.由二者恰好完全反应的微观示意图,可以看出,反应的实质是氢离子和氢氧根离子结合生成水分子,反应后溶剂质量增加,故选项说法错误。C.由二者恰好完全反应的微观示意图,可以看出,反应的实质是氢离子和氢氧根离子结合生成水分子,反应后溶液为氯化钠溶液,呈中性,故选项说法正确。D.化学反应前后元素种类不变,故选项说法错误。故选:C。
感谢聆听
第八章 常见的酸、碱、盐
8.3 酸和碱的反应
1.理解酸和碱具有通性的原因。
2.认识复分解反应,知道中和反应是复分解反应的一种特殊形式。
3.能从微观粒子的角度认识酸碱中和反应,了解中和反应的实际应用。
教学目标
目 录/
1.
酸和碱的组成
2.
中和反应
3.
中和反应的应用
PART 01
酸和碱的组成
从实验可知,蒸馏水、酒精不导电,而酸溶液和碱溶液能够导电。这说明酸、碱溶液中存在带电的粒子。
不亮
不亮
亮
亮
亮
亮
分析---这些带电的粒子是什么
可见,酸溶液中的阳离子都是氢离子,对应的阴离子是各种酸的酸根离子。酸溶液中都含有氢离子,所以酸有相似的化学性质。碱溶液中的阴离子都是氢氧根离子,阳离子为金属离子。碱溶液中都含有氢氧根离子,所以碱有相似的化学性质。
PART 02
中和反应
编号 实验操作 实验现象
① 取3 mL稀氢氧化钠溶液于试管中,逐滴加入稀盐酸 无明显现象
② 取3 mL NaOH溶液于试管中,滴1、2滴酚酞溶液 溶液变红
③ 逐渐往NaOH溶液中滴稀盐酸,振荡 最初溶液颜色无明显变化,最后滴人一滴,溶液颜色突然消失
④ 向上述刚好褪色的溶液中再滴两滴NaOH溶液,振荡 溶液又变为红色
⑤ 再次滴入微量稀盐酸,振荡 溶液又变为无色
【结论】
NaOH 和HCI发生了化学反应,反应的化学方程式为:
NaOH+HCI=NaCI+HO,即酸和碱可以发生化学反应,生成盐和水。
酸跟碱生成盐和水的反应,叫作中和反应。
酸和碱的主要化学性质
概念解读-----复分解反应
链接教材P239讨论与交流
1.若用AB和CD分别表示两种化合物,如何表示复分解反应的通式
2.中和反应和复分解反应两者有什么关系 为什么
AB+CD=AC+BD
中和反应属于复分解反应,复分解反应包含中和反应。复分解反应是两种化合物互相交换成分生成另外两种化合物的反应;中和反应是酸跟碱生成盐和水的反应,故是复分解反应的一个特殊类型。金属氧化物和酸、酸和盐、碱和盐等的反应也是复分解反应。
链接教材P239讨论与交流
3.我们已经学习过化合、分解、置换、复分解等各种基本反应类型。
你能归纳出它们各自的特点,并准确判断某个具体化学反应属于什么基本反应类型吗 请举例说明。
化合反应 分解反应 置换反应 复分解反应
定义 由两种或两种以上的物质生成另一种物质的反应 一种物质生成两种或两种以上其他物质的反应 由一种单质与一种化合物反应,生成另一种单质与另一种化合物的反应 由两种化合物互相交换成分,生成另外两种化合物的反应
特点 多变一 一变多 单换单 双交换,价不变
PART 03
中和反应的应用
酸碱中和在日常的生产和生活中有广泛的应用。
①改良酸性或碱性的土壤:向放干的鱼塘底撒熟石灰中和鱼塘底泥中过多的有机酸;用熟石灰改良酸性土壤。
②废水处理:废水中的酸性物质(如硫酸、盐酸)要先用碱性物质(如烧碱、熟石灰)将其中和成中性后再排放,否则会造成水体污染。
③医药应用:蚂蚁、蚊虫叮咬后涂抹弱碱性的肥皂水、小苏打水等减轻疼痛;胃酸(主要是盐酸)过多的病人服用碱性的“胃舒平”[主要成分为Al(OH)3]或小苏打片(主要成分为NaHCO3)进行治疗。
④调节溶液的酸碱性:实验时经常需要将溶液的pH控制在某一特定范围内。当溶液的酸性或碱性太强或太弱时,可以加适当的碱或酸进行调节。
课堂练习
1.中和反应在生产和生活中有着广泛的应用。下列应用与中和反应原理一定无关的是( )A.服用含氢氧化铝的药物治疗胃酸过多症
B.用稀硫酸处理印染厂的碱性废水
C.在工业上,用盐酸来除铁锈
D.在蚊虫叮咬处涂抹稀氨水减轻痛痒
【解答】解:A.服用含氢氧化铝的药物治疗胃酸过多症,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。B.用稀硫酸处理印染厂的碱性废水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。C.在工业上,用盐酸来除铁锈,是铁锈的主要成分氧化铁与稀盐酸反应,该反应不是酸与碱反应生成盐和水的反应,不属于中和反应,故选项正确。D.在蚊虫叮咬处抹稀氨水以减轻瘙痒疼痛,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。故选:C。
2.某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是( )
A.向图中c点所示溶液中滴加无色酚酞,溶液不变色
B.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯
C.图中a点所示溶液中,含有的溶质是NaCl和NaOH
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应
【解答】解:A.c点溶液显碱性,向图中c点所示溶液中滴加无色酚酞,溶液变红色,该选项说法不正确;B.实验过程中,溶液pH由小于7逐渐升高至大于7,是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的烧杯中,该选项说法不正确;C.图中a点所示溶液中,含有的溶质是NaCl和HCl,该选项说法不正确;D.由a点到b点的pH变化过程证明酸和碱发生了中和反应,这是因为过程中溶液由显酸性变成显中性,该选项说法正确。故选:D。
3.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。由此分析下列说法正确的是( )
A.反应前后阴、阳离子的总数目不变 B.反应前后溶剂质量不变
C.反应后溶液呈中性
D.反应前后元素种类发生了变化
【解答】解:A.由二者恰好完全反应的微观示意图,可以看出,反应的实质是氢离子和氢氧根离子结合生成水分子,反应前后阴、阳离子的总数目减少,故选项说法错误。B.由二者恰好完全反应的微观示意图,可以看出,反应的实质是氢离子和氢氧根离子结合生成水分子,反应后溶剂质量增加,故选项说法错误。C.由二者恰好完全反应的微观示意图,可以看出,反应的实质是氢离子和氢氧根离子结合生成水分子,反应后溶液为氯化钠溶液,呈中性,故选项说法正确。D.化学反应前后元素种类不变,故选项说法错误。故选:C。
感谢聆听
