7.2-2 来自石油和煤的化工原料---苯 课件 (共18张PPT) 2022-2023学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 7.2-2 来自石油和煤的化工原料---苯 课件 (共18张PPT) 2022-2023学年高一下学期化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-24 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
7.2-2 来自石油和煤的化工原料
---苯
【温故知新】
乙烯
结构
物理性质
化学性质
制备
平面结构,键角:120°;结构简式CH2=CH2
无色,稍有气味的气体 ,密度比空气稍小,难溶于水
(1)可燃性
(2)可使酸性高锰酸钾溶液褪色
(3)加成反应
(4)加聚反应
CH3CH2OH
浓硫酸
170℃
CH2=CH2↑ + H2O
知识与技能
1、能记住苯的物理性质及重要的用途
2、 能记住苯分子的结构特点
3、会运用苯的化学性质解决问题
Michael Faraday
(1791-1867)
1825年,英国科学家法拉第在煤气灯中首先发现苯,并测得其含碳量,确定其最简式为CH;
1834年,德国科学家米希尔里希制得苯,并将其命名为苯;
之后,法国化学家日拉尔等确定其分子量为78,苯分子式为 。
C6H6
苯的发现
一、苯的物理性质
状态:
颜色:
气味:
毒性:
水溶性:
挥发性:
密度:
液态
无色
有特殊气味
有毒
不溶于水
易挥发
比水小
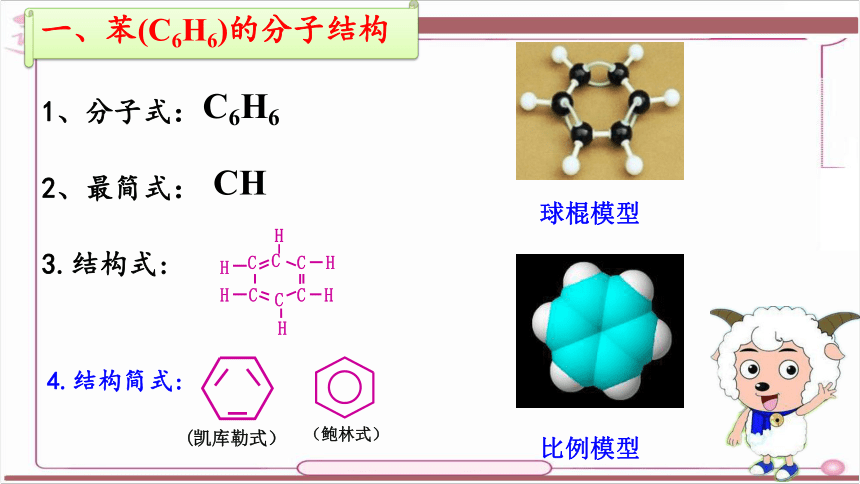
一、苯(C6H6)的分子结构
球棍模型
比例模型
1、分子式:
C6H6
CH
3.结构式:
2、最简式:
4.结构简式:
(12 个原子同一平面)
⑵碳碳键介于单键和双键之间的独特的键。
(既不是碳碳单键也不是碳碳双键)
⑴平面正六边形;
5、分子结构:
2C6H6 + 15O2 12CO2 + 6H2O
点燃
产生大量的黑烟,放出大量热量。
1、氧化反应 (可燃性)
三、苯的化学性质
甲烷
乙烯
苯
2、取代反应
(1)苯与液溴(纯溴)的取代反应
+ Br2
Br
+ HBr
FeBr3
溴苯
反应装置:
反应现象:
◇导管口有白雾,锥形瓶中滴入AgNO3溶液,出现浅黄色沉淀;
◇烧瓶中液体倒入盛有水的烧杯中,烧 杯底部出现油状的褐色液体。
注意:
①取代反应用卤素单质,不可用卤素溶液
②溴苯不溶于水,密度比水大的无色油状液体,(溶解了溴时呈褐色)
+ HNO3
浓硫酸
△
NO2
+ H2O
硝基苯
① 硝基苯是无色有苦杏仁味的油状液体,不溶于水,密度比水大,有毒。
③条件: 50-60oC 水浴加热
④浓H2SO4的作用 : 催化剂 吸水剂
注意事项:
(2)苯与浓硝酸的取代反应(硝化反应)
②加试剂顺序:浓硝酸→浓硫酸→苯
③与硫酸的取代反应:
苯+浓硫酸在加热的条件下反应后互溶
H
+ HO—SO3H
+ H—OH
SO3H
加热
3、加成反应
由于苯分子的碳碳键介于单键与双键之间,所以在一定条件下,苯仍可以与某些物质发生加成反应。
环已烷
苯跟氢气在镍的催化下,加热可生成环己烷:
+ 3H2
Ni
Δ
思考:苯能不能使酸性高猛酸钾、溴水褪色?
【思考与交流】
如何用实验证明苯中的碳碳键是一种介于单双键之间的一种特殊的键,而不是单双键交替
分层:上层无色
分层:下层紫色
分层:上层橙黄色
分层:下层无色
1ml溴水
2ml苯
振荡
2ml苯
1mlKMnO4(H+)溶液
振荡
烷烃 烯烃 苯
与Br2作用 Br2试剂
反应条件
反应类型
与酸性KMnO4作用
点燃 现象
结论
纯溴
溴水
纯溴
光照
取代
加成
催化剂
取代
现象
结论
不褪色
褪色
不褪色
不被 酸性KMnO4溶液氧化
易被酸性KMnO4溶液 氧化
苯不被酸性 KMnO4溶液氧化
火焰颜色浅,无烟
火焰明亮,有黑烟
火焰明亮,有浓烟
含碳量低
含碳量较高
含碳量高
(1)有机溶剂;
(2)重要的化工原料。
四、苯的用途
苯
小结
结构
物理性质
化学性质
平面结构,键角:120°;结构简式CH2=CH2
无色,有特殊气味的气体 ,密度比水小,难溶于水
(1)可燃性
(2)不可使酸性高锰酸钾溶液褪色
(3)加成反应
(4)取代反应
7.2-2 来自石油和煤的化工原料
---苯
【温故知新】
乙烯
结构
物理性质
化学性质
制备
平面结构,键角:120°;结构简式CH2=CH2
无色,稍有气味的气体 ,密度比空气稍小,难溶于水
(1)可燃性
(2)可使酸性高锰酸钾溶液褪色
(3)加成反应
(4)加聚反应
CH3CH2OH
浓硫酸
170℃
CH2=CH2↑ + H2O
知识与技能
1、能记住苯的物理性质及重要的用途
2、 能记住苯分子的结构特点
3、会运用苯的化学性质解决问题
Michael Faraday
(1791-1867)
1825年,英国科学家法拉第在煤气灯中首先发现苯,并测得其含碳量,确定其最简式为CH;
1834年,德国科学家米希尔里希制得苯,并将其命名为苯;
之后,法国化学家日拉尔等确定其分子量为78,苯分子式为 。
C6H6
苯的发现
一、苯的物理性质
状态:
颜色:
气味:
毒性:
水溶性:
挥发性:
密度:
液态
无色
有特殊气味
有毒
不溶于水
易挥发
比水小
一、苯(C6H6)的分子结构
球棍模型
比例模型
1、分子式:
C6H6
CH
3.结构式:
2、最简式:
4.结构简式:
(12 个原子同一平面)
⑵碳碳键介于单键和双键之间的独特的键。
(既不是碳碳单键也不是碳碳双键)
⑴平面正六边形;
5、分子结构:
2C6H6 + 15O2 12CO2 + 6H2O
点燃
产生大量的黑烟,放出大量热量。
1、氧化反应 (可燃性)
三、苯的化学性质
甲烷
乙烯
苯
2、取代反应
(1)苯与液溴(纯溴)的取代反应
+ Br2
Br
+ HBr
FeBr3
溴苯
反应装置:
反应现象:
◇导管口有白雾,锥形瓶中滴入AgNO3溶液,出现浅黄色沉淀;
◇烧瓶中液体倒入盛有水的烧杯中,烧 杯底部出现油状的褐色液体。
注意:
①取代反应用卤素单质,不可用卤素溶液
②溴苯不溶于水,密度比水大的无色油状液体,(溶解了溴时呈褐色)
+ HNO3
浓硫酸
△
NO2
+ H2O
硝基苯
① 硝基苯是无色有苦杏仁味的油状液体,不溶于水,密度比水大,有毒。
③条件: 50-60oC 水浴加热
④浓H2SO4的作用 : 催化剂 吸水剂
注意事项:
(2)苯与浓硝酸的取代反应(硝化反应)
②加试剂顺序:浓硝酸→浓硫酸→苯
③与硫酸的取代反应:
苯+浓硫酸在加热的条件下反应后互溶
H
+ HO—SO3H
+ H—OH
SO3H
加热
3、加成反应
由于苯分子的碳碳键介于单键与双键之间,所以在一定条件下,苯仍可以与某些物质发生加成反应。
环已烷
苯跟氢气在镍的催化下,加热可生成环己烷:
+ 3H2
Ni
Δ
思考:苯能不能使酸性高猛酸钾、溴水褪色?
【思考与交流】
如何用实验证明苯中的碳碳键是一种介于单双键之间的一种特殊的键,而不是单双键交替
分层:上层无色
分层:下层紫色
分层:上层橙黄色
分层:下层无色
1ml溴水
2ml苯
振荡
2ml苯
1mlKMnO4(H+)溶液
振荡
烷烃 烯烃 苯
与Br2作用 Br2试剂
反应条件
反应类型
与酸性KMnO4作用
点燃 现象
结论
纯溴
溴水
纯溴
光照
取代
加成
催化剂
取代
现象
结论
不褪色
褪色
不褪色
不被 酸性KMnO4溶液氧化
易被酸性KMnO4溶液 氧化
苯不被酸性 KMnO4溶液氧化
火焰颜色浅,无烟
火焰明亮,有黑烟
火焰明亮,有浓烟
含碳量低
含碳量较高
含碳量高
(1)有机溶剂;
(2)重要的化工原料。
四、苯的用途
苯
小结
结构
物理性质
化学性质
平面结构,键角:120°;结构简式CH2=CH2
无色,有特殊气味的气体 ,密度比水小,难溶于水
(1)可燃性
(2)不可使酸性高锰酸钾溶液褪色
(3)加成反应
(4)取代反应
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
