福建省福州市2022-2023学年高一上学期期末质量抽测化学试题(含答案)
文档属性
| 名称 | 福建省福州市2022-2023学年高一上学期期末质量抽测化学试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 561.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-24 14:33:52 | ||
图片预览



文档简介
福州市2022-2023学年高一上学期期末质量抽测
化学试卷
第Ⅰ卷(选择题 40分)
一、选择题(本大题有20小题,每小题2分,共40分.每小题只有一个选项符合题意)
1.《梦溪笔谈》中记载了“熬胆矾铁釜,久之亦化为铜”,该化学反应的基本类型是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.硫磺固体属于危险品,其运载交通工具上应贴的标识为( )
A. B. C. D.
3.化学与生活密切相关,下列说法正确的是( )
A.碳酸氢钠可做食品膨松剂
B.焰火中红色来源于钠盐灼烧
C.氯气与二氧化硫混合使用可以提高漂白效果
D.维生素C可将转化为,说明维生素C具有氧化性
4.嫦娥五号将月壤带回地球,科学家深入研究表明月壤富含Fe、He、、、FeO、CaO等物质,下列说法错误的是( )
A.月壤中的是金属氧化物 B.月壤中的CaO是碱性氧化物
C.月壤中的铁是电解质 D.月壤是混合物
5.放射性元素()可用在灵敏度极高的烟雾传感器中,下列说法正确的是( )
A.Am质子数146 B.Am核外电子数为241
C.Am质量数为336 D.Am中子数为146
6.下列实验操作规范且能达到目的是
实验目的 实验操作
A 称取2.0gNaOH固体 先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体
B 配制的溶液 称取固体1.580g,放入100mL容量瓶中,加水稀释到刻度线
C 证明与水反应放热 用棉花包裹后滴几滴水,棉花燃烧,说明该反应放出热量
D 比较钠、铁的活泼性 把钠块投入溶液中
A.A B.B C.C D.D
7.下列溶液中物质的量浓度最大的是( )
A.的溶液 B.的溶液
C.的溶液 D.的溶液
8.金刚石和石墨的结构如图,二者间的相互关系是( )
A.同种单质 B.同分异构体 C.同位素 D.同素异形体
9.在给定条件下,下列物质间所示转化可以实现的是( )
A. B. C. D.
10.黑火药发生爆炸的主要反应为,下列说法错误的是( )
A.中存在离子键和共价键 B.分子的结构式为N-N
C.固态是分子晶体 D.是离子化合物
11.当光束通过下列分散系时,能产生明显丁达尔效应的是( )
A.石灰乳 B.食盐水 C.医用酒精 D.氢氧化铝胶体
12.下列物质中的氯元素既能被氧化又能被还原的是( )
A.NaCl B.HCl C. D.
13.设为阿伏加德罗常数的值,下列说法正确的是( )
A.原子所含质子数为 B.分子所含原子数为
C.标准状况下,22.4L溴单质中分子数目为 D.溶液中,数目为
14.下列各组离子能大量共存的是( )
A.在饱和氯水中:、、 B.在氯化钠溶液中:、、
C.在酸性溶液中:、、 D.在碱性溶液中:、、
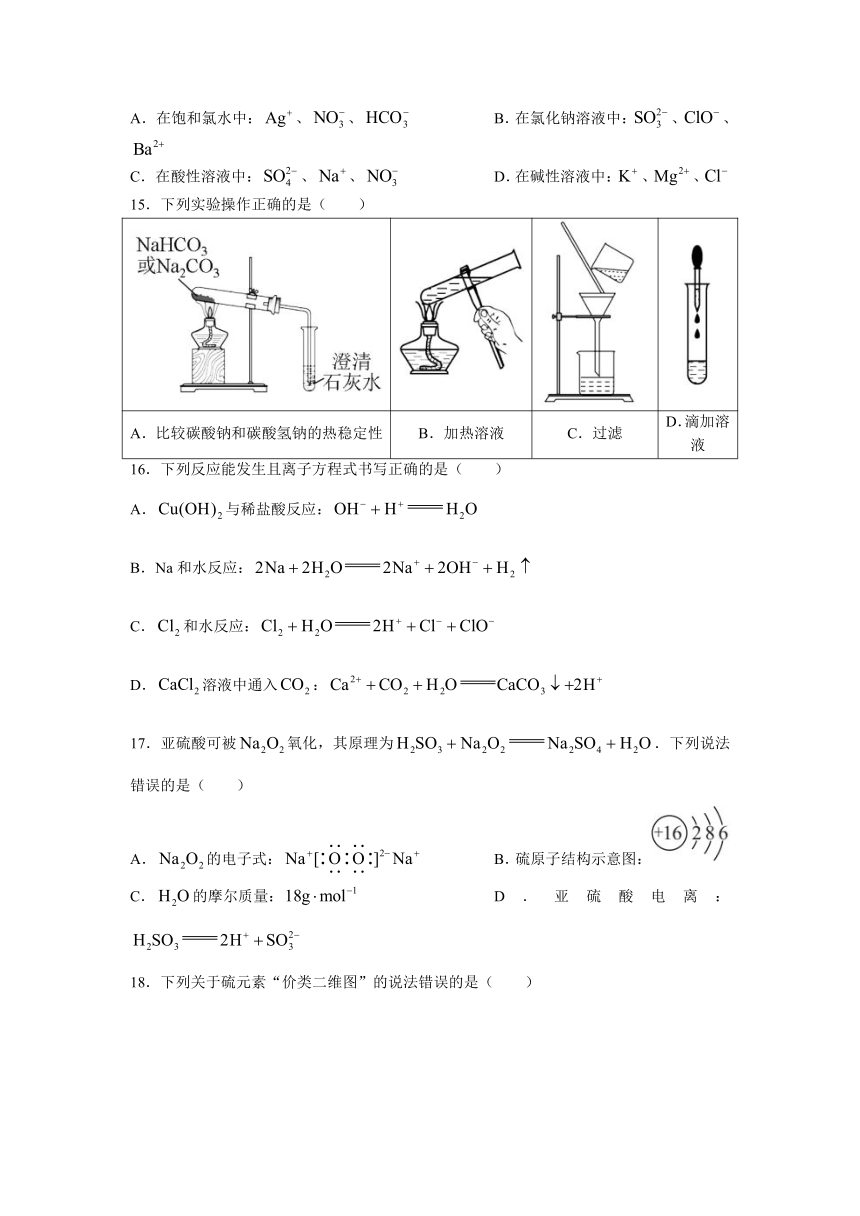
15.下列实验操作正确的是( )
A.比较碳酸钠和碳酸氢钠的热稳定性 B.加热溶液 C.过滤 D.滴加溶液
16.下列反应能发生且离子方程式书写正确的是( )
A.与稀盐酸反应:
B.Na和水反应:
C.和水反应:
D.溶液中通入:
17.亚硫酸可被氧化,其原理为.下列说法错误的是( )
A.的电子式: B.硫原子结构示意图:
C.的摩尔质量: D.亚硫酸电离:
18.下列关于硫元素“价类二维图”的说法错误的是( )
A.a→b硫元素由游离态转变为化合态
B.d溶液久置于空气中易变质
C.向f溶液中通入氯气可转化为含有g的溶液
D.将气体c通入石蕊溶液中,溶液变红
19.某化工厂基于“绿色化学”理念设计了如下治污工艺流程,下列说法错误的是( )
A.该流程可用于吸收
B.可用做该反应过程的催化剂
C.该过程的总反应为
D.由转化为的过程中,氧化剂和还原剂的物质的量之比为2∶1
20.海水资源综合利用的部分过程如下图所示,下列说法错误的是( )
海水 →淡化:淡水
→制盐工业:粗盐→精盐
→制溴工业:
→制镁工业:
A.蒸馏海水可获得淡水
B.为除粗盐中的、、,可依次加入足量的、、溶液
C.在制溴工业中,通过氧化、还原、再氧化的步骤实现了溴的富集
D.在制镁工业中,可用贝壳为原料生产石灰乳以沉淀
第Ⅱ卷(非选择题 60分)
二、非选择题(本大题共5小题,共60分)
21.(12分)下表是元素周期表的一部分,根据表中所给的10种元素,按要求使用化学用语作答.
族 周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
1 ①
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
(1)金属性最强的元素是_______(填元素符号);单质化学性质最稳定的元素是_______(填元素符号).
(2)①、⑥、⑨原子半径由大到小的顺序是_______(填元素符号),⑧最高价氧化物的水化物化学式为_______.
(3)⑦最高价氧化物的化学式是_______,已知该物质属于酸性氧化物,写出它与氢氧化钠溶液反应的化学方程式_______.
22.(12分)在严格控制用量的情况下,可作为食品添加剂.
(1)在制备食糖的过程中,用二氧化硫对糖汁进行熏制,可使糖汁脱色,该过程说明具有_______性.
(2)实验室制的原理为:.用与足量硫酸反应,理论上可制得标准状况下的体积为_______L.
(3)将通入高锰酸钾溶液中,请配平该方程式,将化学计量数标在横线处.
,若参加反应,转移的电子数为_______.
(4)的过度排放会造成_______等环境问题.为避免对环境造成不良影响,工业上常用的吸收剂为_______.
23.(10分)硫酸是常用的化工原料.
(1)目前工业上制硫酸的主要原料为空气和_______.
(2)浓硫酸的性质与稀硫酸有很大不同,取2g蔗糖放入大试管中,加2~3滴水,再加入约3mL浓硫酸,迅速搅拌,然后塞紧带玻璃导管的橡皮塞,将玻璃导管的另一端插入盛有品红溶液的试管中,溶液褪色.上述涉及颜色变化的反应体现了浓硫酸的_______性和_______性.
(3)用质量分数98%的浓硫酸(密度)配制的溶液,需量取浓_______mL(精确到0.1),配制过程需要用到下列仪器中的_______、_______(填序号).
若使用长期敞口放置的浓配制溶液,则配出的稀硫酸浓度_______(填“偏高”、“偏低”或“无影响”).
24.(13分)某化学兴趣小组在实验室中利用侯氏制碱法制备,进一步处理得到产品和,实验流程如图:
回答下列问题:
(1)实验室用大理石和稀盐酸制备,该反应的离子方程式是_______.为除掉中混有的HCl气体,可选用的最佳试剂是饱和_______溶液(填化学式).
(2)反应完成后,将混合物经操作I_______(填操作名称)得到固体和滤液.
①固体受热分解的化学方程式为_______,将气体A通过足量固体后生成的气体为_______(填化学式).
②向滤液中加入NaCl粉末,存在NaCl(固体)(溶液)→NaCl(溶液)(固体)过程.为使沉淀充分析出并分离,根据NaCl和溶解度曲线,需采用的操作为_______、_______、过滤、洗涤、干燥.
(3)在该工艺流程中可循环使用的物质为_______、_______.
25.(13分)某小组实验室制备氯气并探究其氧化性,实验装置如下图(夹持与加热装置已略).
(1)装置A为氯气的发生装置,写出该装置中发生反应的化学方程式_______,其中氧化剂和还原剂的物质的量之比为_______.
(2)C试管中为KI溶液,反应一段时间后,C处的实验现象为_______,反应的离子方程式为_______.取C中少量溶液于试管中,加,充分振荡并静置,观察到的现象是溶液分层,上层溶液为_______色,下层溶液为_______色.
(3)装置D中的溶液为_______,其作用是_______.
福州市2022-2023学年高一上学期期末质量抽测
化学科参考答案
一、单选题(每题2分,共40分)
序号 1 2 3 4 5 6 7 8 9 10
答案 C D A C D C B D B B
序号 11 12 13 14 15 16 17 18 19 20
答案 D C B C A B D A D B
二、填空题(共60分)
21.(12分)
(1)Na(填元素名称不得分)
Ar(填元素名称不得分)
(2)Al,Cl,H或Al>Cl>H(顺序写反不得分)
(填物质名称不得分)
(3)(填物质名称不得分)
(未配平或漏写条件得1分,下同)
22.(12分)
(1)漂白
(2)1.12
(3)2 5 2 2 1 2
或(2或2mol均不得分)
(4)酸雨(或土壤酸化、水体酸化等其它合理答案)
生石灰(或石灰乳、氨水等合理答案,氢氧化钠或氢氧化钠溶液不得分)
23.(10分)
(1)单质硫(S)或硫铁矿(化学式和名称均得分)
(2)脱水性 强氧化性(顺序颠倒不扣分)
(3)1.4 ②④ 偏低
24.(13分)
(1)
(2)过滤
①
(填物质名称不得分)
②蒸发浓缩、冷却结晶
(3)
(4)食盐水(或)
25.(13分)
(1)
1∶2
(3)溶液变成棕黄色(溶液变成棕色或褐色均可)(2分)
无色(或浅黄色、浅棕色等其它合理答案)
紫红色(或紫色等其它合理答案)
(4)(或其他碱溶液,;溶液不可)
吸收氯气,防止污染空气
化学试卷
第Ⅰ卷(选择题 40分)
一、选择题(本大题有20小题,每小题2分,共40分.每小题只有一个选项符合题意)
1.《梦溪笔谈》中记载了“熬胆矾铁釜,久之亦化为铜”,该化学反应的基本类型是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.硫磺固体属于危险品,其运载交通工具上应贴的标识为( )
A. B. C. D.
3.化学与生活密切相关,下列说法正确的是( )
A.碳酸氢钠可做食品膨松剂
B.焰火中红色来源于钠盐灼烧
C.氯气与二氧化硫混合使用可以提高漂白效果
D.维生素C可将转化为,说明维生素C具有氧化性
4.嫦娥五号将月壤带回地球,科学家深入研究表明月壤富含Fe、He、、、FeO、CaO等物质,下列说法错误的是( )
A.月壤中的是金属氧化物 B.月壤中的CaO是碱性氧化物
C.月壤中的铁是电解质 D.月壤是混合物
5.放射性元素()可用在灵敏度极高的烟雾传感器中,下列说法正确的是( )
A.Am质子数146 B.Am核外电子数为241
C.Am质量数为336 D.Am中子数为146
6.下列实验操作规范且能达到目的是
实验目的 实验操作
A 称取2.0gNaOH固体 先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体
B 配制的溶液 称取固体1.580g,放入100mL容量瓶中,加水稀释到刻度线
C 证明与水反应放热 用棉花包裹后滴几滴水,棉花燃烧,说明该反应放出热量
D 比较钠、铁的活泼性 把钠块投入溶液中
A.A B.B C.C D.D
7.下列溶液中物质的量浓度最大的是( )
A.的溶液 B.的溶液
C.的溶液 D.的溶液
8.金刚石和石墨的结构如图,二者间的相互关系是( )
A.同种单质 B.同分异构体 C.同位素 D.同素异形体
9.在给定条件下,下列物质间所示转化可以实现的是( )
A. B. C. D.
10.黑火药发生爆炸的主要反应为,下列说法错误的是( )
A.中存在离子键和共价键 B.分子的结构式为N-N
C.固态是分子晶体 D.是离子化合物
11.当光束通过下列分散系时,能产生明显丁达尔效应的是( )
A.石灰乳 B.食盐水 C.医用酒精 D.氢氧化铝胶体
12.下列物质中的氯元素既能被氧化又能被还原的是( )
A.NaCl B.HCl C. D.
13.设为阿伏加德罗常数的值,下列说法正确的是( )
A.原子所含质子数为 B.分子所含原子数为
C.标准状况下,22.4L溴单质中分子数目为 D.溶液中,数目为
14.下列各组离子能大量共存的是( )
A.在饱和氯水中:、、 B.在氯化钠溶液中:、、
C.在酸性溶液中:、、 D.在碱性溶液中:、、
15.下列实验操作正确的是( )
A.比较碳酸钠和碳酸氢钠的热稳定性 B.加热溶液 C.过滤 D.滴加溶液
16.下列反应能发生且离子方程式书写正确的是( )
A.与稀盐酸反应:
B.Na和水反应:
C.和水反应:
D.溶液中通入:
17.亚硫酸可被氧化,其原理为.下列说法错误的是( )
A.的电子式: B.硫原子结构示意图:
C.的摩尔质量: D.亚硫酸电离:
18.下列关于硫元素“价类二维图”的说法错误的是( )
A.a→b硫元素由游离态转变为化合态
B.d溶液久置于空气中易变质
C.向f溶液中通入氯气可转化为含有g的溶液
D.将气体c通入石蕊溶液中,溶液变红
19.某化工厂基于“绿色化学”理念设计了如下治污工艺流程,下列说法错误的是( )
A.该流程可用于吸收
B.可用做该反应过程的催化剂
C.该过程的总反应为
D.由转化为的过程中,氧化剂和还原剂的物质的量之比为2∶1
20.海水资源综合利用的部分过程如下图所示,下列说法错误的是( )
海水 →淡化:淡水
→制盐工业:粗盐→精盐
→制溴工业:
→制镁工业:
A.蒸馏海水可获得淡水
B.为除粗盐中的、、,可依次加入足量的、、溶液
C.在制溴工业中,通过氧化、还原、再氧化的步骤实现了溴的富集
D.在制镁工业中,可用贝壳为原料生产石灰乳以沉淀
第Ⅱ卷(非选择题 60分)
二、非选择题(本大题共5小题,共60分)
21.(12分)下表是元素周期表的一部分,根据表中所给的10种元素,按要求使用化学用语作答.
族 周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
1 ①
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
(1)金属性最强的元素是_______(填元素符号);单质化学性质最稳定的元素是_______(填元素符号).
(2)①、⑥、⑨原子半径由大到小的顺序是_______(填元素符号),⑧最高价氧化物的水化物化学式为_______.
(3)⑦最高价氧化物的化学式是_______,已知该物质属于酸性氧化物,写出它与氢氧化钠溶液反应的化学方程式_______.
22.(12分)在严格控制用量的情况下,可作为食品添加剂.
(1)在制备食糖的过程中,用二氧化硫对糖汁进行熏制,可使糖汁脱色,该过程说明具有_______性.
(2)实验室制的原理为:.用与足量硫酸反应,理论上可制得标准状况下的体积为_______L.
(3)将通入高锰酸钾溶液中,请配平该方程式,将化学计量数标在横线处.
,若参加反应,转移的电子数为_______.
(4)的过度排放会造成_______等环境问题.为避免对环境造成不良影响,工业上常用的吸收剂为_______.
23.(10分)硫酸是常用的化工原料.
(1)目前工业上制硫酸的主要原料为空气和_______.
(2)浓硫酸的性质与稀硫酸有很大不同,取2g蔗糖放入大试管中,加2~3滴水,再加入约3mL浓硫酸,迅速搅拌,然后塞紧带玻璃导管的橡皮塞,将玻璃导管的另一端插入盛有品红溶液的试管中,溶液褪色.上述涉及颜色变化的反应体现了浓硫酸的_______性和_______性.
(3)用质量分数98%的浓硫酸(密度)配制的溶液,需量取浓_______mL(精确到0.1),配制过程需要用到下列仪器中的_______、_______(填序号).
若使用长期敞口放置的浓配制溶液,则配出的稀硫酸浓度_______(填“偏高”、“偏低”或“无影响”).
24.(13分)某化学兴趣小组在实验室中利用侯氏制碱法制备,进一步处理得到产品和,实验流程如图:
回答下列问题:
(1)实验室用大理石和稀盐酸制备,该反应的离子方程式是_______.为除掉中混有的HCl气体,可选用的最佳试剂是饱和_______溶液(填化学式).
(2)反应完成后,将混合物经操作I_______(填操作名称)得到固体和滤液.
①固体受热分解的化学方程式为_______,将气体A通过足量固体后生成的气体为_______(填化学式).
②向滤液中加入NaCl粉末,存在NaCl(固体)(溶液)→NaCl(溶液)(固体)过程.为使沉淀充分析出并分离,根据NaCl和溶解度曲线,需采用的操作为_______、_______、过滤、洗涤、干燥.
(3)在该工艺流程中可循环使用的物质为_______、_______.
25.(13分)某小组实验室制备氯气并探究其氧化性,实验装置如下图(夹持与加热装置已略).
(1)装置A为氯气的发生装置,写出该装置中发生反应的化学方程式_______,其中氧化剂和还原剂的物质的量之比为_______.
(2)C试管中为KI溶液,反应一段时间后,C处的实验现象为_______,反应的离子方程式为_______.取C中少量溶液于试管中,加,充分振荡并静置,观察到的现象是溶液分层,上层溶液为_______色,下层溶液为_______色.
(3)装置D中的溶液为_______,其作用是_______.
福州市2022-2023学年高一上学期期末质量抽测
化学科参考答案
一、单选题(每题2分,共40分)
序号 1 2 3 4 5 6 7 8 9 10
答案 C D A C D C B D B B
序号 11 12 13 14 15 16 17 18 19 20
答案 D C B C A B D A D B
二、填空题(共60分)
21.(12分)
(1)Na(填元素名称不得分)
Ar(填元素名称不得分)
(2)Al,Cl,H或Al>Cl>H(顺序写反不得分)
(填物质名称不得分)
(3)(填物质名称不得分)
(未配平或漏写条件得1分,下同)
22.(12分)
(1)漂白
(2)1.12
(3)2 5 2 2 1 2
或(2或2mol均不得分)
(4)酸雨(或土壤酸化、水体酸化等其它合理答案)
生石灰(或石灰乳、氨水等合理答案,氢氧化钠或氢氧化钠溶液不得分)
23.(10分)
(1)单质硫(S)或硫铁矿(化学式和名称均得分)
(2)脱水性 强氧化性(顺序颠倒不扣分)
(3)1.4 ②④ 偏低
24.(13分)
(1)
(2)过滤
①
(填物质名称不得分)
②蒸发浓缩、冷却结晶
(3)
(4)食盐水(或)
25.(13分)
(1)
1∶2
(3)溶液变成棕黄色(溶液变成棕色或褐色均可)(2分)
无色(或浅黄色、浅棕色等其它合理答案)
紫红色(或紫色等其它合理答案)
(4)(或其他碱溶液,;溶液不可)
吸收氯气,防止污染空气
同课章节目录
