7.1 溶解与乳化 同步练习 2022-2023学年粤教版九年级下册化学(含答案)
文档属性
| 名称 | 7.1 溶解与乳化 同步练习 2022-2023学年粤教版九年级下册化学(含答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 66.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-25 00:00:00 | ||
图片预览




文档简介
7.1 溶解与乳化 同步练习
一、单选题
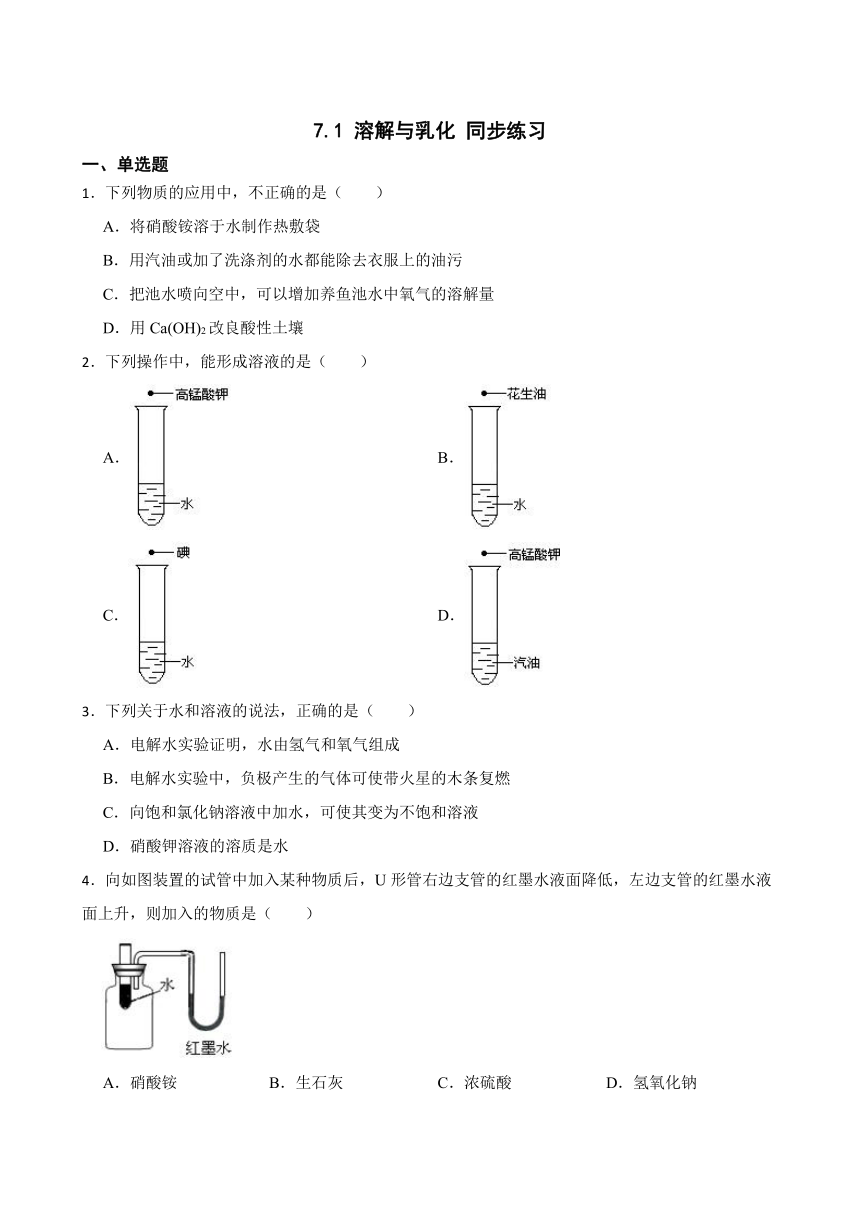
1.下列物质的应用中,不正确的是( )
A.将硝酸铵溶于水制作热敷袋
B.用汽油或加了洗涤剂的水都能除去衣服上的油污
C.把池水喷向空中,可以增加养鱼池水中氧气的溶解量
D.用Ca(OH)2改良酸性土壤
2.下列操作中,能形成溶液的是( )
A. B.
C. D.
3.下列关于水和溶液的说法,正确的是( )
A.电解水实验证明,水由氢气和氧气组成
B.电解水实验中,负极产生的气体可使带火星的木条复燃
C.向饱和氯化钠溶液中加水,可使其变为不饱和溶液
D.硝酸钾溶液的溶质是水
4.向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
A.硝酸铵 B.生石灰 C.浓硫酸 D.氢氧化钠
5.生活中常见的下列物质,不属于溶液的是( )
A.糖水 B.碘酒 C.雪碧汽水 D.蒸馏水
6.生产、生活中的下列做法,错误的是( )
A.制糖工业中用活性炭脱色
B.用钢刷来擦洗铝制品
C.安装天然气报警器应装在高处
D.使用洗发精来清洗头发上的油脂
7.下列说法正确的是( )
A.均一、稳定的液体都是溶液
B.溶质均以离子形式分散到溶剂中
C.同一温度下,硝酸钾的饱和溶液比不饱和溶液溶质质量分数大
D.饱和溶液析出晶体后溶质质量分数一定变小
8.医生有时给患者开一种叫做PP粉的杀菌消毒外用药,它的水溶液是红色.这种物质可能是( )
A.硫酸亚铁 B.食盐 C.硫酸铜 D.高锰酸钾
9.下列物质溶于水后,能形成无色溶液的是( )
A.高锰酸钾 B.蔗糖 C.植物油 D.面粉
10.物质加入水中,不能形成溶液的是( )
A.烧碱 B.冰 C.胆矾 D.食盐
11.在家中,小明取少量的下列物质分别放入水中,充分搅拌,其中能形成溶液的是( )
A.面粉 B.蔗糖 C.芝麻糊 D.植物油
12.在化学学习中,归纳推理是一种常用方法,下列推理正确的是( )
A.水是一种常见的溶剂,所以水可以溶解所有的物质
B.酸性溶液的pH<7,所以pH<7的溶液一定是酸性溶液
C.燃烧反应要与氧气接触,所以可燃物与氧气接触就一定能燃烧
D.燃料都有可燃性,所以有可燃性的物质一定适合做燃料
二、填空题
13.溶质的质量分数= ,溶质的质量= .
14.下列两种说法都是错误的,请你列举出一个具体实例,否定错误说法.
错误说法 否定错误说法的实例
(1)溶液一定都是无色的
(2)分解反应中一定有单质生成
15.(1)下列物质充分混合搅拌后,可形成溶液的是(填序号) .
①碘和酒精;②粉笔末和水;③植物油和水;④植物油和食盐.
(2)请你各举出一个实例,说明下列有关溶液的叙述是错误的.
①溶液一定是无色的.实例: ;
②均一、稳定的液体都是溶液.实例: ;
③溶液中的溶质一定是固体.实例: .
16.电火花点火使家用天然气燃烧满足的条件是 。用洗洁精除去衣服上的油污是利用洗洁精的 作用。2020年12月17日凌晨,嫦娥五号返回器携带1731g月球土壤成功着陆,经研究发现月壤中存在天然的铁、金、银、铅、锌、铜等金属颗粒。根据铁锈蚀的条件分析,铁在月球上不锈蚀的原因是 。
17.农业废弃物是指农业生产过程中废弃的物质,如秸秆、蔗渣等。闽籍科学家张俐娜发明了一种快速溶解农业废弃物的“神奇溶剂”。该“神奇溶剂”中氢氧化钠、尿素和水的质量比为7:12:81。
(1)“神奇溶剂”是一种溶液,其溶质有 。
(2)某次生产需用到100kg“神奇溶剂”。现利用氢氧化钠溶液和尿素来配制,所用的氢氧化钠溶液的溶质质量分数为 (列出计算式即可)。
18.多角度认识溶液,有助于我们更好地了解其在生产生活中的重要作用.
(1)溶液的形成
①将适量调味品加入水中,充分搅拌后不能形成溶液的是 (填标号).
A.食盐 B.蔗糖 C.花生油
②将生石灰和足量的水充分搅拌后静置,取上层溶液即为澄清石灰水.写出生石灰与水反应的化学方程式 .
(2)溶液的性质
①关于溶液的说法正确的有 (填标号).
A.盐酸是纯净物 B.溶液是均一、稳定的
C.溶液的酸碱度可用石蕊溶液测定 D.饱和溶液不一定是浓溶液
②常温下,将某固态物质A溶于水,形成饱和溶液(如图1),进行以下实验.回答下列问题:
a.该物质的溶解度随温度升高而 (填“增大”或“减小”)
b.往溶液Ⅱ中加入少量高锰酸钾完全溶解,溶液呈紫红色.据此现象,写出对“饱和溶液”概念的理解 .
③常温下,该物质在不同质量的水中溶解达到饱和状态,溶质的质量与水的质量关系如图2所示.
a.常温时,该物质的溶解度是 g.
b.D点时,该溶液的溶质质量分数为 (结果精确到0.1%)
c.将A点状态的溶液变化到C点状态的操作步骤为 .
d.图中A、B、C三个点表示溶液中溶质质量分数从大到小的关系是 .
(3)溶液的用途
生活中溶液由许多用途,例如:碘酒能用于杀菌消毒;请再举一个生活中溶液应用的实例: .
三、综合题
19.溶液在生产、生活中起着十分重要的作用。
(1)我国科学家屠呦呦因为对青蒿素的研究取得巨大成就而荣获了诺贝尔奖。她用乙醚代替水成功提取出青蒿素,说明研究青蒿素在不同的 (选填“溶质”或“溶剂”)中的溶解性很有价值。为了提高药物在水中或油中的溶解性,对其进行了分子结构修饰,说明物质的 决定物质的性质。
(2)生理盐水是医疗上常用的一种溶液,100mL生理盐水(其密度可近似看做1g/cm3)中含有0.9g医用氯化钠,该溶液中溶质质量分数为 。一瓶合格的生理盐水密封放置一段时间后,不会出现浑浊现象,原因是 。
(3)氯化钠主要存在于海水中,海水晒盐能够得到粗盐和卤水。卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线。分别将t2℃的MgCl2、KCl和MgSO4三种物质的饱和溶液降温到t1℃时,溶液中溶质质量分数从大到小的关系是 。
(4)某同学利用实验探究NaCl在水中的溶解度,所得数据记录如下
序号 温度 水质量 加入NaCl质量 溶液质量
① 20℃ 25g 9g 34g
② 20℃ 50g 20g 68g
③ 20℃ 100g 34g 134g
④ 20℃ 150g 54g 204g
上述实验中,所得溶液为饱和溶液的是 (填数字序号)。
20.溶液在生产、生活中起着十分重要的作用.请回答下列问题:
(1)可以作为溶质的是 .
A.只有固体 B.只有液体
C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为 ,水的体积为 mL(水的密度近似看作1g/cm3).
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如图1.t1℃时,甲物质的溶解度是 .t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是 (填“甲”或“乙”)物质的饱和溶液.
(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高.则可能的组合是 .
选项 x y
A 水 氧化钙
B 水 硝酸铵
C 浓硫酸 水
D 稀盐酸 镁
21.
(1)从物质分类来看,澄清石灰水属于 物(选填“纯净”或“混合”),其溶质属于 (选填“单质”或“化合物”或“氧化物”)。
(2)某澄清石灰水中含有氢氧化钙1.48g,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是 ?
22.KNO3和NaCl在不同温度时的溶解度如下图所示,请回答下列问题:
温度/℃ 0 10 20 30 40 50 60 70
溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8
(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图所示:
图中能表示KNO3溶解度曲线的是 (选填“A”或“B”)
(2)由表中数据分析可知,20℃时40gNaCl溶解在50g水中得到溶液 g。
(3)硝酸钾中含有少量氯化钠时,可通过 (选填“蒸发结晶”或“降温结晶”)的方法提纯。
答案解析部分
1.【答案】A
2.【答案】A
3.【答案】C
4.【答案】A
5.【答案】D
6.【答案】B
7.【答案】C
8.【答案】D
9.【答案】B
10.【答案】B
11.【答案】B
12.【答案】B
13.【答案】×100%;溶液的质量×溶质质量分数
14.【答案】硫酸铜溶液是蓝色的(合理即可);碳酸分解生成二氧化碳和水(合理即可)
15.【答案】①;硫酸铜溶液(或碘酒);蒸馏水;氯化氢气体(或酒精)
16.【答案】温度达到天然气的着火点;乳化;月球上缺少氧气(或月球上缺少氧气和水)
17.【答案】(1)氢氧化钠、尿素
(2)
18.【答案】C;CaO+H2O═Ca(OH)2;BD;减小;一定温度下,某物质的饱和溶液对于其它物质不一定是饱和的;40;28.6%;常温下,往A状态的溶液中加入20g溶质和20g水,使之充分溶解;C、A、B;生理盐水给病人补充水分
19.【答案】(1)溶剂;结构
(2)0.9%;溶液是均一的、稳定的
(3)MgCl2>KCl=MgSO4
(4)①②④
20.【答案】(1)D
(2)16g;84
(3)40g;乙
(4)AD
21.【答案】(1)混合;化合物
(2)0.88g
22.【答案】(1)A
(2)68
(3)降温结晶
一、单选题
1.下列物质的应用中,不正确的是( )
A.将硝酸铵溶于水制作热敷袋
B.用汽油或加了洗涤剂的水都能除去衣服上的油污
C.把池水喷向空中,可以增加养鱼池水中氧气的溶解量
D.用Ca(OH)2改良酸性土壤
2.下列操作中,能形成溶液的是( )
A. B.
C. D.
3.下列关于水和溶液的说法,正确的是( )
A.电解水实验证明,水由氢气和氧气组成
B.电解水实验中,负极产生的气体可使带火星的木条复燃
C.向饱和氯化钠溶液中加水,可使其变为不饱和溶液
D.硝酸钾溶液的溶质是水
4.向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
A.硝酸铵 B.生石灰 C.浓硫酸 D.氢氧化钠
5.生活中常见的下列物质,不属于溶液的是( )
A.糖水 B.碘酒 C.雪碧汽水 D.蒸馏水
6.生产、生活中的下列做法,错误的是( )
A.制糖工业中用活性炭脱色
B.用钢刷来擦洗铝制品
C.安装天然气报警器应装在高处
D.使用洗发精来清洗头发上的油脂
7.下列说法正确的是( )
A.均一、稳定的液体都是溶液
B.溶质均以离子形式分散到溶剂中
C.同一温度下,硝酸钾的饱和溶液比不饱和溶液溶质质量分数大
D.饱和溶液析出晶体后溶质质量分数一定变小
8.医生有时给患者开一种叫做PP粉的杀菌消毒外用药,它的水溶液是红色.这种物质可能是( )
A.硫酸亚铁 B.食盐 C.硫酸铜 D.高锰酸钾
9.下列物质溶于水后,能形成无色溶液的是( )
A.高锰酸钾 B.蔗糖 C.植物油 D.面粉
10.物质加入水中,不能形成溶液的是( )
A.烧碱 B.冰 C.胆矾 D.食盐
11.在家中,小明取少量的下列物质分别放入水中,充分搅拌,其中能形成溶液的是( )
A.面粉 B.蔗糖 C.芝麻糊 D.植物油
12.在化学学习中,归纳推理是一种常用方法,下列推理正确的是( )
A.水是一种常见的溶剂,所以水可以溶解所有的物质
B.酸性溶液的pH<7,所以pH<7的溶液一定是酸性溶液
C.燃烧反应要与氧气接触,所以可燃物与氧气接触就一定能燃烧
D.燃料都有可燃性,所以有可燃性的物质一定适合做燃料
二、填空题
13.溶质的质量分数= ,溶质的质量= .
14.下列两种说法都是错误的,请你列举出一个具体实例,否定错误说法.
错误说法 否定错误说法的实例
(1)溶液一定都是无色的
(2)分解反应中一定有单质生成
15.(1)下列物质充分混合搅拌后,可形成溶液的是(填序号) .
①碘和酒精;②粉笔末和水;③植物油和水;④植物油和食盐.
(2)请你各举出一个实例,说明下列有关溶液的叙述是错误的.
①溶液一定是无色的.实例: ;
②均一、稳定的液体都是溶液.实例: ;
③溶液中的溶质一定是固体.实例: .
16.电火花点火使家用天然气燃烧满足的条件是 。用洗洁精除去衣服上的油污是利用洗洁精的 作用。2020年12月17日凌晨,嫦娥五号返回器携带1731g月球土壤成功着陆,经研究发现月壤中存在天然的铁、金、银、铅、锌、铜等金属颗粒。根据铁锈蚀的条件分析,铁在月球上不锈蚀的原因是 。
17.农业废弃物是指农业生产过程中废弃的物质,如秸秆、蔗渣等。闽籍科学家张俐娜发明了一种快速溶解农业废弃物的“神奇溶剂”。该“神奇溶剂”中氢氧化钠、尿素和水的质量比为7:12:81。
(1)“神奇溶剂”是一种溶液,其溶质有 。
(2)某次生产需用到100kg“神奇溶剂”。现利用氢氧化钠溶液和尿素来配制,所用的氢氧化钠溶液的溶质质量分数为 (列出计算式即可)。
18.多角度认识溶液,有助于我们更好地了解其在生产生活中的重要作用.
(1)溶液的形成
①将适量调味品加入水中,充分搅拌后不能形成溶液的是 (填标号).
A.食盐 B.蔗糖 C.花生油
②将生石灰和足量的水充分搅拌后静置,取上层溶液即为澄清石灰水.写出生石灰与水反应的化学方程式 .
(2)溶液的性质
①关于溶液的说法正确的有 (填标号).
A.盐酸是纯净物 B.溶液是均一、稳定的
C.溶液的酸碱度可用石蕊溶液测定 D.饱和溶液不一定是浓溶液
②常温下,将某固态物质A溶于水,形成饱和溶液(如图1),进行以下实验.回答下列问题:
a.该物质的溶解度随温度升高而 (填“增大”或“减小”)
b.往溶液Ⅱ中加入少量高锰酸钾完全溶解,溶液呈紫红色.据此现象,写出对“饱和溶液”概念的理解 .
③常温下,该物质在不同质量的水中溶解达到饱和状态,溶质的质量与水的质量关系如图2所示.
a.常温时,该物质的溶解度是 g.
b.D点时,该溶液的溶质质量分数为 (结果精确到0.1%)
c.将A点状态的溶液变化到C点状态的操作步骤为 .
d.图中A、B、C三个点表示溶液中溶质质量分数从大到小的关系是 .
(3)溶液的用途
生活中溶液由许多用途,例如:碘酒能用于杀菌消毒;请再举一个生活中溶液应用的实例: .
三、综合题
19.溶液在生产、生活中起着十分重要的作用。
(1)我国科学家屠呦呦因为对青蒿素的研究取得巨大成就而荣获了诺贝尔奖。她用乙醚代替水成功提取出青蒿素,说明研究青蒿素在不同的 (选填“溶质”或“溶剂”)中的溶解性很有价值。为了提高药物在水中或油中的溶解性,对其进行了分子结构修饰,说明物质的 决定物质的性质。
(2)生理盐水是医疗上常用的一种溶液,100mL生理盐水(其密度可近似看做1g/cm3)中含有0.9g医用氯化钠,该溶液中溶质质量分数为 。一瓶合格的生理盐水密封放置一段时间后,不会出现浑浊现象,原因是 。
(3)氯化钠主要存在于海水中,海水晒盐能够得到粗盐和卤水。卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线。分别将t2℃的MgCl2、KCl和MgSO4三种物质的饱和溶液降温到t1℃时,溶液中溶质质量分数从大到小的关系是 。
(4)某同学利用实验探究NaCl在水中的溶解度,所得数据记录如下
序号 温度 水质量 加入NaCl质量 溶液质量
① 20℃ 25g 9g 34g
② 20℃ 50g 20g 68g
③ 20℃ 100g 34g 134g
④ 20℃ 150g 54g 204g
上述实验中,所得溶液为饱和溶液的是 (填数字序号)。
20.溶液在生产、生活中起着十分重要的作用.请回答下列问题:
(1)可以作为溶质的是 .
A.只有固体 B.只有液体
C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为 ,水的体积为 mL(水的密度近似看作1g/cm3).
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如图1.t1℃时,甲物质的溶解度是 .t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是 (填“甲”或“乙”)物质的饱和溶液.
(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高.则可能的组合是 .
选项 x y
A 水 氧化钙
B 水 硝酸铵
C 浓硫酸 水
D 稀盐酸 镁
21.
(1)从物质分类来看,澄清石灰水属于 物(选填“纯净”或“混合”),其溶质属于 (选填“单质”或“化合物”或“氧化物”)。
(2)某澄清石灰水中含有氢氧化钙1.48g,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是 ?
22.KNO3和NaCl在不同温度时的溶解度如下图所示,请回答下列问题:
温度/℃ 0 10 20 30 40 50 60 70
溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8
(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图所示:
图中能表示KNO3溶解度曲线的是 (选填“A”或“B”)
(2)由表中数据分析可知,20℃时40gNaCl溶解在50g水中得到溶液 g。
(3)硝酸钾中含有少量氯化钠时,可通过 (选填“蒸发结晶”或“降温结晶”)的方法提纯。
答案解析部分
1.【答案】A
2.【答案】A
3.【答案】C
4.【答案】A
5.【答案】D
6.【答案】B
7.【答案】C
8.【答案】D
9.【答案】B
10.【答案】B
11.【答案】B
12.【答案】B
13.【答案】×100%;溶液的质量×溶质质量分数
14.【答案】硫酸铜溶液是蓝色的(合理即可);碳酸分解生成二氧化碳和水(合理即可)
15.【答案】①;硫酸铜溶液(或碘酒);蒸馏水;氯化氢气体(或酒精)
16.【答案】温度达到天然气的着火点;乳化;月球上缺少氧气(或月球上缺少氧气和水)
17.【答案】(1)氢氧化钠、尿素
(2)
18.【答案】C;CaO+H2O═Ca(OH)2;BD;减小;一定温度下,某物质的饱和溶液对于其它物质不一定是饱和的;40;28.6%;常温下,往A状态的溶液中加入20g溶质和20g水,使之充分溶解;C、A、B;生理盐水给病人补充水分
19.【答案】(1)溶剂;结构
(2)0.9%;溶液是均一的、稳定的
(3)MgCl2>KCl=MgSO4
(4)①②④
20.【答案】(1)D
(2)16g;84
(3)40g;乙
(4)AD
21.【答案】(1)混合;化合物
(2)0.88g
22.【答案】(1)A
(2)68
(3)降温结晶
