7.3 溶液浓稀的表示 同步练习 2022-2023学年粤教版九年级下册化学(含答案)
文档属性
| 名称 | 7.3 溶液浓稀的表示 同步练习 2022-2023学年粤教版九年级下册化学(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 176.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-25 00:00:00 | ||
图片预览



文档简介
7.3 溶液浓稀的表示 同步练习
一、单选题
1.实验室配制50g溶质质量分数为15%的氧氯化钠溶液。下列说法正确的是()
A.托盘天平未经调零即用来称取氯化钠固体
B.称量时托盘天平指针偏左,移动游码至天平平衡
C.量取水时,用规格为50mL的量筒
D.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
2.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A.随温度升高,a、b、c三种物质的溶解度均增大
B.t2℃时,把50ga放入50g水中,可得到100ga的饱和溶液
C.将t2℃时等质量的a、b饱和溶液降温到t1℃,析出晶体的质量a大于b
D.t1℃时,a、c的溶解度相等,则两溶液的溶质质量分数也相等
3.实验室用质量分数为6%的氯化钠溶液(密度为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液。下列说法正确的是( )
A.实验步骤:计算、称量、溶解、装瓶
B.量取6%的氯化钠溶液时选用100mL的量筒
C.需要加水的质量是50g
D.量取水时仰视会使配制的氯化钠溶液浓度偏小
4.将8克SO 3溶于192克水中,所得溶液的质量分数是( )
A.4% B.8% C.98% D.4.9%
5.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。下列有关说法正确的是( )
A.甲的溶解度大于乙
B.升高温度可将接近饱和的甲溶液变为饱和溶液
C.t2℃时,甲的饱和溶液的溶质质量分数为25%
D.将t2℃时甲、乙、丙的饱和溶液降温至t1℃,溶质的质量分数由大到小的顺序为乙>甲>丙
6.炎热的夏天,小林打开冰箱,从4℃的储藏室里拿出一杯底部有少量蔗糖晶体的溶液a,在室温下放置一段时间后,发现晶体消失了,得到溶液b.判断下列说法正确的是( )
A.4℃时,a溶液一定是饱和溶液
B.室温下,b溶液一定是饱和溶液
C.蔗糖晶体的溶解度随温度的升高而降低
D.a溶液的溶质质量分数大于b溶液的溶质质量分数
7.甲、乙两种物质的溶解度曲线如图所示.下列说法不正确的是( )
A.20℃时,乙物质的溶解度为30g
B.20℃时,乙物质的饱和溶液的浓度一定大于甲物质
C.甲乙两种物质的饱和溶液从50℃降温到40℃,浓度变得相等
D.50℃时,乙的饱和溶液溶质质量分数为16.7%
8.下列图①~④分别与相应的操作过程相对应,其中正确的是( )
A. 在恒温的条件下,将足量的氯化钠饱和溶液蒸发适量的水分
B. 向露置在空气中部分变质的氢氧化钠溶液中加入稀盐酸
C. 向氢氧化钠溶液中不断加水稀释
D. 相同质量的且过量的锌粉和铁粉,分别与质量和质量分数相同的稀盐酸反应
9.在配置50g 10%的氯化钠溶液时,下列情况可能导致溶液中氯化钠质量分数小于10%的是( )
①用量筒量取水时俯视读数;②配制溶液的烧杯用少量蒸馏水润洗;③在托盘天平的左盘放砝码右盘放氯化钠;④将水倒入烧杯时,有少量水溅出;⑤溶解时,用玻璃棒搅拌过快,使少量溶液溅出.
A.①②③④⑤ B.只有②③
C.只有①②③ D.只有②③⑤
10.实验室用氯化钠固体配制质量分数为6%的氯化钠溶液,不需要用到的仪器是( )
A.烧杯 B.量筒 C.集气瓶 D.托盘天平
11.20℃时,100g水中最多能溶解35g氯化钾,此时,50g氯化钾饱和溶液中溶质的质量分数是( )
A.25.9% B.35% C.17.5% D.70%
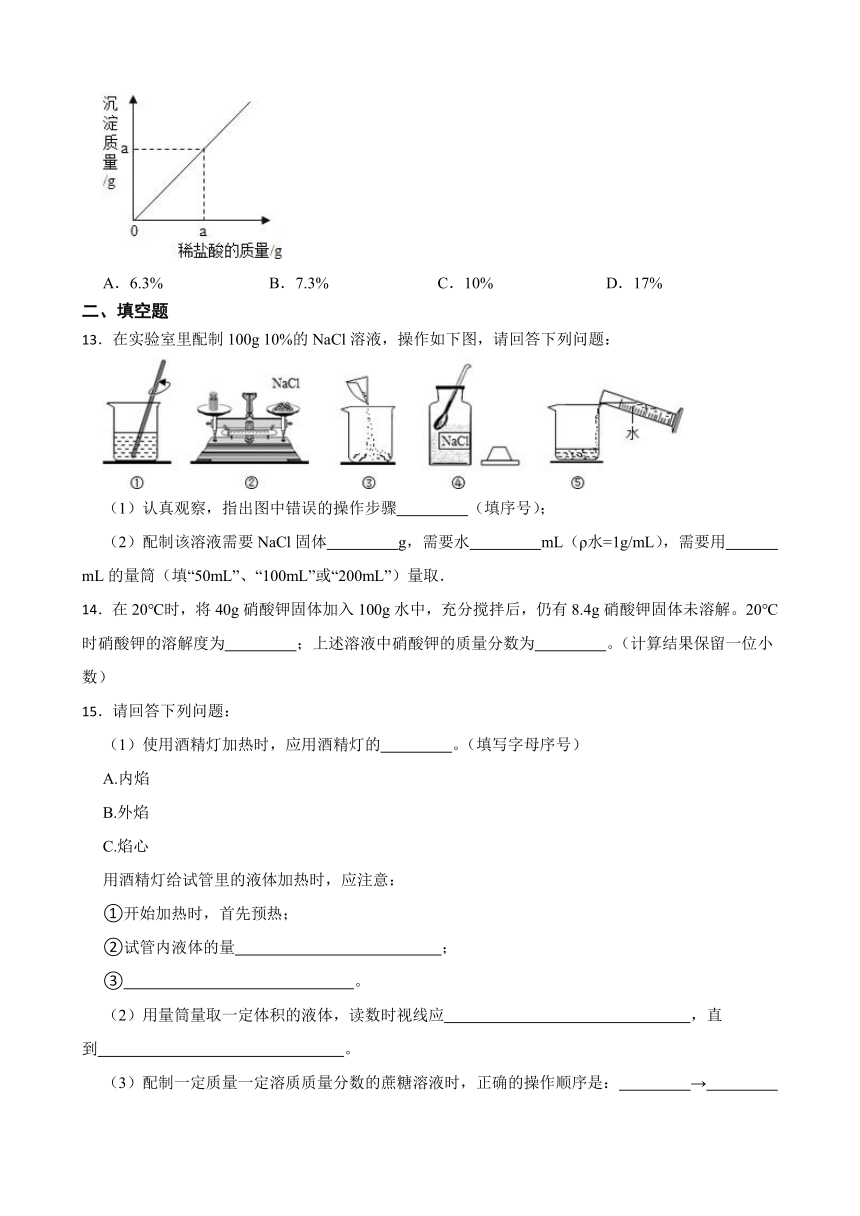
12.向溶质的质量分数为17%的硝酸银溶液中逐滴滴入稀盐酸,测得滴入盐酸的质量与生成沉淀的质量有如图所示关系,则恰好完全反应时所得溶液中溶质的质量分数为( )
A.6.3% B.7.3% C.10% D.17%
二、填空题
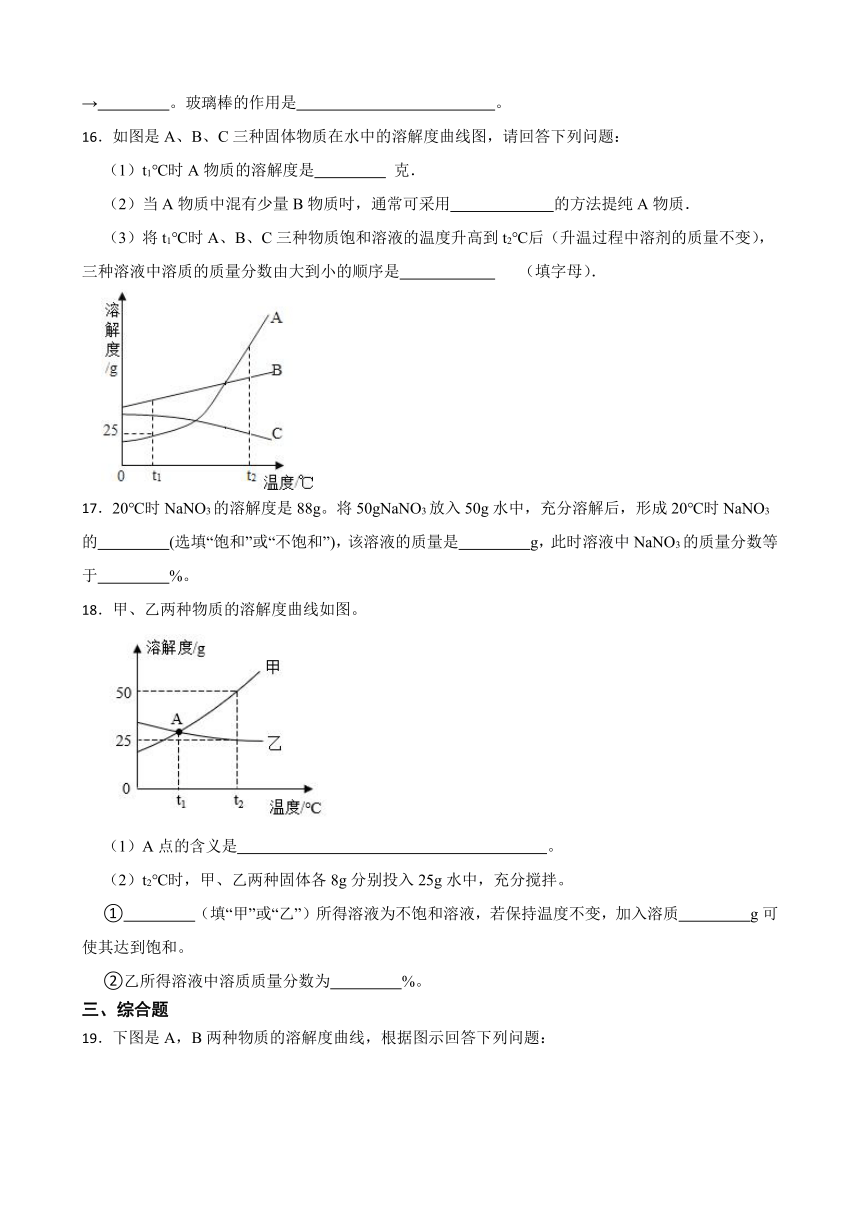
13.在实验室里配制100g 10%的NaCl溶液,操作如下图,请回答下列问题:
(1)认真观察,指出图中错误的操作步骤 (填序号);
(2)配制该溶液需要NaCl固体 g,需要水 mL(ρ水=1g/mL),需要用 mL的量筒(填“50mL”、“100mL”或“200mL”)量取.
14.在20℃时,将40g硝酸钾固体加入100g水中,充分搅拌后,仍有8.4g硝酸钾固体未溶解。20℃时硝酸钾的溶解度为 ;上述溶液中硝酸钾的质量分数为 。(计算结果保留一位小数)
15.请回答下列问题:
(1)使用酒精灯加热时,应用酒精灯的 。(填写字母序号)
A.内焰
B.外焰
C.焰心
用酒精灯给试管里的液体加热时,应注意:
①开始加热时,首先预热;
②试管内液体的量 ;
③ 。
(2)用量筒量取一定体积的液体,读数时视线应 ,直到 。
(3)配制一定质量一定溶质质量分数的蔗糖溶液时,正确的操作顺序是: → → 。玻璃棒的作用是 。
16.如图是A、B、C三种固体物质在水中的溶解度曲线图,请回答下列问题:
(1)t1℃时A物质的溶解度是 克.
(2)当A物质中混有少量B物质吋,通常可采用 的方法提纯A物质.
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃后(升温过程中溶剂的质量不变),三种溶液中溶质的质量分数由大到小的顺序是 (填字母).
17.20℃时NaNO3的溶解度是88g。将50gNaNO3放入50g水中,充分溶解后,形成20℃时NaNO3的 (选填“饱和”或“不饱和”),该溶液的质量是 g,此时溶液中NaNO3的质量分数等于 %。
18.甲、乙两种物质的溶解度曲线如图。
(1)A点的含义是 。
(2)t2℃时,甲、乙两种固体各8g分别投入25g水中,充分搅拌。
① (填“甲”或“乙”)所得溶液为不饱和溶液,若保持温度不变,加入溶质 g可使其达到饱和。
②乙所得溶液中溶质质量分数为 %。
三、综合题
19.下图是A,B两种物质的溶解度曲线,根据图示回答下列问题:
(1)t1℃时,向两只盛有100g水的烧杯中,分别加入A.B两种物质至不能溶解为止,所得溶液的溶质质量分数较大的是 溶液(填“A”或“B”)。
(2)t2℃时,欲配制等质量的A,B两种物质的饱和溶液,所需水的质量关系是A B。 (填写“>”、“<”或“=”,下同)
(3)将t2℃的A,B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是A B。
(4)将t2℃的A,B两种物质的饱和溶液各200g,升温至t3℃,欲使它们仍为饱和溶液,若不改变溶剂质量,所需加入固体溶质的质量关系是A B。
20.为测定实验室中某过氧化氢溶液的溶质质量分数,小明取25.0g 过氧化氢溶液放入烧杯中,然后进行如图Z5﹣1所示的实验.请计算:
(1)生成氧气的质量为 g.
(2)过氧化氢的质量分数为多少?
21.多角度认识溶液,有助于我们更好地了解其在生产生活中的重要作用。
(1)食盐是重要的调味品,其主要成分氯化钠是由 (选填“分子”、“原子”或“离子”)构成的;氯化钠固体不导电,但氯化钠溶液导电,是由于氯化钠溶液中存在能自由移动的 (填两种离子符号)。
(2)配制50 g溶质质量分数15%的氯化钠溶液。
①计算并称量:用托盘天平称量7.5g氯化钠固体,用量筒量取 mL水。
②溶解:溶解时需要用到玻璃棒,它的作用是 。
③下列实验操作中,会引起溶质质量分数偏差的有 。
A.称量药品时,药品和砝码放反 B.量取水时俯视读数 C.装瓶时洒出少量溶液
(3)25℃时,向下列4只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。依据实验和溶解度曲线回答下问题。
①烧杯①中溶液的质量为 。
②上述溶液为饱和溶液的是 (填烧杯序号)。
③能将不饱和KCl溶液变为饱和KCl溶液的方法正确的是 (填序号,下同)。
A.升高温度 B.加水 C.加KCl固体 D.倒出部分溶液
④烧杯④中溶液的溶质质量分数约为 。
A.26% B.29% C.35% D.40%
22.水是生命之源,请用所学知识回答有关水的问题。
(1)保持水的化学性质的最小微粒是 。
(2)“生命吸管”(见图)是一种小型便携水净化器,可以将污水直接净化为饮用水。“生命吸管”实际上是一根塑料管,里面装有网丝、注入了活性炭和碘的树脂。其中,网丝起 作用,活性炭起 作用,碘的树脂起 作用。
(3)为了人类和社会经济的可持续发展,我们必须爱护水资源,节约用水是每个公民的责任和义务。下列做法属于节约用水的是 (填序号)
A 城市生活废水直接排入河流
B 农业上合理使用化肥和农药
C 工业废水处理后循环使用
D 用水后及时关闭水龙头
(4)在化学实验室中水还能用于配制溶液,某同学欲配制100g溶质质量分数为5%的氯化钠溶液。
①若用氯化钠固体和水配制,实验步骤为计算、 、溶解;
②若在量取水的过程中仰视读数,则所配溶液的溶质质量分数会 (填“偏大”“偏小”或“不变”)。
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】D
4.【答案】D
5.【答案】D
6.【答案】A
7.【答案】C
8.【答案】B
9.【答案】B
10.【答案】C
11.【答案】A
12.【答案】A
13.【答案】(1)②
(2)10g;90g;100
14.【答案】31.6g;24.0%
15.【答案】(1)B;不能超过试管容积的 ;试管口不可对着自己或他人
(2)平视凹液面(或平视刻度线);凹液面的最低点与刻度线相切
(3)计算;称量;溶解;搅拌,加快蔗糖的溶解
16.【答案】25;降温结晶;B>C>A
17.【答案】饱和;94;46.8
18.【答案】(1)t1℃时,甲、乙两种物质的溶解度相等
(2)甲;4.5;20
19.【答案】(1)B
(2)=
(3)>
(4)>
20.【答案】(1)3.2
(2)解:设25.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2 2H2O+O2↑
68 32
x 3.2g
=
x=6.8g
过氧化氢的质量分数为: ×100%=27.2%.
21.【答案】(1)离子;Na+、Cl-
(2)42.5;搅拌,加速溶解;AB##BA
(3)110g;④;C;A
22.【答案】(1)水分子
(2)过滤;吸附;消毒
(3)CD
(4)称量;偏小
一、单选题
1.实验室配制50g溶质质量分数为15%的氧氯化钠溶液。下列说法正确的是()
A.托盘天平未经调零即用来称取氯化钠固体
B.称量时托盘天平指针偏左,移动游码至天平平衡
C.量取水时,用规格为50mL的量筒
D.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
2.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A.随温度升高,a、b、c三种物质的溶解度均增大
B.t2℃时,把50ga放入50g水中,可得到100ga的饱和溶液
C.将t2℃时等质量的a、b饱和溶液降温到t1℃,析出晶体的质量a大于b
D.t1℃时,a、c的溶解度相等,则两溶液的溶质质量分数也相等
3.实验室用质量分数为6%的氯化钠溶液(密度为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液。下列说法正确的是( )
A.实验步骤:计算、称量、溶解、装瓶
B.量取6%的氯化钠溶液时选用100mL的量筒
C.需要加水的质量是50g
D.量取水时仰视会使配制的氯化钠溶液浓度偏小
4.将8克SO 3溶于192克水中,所得溶液的质量分数是( )
A.4% B.8% C.98% D.4.9%
5.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。下列有关说法正确的是( )
A.甲的溶解度大于乙
B.升高温度可将接近饱和的甲溶液变为饱和溶液
C.t2℃时,甲的饱和溶液的溶质质量分数为25%
D.将t2℃时甲、乙、丙的饱和溶液降温至t1℃,溶质的质量分数由大到小的顺序为乙>甲>丙
6.炎热的夏天,小林打开冰箱,从4℃的储藏室里拿出一杯底部有少量蔗糖晶体的溶液a,在室温下放置一段时间后,发现晶体消失了,得到溶液b.判断下列说法正确的是( )
A.4℃时,a溶液一定是饱和溶液
B.室温下,b溶液一定是饱和溶液
C.蔗糖晶体的溶解度随温度的升高而降低
D.a溶液的溶质质量分数大于b溶液的溶质质量分数
7.甲、乙两种物质的溶解度曲线如图所示.下列说法不正确的是( )
A.20℃时,乙物质的溶解度为30g
B.20℃时,乙物质的饱和溶液的浓度一定大于甲物质
C.甲乙两种物质的饱和溶液从50℃降温到40℃,浓度变得相等
D.50℃时,乙的饱和溶液溶质质量分数为16.7%
8.下列图①~④分别与相应的操作过程相对应,其中正确的是( )
A. 在恒温的条件下,将足量的氯化钠饱和溶液蒸发适量的水分
B. 向露置在空气中部分变质的氢氧化钠溶液中加入稀盐酸
C. 向氢氧化钠溶液中不断加水稀释
D. 相同质量的且过量的锌粉和铁粉,分别与质量和质量分数相同的稀盐酸反应
9.在配置50g 10%的氯化钠溶液时,下列情况可能导致溶液中氯化钠质量分数小于10%的是( )
①用量筒量取水时俯视读数;②配制溶液的烧杯用少量蒸馏水润洗;③在托盘天平的左盘放砝码右盘放氯化钠;④将水倒入烧杯时,有少量水溅出;⑤溶解时,用玻璃棒搅拌过快,使少量溶液溅出.
A.①②③④⑤ B.只有②③
C.只有①②③ D.只有②③⑤
10.实验室用氯化钠固体配制质量分数为6%的氯化钠溶液,不需要用到的仪器是( )
A.烧杯 B.量筒 C.集气瓶 D.托盘天平
11.20℃时,100g水中最多能溶解35g氯化钾,此时,50g氯化钾饱和溶液中溶质的质量分数是( )
A.25.9% B.35% C.17.5% D.70%
12.向溶质的质量分数为17%的硝酸银溶液中逐滴滴入稀盐酸,测得滴入盐酸的质量与生成沉淀的质量有如图所示关系,则恰好完全反应时所得溶液中溶质的质量分数为( )
A.6.3% B.7.3% C.10% D.17%
二、填空题
13.在实验室里配制100g 10%的NaCl溶液,操作如下图,请回答下列问题:
(1)认真观察,指出图中错误的操作步骤 (填序号);
(2)配制该溶液需要NaCl固体 g,需要水 mL(ρ水=1g/mL),需要用 mL的量筒(填“50mL”、“100mL”或“200mL”)量取.
14.在20℃时,将40g硝酸钾固体加入100g水中,充分搅拌后,仍有8.4g硝酸钾固体未溶解。20℃时硝酸钾的溶解度为 ;上述溶液中硝酸钾的质量分数为 。(计算结果保留一位小数)
15.请回答下列问题:
(1)使用酒精灯加热时,应用酒精灯的 。(填写字母序号)
A.内焰
B.外焰
C.焰心
用酒精灯给试管里的液体加热时,应注意:
①开始加热时,首先预热;
②试管内液体的量 ;
③ 。
(2)用量筒量取一定体积的液体,读数时视线应 ,直到 。
(3)配制一定质量一定溶质质量分数的蔗糖溶液时,正确的操作顺序是: → → 。玻璃棒的作用是 。
16.如图是A、B、C三种固体物质在水中的溶解度曲线图,请回答下列问题:
(1)t1℃时A物质的溶解度是 克.
(2)当A物质中混有少量B物质吋,通常可采用 的方法提纯A物质.
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃后(升温过程中溶剂的质量不变),三种溶液中溶质的质量分数由大到小的顺序是 (填字母).
17.20℃时NaNO3的溶解度是88g。将50gNaNO3放入50g水中,充分溶解后,形成20℃时NaNO3的 (选填“饱和”或“不饱和”),该溶液的质量是 g,此时溶液中NaNO3的质量分数等于 %。
18.甲、乙两种物质的溶解度曲线如图。
(1)A点的含义是 。
(2)t2℃时,甲、乙两种固体各8g分别投入25g水中,充分搅拌。
① (填“甲”或“乙”)所得溶液为不饱和溶液,若保持温度不变,加入溶质 g可使其达到饱和。
②乙所得溶液中溶质质量分数为 %。
三、综合题
19.下图是A,B两种物质的溶解度曲线,根据图示回答下列问题:
(1)t1℃时,向两只盛有100g水的烧杯中,分别加入A.B两种物质至不能溶解为止,所得溶液的溶质质量分数较大的是 溶液(填“A”或“B”)。
(2)t2℃时,欲配制等质量的A,B两种物质的饱和溶液,所需水的质量关系是A B。 (填写“>”、“<”或“=”,下同)
(3)将t2℃的A,B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是A B。
(4)将t2℃的A,B两种物质的饱和溶液各200g,升温至t3℃,欲使它们仍为饱和溶液,若不改变溶剂质量,所需加入固体溶质的质量关系是A B。
20.为测定实验室中某过氧化氢溶液的溶质质量分数,小明取25.0g 过氧化氢溶液放入烧杯中,然后进行如图Z5﹣1所示的实验.请计算:
(1)生成氧气的质量为 g.
(2)过氧化氢的质量分数为多少?
21.多角度认识溶液,有助于我们更好地了解其在生产生活中的重要作用。
(1)食盐是重要的调味品,其主要成分氯化钠是由 (选填“分子”、“原子”或“离子”)构成的;氯化钠固体不导电,但氯化钠溶液导电,是由于氯化钠溶液中存在能自由移动的 (填两种离子符号)。
(2)配制50 g溶质质量分数15%的氯化钠溶液。
①计算并称量:用托盘天平称量7.5g氯化钠固体,用量筒量取 mL水。
②溶解:溶解时需要用到玻璃棒,它的作用是 。
③下列实验操作中,会引起溶质质量分数偏差的有 。
A.称量药品时,药品和砝码放反 B.量取水时俯视读数 C.装瓶时洒出少量溶液
(3)25℃时,向下列4只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。依据实验和溶解度曲线回答下问题。
①烧杯①中溶液的质量为 。
②上述溶液为饱和溶液的是 (填烧杯序号)。
③能将不饱和KCl溶液变为饱和KCl溶液的方法正确的是 (填序号,下同)。
A.升高温度 B.加水 C.加KCl固体 D.倒出部分溶液
④烧杯④中溶液的溶质质量分数约为 。
A.26% B.29% C.35% D.40%
22.水是生命之源,请用所学知识回答有关水的问题。
(1)保持水的化学性质的最小微粒是 。
(2)“生命吸管”(见图)是一种小型便携水净化器,可以将污水直接净化为饮用水。“生命吸管”实际上是一根塑料管,里面装有网丝、注入了活性炭和碘的树脂。其中,网丝起 作用,活性炭起 作用,碘的树脂起 作用。
(3)为了人类和社会经济的可持续发展,我们必须爱护水资源,节约用水是每个公民的责任和义务。下列做法属于节约用水的是 (填序号)
A 城市生活废水直接排入河流
B 农业上合理使用化肥和农药
C 工业废水处理后循环使用
D 用水后及时关闭水龙头
(4)在化学实验室中水还能用于配制溶液,某同学欲配制100g溶质质量分数为5%的氯化钠溶液。
①若用氯化钠固体和水配制,实验步骤为计算、 、溶解;
②若在量取水的过程中仰视读数,则所配溶液的溶质质量分数会 (填“偏大”“偏小”或“不变”)。
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】D
4.【答案】D
5.【答案】D
6.【答案】A
7.【答案】C
8.【答案】B
9.【答案】B
10.【答案】C
11.【答案】A
12.【答案】A
13.【答案】(1)②
(2)10g;90g;100
14.【答案】31.6g;24.0%
15.【答案】(1)B;不能超过试管容积的 ;试管口不可对着自己或他人
(2)平视凹液面(或平视刻度线);凹液面的最低点与刻度线相切
(3)计算;称量;溶解;搅拌,加快蔗糖的溶解
16.【答案】25;降温结晶;B>C>A
17.【答案】饱和;94;46.8
18.【答案】(1)t1℃时,甲、乙两种物质的溶解度相等
(2)甲;4.5;20
19.【答案】(1)B
(2)=
(3)>
(4)>
20.【答案】(1)3.2
(2)解:设25.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2 2H2O+O2↑
68 32
x 3.2g
=
x=6.8g
过氧化氢的质量分数为: ×100%=27.2%.
21.【答案】(1)离子;Na+、Cl-
(2)42.5;搅拌,加速溶解;AB##BA
(3)110g;④;C;A
22.【答案】(1)水分子
(2)过滤;吸附;消毒
(3)CD
(4)称量;偏小
