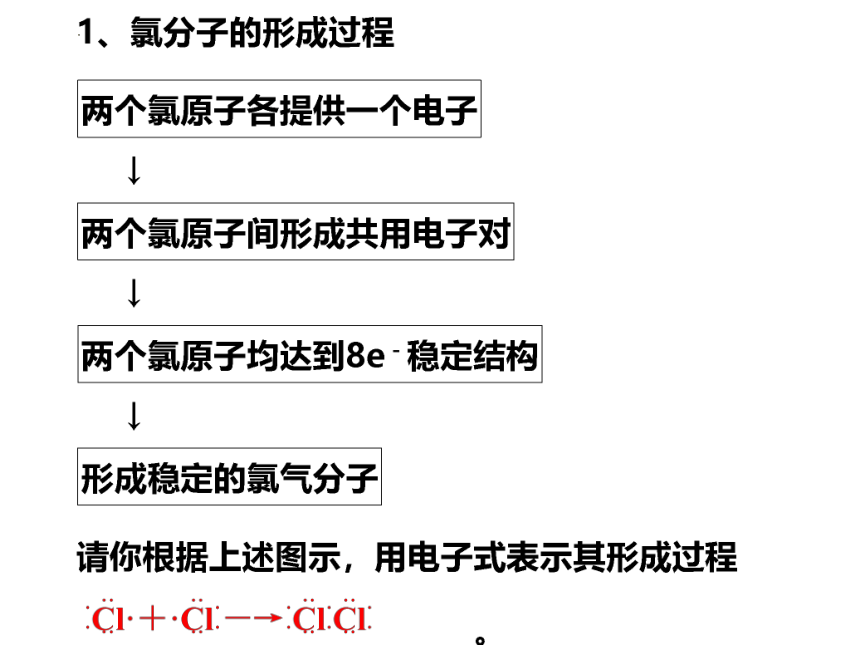
化学人教版(2019)必修第一册4.3.2.共价键(共17张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册4.3.2.共价键(共17张ppt) |
|
|
| 格式 | zip | ||
| 文件大小 | 373.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-27 00:00:00 | ||
图片预览




文档简介
(共17张PPT)
2、 H· 和 原子形成HCl过程中,能否形成离子键?为什么?
HCl分子不是通过离子键来形成,是通过什么方式结合的呢?
不能,因非金属元素的原子均有获得电子的倾向。
Cl
·
·
·
·
·
·
·
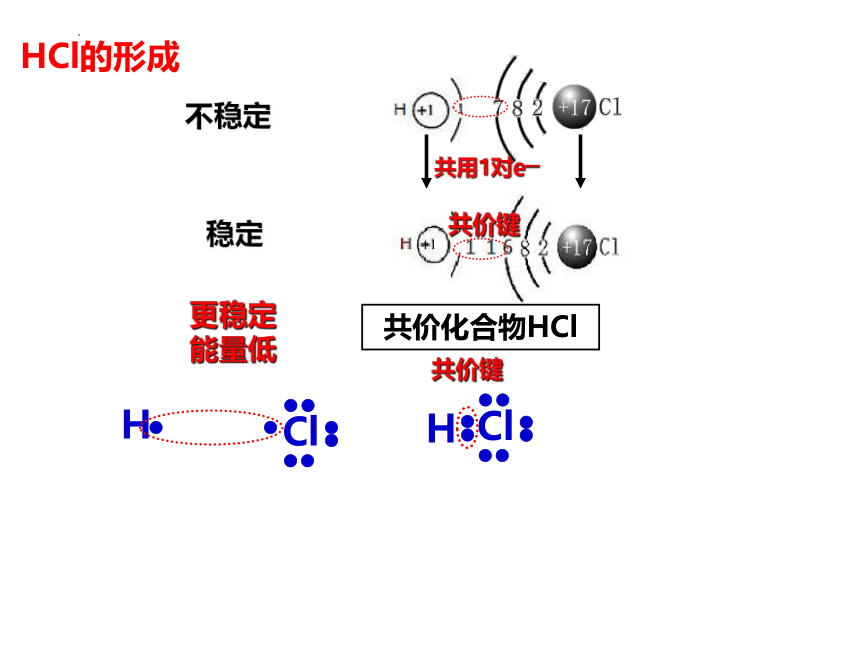
不稳定
共用1对e—
稳定
共价化合物HCl
更稳定
能量低
H
Cl
H
Cl
共价键
共价键
HCl的形成
成键方式 成键粒子 键的本质 成键元素(判断依据)
离子键
共价键
得失电子
阴阳离子
静电作用
活泼金属 + 活泼非金属
包括:
正价原子团
如:NH4+
包括:
负价原子团
如:OH-
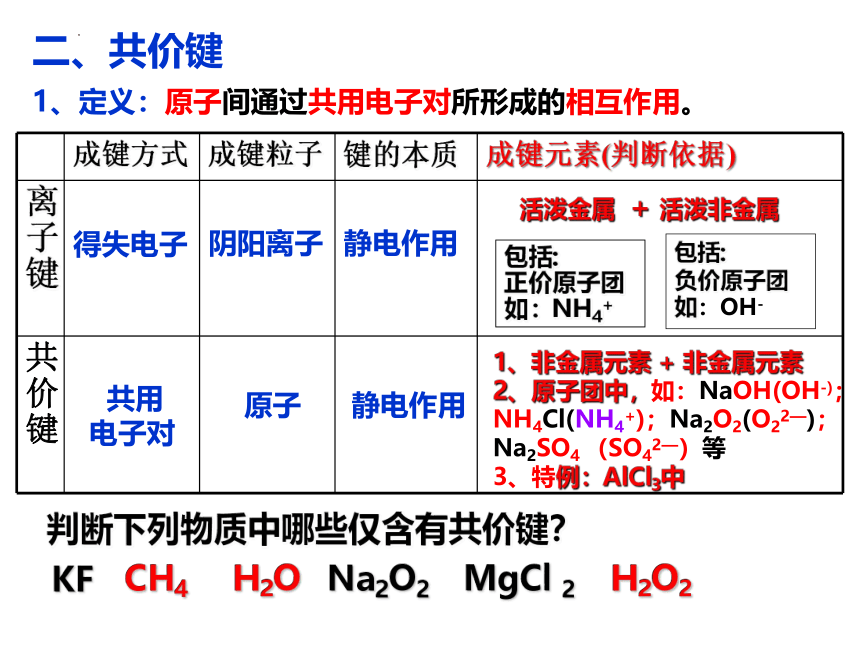
二、共价键
1、定义:原子间通过共用电子对所形成的相互作用。
共用
电子对
原子
静电作用
1、非金属元素 + 非金属元素
2、原子团中,如:NaOH(OH-);NH4Cl(NH4+);Na2O2(O22—);Na2SO4 (SO42—)等
3、特例:AlCl3中
判断下列物质中哪些仅含有共价键?
KF
CH4
MgCl 2
H2O
H2O2
Na2O2
CH4
H2O
H2O2
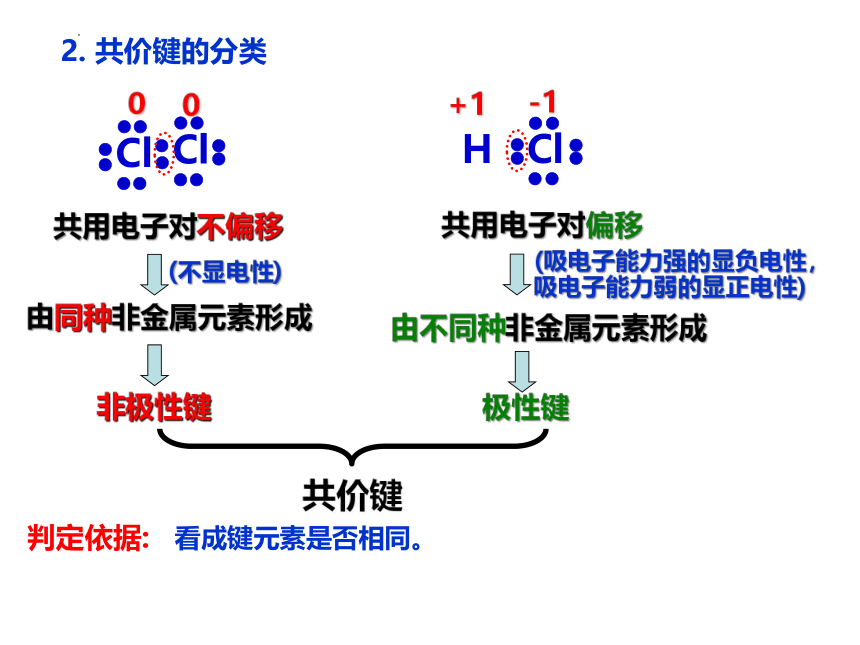
2. 共价键的分类
共用电子对不偏移
共用电子对偏移
由不同种非金属元素形成
由同种非金属元素形成
非极性键
极性键
共价键
Cl
Cl
H
Cl
判定依据:
(不显电性)
(吸电子能力强的显负电性,
吸电子能力弱的显正电性)
0
0
+1
-1
看成键元素是否相同。
2、共价化合物
(1)定义:仅含共价键的化合物叫共价化合物。
注: 共价化合物中一定含有共价键。
含有共价键的化合物不一定是共价化合物,
离子化合物中也可能含有共价键。
如:NaOH、Na2O2等
(2)常见的共价化合物类型:
①非金属氧化物(CO2、SO2等)
②非金属氢化物(H2O、NH3、HCl等)
③酸(H2SO4、HNO3等)
④没有成盐的有机物
从元素种类角度判断,下列物质:
属于离子化合物有_______________;
共价化合物有____________。
①He ②HD
③CaO ④CO2
⑤CaF2 ⑥MgS
⑦AlCl3 ⑧Na2SO4
⑨HNO3 ⑩Ca(OH)2
③ ⑤ ⑥ ⑧ ⑩
④ ⑦ ⑨
H
Cl
× ×
× ×
× ×
× ×
Cl
× ×
× ×
× ×
Cl
× ×
× ×
× ×
× ×
HCl的电子式
Cl2的电子式
3、表示方法
(1)电子式
(2)结构式:
如:H-Cl
Cl-Cl
用一根短线表示一对共用电子。其他电子一律省去
注意:用电子式表示共用电子对形成的分子时,
不标 [ ] 和电荷。
(3)分子的空间结构
4、用电子式表示共价化合物形成过程
H2 O1
确定原子的个数
2H + O
写出电子式
写出电子式
2H
×
O
+
O
×
×
H
H
H1 Cl1
确定原子的个数
H + Cl
写出电子式
写出电子式
H
×
Cl
+
Cl
×
H
O
O
N
N
O2:
N2:
书写规律:
看最外层电子数与稳定结构(2或8电子)比,缺几个,共用几对,其余电子成双成对。
练一练:写出下列物质的电子式和结构式:
(1)O2、N2
CO2:
NH3:
C
O
O
N
H
H
H
练一练:写出下列物质的电子式和结构式:
(2)CO2、H2O、NH3、CH4、HClO、H2O2
书写方法:
先想共几对,要共用多对的摆中间,只共用一对的摆边上。可以先写结构式再画电子式。
CH4:
C
H
H
H
H
练一练:写出下列物质的电子式和结构式:
(2)CO2、H2O、NH3、CH4、HClO、H2O2
HClO:
H2O2 :
练一练:写出下列物质的电子式:
(3)NH4Cl、NaOH、Na2O2
5、共价化合物与离子化合物的比较。
比较项目 离子化合物 共价化合物
定义 阴、阳离子之间以离子键相结合形成的化合物 原子间以共用电子对形成的化合物
构成粒子 阴、阳离子 原子
粒子间的作用 离子键 共价键
熔点、沸点 较高 一般较低,少部分很高
比较项目 离子化合物 共价化合物
导电性 熔融态或 水溶液导电 熔融态不导电,溶于水有的导电(如硫酸),有的不导电
(如蔗糖)
熔化时破 坏的作用力 一定破坏 离子键 不一定破坏共价键
实例 强碱、大多数盐、活泼金属的氧化物等 酸、非金属的氢化物、
非金属的氧化物等
2、 H· 和 原子形成HCl过程中,能否形成离子键?为什么?
HCl分子不是通过离子键来形成,是通过什么方式结合的呢?
不能,因非金属元素的原子均有获得电子的倾向。
Cl
·
·
·
·
·
·
·
不稳定
共用1对e—
稳定
共价化合物HCl
更稳定
能量低
H
Cl
H
Cl
共价键
共价键
HCl的形成
成键方式 成键粒子 键的本质 成键元素(判断依据)
离子键
共价键
得失电子
阴阳离子
静电作用
活泼金属 + 活泼非金属
包括:
正价原子团
如:NH4+
包括:
负价原子团
如:OH-
二、共价键
1、定义:原子间通过共用电子对所形成的相互作用。
共用
电子对
原子
静电作用
1、非金属元素 + 非金属元素
2、原子团中,如:NaOH(OH-);NH4Cl(NH4+);Na2O2(O22—);Na2SO4 (SO42—)等
3、特例:AlCl3中
判断下列物质中哪些仅含有共价键?
KF
CH4
MgCl 2
H2O
H2O2
Na2O2
CH4
H2O
H2O2
2. 共价键的分类
共用电子对不偏移
共用电子对偏移
由不同种非金属元素形成
由同种非金属元素形成
非极性键
极性键
共价键
Cl
Cl
H
Cl
判定依据:
(不显电性)
(吸电子能力强的显负电性,
吸电子能力弱的显正电性)
0
0
+1
-1
看成键元素是否相同。
2、共价化合物
(1)定义:仅含共价键的化合物叫共价化合物。
注: 共价化合物中一定含有共价键。
含有共价键的化合物不一定是共价化合物,
离子化合物中也可能含有共价键。
如:NaOH、Na2O2等
(2)常见的共价化合物类型:
①非金属氧化物(CO2、SO2等)
②非金属氢化物(H2O、NH3、HCl等)
③酸(H2SO4、HNO3等)
④没有成盐的有机物
从元素种类角度判断,下列物质:
属于离子化合物有_______________;
共价化合物有____________。
①He ②HD
③CaO ④CO2
⑤CaF2 ⑥MgS
⑦AlCl3 ⑧Na2SO4
⑨HNO3 ⑩Ca(OH)2
③ ⑤ ⑥ ⑧ ⑩
④ ⑦ ⑨
H
Cl
× ×
× ×
× ×
× ×
Cl
× ×
× ×
× ×
Cl
× ×
× ×
× ×
× ×
HCl的电子式
Cl2的电子式
3、表示方法
(1)电子式
(2)结构式:
如:H-Cl
Cl-Cl
用一根短线表示一对共用电子。其他电子一律省去
注意:用电子式表示共用电子对形成的分子时,
不标 [ ] 和电荷。
(3)分子的空间结构
4、用电子式表示共价化合物形成过程
H2 O1
确定原子的个数
2H + O
写出电子式
写出电子式
2H
×
O
+
O
×
×
H
H
H1 Cl1
确定原子的个数
H + Cl
写出电子式
写出电子式
H
×
Cl
+
Cl
×
H
O
O
N
N
O2:
N2:
书写规律:
看最外层电子数与稳定结构(2或8电子)比,缺几个,共用几对,其余电子成双成对。
练一练:写出下列物质的电子式和结构式:
(1)O2、N2
CO2:
NH3:
C
O
O
N
H
H
H
练一练:写出下列物质的电子式和结构式:
(2)CO2、H2O、NH3、CH4、HClO、H2O2
书写方法:
先想共几对,要共用多对的摆中间,只共用一对的摆边上。可以先写结构式再画电子式。
CH4:
C
H
H
H
H
练一练:写出下列物质的电子式和结构式:
(2)CO2、H2O、NH3、CH4、HClO、H2O2
HClO:
H2O2 :
练一练:写出下列物质的电子式:
(3)NH4Cl、NaOH、Na2O2
5、共价化合物与离子化合物的比较。
比较项目 离子化合物 共价化合物
定义 阴、阳离子之间以离子键相结合形成的化合物 原子间以共用电子对形成的化合物
构成粒子 阴、阳离子 原子
粒子间的作用 离子键 共价键
熔点、沸点 较高 一般较低,少部分很高
比较项目 离子化合物 共价化合物
导电性 熔融态或 水溶液导电 熔融态不导电,溶于水有的导电(如硫酸),有的不导电
(如蔗糖)
熔化时破 坏的作用力 一定破坏 离子键 不一定破坏共价键
实例 强碱、大多数盐、活泼金属的氧化物等 酸、非金属的氢化物、
非金属的氧化物等
