10.3 金属的冶炼与防护 同步练习(含答案) 2022-2023学年北京课改版九年级下册化学
文档属性
| 名称 | 10.3 金属的冶炼与防护 同步练习(含答案) 2022-2023学年北京课改版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 101.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-27 00:00:00 | ||
图片预览

文档简介
10.3 金属的冶炼与防护 同步练习
一、单选题
1.某些食品包装袋内有一包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”.下列物质属于“双吸剂”的是( )
A.铁粉 B.碳粉 C.碱石灰 D.生石灰
2.下列实验现象记录正确的是( )
A.把铜丝放入硫酸铝溶液中,紫红色固体表面产生银白色固体,溶液变成蓝色
B.向氢氧化钾溶液中滴入氯化铁溶液,有浅绿色沉淀生成
C.将一氧化碳通入灼热的氧化铁,红棕色粉末逐渐变为黑色粉末
D.将燃着的木炭伸入氧气中,产生白色火焰,放出热量
3.下列关于实验室模拟工业炼铁的过程说法错误的是()
A.实验前要检查装置气密性
B.实验开始要先通一段时间一氧化碳再加热
C.实验结束后要先停止一氧化碳再停止加热
D.实验过程要注意尾气处理
4.下列物质露置在空气中,能与氧气、水蒸气同时发生反应的是( )
A.铁粉 B.生石灰
C.浓硫酸 D.氢氧化钠固体
5.材料科学日益成为一门重要的学科,分类研究法是研究化学材料的常用方法。现有制作食品级容器的304不锈钢材料,它与下列哪组属于同一类材料()
A.天然材料:地衣提取液、叶绿素
B.合成材料:有机玻璃、合成纤维
C.金属材料:青铜、18K黄金
D.非金属材料:熟石灰、大理石
6.材料中的化学。下列关于金属材料的说法正确的是( )
A.常温下,铝较耐腐蚀,说明铝的活动性较弱
B.钢是铁的合金,氧化铁也是铁的合金
C.通常情况下,铝合金的硬度小于纯铝
D.防锈蚀和回收利用都是保护金属资源的有效途径
7.2018年10月,南通被授予“国家森林城市”称号。为了使南通这座江风海韵森林城变得天更蓝、水更清、景更美,下列做法应该禁止的是()
A.工业废水直接排入河流 B.加强对烟花爆竹燃放管理
C.生产生活垃圾分类放置 D.鼓励对旧金属回收再利用
8.下列措施有利于防止铁制品锈蚀的是( )
A.农具上的铁锈没有及时除去
B.切过酸菜的菜刀不及时清洗
C.工地上的钢管堆放在潮湿的地方
D.剪刀不用时涂上油并放在干燥处
9.下列说法正确的是( )
A.酒精灯中的酒精洒了,在桌上燃烧起来,不要惊慌,应立即用水浇灭
B.把铁粉和炭粉混合均匀后就得到了铁的合金
C.保护金属资源的有效途径至少有三种
D.被雨水淋湿的自行车须先用干布擦净后才能用带油的布擦
10.下列关于碳及其化合物的说法正确的是( )
A.焦炭还原氧化铜发生的是置换反应
B.CO2的过量排放是导致酸雨的主要原因
C.铅笔字迹易变模糊是因为常温下石墨的化学性质活泼
D.CO和CO2都是大气污染物
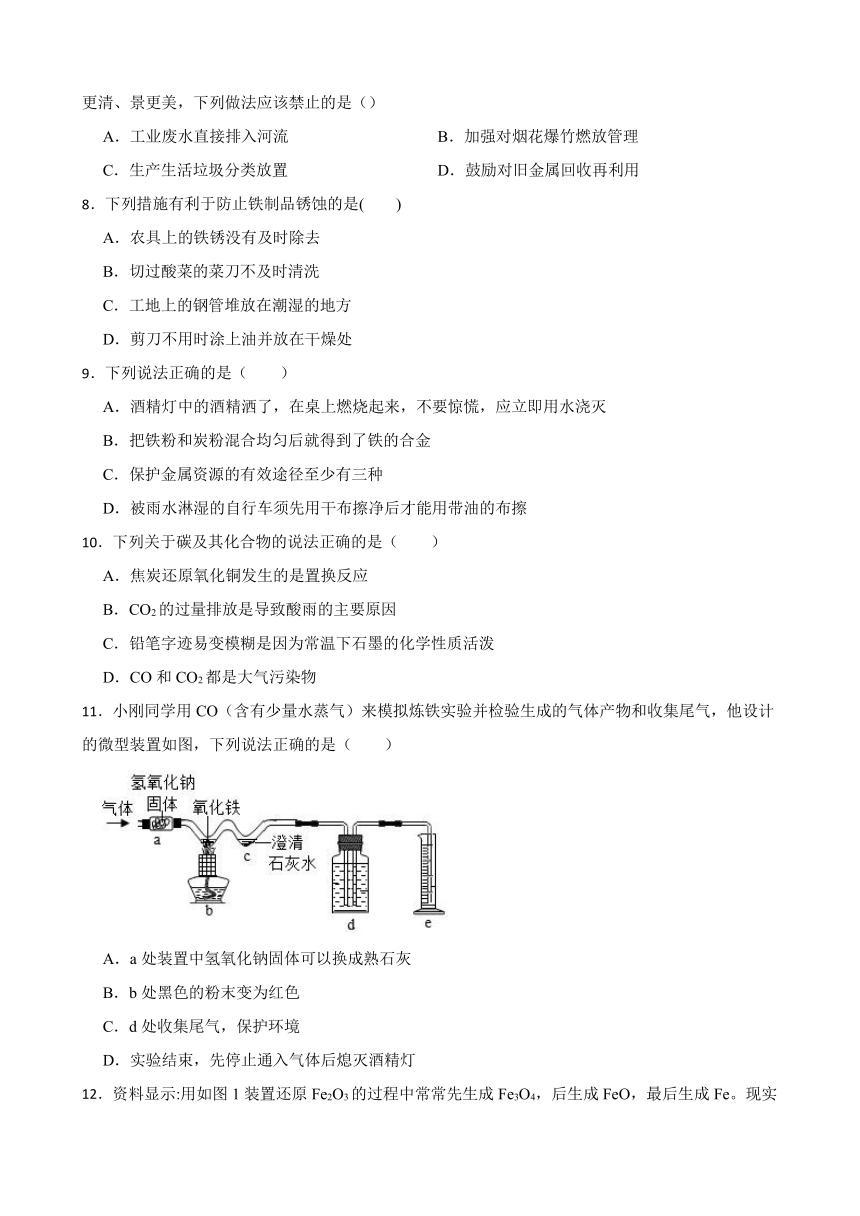
11.小刚同学用CO(含有少量水蒸气)来模拟炼铁实验并检验生成的气体产物和收集尾气,他设计的微型装置如图,下列说法正确的是( )
A.a处装置中氢氧化钠固体可以换成熟石灰
B.b处黑色的粉末变为红色
C.d处收集尾气,保护环境
D.实验结束,先停止通入气体后熄灭酒精灯
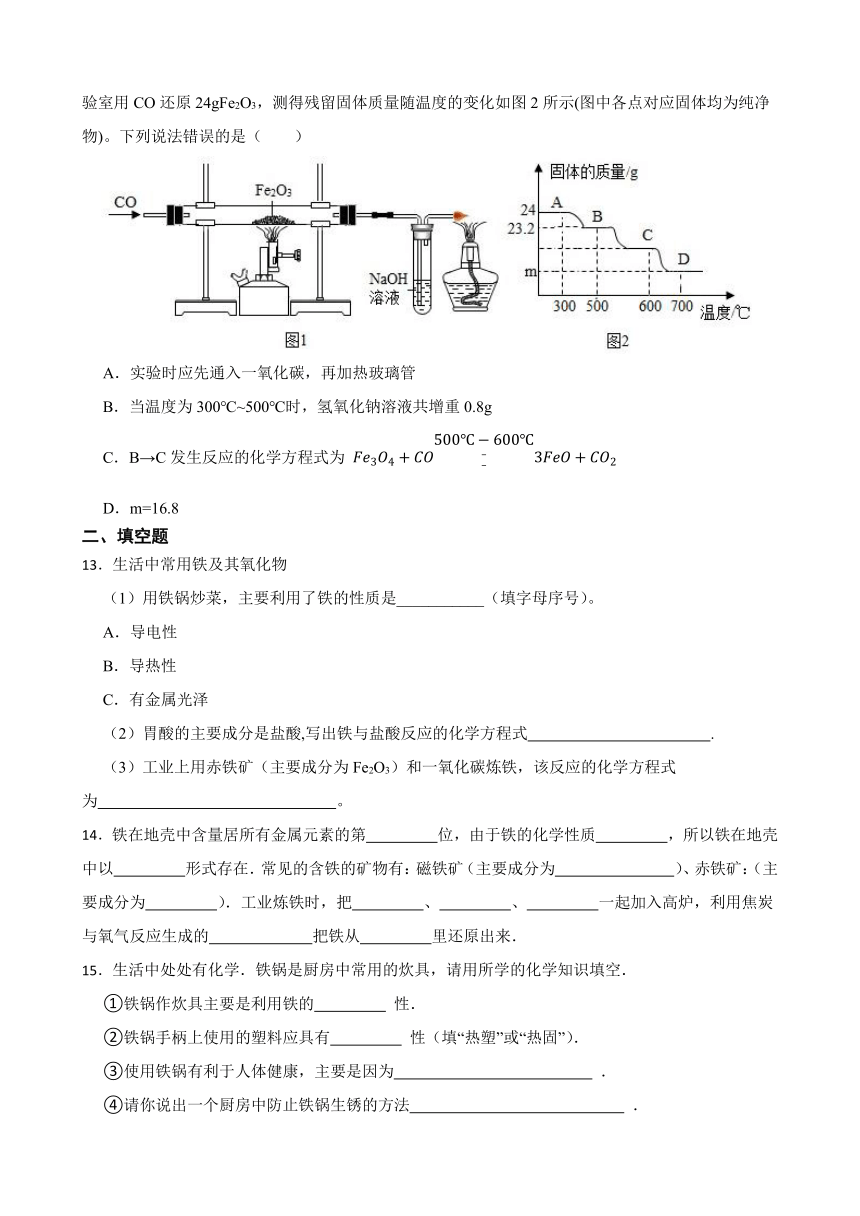
12.资料显示:用如图1装置还原Fe2O3的过程中常常先生成Fe3O4,后生成FeO,最后生成Fe。现实验室用CO还原24gFe2O3,测得残留固体质量随温度的变化如图2所示(图中各点对应固体均为纯净物)。下列说法错误的是( )
A.实验时应先通入一氧化碳,再加热玻璃管
B.当温度为300℃~500℃时,氢氧化钠溶液共增重0.8g
C.B→C发生反应的化学方程式为
D.m=16.8
二、填空题
13.生活中常用铁及其氧化物
(1)用铁锅炒菜,主要利用了铁的性质是___________(填字母序号)。
A.导电性
B.导热性
C.有金属光泽
(2)胃酸的主要成分是盐酸,写出铁与盐酸反应的化学方程式 .
(3)工业上用赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁,该反应的化学方程式为 。
14.铁在地壳中含量居所有金属元素的第 位,由于铁的化学性质 ,所以铁在地壳中以 形式存在.常见的含铁的矿物有:磁铁矿(主要成分为 )、赤铁矿:(主要成分为 ).工业炼铁时,把 、 、 一起加入高炉,利用焦炭与氧气反应生成的 把铁从 里还原出来.
15.生活中处处有化学.铁锅是厨房中常用的炊具,请用所学的化学知识填空.
①铁锅作炊具主要是利用铁的 性.
②铁锅手柄上使用的塑料应具有 性(填“热塑”或“热固”).
③使用铁锅有利于人体健康,主要是因为 .
④请你说出一个厨房中防止铁锅生锈的方法 .
16.冶炼金属的常用方法有 、 、 .
17.2014年11月,乐山人民翘首以盼的“成﹣绵﹣乐”高速列车(又称高铁)终于通车了.这不仅对了山、成都、绵阳,对四川乃至西南地区的社会经济发展都会带来积极而深远的影响.
结合所学的化学知识,回答下列有关的问题:
(一)高铁列车上可提供下列用品:纯净水、食盐、橙汁、牛奶、饼干、蔗糖等.
(1)写出:①食盐化学式 ;②两个水分子 ;
(2)上述物质中,含蛋白质最丰富的物质是 ;含维生素最丰富的物质是 ;.
(3)从宏观角度看,水是由 组成的.
(二)修建铁路所需大量钢铁是以铁矿石为主要原料冶炼而得.
(1)写出用一氧化碳和赤铁矿炼铁的化学方程式 ;
(2)钢是含0.03%﹣2% 的铁合金;
(3)雨后的铁轨表面易产生少量的锈迹,这是因为 ;
(4)实验室可用盐酸除铁锈,其化学方程式为 ;
(三)与高铁的电动列车形成鲜明对比的是以煤炭燃烧为动力的乐山嘉阳小火车,它是目前世界上仅存的少数几辆仍在运行的蒸汽机车之一,被称为“工业文明的活化石”.
(1)煤炭燃烧应具备的条件:①与空气(或氧气)接触,② ;
(2)从化学的角度分析蒸汽列车被电动列车淘汰的原因(任举一点) .
18.如图是探究铁钉锈蚀的实验。一段时间后,观察到 U 型管中红墨水液面的变化是 ;对比 a、b 两个实验,可得出铁生锈的一个条件是 ;工业上常用稀硫酸除铁锈,反应的化学方程式为 。
三、综合题
19.我国古代的物质文明华夏民族在认识、改造和应用物质方面有着辉煌的历史.
①东晋《抱扑子》中记载:“以曾青涂铁,铁赤色如铜”(“曾青”即硫酸铜溶液).
②战国《周礼》中记载;“煤饼烧砺房成灰”(“砺房”即牡砺壳,主要成分是碳酸钙).将“灰”溶于水可制得沤浸树皮脱胶的碱液.
③元代《庚道集》中记载:“点铜戍银”(即单质锏与砷熔合形成银白色的物质).
请运用你学过的化学知识回答下列问题;
(1)在①~③中,发生了化学变化的是 (填编号)其中发生分解反应的化学方程式为 .
(2)①中发生变化的化学方程式为 ,该反应中发生有效的相互作用而促使变化发生的微粒是(写出微粒符号) .
(3)②中“灰”溶于水的变化中,其能量的转化形式是 .
(4)③中的“银”是否属于合金? .
20.生活中处处是化学。
(1)加了洗涤剂的水能除去衣服上的油污,是因为洗涤剂有 的功能。
(2)铁制品锈蚀的过程,实际上是铁与空气中的 等发生化学反应的过程。
(3)碳素笔写字,可以很长时间也不褪色的原因: 。
(4)在人体组织里,葡萄糖(C6H12O6)在酶的作用下缓慢氧化,同时放出能量,供机体活动和维持体温的需要,该反应的化学方程式 。
(5)洁厕灵常常是蓝色的,请猜测里面可能含有 物质。
21.化学与生活密切相关,请结合实际填空:
(1)学校实验室有一批生锈报废的铁架台,它们生锈的原因是 .
(2)城市中人行天桥的建成,极大地方便了市民安全出行,建桥使用的不锈钢属于 材料.
(3)大量煤燃烧产生的SO2,机动车尾气排放出来的氮氧化物,它们与水反应降落在地面上形成 .
(4)科学膳食是人类健康的保障,下表是某学校食堂的食谱,从所含营养素角度分析
主食 米饭 馒头
副食 红烧肉 鸡蛋 豆腐汤
饮料 纯净水 可乐
(除无机盐),你认为食谱中还应添加 (填字母)
A.牛肉 B.清蒸鱼 C.青菜 D.牛奶.
22.化学是一门以实验为基础的科学,下面是初中化学中几个重要的对比实验。
(1)实验1中,观察到铜片上的白磷燃烧而红磷不燃烧,可得出可燃物燃烧的一个条件为 。
(2)实验2中,观察到A烧杯中的现象是 ,由此可验证分子的性质是 。
(3)实验3中,对比铁钉表面的不同现象,可推知防止铁生锈的原理是 。
答案解析部分
1.【答案】A
2.【答案】C
3.【答案】C
4.【答案】A
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】D
9.【答案】D
10.【答案】A
11.【答案】C
12.【答案】B
13.【答案】(1)B
(2)Fe+2HCl=FeCl2+H2↑
(3)Fe2O3+3CO 2Fe+3CO2
14.【答案】二;活泼;化合物;四氧化三铁;氧化铁;铁矿石;焦炭;石灰石;一氧化碳;化合物
15.【答案】导热;热固;能够为人体提供铁元素;保持铁锅表面洁净、干燥
16.【答案】电解法;热还原法;热分解法
17.【答案】NaCl;2H2O;牛奶;橙汁;氢、氧元素;3CO+Fe2O32Fe+3CO2;碳;铁在潮湿的空气中易生锈;Fe2O3+6HCl=2FeCl3+3H2O;温度达到着火点;对环境有污染
18.【答案】左高右低;与水接触;
19.【答案】(1)①②;CaCO3 CaO+CO2↑
(2)Fe+CuSO4=FeSO4+Cu;Fe失电子变成Fe2+、Cu2+得电子变成Cu
(3)化学能转化为热能
(4)是(或属于)
20.【答案】(1)乳化
(2)氧气和水
(3)常温下碳的化学性质不活泼
(4)
(5)铜离子溶液
21.【答案】(1)铁与空气中的水蒸气和氧气接触发生了化学反应
(2)金属
(3)酸雨
(4)C
22.【答案】(1)温度达到可燃物的着火点
(2)溶液由无色变为红色;分子不断地运动着
(3)隔绝水或隔绝氧气(或空气)
一、单选题
1.某些食品包装袋内有一包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”.下列物质属于“双吸剂”的是( )
A.铁粉 B.碳粉 C.碱石灰 D.生石灰
2.下列实验现象记录正确的是( )
A.把铜丝放入硫酸铝溶液中,紫红色固体表面产生银白色固体,溶液变成蓝色
B.向氢氧化钾溶液中滴入氯化铁溶液,有浅绿色沉淀生成
C.将一氧化碳通入灼热的氧化铁,红棕色粉末逐渐变为黑色粉末
D.将燃着的木炭伸入氧气中,产生白色火焰,放出热量
3.下列关于实验室模拟工业炼铁的过程说法错误的是()
A.实验前要检查装置气密性
B.实验开始要先通一段时间一氧化碳再加热
C.实验结束后要先停止一氧化碳再停止加热
D.实验过程要注意尾气处理
4.下列物质露置在空气中,能与氧气、水蒸气同时发生反应的是( )
A.铁粉 B.生石灰
C.浓硫酸 D.氢氧化钠固体
5.材料科学日益成为一门重要的学科,分类研究法是研究化学材料的常用方法。现有制作食品级容器的304不锈钢材料,它与下列哪组属于同一类材料()
A.天然材料:地衣提取液、叶绿素
B.合成材料:有机玻璃、合成纤维
C.金属材料:青铜、18K黄金
D.非金属材料:熟石灰、大理石
6.材料中的化学。下列关于金属材料的说法正确的是( )
A.常温下,铝较耐腐蚀,说明铝的活动性较弱
B.钢是铁的合金,氧化铁也是铁的合金
C.通常情况下,铝合金的硬度小于纯铝
D.防锈蚀和回收利用都是保护金属资源的有效途径
7.2018年10月,南通被授予“国家森林城市”称号。为了使南通这座江风海韵森林城变得天更蓝、水更清、景更美,下列做法应该禁止的是()
A.工业废水直接排入河流 B.加强对烟花爆竹燃放管理
C.生产生活垃圾分类放置 D.鼓励对旧金属回收再利用
8.下列措施有利于防止铁制品锈蚀的是( )
A.农具上的铁锈没有及时除去
B.切过酸菜的菜刀不及时清洗
C.工地上的钢管堆放在潮湿的地方
D.剪刀不用时涂上油并放在干燥处
9.下列说法正确的是( )
A.酒精灯中的酒精洒了,在桌上燃烧起来,不要惊慌,应立即用水浇灭
B.把铁粉和炭粉混合均匀后就得到了铁的合金
C.保护金属资源的有效途径至少有三种
D.被雨水淋湿的自行车须先用干布擦净后才能用带油的布擦
10.下列关于碳及其化合物的说法正确的是( )
A.焦炭还原氧化铜发生的是置换反应
B.CO2的过量排放是导致酸雨的主要原因
C.铅笔字迹易变模糊是因为常温下石墨的化学性质活泼
D.CO和CO2都是大气污染物
11.小刚同学用CO(含有少量水蒸气)来模拟炼铁实验并检验生成的气体产物和收集尾气,他设计的微型装置如图,下列说法正确的是( )
A.a处装置中氢氧化钠固体可以换成熟石灰
B.b处黑色的粉末变为红色
C.d处收集尾气,保护环境
D.实验结束,先停止通入气体后熄灭酒精灯
12.资料显示:用如图1装置还原Fe2O3的过程中常常先生成Fe3O4,后生成FeO,最后生成Fe。现实验室用CO还原24gFe2O3,测得残留固体质量随温度的变化如图2所示(图中各点对应固体均为纯净物)。下列说法错误的是( )
A.实验时应先通入一氧化碳,再加热玻璃管
B.当温度为300℃~500℃时,氢氧化钠溶液共增重0.8g
C.B→C发生反应的化学方程式为
D.m=16.8
二、填空题
13.生活中常用铁及其氧化物
(1)用铁锅炒菜,主要利用了铁的性质是___________(填字母序号)。
A.导电性
B.导热性
C.有金属光泽
(2)胃酸的主要成分是盐酸,写出铁与盐酸反应的化学方程式 .
(3)工业上用赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁,该反应的化学方程式为 。
14.铁在地壳中含量居所有金属元素的第 位,由于铁的化学性质 ,所以铁在地壳中以 形式存在.常见的含铁的矿物有:磁铁矿(主要成分为 )、赤铁矿:(主要成分为 ).工业炼铁时,把 、 、 一起加入高炉,利用焦炭与氧气反应生成的 把铁从 里还原出来.
15.生活中处处有化学.铁锅是厨房中常用的炊具,请用所学的化学知识填空.
①铁锅作炊具主要是利用铁的 性.
②铁锅手柄上使用的塑料应具有 性(填“热塑”或“热固”).
③使用铁锅有利于人体健康,主要是因为 .
④请你说出一个厨房中防止铁锅生锈的方法 .
16.冶炼金属的常用方法有 、 、 .
17.2014年11月,乐山人民翘首以盼的“成﹣绵﹣乐”高速列车(又称高铁)终于通车了.这不仅对了山、成都、绵阳,对四川乃至西南地区的社会经济发展都会带来积极而深远的影响.
结合所学的化学知识,回答下列有关的问题:
(一)高铁列车上可提供下列用品:纯净水、食盐、橙汁、牛奶、饼干、蔗糖等.
(1)写出:①食盐化学式 ;②两个水分子 ;
(2)上述物质中,含蛋白质最丰富的物质是 ;含维生素最丰富的物质是 ;.
(3)从宏观角度看,水是由 组成的.
(二)修建铁路所需大量钢铁是以铁矿石为主要原料冶炼而得.
(1)写出用一氧化碳和赤铁矿炼铁的化学方程式 ;
(2)钢是含0.03%﹣2% 的铁合金;
(3)雨后的铁轨表面易产生少量的锈迹,这是因为 ;
(4)实验室可用盐酸除铁锈,其化学方程式为 ;
(三)与高铁的电动列车形成鲜明对比的是以煤炭燃烧为动力的乐山嘉阳小火车,它是目前世界上仅存的少数几辆仍在运行的蒸汽机车之一,被称为“工业文明的活化石”.
(1)煤炭燃烧应具备的条件:①与空气(或氧气)接触,② ;
(2)从化学的角度分析蒸汽列车被电动列车淘汰的原因(任举一点) .
18.如图是探究铁钉锈蚀的实验。一段时间后,观察到 U 型管中红墨水液面的变化是 ;对比 a、b 两个实验,可得出铁生锈的一个条件是 ;工业上常用稀硫酸除铁锈,反应的化学方程式为 。
三、综合题
19.我国古代的物质文明华夏民族在认识、改造和应用物质方面有着辉煌的历史.
①东晋《抱扑子》中记载:“以曾青涂铁,铁赤色如铜”(“曾青”即硫酸铜溶液).
②战国《周礼》中记载;“煤饼烧砺房成灰”(“砺房”即牡砺壳,主要成分是碳酸钙).将“灰”溶于水可制得沤浸树皮脱胶的碱液.
③元代《庚道集》中记载:“点铜戍银”(即单质锏与砷熔合形成银白色的物质).
请运用你学过的化学知识回答下列问题;
(1)在①~③中,发生了化学变化的是 (填编号)其中发生分解反应的化学方程式为 .
(2)①中发生变化的化学方程式为 ,该反应中发生有效的相互作用而促使变化发生的微粒是(写出微粒符号) .
(3)②中“灰”溶于水的变化中,其能量的转化形式是 .
(4)③中的“银”是否属于合金? .
20.生活中处处是化学。
(1)加了洗涤剂的水能除去衣服上的油污,是因为洗涤剂有 的功能。
(2)铁制品锈蚀的过程,实际上是铁与空气中的 等发生化学反应的过程。
(3)碳素笔写字,可以很长时间也不褪色的原因: 。
(4)在人体组织里,葡萄糖(C6H12O6)在酶的作用下缓慢氧化,同时放出能量,供机体活动和维持体温的需要,该反应的化学方程式 。
(5)洁厕灵常常是蓝色的,请猜测里面可能含有 物质。
21.化学与生活密切相关,请结合实际填空:
(1)学校实验室有一批生锈报废的铁架台,它们生锈的原因是 .
(2)城市中人行天桥的建成,极大地方便了市民安全出行,建桥使用的不锈钢属于 材料.
(3)大量煤燃烧产生的SO2,机动车尾气排放出来的氮氧化物,它们与水反应降落在地面上形成 .
(4)科学膳食是人类健康的保障,下表是某学校食堂的食谱,从所含营养素角度分析
主食 米饭 馒头
副食 红烧肉 鸡蛋 豆腐汤
饮料 纯净水 可乐
(除无机盐),你认为食谱中还应添加 (填字母)
A.牛肉 B.清蒸鱼 C.青菜 D.牛奶.
22.化学是一门以实验为基础的科学,下面是初中化学中几个重要的对比实验。
(1)实验1中,观察到铜片上的白磷燃烧而红磷不燃烧,可得出可燃物燃烧的一个条件为 。
(2)实验2中,观察到A烧杯中的现象是 ,由此可验证分子的性质是 。
(3)实验3中,对比铁钉表面的不同现象,可推知防止铁生锈的原理是 。
答案解析部分
1.【答案】A
2.【答案】C
3.【答案】C
4.【答案】A
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】D
9.【答案】D
10.【答案】A
11.【答案】C
12.【答案】B
13.【答案】(1)B
(2)Fe+2HCl=FeCl2+H2↑
(3)Fe2O3+3CO 2Fe+3CO2
14.【答案】二;活泼;化合物;四氧化三铁;氧化铁;铁矿石;焦炭;石灰石;一氧化碳;化合物
15.【答案】导热;热固;能够为人体提供铁元素;保持铁锅表面洁净、干燥
16.【答案】电解法;热还原法;热分解法
17.【答案】NaCl;2H2O;牛奶;橙汁;氢、氧元素;3CO+Fe2O32Fe+3CO2;碳;铁在潮湿的空气中易生锈;Fe2O3+6HCl=2FeCl3+3H2O;温度达到着火点;对环境有污染
18.【答案】左高右低;与水接触;
19.【答案】(1)①②;CaCO3 CaO+CO2↑
(2)Fe+CuSO4=FeSO4+Cu;Fe失电子变成Fe2+、Cu2+得电子变成Cu
(3)化学能转化为热能
(4)是(或属于)
20.【答案】(1)乳化
(2)氧气和水
(3)常温下碳的化学性质不活泼
(4)
(5)铜离子溶液
21.【答案】(1)铁与空气中的水蒸气和氧气接触发生了化学反应
(2)金属
(3)酸雨
(4)C
22.【答案】(1)温度达到可燃物的着火点
(2)溶液由无色变为红色;分子不断地运动着
(3)隔绝水或隔绝氧气(或空气)
