第二章第二节第一课时氯气(共21张PPT)2022-2023学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 第二章第二节第一课时氯气(共21张PPT)2022-2023学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-28 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
氯及其化合物(第1课时)
1774年,舍勒将MnO2与浓盐酸混合加热,产生了一种黄绿色的气体。直到1810年,英国化学家戴维以大量的实验事实为根据,他将这种元素命名为chlorine(Cl2)
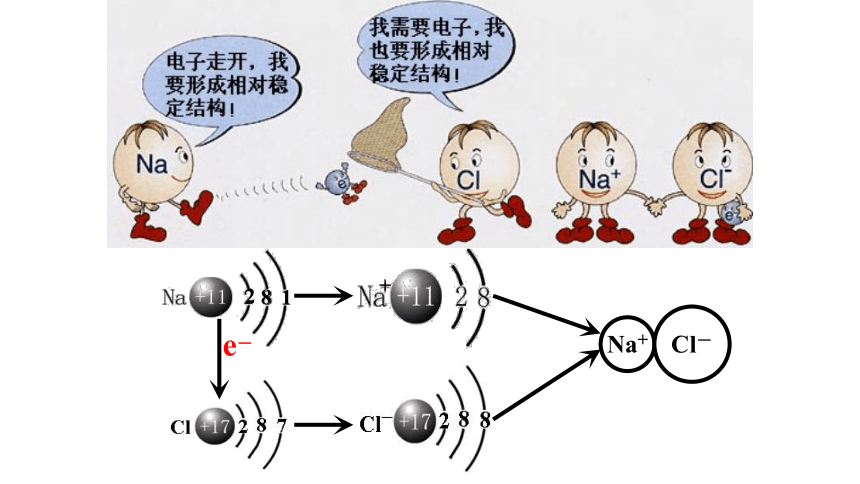
e-
Na+
Cl-
1
8
2
+
氯离子的存在及在人体中的作用
人体体液中的Na+和Cl-对于调节体液的物理和化学特性,保证体内正常的生理活动和功能发挥着重要的作用。人体所需要的钠元素和氯元素除了来自食物外,还要通过食盐来补充。以NaCl为主要成分的食盐是重要的调味剂。氯元素是重要的“成盐元素”,主要以NaCl的形式存在于海水和陆地的盐矿中。据探测,海洋中含盐 3%,主要为NaCl,此外,因为还有MgCl2、MgSO4等盐类,致使海水既咸又苦,不能直接饮用。海洋是包括NaCl在内的巨大的资源宝库。
Cl2的发现和确认
2、舍勒发现氯气的方法至今还是制取氯气的主要
方法之一。请写出舍勒发现氯气的化学方程式?
MnO2 + HCl(浓) Cl2↑+…
-1
+4
0
MnO2+4HCl(浓) Cl2↑+MnCl2+2H2O
【思考与交流】
1、从氯气的发现到确认为一种新的元素,时间长达30
多年。你从这一史实中得到什么启示?
启示1:科学研究需要有正确的理论作指导。
启示2:科学研究需要以大量事实为依据,只有大量事
实才能推翻错误的理论。
启示3:科学研究需要有热爱科学和奉献科学的精神。
2、舍勒发现氯气的方法至今还是制取氯气的主要
方法之一。请写出舍勒发现氯气的化学方程式?
新华网报道:2005年3月29日,京沪高速公路淮安段一辆满载液氯的罐车和迎面来车相撞,大量液氯外泄。据目击者描述:“一股黄绿色的气体就像探照灯光一样,‘唰’地射向高空,足有5米高,并有刺鼻的气味,眼睛也熏得有些睁不开。”事发后消防队员不断地用水枪喷射,但时值西南风,氯气迅速向东北方扩散 ,造成350人中毒进医院救治,附近居民采取应急措施,疏散到一高坡上。
京沪高速公路氯气泄漏事件
1、色、态:
2、气 味:
3、密度(与空气比):
4、水溶性:
5、三态变化:
一、氯气的物理性质
氯气
液氯
固态氯
黄绿色气体
刺激性气味
大
可溶于水
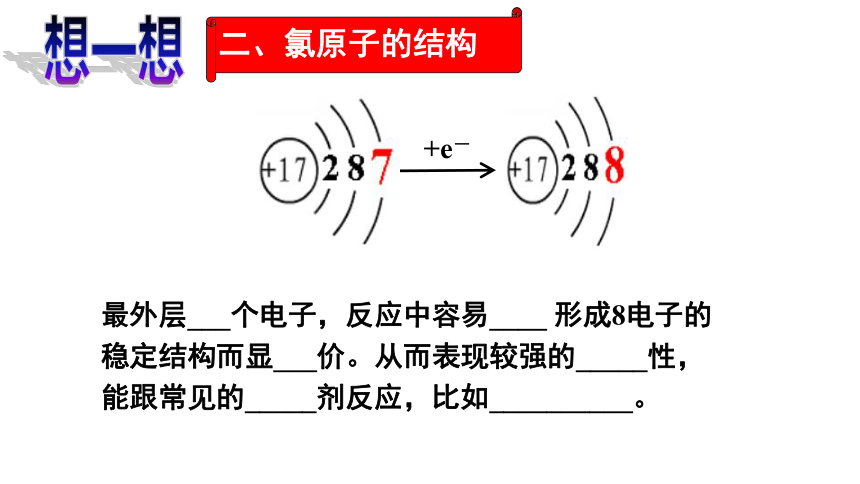
最外层___个电子,反应中容易____ 形成8电子的稳定结构而显___价。从而表现较强的_____性,能跟常见的_____剂反应,比如__________。
+e-
二、氯原子的结构
三、氯气的化学性质
1、氯气与金属的反应
【写一写】
2Na + Cl2 2NaCl
Cu + Cl2 CuCl2
2Fe + 3Cl2 2FeCl3
点燃
点燃
点燃
三、氯气的化学性质
2、氯气与H2的反应
H2 + Cl2 2HCl
点燃
现象:纯净的氢气在氯气中安静地燃烧,
发出______火焰,放出大量的热,
瓶口有大量_____产生。
苍白色
白雾
【思考与交流】
通过H2在Cl2燃烧的实验,你对燃烧的条件及其本质有什么新的认识
(1)燃烧是否一定需要氧气参加?__________
(2)燃烧的本质是__________反应(类型)。
H2 + Cl2 2HCl
点燃
2H2 + O2 2H2O
点燃
(3)任何发光放热的剧烈的化学反应叫做燃烧。
H2 + Cl2 2HCl
点燃
氯气与单质的反应
2Na + Cl2 2NaCl
Cu + Cl2 CuCl2
2Fe + 3Cl2 2FeCl3
点燃
点燃
点燃
(1)四个反应的氧化剂是什么物质?
(2)Cl2在反应中均从__价变为__价。
(3)Fe、Cu在化合物中常见有那些价态?
Cl2在反应中容易____电子,从而使Cl显__价,表现出较强的____性,能将变价金属氧化成__价态。
0
-1
0
-1
0
-1
得到
-1
氧化
高
三、氯气的化学性质
1.【提出问题 】
氯气与水反应
氯气能否与H2O反应?其成分是什么?
2.【猜想与假设】
假设一:氯气与水不反应,则只溶解成分是:
假设二:氯气与水会要反应,则可能成分是:
Cl2、H2O
HCl(H+ + Cl-)+???
实验
目的 探究Cl2和水是否反应
实验方案
操作
现象
实验结论
探究2:氯水中有无H+
探究1:氯水中有无Cl-
氯水中没有H+,
假设二不成立。
氯水中有 Cl-,
假设二成立。
3.【设计并进行实验】
氯水+石蕊试液
氯水+硝酸银+稀硝酸
有白色沉淀生成
溶液未变红
4.【反思并进一步探究】
方案:在石蕊试液中逐滴加入氯水
现 象:
氯水中有种成分具有漂白性
氯水中有H+存在,假设二成立。
新问题:氯水中哪一种成分具有漂白性?
盐酸、Cl2、?
结 论:
先变红后褪色
干燥红布条的接触物 现 象 结 论
盐 酸
干燥Cl2
湿润的Cl2
探究:氯水中具有漂白性的物质是什么?
红布条未褪色
红布条未褪色
红布条褪色
起漂白作用的不是盐酸
起漂白作用的不是Cl2
具有漂白性的物质是
氯气与水反应生成的
新的物质
氯气与水反应
三、氯气的化学性质
3、氯气与H2O的反应
Cl2 + H2O = HCl + HClO
2HClO 2HCl+O2↑
光照
HClO
弱酸性
强氧化性
漂白性
不稳定性:
结构
性质
知识小结
1.与金属反应(Na、Fe、Cu等)
2.与非金属反应(H2等)
3.与水反应
强氧化性
用途
+e-
学会分析:
1、下列氯化物不可以由金属和氯气直接反应制得的是( )
A.CuCl2 B.MgCl2 C.FeCl2 D.AlCl3
学会比较:
2、下列说法正确的是( )
A.Cl和Cl-的化学性质一样
B.干燥氯气不具有漂白性
C.Cl2有毒,Cl-也有毒
D.Cl2和Cl-都是黄绿色
学会应用:
3、氯气可以用来消灭田鼠,为此将Cl2通过软管灌入洞中,
这是利用了Cl2下列性质中的( )
①黄绿色 ②密度比较大 ③有毒
④较易液化 ⑤溶解于水
A.①②③ B.②③ C.③④ D.③④⑤
C
B
B
练一练
2、若你周围不幸发生氯气泄漏事故,你
怎样用已有化学知识进行恰当处理?
1、新制氯水与久置氯水各含有哪些粒子?
性质有何不同?
作 业
3、思考Cl2能否与碱发生反应?若能,生
成物是什么?
氯及其化合物(第1课时)
1774年,舍勒将MnO2与浓盐酸混合加热,产生了一种黄绿色的气体。直到1810年,英国化学家戴维以大量的实验事实为根据,他将这种元素命名为chlorine(Cl2)
e-
Na+
Cl-
1
8
2
+
氯离子的存在及在人体中的作用
人体体液中的Na+和Cl-对于调节体液的物理和化学特性,保证体内正常的生理活动和功能发挥着重要的作用。人体所需要的钠元素和氯元素除了来自食物外,还要通过食盐来补充。以NaCl为主要成分的食盐是重要的调味剂。氯元素是重要的“成盐元素”,主要以NaCl的形式存在于海水和陆地的盐矿中。据探测,海洋中含盐 3%,主要为NaCl,此外,因为还有MgCl2、MgSO4等盐类,致使海水既咸又苦,不能直接饮用。海洋是包括NaCl在内的巨大的资源宝库。
Cl2的发现和确认
2、舍勒发现氯气的方法至今还是制取氯气的主要
方法之一。请写出舍勒发现氯气的化学方程式?
MnO2 + HCl(浓) Cl2↑+…
-1
+4
0
MnO2+4HCl(浓) Cl2↑+MnCl2+2H2O
【思考与交流】
1、从氯气的发现到确认为一种新的元素,时间长达30
多年。你从这一史实中得到什么启示?
启示1:科学研究需要有正确的理论作指导。
启示2:科学研究需要以大量事实为依据,只有大量事
实才能推翻错误的理论。
启示3:科学研究需要有热爱科学和奉献科学的精神。
2、舍勒发现氯气的方法至今还是制取氯气的主要
方法之一。请写出舍勒发现氯气的化学方程式?
新华网报道:2005年3月29日,京沪高速公路淮安段一辆满载液氯的罐车和迎面来车相撞,大量液氯外泄。据目击者描述:“一股黄绿色的气体就像探照灯光一样,‘唰’地射向高空,足有5米高,并有刺鼻的气味,眼睛也熏得有些睁不开。”事发后消防队员不断地用水枪喷射,但时值西南风,氯气迅速向东北方扩散 ,造成350人中毒进医院救治,附近居民采取应急措施,疏散到一高坡上。
京沪高速公路氯气泄漏事件
1、色、态:
2、气 味:
3、密度(与空气比):
4、水溶性:
5、三态变化:
一、氯气的物理性质
氯气
液氯
固态氯
黄绿色气体
刺激性气味
大
可溶于水
最外层___个电子,反应中容易____ 形成8电子的稳定结构而显___价。从而表现较强的_____性,能跟常见的_____剂反应,比如__________。
+e-
二、氯原子的结构
三、氯气的化学性质
1、氯气与金属的反应
【写一写】
2Na + Cl2 2NaCl
Cu + Cl2 CuCl2
2Fe + 3Cl2 2FeCl3
点燃
点燃
点燃
三、氯气的化学性质
2、氯气与H2的反应
H2 + Cl2 2HCl
点燃
现象:纯净的氢气在氯气中安静地燃烧,
发出______火焰,放出大量的热,
瓶口有大量_____产生。
苍白色
白雾
【思考与交流】
通过H2在Cl2燃烧的实验,你对燃烧的条件及其本质有什么新的认识
(1)燃烧是否一定需要氧气参加?__________
(2)燃烧的本质是__________反应(类型)。
H2 + Cl2 2HCl
点燃
2H2 + O2 2H2O
点燃
(3)任何发光放热的剧烈的化学反应叫做燃烧。
H2 + Cl2 2HCl
点燃
氯气与单质的反应
2Na + Cl2 2NaCl
Cu + Cl2 CuCl2
2Fe + 3Cl2 2FeCl3
点燃
点燃
点燃
(1)四个反应的氧化剂是什么物质?
(2)Cl2在反应中均从__价变为__价。
(3)Fe、Cu在化合物中常见有那些价态?
Cl2在反应中容易____电子,从而使Cl显__价,表现出较强的____性,能将变价金属氧化成__价态。
0
-1
0
-1
0
-1
得到
-1
氧化
高
三、氯气的化学性质
1.【提出问题 】
氯气与水反应
氯气能否与H2O反应?其成分是什么?
2.【猜想与假设】
假设一:氯气与水不反应,则只溶解成分是:
假设二:氯气与水会要反应,则可能成分是:
Cl2、H2O
HCl(H+ + Cl-)+???
实验
目的 探究Cl2和水是否反应
实验方案
操作
现象
实验结论
探究2:氯水中有无H+
探究1:氯水中有无Cl-
氯水中没有H+,
假设二不成立。
氯水中有 Cl-,
假设二成立。
3.【设计并进行实验】
氯水+石蕊试液
氯水+硝酸银+稀硝酸
有白色沉淀生成
溶液未变红
4.【反思并进一步探究】
方案:在石蕊试液中逐滴加入氯水
现 象:
氯水中有种成分具有漂白性
氯水中有H+存在,假设二成立。
新问题:氯水中哪一种成分具有漂白性?
盐酸、Cl2、?
结 论:
先变红后褪色
干燥红布条的接触物 现 象 结 论
盐 酸
干燥Cl2
湿润的Cl2
探究:氯水中具有漂白性的物质是什么?
红布条未褪色
红布条未褪色
红布条褪色
起漂白作用的不是盐酸
起漂白作用的不是Cl2
具有漂白性的物质是
氯气与水反应生成的
新的物质
氯气与水反应
三、氯气的化学性质
3、氯气与H2O的反应
Cl2 + H2O = HCl + HClO
2HClO 2HCl+O2↑
光照
HClO
弱酸性
强氧化性
漂白性
不稳定性:
结构
性质
知识小结
1.与金属反应(Na、Fe、Cu等)
2.与非金属反应(H2等)
3.与水反应
强氧化性
用途
+e-
学会分析:
1、下列氯化物不可以由金属和氯气直接反应制得的是( )
A.CuCl2 B.MgCl2 C.FeCl2 D.AlCl3
学会比较:
2、下列说法正确的是( )
A.Cl和Cl-的化学性质一样
B.干燥氯气不具有漂白性
C.Cl2有毒,Cl-也有毒
D.Cl2和Cl-都是黄绿色
学会应用:
3、氯气可以用来消灭田鼠,为此将Cl2通过软管灌入洞中,
这是利用了Cl2下列性质中的( )
①黄绿色 ②密度比较大 ③有毒
④较易液化 ⑤溶解于水
A.①②③ B.②③ C.③④ D.③④⑤
C
B
B
练一练
2、若你周围不幸发生氯气泄漏事故,你
怎样用已有化学知识进行恰当处理?
1、新制氯水与久置氯水各含有哪些粒子?
性质有何不同?
作 业
3、思考Cl2能否与碱发生反应?若能,生
成物是什么?
