课题1课时2 生活中常见的盐(2)-九年级化学下册同步教学精品课件(人教版)(课件23页)
文档属性
| 名称 | 课题1课时2 生活中常见的盐(2)-九年级化学下册同步教学精品课件(人教版)(课件23页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 100.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-01 00:00:00 | ||
图片预览









文档简介
(共44张PPT)
第十一单元
课题1 生活中常见的盐
课时2
1.了解碳酸钠、碳酸氢钠、碳酸钙的组成及其在生活中的主要用途;。
3.初步学会鉴定某些离子的方法。
2.能判断复分解反应的类型及发生条件。
二、碳酸钠、碳酸氢钠、碳酸钙
1、碳酸钠
化学式
俗 称
颜色状态
主要用途
Na2CO3
纯碱、苏打
用于玻璃、造纸、纺织和洗涤剂生产等。
白色固体
2、碳酸氢钠
化学式
俗 称
颜色状态
主要用途
NaHCO3
小苏打
白色固体
焙制糕点所用的 ;
医疗上治疗 。
发酵粉
胃酸过多
3、碳酸钙
化学式
俗 称
颜色状态
主要用途
CaCO3
大理石、石灰石
白色固体
是重要的 材料;
医药上作为 。
建筑
补钙剂
拓展视野
盐溶液不一定呈中性。
碳酸钠(Na2CO3)是一种盐,不属于碱,但其水溶液呈碱性,能使无色酚酞溶液变红。
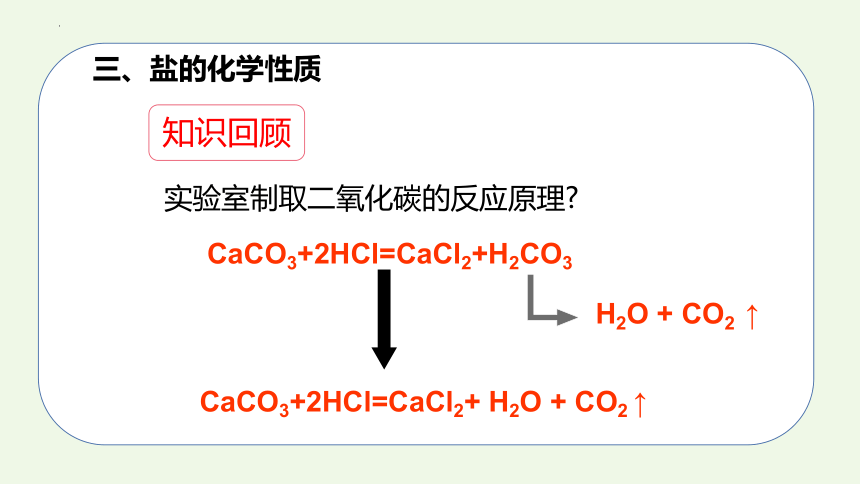
三、盐的化学性质
知识回顾
实验室制取二氧化碳的反应原理
CaCO3+2HCl=CaCl2+H2CO3
H2O + CO2 ↑
CaCO3+2HCl=CaCl2+ H2O + CO2 ↑
讨论
比较碳酸钙与碳酸钠和碳酸氢钠的组成,推断碳酸钠和碳酸氢钠是否也能发生上述类似的反应。
CaCO3+2HCl=CaCl2+ H2O + CO2 ↑
向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的橡胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中(如图)观察现象。
用碳酸氢钠代替碳酸钠进行上述实验,并分析现象。
碳酸钠+盐酸 碳酸氢钠+盐酸
现象 分析 白色固体消失,有气泡冒出,澄清石灰水变浑浊。
碳酸钠(碳酸氢钠)与盐酸反应生成了CO2气体使澄清石灰水变浑浊。
Na2CO3+2HCl = 2NaCl+H2O +CO2 ↑
NaHCO3+HCl = NaCl +H2O +CO2 ↑
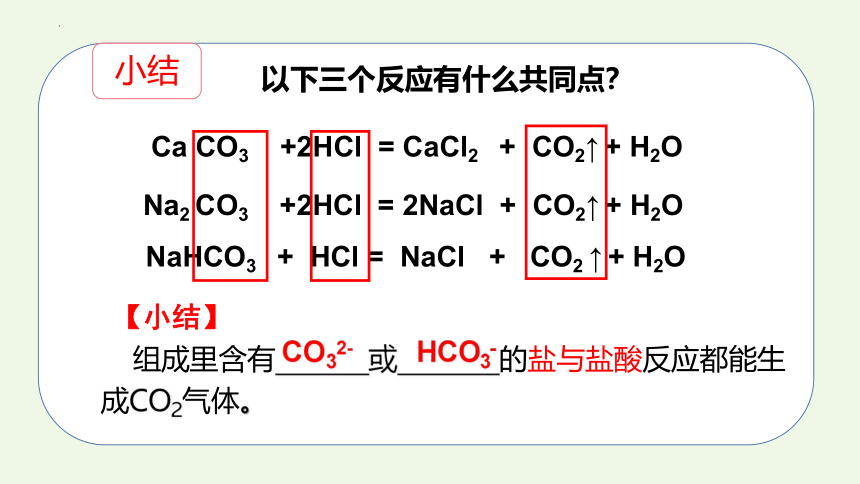
以下三个反应有什么共同点?
Ca CO3 +2HCl = CaCl2 + CO2↑ + H2O
Na2 CO3 +2HCl = 2NaCl + CO2↑ + H2O
NaHCO3 + HCl = NaCl + CO2 ↑ + H2O
【小结】
组成里含有 或 的盐与盐酸反应都能生成CO2气体。
CO32-
HCO3-
小结
1、已知珍珠(或贝壳)的主要成分为CaCO3,请设计实验验证珍珠(或鸡蛋壳)中含有CaCO3。
想一想
取样于试管,加入适量稀盐酸,若有气泡产生,将气体通入澄清石灰水水,若澄清的石灰水变浑浊,则好有碳酸钙。
向盛有少量碳酸钠溶液的试管里滴入澄清石灰水,观察并分析现象。
现象
分析
溶液变浑浊
碳酸钠与澄清石灰水反应生成了不溶于水的物质
Na2CO3+Ca(OH)2 = CaCO3↓+2NaOH
复分解反应
分析上述反应,它们都发生在溶液中,都是由两种化合物互相交换成分,生成另外两种化合物的反应,这样的反应叫做复分解反应。
CaCO3 + 2HCl = CaCl2 + H2O + CO2 ↑
Na2CO3 + 2HCl = 2NaCl+H2O +CO2 ↑
NaHCO3 + HCl = NaCl +H2O +CO2 ↑
Na2CO3 +Ca(OH)2 = CaCO3↓+2NaOH
四、复分解反应发生的条件
向两支分别盛有少量氢氧化钠溶液和氯化钡溶液的试管中滴加硫酸铜溶液,观察现象并填写下表。
CuSO4溶液+NaOH溶液 CuSO4溶液+BaCl2溶液
现象
化学方程式
讨论
生成蓝色沉淀
生成白色沉淀
CuSO4+2NaOH=
Cu(OH)2↓+Na2SO4
CuSO4+BaCl2=
BaSO4↓+CuCl2
1.上述两个反应是否属于复分解反应 观察到的现象有什么共同之处
属于,都有沉淀产生
2.前面学过的酸碱中和反应是否也属于复分解反应 中和反应的生成物中,相同的生成物是什么
3.碳酸钠、碳酸钙等含碳酸根的盐与盐酸发生复分解反应时,可观察到的共同现象是什么
讨论
属于,都生成水
有气泡产生。
酸、碱、盐之间并不是都能发生复分解反应。只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
探究
NaOH溶液 NaCl 溶液 K2CO3溶液 Ba(NO3)2溶液
稀硫酸
判断依据 (生成物)
水
反应
水、气体
沉淀
不反应
反应
反应
设计实验证明你的判断。
根据复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液之间是否能发生反应。
2、如何证明稀硫酸和氯化钠没有发生反应?
想一想
Cl-
Na+
H+
H+
SO42-
Cl-
Na+
若发生反应,溶液中某些离子会消失,可通过检验溶液中的离子的有无来证明。
1.检验H+
2.检验SO42-
3.检验Cl-
石蕊、活泼金属、金属氧化物,碳酸盐、碳酸氢盐
①滴加稀盐酸,无明显现象;
②滴加氯化钡溶液,产生白色沉淀。
①滴加稀硝酸,无明显现象;
②滴加硝酸银溶液,产生白色沉淀。
拓展视野
侯德榜(1890-1974)
我国著名的制纯碱(碳酸钠)专家。
他的“侯氏联合制碱法”为我国民族化学工业赢得了声誉。
总结
盐与碱的反应
盐与金属的反应
盐的化学性质
盐与盐的反应
盐与酸的反应
复分解反应发生的条件:生成物中有气体、沉淀或水
1. 下列物质的化学名称与俗名,对应错误的是 ( )
A.汞——水银
B.氧化钙——熟石灰、消石灰
C.碳酸氢钠——小苏打
D.氢氧化钠——烧碱、火碱、苛性钠
B
2. 下列物质的名称(或俗名)、化学式和类别,三者不完全相符的是( )
A.硫酸、H2SO4、酸 B. 纯碱、NaOH、碱
C.生石灰、CaO、氧化物 D. 硫酸铜、CuSO4、盐
B
3、下列物质名称、俗名、化学式完全对应的是( )
A.碳酸氢钠、小苏打、Na2CO3
B.碳酸钠、纯碱、NaHCO3
C.氢氧化钙、生石灰、Ca(OH)2
D.氢氧化钠、苛性钠、NaOH
D
4.下列有关盐的用途中,叙述错误的是( )
A.碳酸氢钠用于焙制糕点
B.亚硝酸钠可用于烹调食物
C.碳酸钙可以作补钙剂
D.碳酸钠可用于玻璃的生产
B
5.下列关于碳酸钠与碳酸氢钠的说法错误的是( )
A.Na2CO3溶液呈碱性
B.NaHCO3固体难溶于水
C.“苏打”是碳酸钠的俗名
D. NaHCO3可用于烘焙糕点
B
6.在下列物质中:
A.食盐; B.碳酸氢钠; C.纯碱; D.碳酸钙;
(1)可用作调味剂的 ;
(2)可用作发酵粉和治疗胃酸过多症的是 。
(3)可用作补钙剂和牙膏填充剂的是 ;
(4)可用于生产玻璃的是 ;
A
B
D
C
通入澄清
石灰水
7.某同学在自己家厨房中找到一种白色粉末,将其带到学校实验室进行实验,实验过程与现象如图所示:
对此粉末的成分判断正确的是( )
A.该粉末一定是碳酸钠
B.该粉末一定是碳酸氢钠
C.该粉末一定是氯化钠
D.该粉末可能是碳酸钠或碳酸氢钠
D
白色粉末
加入水
无色溶液
加入盐酸
产生无色无味气体
白色沉淀
8.下列反应中不属于复分解反应的是( )
A. H2SO4+Ca(OH)2 = CaSO4 + 2H2O
B. H2SO4+BaCl2 = BaSO4↓+ 2HCl
C.2HCl+Fe = FeCl2+H2↑
D. 2HCl+CaCO3 = CaCl2+H2O+CO2↑
C
9.下列化学反应属于复分解反应的是( )
A. Zn+H2SO4 = ZnSO4+H2↑
B. 2KMnO4 = K2MnO4+MnO2+O2↑
C. CaO+H2O = Ca(OH)2
D. CuSO4+2NaOH = Cu(OH)2↓+Na2SO4
D
10.下列反应属于复分解反应的是( )
A.2NaOH+CO2 = Na2CO3+H2O
B.2CuO+C = 2Cu+CO2↑
C.CuO+H2SO4 = CuSO4+H2O
D.CH4+2O2 = CO2+2H2O
高温
点燃
C
11.下列各组物质的溶液混合后,不能发生反应的是( )
A. NaCl和H2SO4 B. NaOH和HCl
C. Na2CO3和H2SO4 D. AgNO3和NaCl
A
12.下列各组物质的溶液,不能发生复分解反应的是( )
A.HCl和Ca(OH)2 B.Na2CO3和H2SO4
C.AgNO3和BaCl2 D.KCl和CuSO4
D
13.下列各组物质的溶液之间能发生复分解反应,且有沉淀生成的是( )
A.H2SO4、Na2CO3 B.NaCl、KNO3
C.NaOH、HCl D.FeCl3、NaOH
D
14.下列各组物质中,能发生复分解反应且反应后溶液总质量变小的是( )
A.铁和硫酸铜溶液
B.氢氧化钠溶液和盐酸
C.稀硫酸和氯化钡溶
D.碳酸钠溶液和氯化钾溶液
C
15.向盛有少量碳酸钠溶液的试管中滴入澄清石灰水,对其中发生的反应的说法错误的是( )
A.反应会产生白色沉淀
B.化学方程式为Ca(OH)2+Na2CO3=CaCO3+2NaOH
C.两种化合物互相交换成分生成另两种化合物
D.属于复分解反应
B
16.在氯化钡溶液中滴入某种溶液,生成白色沉淀。有关说法错误的是( )
A.滴入的可能是硝酸银溶液
B.反应后溶液可能呈酸性
C.白色沉淀可能溶于盐酸
D.该反应不是复分解反应
D
17.在“P+Q→盐+水”的反应中,物质P和Q不可能是( )
A.HCl和Ca(OH)2 B. SO2和NaOH
C.Fe2O3和H2SO4 D. H2SO4和ZnCl2
D
19.除去下列各物质中混有的少量杂质(括号内为杂质),下列方法中不正确的是( )
A.铜粉(CuO)——加入过量的稀硫酸,过滤
B.H2(HCl)——通过足量的氢氧化钠溶液,干燥
C.NaCl溶液(Na2SO4)——加入适量的Ba(NO3)2溶液,
过滤
D.CaCl2溶液(HCl)——加入过量的碳酸钙粉末,过滤
C
20.下列各组物质的鉴别方法不能够达到预期目的是( )
编号 被鉴别物质 鉴别方法
A O2与CO2 分别通入澄清石灰水中
B HCl与H2SO4 分别滴加BaCl2溶液
C Ca(OH)2溶液与Na2CO3溶液 分别滴加酚酞溶液
D CuCl2溶液与Cu(NO3)2溶液 分别滴加AgNO3溶液
C
21.化学小组同学用图所示装置做了两个兴趣实验。
(1)若观察到a中固体减少,有大量的气泡产生,b中溶液无明显变化。推测固体可能是下列物质中的 _____(填字母)。
A.银 B.锌
C.氢氧化钙 D.碳酸钙
(2)若固体为碳酸氢钠粉末,
则整个装置中可观察到的现象有
。
a中固体减少,产生大量气泡,b中澄清石灰水变浑浊
B
22.小波用实验方法区别稀盐酸和硫酸钠溶液(记作A、B)
(1)他向A、B两溶液中分别加入Na2CO3溶液,观察到
A溶液中产生无色气体。则A是 ,发生反应的化学
方程式为 。
(2)他向A、B两溶液中分别加入BaCl2溶液,B溶液中
的现象是 。
(3)他还用了下列试剂中的一种区别A、B两溶液,这种
试剂是 (填序号)。
①石蕊试液 ②CuSO4溶液
③醋酸溶液 ④KCl溶液
稀盐酸
Na2CO3+2HCl=2NaCl+H2O+CO2↑
有白色沉淀生成
①
24.向稀硫酸中滴加Na2CO3溶液,该反应的微观本质可用下图表示,
请填上相关粒子的符号:A ;B ;C ;D E ;写出该反应的本质__________________________
SO42-
H2O
CO2
Na+
Na+
2H++CO32-=H2O+CO2
第十一单元
课题1 生活中常见的盐
课时2
1.了解碳酸钠、碳酸氢钠、碳酸钙的组成及其在生活中的主要用途;。
3.初步学会鉴定某些离子的方法。
2.能判断复分解反应的类型及发生条件。
二、碳酸钠、碳酸氢钠、碳酸钙
1、碳酸钠
化学式
俗 称
颜色状态
主要用途
Na2CO3
纯碱、苏打
用于玻璃、造纸、纺织和洗涤剂生产等。
白色固体
2、碳酸氢钠
化学式
俗 称
颜色状态
主要用途
NaHCO3
小苏打
白色固体
焙制糕点所用的 ;
医疗上治疗 。
发酵粉
胃酸过多
3、碳酸钙
化学式
俗 称
颜色状态
主要用途
CaCO3
大理石、石灰石
白色固体
是重要的 材料;
医药上作为 。
建筑
补钙剂
拓展视野
盐溶液不一定呈中性。
碳酸钠(Na2CO3)是一种盐,不属于碱,但其水溶液呈碱性,能使无色酚酞溶液变红。
三、盐的化学性质
知识回顾
实验室制取二氧化碳的反应原理
CaCO3+2HCl=CaCl2+H2CO3
H2O + CO2 ↑
CaCO3+2HCl=CaCl2+ H2O + CO2 ↑
讨论
比较碳酸钙与碳酸钠和碳酸氢钠的组成,推断碳酸钠和碳酸氢钠是否也能发生上述类似的反应。
CaCO3+2HCl=CaCl2+ H2O + CO2 ↑
向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的橡胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中(如图)观察现象。
用碳酸氢钠代替碳酸钠进行上述实验,并分析现象。
碳酸钠+盐酸 碳酸氢钠+盐酸
现象 分析 白色固体消失,有气泡冒出,澄清石灰水变浑浊。
碳酸钠(碳酸氢钠)与盐酸反应生成了CO2气体使澄清石灰水变浑浊。
Na2CO3+2HCl = 2NaCl+H2O +CO2 ↑
NaHCO3+HCl = NaCl +H2O +CO2 ↑
以下三个反应有什么共同点?
Ca CO3 +2HCl = CaCl2 + CO2↑ + H2O
Na2 CO3 +2HCl = 2NaCl + CO2↑ + H2O
NaHCO3 + HCl = NaCl + CO2 ↑ + H2O
【小结】
组成里含有 或 的盐与盐酸反应都能生成CO2气体。
CO32-
HCO3-
小结
1、已知珍珠(或贝壳)的主要成分为CaCO3,请设计实验验证珍珠(或鸡蛋壳)中含有CaCO3。
想一想
取样于试管,加入适量稀盐酸,若有气泡产生,将气体通入澄清石灰水水,若澄清的石灰水变浑浊,则好有碳酸钙。
向盛有少量碳酸钠溶液的试管里滴入澄清石灰水,观察并分析现象。
现象
分析
溶液变浑浊
碳酸钠与澄清石灰水反应生成了不溶于水的物质
Na2CO3+Ca(OH)2 = CaCO3↓+2NaOH
复分解反应
分析上述反应,它们都发生在溶液中,都是由两种化合物互相交换成分,生成另外两种化合物的反应,这样的反应叫做复分解反应。
CaCO3 + 2HCl = CaCl2 + H2O + CO2 ↑
Na2CO3 + 2HCl = 2NaCl+H2O +CO2 ↑
NaHCO3 + HCl = NaCl +H2O +CO2 ↑
Na2CO3 +Ca(OH)2 = CaCO3↓+2NaOH
四、复分解反应发生的条件
向两支分别盛有少量氢氧化钠溶液和氯化钡溶液的试管中滴加硫酸铜溶液,观察现象并填写下表。
CuSO4溶液+NaOH溶液 CuSO4溶液+BaCl2溶液
现象
化学方程式
讨论
生成蓝色沉淀
生成白色沉淀
CuSO4+2NaOH=
Cu(OH)2↓+Na2SO4
CuSO4+BaCl2=
BaSO4↓+CuCl2
1.上述两个反应是否属于复分解反应 观察到的现象有什么共同之处
属于,都有沉淀产生
2.前面学过的酸碱中和反应是否也属于复分解反应 中和反应的生成物中,相同的生成物是什么
3.碳酸钠、碳酸钙等含碳酸根的盐与盐酸发生复分解反应时,可观察到的共同现象是什么
讨论
属于,都生成水
有气泡产生。
酸、碱、盐之间并不是都能发生复分解反应。只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
探究
NaOH溶液 NaCl 溶液 K2CO3溶液 Ba(NO3)2溶液
稀硫酸
判断依据 (生成物)
水
反应
水、气体
沉淀
不反应
反应
反应
设计实验证明你的判断。
根据复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液之间是否能发生反应。
2、如何证明稀硫酸和氯化钠没有发生反应?
想一想
Cl-
Na+
H+
H+
SO42-
Cl-
Na+
若发生反应,溶液中某些离子会消失,可通过检验溶液中的离子的有无来证明。
1.检验H+
2.检验SO42-
3.检验Cl-
石蕊、活泼金属、金属氧化物,碳酸盐、碳酸氢盐
①滴加稀盐酸,无明显现象;
②滴加氯化钡溶液,产生白色沉淀。
①滴加稀硝酸,无明显现象;
②滴加硝酸银溶液,产生白色沉淀。
拓展视野
侯德榜(1890-1974)
我国著名的制纯碱(碳酸钠)专家。
他的“侯氏联合制碱法”为我国民族化学工业赢得了声誉。
总结
盐与碱的反应
盐与金属的反应
盐的化学性质
盐与盐的反应
盐与酸的反应
复分解反应发生的条件:生成物中有气体、沉淀或水
1. 下列物质的化学名称与俗名,对应错误的是 ( )
A.汞——水银
B.氧化钙——熟石灰、消石灰
C.碳酸氢钠——小苏打
D.氢氧化钠——烧碱、火碱、苛性钠
B
2. 下列物质的名称(或俗名)、化学式和类别,三者不完全相符的是( )
A.硫酸、H2SO4、酸 B. 纯碱、NaOH、碱
C.生石灰、CaO、氧化物 D. 硫酸铜、CuSO4、盐
B
3、下列物质名称、俗名、化学式完全对应的是( )
A.碳酸氢钠、小苏打、Na2CO3
B.碳酸钠、纯碱、NaHCO3
C.氢氧化钙、生石灰、Ca(OH)2
D.氢氧化钠、苛性钠、NaOH
D
4.下列有关盐的用途中,叙述错误的是( )
A.碳酸氢钠用于焙制糕点
B.亚硝酸钠可用于烹调食物
C.碳酸钙可以作补钙剂
D.碳酸钠可用于玻璃的生产
B
5.下列关于碳酸钠与碳酸氢钠的说法错误的是( )
A.Na2CO3溶液呈碱性
B.NaHCO3固体难溶于水
C.“苏打”是碳酸钠的俗名
D. NaHCO3可用于烘焙糕点
B
6.在下列物质中:
A.食盐; B.碳酸氢钠; C.纯碱; D.碳酸钙;
(1)可用作调味剂的 ;
(2)可用作发酵粉和治疗胃酸过多症的是 。
(3)可用作补钙剂和牙膏填充剂的是 ;
(4)可用于生产玻璃的是 ;
A
B
D
C
通入澄清
石灰水
7.某同学在自己家厨房中找到一种白色粉末,将其带到学校实验室进行实验,实验过程与现象如图所示:
对此粉末的成分判断正确的是( )
A.该粉末一定是碳酸钠
B.该粉末一定是碳酸氢钠
C.该粉末一定是氯化钠
D.该粉末可能是碳酸钠或碳酸氢钠
D
白色粉末
加入水
无色溶液
加入盐酸
产生无色无味气体
白色沉淀
8.下列反应中不属于复分解反应的是( )
A. H2SO4+Ca(OH)2 = CaSO4 + 2H2O
B. H2SO4+BaCl2 = BaSO4↓+ 2HCl
C.2HCl+Fe = FeCl2+H2↑
D. 2HCl+CaCO3 = CaCl2+H2O+CO2↑
C
9.下列化学反应属于复分解反应的是( )
A. Zn+H2SO4 = ZnSO4+H2↑
B. 2KMnO4 = K2MnO4+MnO2+O2↑
C. CaO+H2O = Ca(OH)2
D. CuSO4+2NaOH = Cu(OH)2↓+Na2SO4
D
10.下列反应属于复分解反应的是( )
A.2NaOH+CO2 = Na2CO3+H2O
B.2CuO+C = 2Cu+CO2↑
C.CuO+H2SO4 = CuSO4+H2O
D.CH4+2O2 = CO2+2H2O
高温
点燃
C
11.下列各组物质的溶液混合后,不能发生反应的是( )
A. NaCl和H2SO4 B. NaOH和HCl
C. Na2CO3和H2SO4 D. AgNO3和NaCl
A
12.下列各组物质的溶液,不能发生复分解反应的是( )
A.HCl和Ca(OH)2 B.Na2CO3和H2SO4
C.AgNO3和BaCl2 D.KCl和CuSO4
D
13.下列各组物质的溶液之间能发生复分解反应,且有沉淀生成的是( )
A.H2SO4、Na2CO3 B.NaCl、KNO3
C.NaOH、HCl D.FeCl3、NaOH
D
14.下列各组物质中,能发生复分解反应且反应后溶液总质量变小的是( )
A.铁和硫酸铜溶液
B.氢氧化钠溶液和盐酸
C.稀硫酸和氯化钡溶
D.碳酸钠溶液和氯化钾溶液
C
15.向盛有少量碳酸钠溶液的试管中滴入澄清石灰水,对其中发生的反应的说法错误的是( )
A.反应会产生白色沉淀
B.化学方程式为Ca(OH)2+Na2CO3=CaCO3+2NaOH
C.两种化合物互相交换成分生成另两种化合物
D.属于复分解反应
B
16.在氯化钡溶液中滴入某种溶液,生成白色沉淀。有关说法错误的是( )
A.滴入的可能是硝酸银溶液
B.反应后溶液可能呈酸性
C.白色沉淀可能溶于盐酸
D.该反应不是复分解反应
D
17.在“P+Q→盐+水”的反应中,物质P和Q不可能是( )
A.HCl和Ca(OH)2 B. SO2和NaOH
C.Fe2O3和H2SO4 D. H2SO4和ZnCl2
D
19.除去下列各物质中混有的少量杂质(括号内为杂质),下列方法中不正确的是( )
A.铜粉(CuO)——加入过量的稀硫酸,过滤
B.H2(HCl)——通过足量的氢氧化钠溶液,干燥
C.NaCl溶液(Na2SO4)——加入适量的Ba(NO3)2溶液,
过滤
D.CaCl2溶液(HCl)——加入过量的碳酸钙粉末,过滤
C
20.下列各组物质的鉴别方法不能够达到预期目的是( )
编号 被鉴别物质 鉴别方法
A O2与CO2 分别通入澄清石灰水中
B HCl与H2SO4 分别滴加BaCl2溶液
C Ca(OH)2溶液与Na2CO3溶液 分别滴加酚酞溶液
D CuCl2溶液与Cu(NO3)2溶液 分别滴加AgNO3溶液
C
21.化学小组同学用图所示装置做了两个兴趣实验。
(1)若观察到a中固体减少,有大量的气泡产生,b中溶液无明显变化。推测固体可能是下列物质中的 _____(填字母)。
A.银 B.锌
C.氢氧化钙 D.碳酸钙
(2)若固体为碳酸氢钠粉末,
则整个装置中可观察到的现象有
。
a中固体减少,产生大量气泡,b中澄清石灰水变浑浊
B
22.小波用实验方法区别稀盐酸和硫酸钠溶液(记作A、B)
(1)他向A、B两溶液中分别加入Na2CO3溶液,观察到
A溶液中产生无色气体。则A是 ,发生反应的化学
方程式为 。
(2)他向A、B两溶液中分别加入BaCl2溶液,B溶液中
的现象是 。
(3)他还用了下列试剂中的一种区别A、B两溶液,这种
试剂是 (填序号)。
①石蕊试液 ②CuSO4溶液
③醋酸溶液 ④KCl溶液
稀盐酸
Na2CO3+2HCl=2NaCl+H2O+CO2↑
有白色沉淀生成
①
24.向稀硫酸中滴加Na2CO3溶液,该反应的微观本质可用下图表示,
请填上相关粒子的符号:A ;B ;C ;D E ;写出该反应的本质__________________________
SO42-
H2O
CO2
Na+
Na+
2H++CO32-=H2O+CO2
同课章节目录
