2022-2023学年高二下学期化学人教版(2019)选择性必修33.1卤代烃(17张PPT)
文档属性
| 名称 | 2022-2023学年高二下学期化学人教版(2019)选择性必修33.1卤代烃(17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-01 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
第三章 卤代烃
一、卤代烃
1、定义:烃分子中的氢原子被卤素原子取代后生成的化合物
称为卤代烃
(1)官能团:碳卤键
(2)卤代烃的表示方法:R—X (X=F、Cl、Br、I),
饱和一卤代烃的通式为CnH2n+1X
一、卤代烃
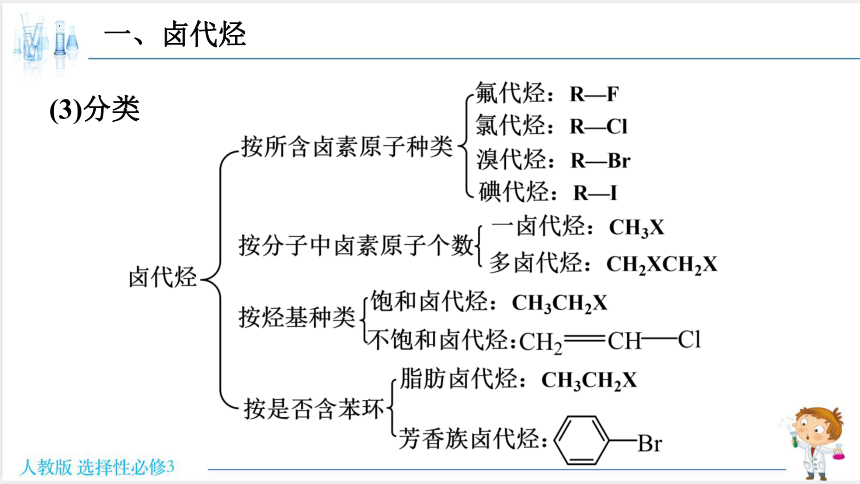
(3)分类
一、卤代烃
2、卤代烃的命名——类似于烃的命名方法:将卤素原子作为取代基
2、编号
1、选主链
选择含官能团的最长碳链作为主链
将卤素原子看做取代基,编号时从距简单取代基近的一端编号,有碳碳双键时从距离碳碳双键近的一端开始编号
3、命名
以相应的烃作母体,卤原子作取代基
一、卤代烃
2、卤代烃的命名——类似于烃的命名方法:将卤素原子作为取代基
2—氯丁烷
CH2—C—CH2—CH3
Cl
CH3
Cl
1,2—二溴乙烷
2-甲基- 1,2-二氯丁烷
3—甲基—3—溴—1—丁烯
一、卤代烃
2、卤代烃的获取
想一想,制取卤代烃的方法有哪些?
烷烃和芳香烃的卤代反应
不饱和烃与卤素单质
卤化氢的加成反应
一、卤代烃
3、物理性质
1、状态: 常温下,除个别为气体外,大多为液体或固体.
(除一氯甲烷、氯乙烷、氯乙烯等少数为气体外)
2、溶解性:难溶于水,可溶于有机溶剂,本身就是良好的溶剂
一、卤代烃
3、物理性质
3、沸点: 卤代烃属于分子晶体,其沸点取决于范德华力。
Ⅰ.随着碳原子数的增加,熔沸点增大
Ⅱ.卤代烃的沸点高于相应的烃 CH3CH3<CH3CH2Br
一、卤代烃
3、物理性质
4、密度: 卤代烃的密度高于相应的烃 CH3CH3<CH3CH2Br
密度随着碳原子数的增加而减小
二、溴乙烷----- CH3CH2Br
1、组成与结构
分子式
C2H5Br
电子式
结构式
结构简式
CH3CH2Br
C2H5Br
2、物理性质
纯净的溴乙烷是无色液体,沸点是38.4 ℃,密度比水的大,难溶于水,可溶于多种有机溶剂(如:乙醇、苯、汽油等)
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)取代反应(水解反应)
取一支试管,滴入10~15滴溴乙烷,再加入1 mL 5% NaOH溶液,振荡后加热,静置。待溶液分层后,用胶头滴管小心吸取少量上层水溶液,移入另一支盛有1 mL稀硝酸的试管中,然后加入2滴AgNO3溶液,观察现象。
反应方程式:
R—OH+NaX
R—X+NaOH
有淡黄色沉淀生成
如何检验卤代烃中卤素原子?
取少量卤代烃于试管中,加入NaOH水溶液,加热,冷却后,加入稀硝酸中和溶液至酸性,再加入AgNO3溶液。
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)取代反应(水解反应)
R—OH+NaX
R—X+NaOH
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)消去反应
向试管中加入5mL溴乙烷和15mL饱和NaOH乙醇溶液,振荡后加热。将产生的气体先通入盛水的试管,再通入盛有酸性高锰酸钾的试管中,观察现象。
反应方程式:
除去挥发出来的乙醇
实验现象:
酸性KMnO4溶液褪色
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)消去反应
向试管中加入5mL溴乙烷和15mL饱和NaOH乙醇溶液,振荡后加热。将产生的气体先通入盛水的试管,再通入盛有酸性高锰酸钾的试管中,观察现象。
反应方程式:
除去挥发出来的乙醇
实验现象:
酸性KMnO4溶液褪色
除酸性高锰酸钾溶液外还可以用溴的四氯化碳溶液来检验丁烯,此时气体还用先通入水中吗?
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)消去反应
条件:与卤素原子直接相连的碳原子的邻位碳
原子上有H原子
三、卤代烃的运用与危害
1、用途
常用作制冷剂(氟利昂)、灭火剂(CCl4)、溶剂(CCl4、氯仿)、麻醉剂、合成有机物等
含氯、溴的氟代烷可对臭氧层产生破坏作用,形成臭氧空洞,危及地球上的生物。氟利昂(以CCl3F为例)破坏臭氧层的反应过程可表示为
2、危害
第三章 卤代烃
一、卤代烃
1、定义:烃分子中的氢原子被卤素原子取代后生成的化合物
称为卤代烃
(1)官能团:碳卤键
(2)卤代烃的表示方法:R—X (X=F、Cl、Br、I),
饱和一卤代烃的通式为CnH2n+1X
一、卤代烃
(3)分类
一、卤代烃
2、卤代烃的命名——类似于烃的命名方法:将卤素原子作为取代基
2、编号
1、选主链
选择含官能团的最长碳链作为主链
将卤素原子看做取代基,编号时从距简单取代基近的一端编号,有碳碳双键时从距离碳碳双键近的一端开始编号
3、命名
以相应的烃作母体,卤原子作取代基
一、卤代烃
2、卤代烃的命名——类似于烃的命名方法:将卤素原子作为取代基
2—氯丁烷
CH2—C—CH2—CH3
Cl
CH3
Cl
1,2—二溴乙烷
2-甲基- 1,2-二氯丁烷
3—甲基—3—溴—1—丁烯
一、卤代烃
2、卤代烃的获取
想一想,制取卤代烃的方法有哪些?
烷烃和芳香烃的卤代反应
不饱和烃与卤素单质
卤化氢的加成反应
一、卤代烃
3、物理性质
1、状态: 常温下,除个别为气体外,大多为液体或固体.
(除一氯甲烷、氯乙烷、氯乙烯等少数为气体外)
2、溶解性:难溶于水,可溶于有机溶剂,本身就是良好的溶剂
一、卤代烃
3、物理性质
3、沸点: 卤代烃属于分子晶体,其沸点取决于范德华力。
Ⅰ.随着碳原子数的增加,熔沸点增大
Ⅱ.卤代烃的沸点高于相应的烃 CH3CH3<CH3CH2Br
一、卤代烃
3、物理性质
4、密度: 卤代烃的密度高于相应的烃 CH3CH3<CH3CH2Br
密度随着碳原子数的增加而减小
二、溴乙烷----- CH3CH2Br
1、组成与结构
分子式
C2H5Br
电子式
结构式
结构简式
CH3CH2Br
C2H5Br
2、物理性质
纯净的溴乙烷是无色液体,沸点是38.4 ℃,密度比水的大,难溶于水,可溶于多种有机溶剂(如:乙醇、苯、汽油等)
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)取代反应(水解反应)
取一支试管,滴入10~15滴溴乙烷,再加入1 mL 5% NaOH溶液,振荡后加热,静置。待溶液分层后,用胶头滴管小心吸取少量上层水溶液,移入另一支盛有1 mL稀硝酸的试管中,然后加入2滴AgNO3溶液,观察现象。
反应方程式:
R—OH+NaX
R—X+NaOH
有淡黄色沉淀生成
如何检验卤代烃中卤素原子?
取少量卤代烃于试管中,加入NaOH水溶液,加热,冷却后,加入稀硝酸中和溶液至酸性,再加入AgNO3溶液。
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)取代反应(水解反应)
R—OH+NaX
R—X+NaOH
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)消去反应
向试管中加入5mL溴乙烷和15mL饱和NaOH乙醇溶液,振荡后加热。将产生的气体先通入盛水的试管,再通入盛有酸性高锰酸钾的试管中,观察现象。
反应方程式:
除去挥发出来的乙醇
实验现象:
酸性KMnO4溶液褪色
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)消去反应
向试管中加入5mL溴乙烷和15mL饱和NaOH乙醇溶液,振荡后加热。将产生的气体先通入盛水的试管,再通入盛有酸性高锰酸钾的试管中,观察现象。
反应方程式:
除去挥发出来的乙醇
实验现象:
酸性KMnO4溶液褪色
除酸性高锰酸钾溶液外还可以用溴的四氯化碳溶液来检验丁烯,此时气体还用先通入水中吗?
二、溴乙烷----- CH3CH2Br
3、化学性质
(1)消去反应
条件:与卤素原子直接相连的碳原子的邻位碳
原子上有H原子
三、卤代烃的运用与危害
1、用途
常用作制冷剂(氟利昂)、灭火剂(CCl4)、溶剂(CCl4、氯仿)、麻醉剂、合成有机物等
含氯、溴的氟代烷可对臭氧层产生破坏作用,形成臭氧空洞,危及地球上的生物。氟利昂(以CCl3F为例)破坏臭氧层的反应过程可表示为
2、危害
