第十一单元 盐 化肥 单元测试卷 (含答案) 2022-2023学年 九年级下册化学人教版
文档属性
| 名称 | 第十一单元 盐 化肥 单元测试卷 (含答案) 2022-2023学年 九年级下册化学人教版 |

|
|
| 格式 | zip | ||
| 文件大小 | 148.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-01 00:00:00 | ||
图片预览


文档简介
第十一单元 盐 化肥 单元测试卷
一、单选题
1.下列各组实验方案中,不能达到实验目的的是( )
选项 实验目的 实验方案
A 区分棉和羊毛 灼烧,闻气味
B 除去CO2气体中的HCl 将气体通过盛有足量NaOH溶液的洗气瓶
C 鉴别Ca(OH)2和NaOH 取样,分别滴加碳酸钠溶液
D 除去N2中的O2 通过灼热的铜网
A.A B.B C.C D.D
2.下列关于化肥的说法正确的是( )
A.过磷酸钙[Ca(H2PO4)2和CaSO4的混合物]属于氮肥
B.凡施用过化肥的蔬菜都会危害健康
C.硫酸钾与熟石灰混合、研磨,能闻到刺激性的气味
D.合理施用化肥能提高农作物的产量
3.下图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合。下列说法中错误的是( )
A.图示有4种分子 B.图示反应前后原子个数不变
C.图示发生了复分解反应 D.图示产物为混合物
4.下列哪种方式不可能用于分离饱和溶液中的溶质和溶剂( )
A.过滤 B.蒸发 C.蒸馏 D.结晶
5.化学与生活息息相关.下列说法中,不合理的是( )
A.干冰可用作环保制冷剂 B.医用酒精可用于杀菌消毒
C.小苏打可用于治疗胃酸过多 D.苛性钠可用作食品的干燥剂
6.用括号内试剂不能一次性将组内物质鉴别出来的是( )
A.NaOH固体、NH4NO3固体、NaCl固体(水)
B.稀盐酸、H2O、Ca(OH)2溶液(紫色石蕊溶液)
C.NaCl溶液、Na2CO3溶液、NaNO3溶液(AgNO3溶液)
D.Ba(NO3)2溶液、MgCl2溶液、K2CO3溶液(稀硫酸)
7.物质的鉴别、分离与除杂是化学研究常用方法,下列实验方法正确的是( )
选项 实验目的 实验方法
A 分离 K2SO4 溶液与 BaSO4 过滤
B 鉴别天然蚕丝与人造丝 取样,分别闻气味
C 区分硝酸铵与氯化钾 加足量水,观察是否溶解
D 除去稀硝酸中的少量AgNO3 加过量稀盐酸,过滤
A.A B.B C.C D.D
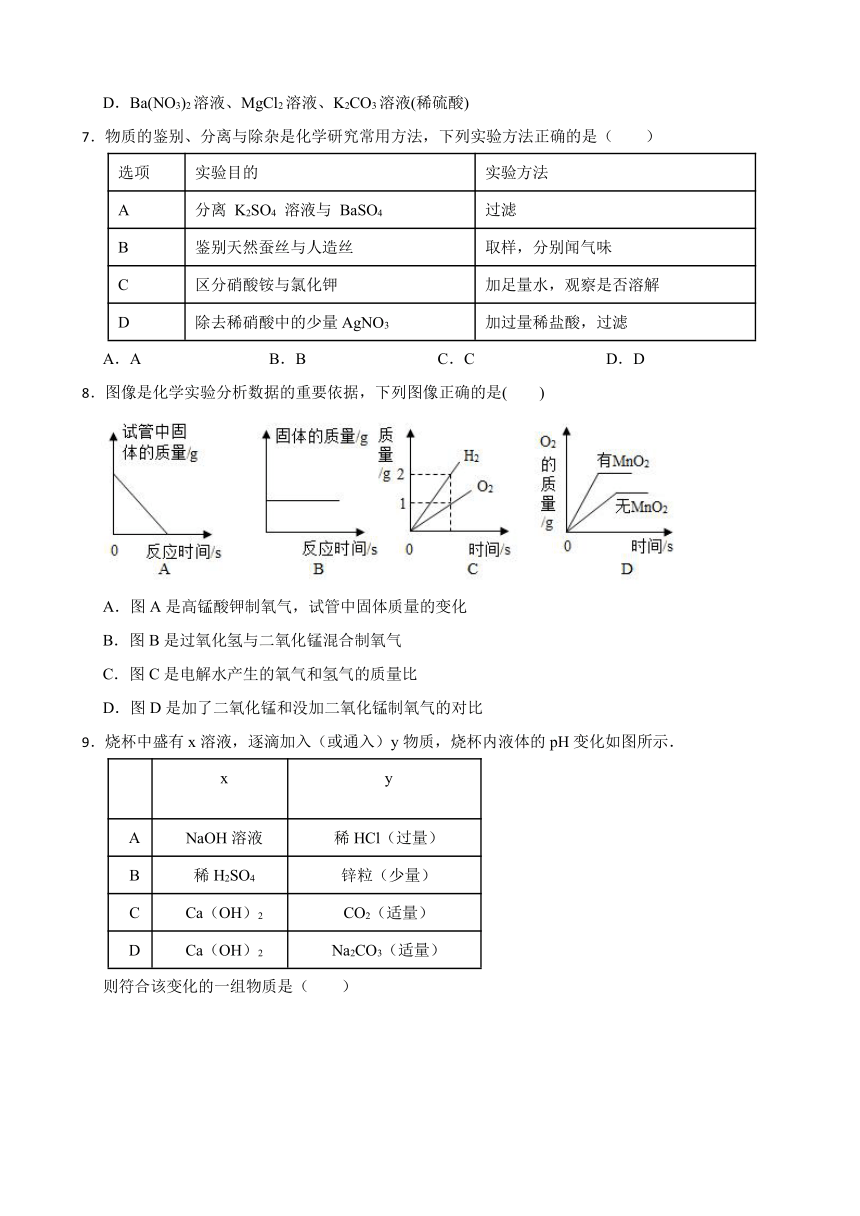
8.图像是化学实验分析数据的重要依据,下列图像正确的是( )
A.图A是高锰酸钾制氧气,试管中固体质量的变化
B.图B是过氧化氢与二氧化锰混合制氧气
C.图C是电解水产生的氧气和氢气的质量比
D.图D是加了二氧化锰和没加二氧化锰制氧气的对比
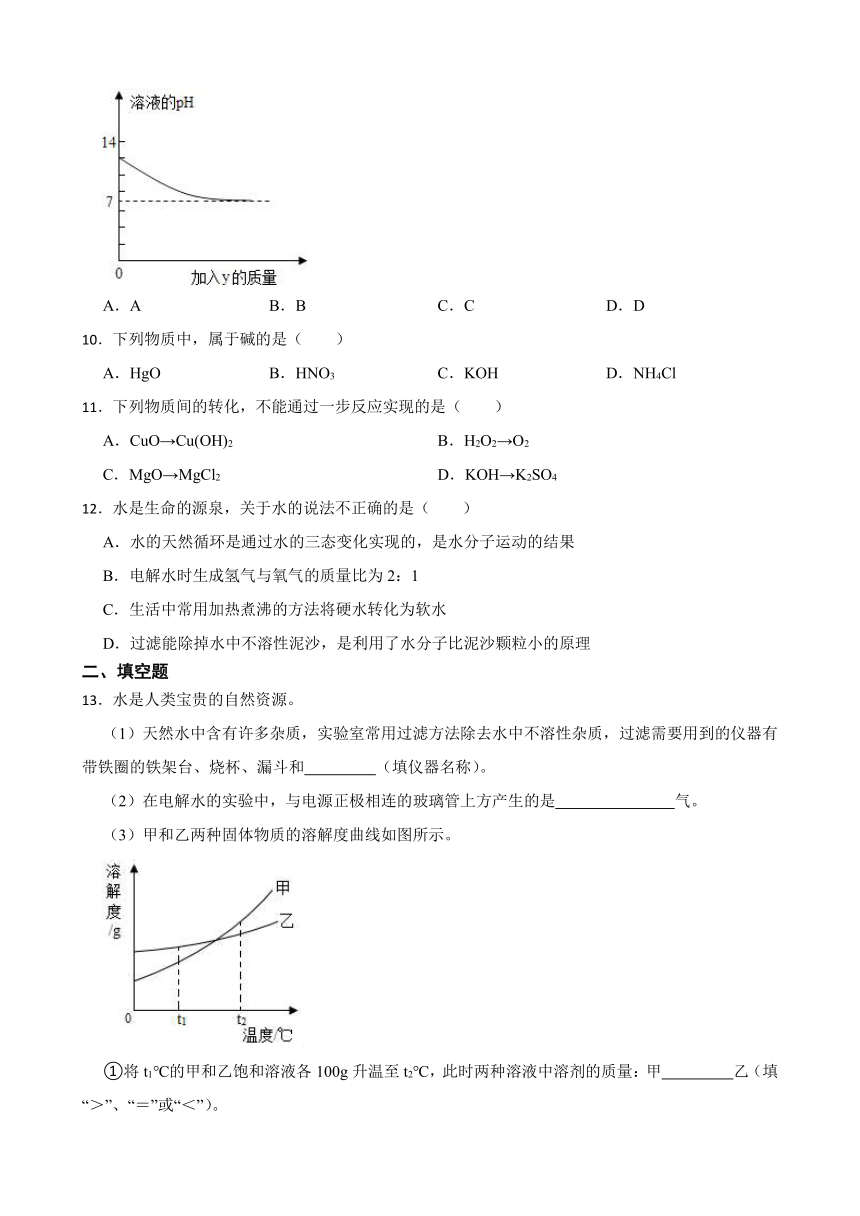
9.烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如图所示.
x y
A NaOH溶液 稀HCl(过量)
B 稀H2SO4 锌粒(少量)
C Ca(OH)2 CO2(适量)
D Ca(OH)2 Na2CO3(适量)
则符合该变化的一组物质是( )
A.A B.B C.C D.D
10.下列物质中,属于碱的是( )
A.HgO B.HNO3 C.KOH D.NH4Cl
11.下列物质间的转化,不能通过一步反应实现的是( )
A.CuO→Cu(OH)2 B.H2O2→O2
C.MgO→MgCl2 D.KOH→K2SO4
12.水是生命的源泉,关于水的说法不正确的是( )
A.水的天然循环是通过水的三态变化实现的,是水分子运动的结果
B.电解水时生成氢气与氧气的质量比为2:1
C.生活中常用加热煮沸的方法将硬水转化为软水
D.过滤能除掉水中不溶性泥沙,是利用了水分子比泥沙颗粒小的原理
二、填空题
13.水是人类宝贵的自然资源。
(1)天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和 (填仪器名称)。
(2)在电解水的实验中,与电源正极相连的玻璃管上方产生的是 气。
(3)甲和乙两种固体物质的溶解度曲线如图所示。
①将t1℃的甲和乙饱和溶液各100g升温至t2℃,此时两种溶液中溶剂的质量:甲 乙(填“>”、“=”或“<”)。
②乙物质中含有少量的甲,可采用 法将乙物质提纯。
14.在2019年年底开始,我国爆发了新冠肺炎,给国家和人民的财产带来巨大的损失,给人民的生命带来严重的威胁,全国人民在党中央的领导下众志成城抗击新冠肺炎。抗疫中用到了许多消毒剂,84消毒液(有效成分为次氯酸钠和二氧化氯(ClO2))是常用消毒剂。
(1)将氯气通入氢氧化钠溶液中可以得到次氯酸钠,根据反应原理推断次氯酸钠的化学式,其反应原理:Cl2+2NaOH=NaCl+H2O+ 。
(2)二氧化氯(ClO2)中氯元素的化合价 ,二氧化氯(ClO2)属于 (填字母序号)。
A、酸
B、碱
C、盐
D、氧化物
(3)84消毒液不能与洁厕灵混合使用,原因是84消毒液中的次氯酸钠与洁厕灵中的盐酸会发生化学反应,生成氯化钠、水和有毒气体氯气,写出其化学反应方程式 。
15. 下列7种物质由H、C、O、S、Ca、Fe中的一种或几种元素组成。
(1)甲在乙中燃烧,火星四射,生成黑色固体。该黑色固体的化学式是 。
(2)甲与丙的溶液反应,可生成一种在标准状况下密度最小的气体。该反应的化学方程式是 。
(3)丁可中和某些工厂污水中含有的丙。丁的溶液可用于检验无色无味的气体X。
写出上述两个反应的化学方程式 、 。
(4)戊由3种元素组成,其相对分子质量为116,工业上常用于制备一种红色物质Y。Y可与丙的溶液反应,溶液变为黄色。在空气中高温煅烧戊,只生成X和Y两种物质,其中戊、Y、X的质量比为29∶20∶11,该反应的化学方程式是 。
16.地球是太阳系八大行星之中唯被液态水所覆盖的星球。
(1)自然界的水需要经过沉降、 、吸附、消毒等多步净化处理才能成为城市生活用水(即自来水)。
(2)自来水中仍含有一些可溶性杂质,需要经过进一步净化才能符合某些实验的要求。
①若自来水中含有较多的可溶性钙和镁的化合物则为硬水。可用来区分软水和硬水的试剂是
②生活中通过 降低水的硬度。
③实验室所用的净化程度较高的水,可以通过 (填分离方法)制取。
(3)爱护水资源一方面需要节约用水,另一方面要防治水体污染。下列措施中,有助于防治水体污染的是 (填字母序号)。
A 禁止使用农药化肥
B 直接将工业废水排入大海
C 集中处理生活污水后再排放 D 园林浇灌改大水漫灌为喷灌、滴灌
17.下列与化学有关的知识,其中归纳完全正确的一组是 .
A.日常物质的区别 B.化学中常见的“三”
H2和CH4﹣﹣点燃后观察火焰颜色 硬水和软水﹣﹣加肥皂水搅拌 三种具有可燃性的气体﹣﹣H2、CO、CH4 三种构成物质的粒子﹣﹣分子、原子、离子
C.除去杂质的方法(括号内为杂质) D.灭火实例和原理
N2(O2)﹣﹣通过灼热的氧化铜 FeCl2(CuCl2)﹣﹣加入过量的铁粉 油锅着火用锅盖盖灭﹣﹣隔绝氧气 住宅失火用水熄灭﹣﹣
18.甲、乙、丙、丁是初中化学中常见的四种物质,它们有如下关系:①甲+乙→H2O,②乙+丁→CO2,③丙+乙→CO2+H2O,则甲是 ,乙中一定含 元素,丙物质是 (填一种最简单的有机化合物)。
三、综合题
19.小刚收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水。其实验过程如下所示。请回答以下问题。
(1)A物质的名称是 ,作用是 ,若经过操作①后,所得液体C中仍有浑浊,其原因可能是 (填写序号);
a.漏斗内的滤纸有破损 b.漏斗下端未靠在烧杯内壁 c.漏斗内液面高于滤纸的边缘
(2)操作②应选用的装置是 (填序号),该过程主要是 变化
(3)小刚取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是 水。操作③应选用的装置是 (填序号),
20.有同学对某铁、金合金废料中金的含量产生了兴趣.他取一定质量的铁、金合金废料,加入足量稀盐酸,充分反应后,放出0.3gH2,剩余固体质量为0.1g.
(1)求废料中铁的质量.
(2)求废料中金的质量分数.
21.A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素。其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分。它们之间的部分转化关系如下图所示(图中反应条件及部分反应物、生成物已省略)。回答下列问题:
(1)写出物质A的化学式: 。
(2)写出由物质C转化为物质B的化学方程式: ,该反应属于基本反应类型中的 反应。
(3)反应C→D可以用于 。
22.海洋中蕴含丰富的化学资源。我国海岸线长3.2万千米,拥有300万平方千米的海洋专属经济区,海洋资源开发前景十分广阔。
(1)镁被誉为海洋里宝贵的“国防元素”。下图是从海水中提取金属镁的流程图,下列说法错误的是 。
a.步骤①→步骤②是为了将氯化镁聚集起来,获得比较纯净的氯化镁
b.步骤②加入的试剂B是稀盐酸
c.步骤③的反应中化学能转化为电能
d.步骤③反应还可得到副产物氯气
(2)某化学兴趣小组的同学取50g某MgCl2溶液于一只洁净干燥的烧杯中,然后逐滴加入10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液质量的关系曲线如图所示。试回答:
①当滴入NaOH溶液20g时(即图中A点),烧杯中溶液里一定大量存在的溶质是 (写化学式)。
②当滴入10%的NaOH溶液40g时(即图中B点),试通过计算,求此时所得不饱和溶液的质量(计算结果精确至0.1g)。
答案解析部分
1.【答案】B
2.【答案】D
3.【答案】C
4.【答案】A
5.【答案】D
6.【答案】C
7.【答案】A
8.【答案】B
9.【答案】C
10.【答案】C
11.【答案】A
12.【答案】B
13.【答案】(1)玻璃棒
(2)氧气(O2)
(3)>;蒸发结晶
14.【答案】(1)NaClO
(2)+4;D
(3)
15.【答案】Fe3O4;Fe + H2SO4 = FeSO4 + H2↑;Ca(OH)2 + H2SO4 = CaSO4 + 2H2O;CO2 + Ca(OH)2 = CaCO3↓+ H2O;4FeCO3 + O2 2Fe2O3 + 4CO2
16.【答案】(1)过滤
(2)肥皂水;煮沸;蒸馏
(3)C
17.【答案】B;降低着火点
18.【答案】氢气;氧;甲烷
19.【答案】(1)明矾;生成胶状物吸附杂质,使杂质沉降来净化水;a、c
(2)Ⅱ;物理
(3)硬;Ⅰ
20.【答案】(1)解:设样品中铁的质量为x
Fe+2HCl═FeCl2+H2↑
56 2
x 0.3g
x=8.4g
(2)解:样品中金的质量分数为: ×100%≈1.2%
21.【答案】(1)O2
(2)CO2+C 2CO;化合
(3)检验二氧化碳气体
22.【答案】(1)c
(2)MgCl2、NaCl;解:设生成的氢氧化镁的质量为xx=2.9g溶液的质量为:50g+40g-2.9g=87.1g答:此时所得不饱和溶液的质量是87.1g。
一、单选题
1.下列各组实验方案中,不能达到实验目的的是( )
选项 实验目的 实验方案
A 区分棉和羊毛 灼烧,闻气味
B 除去CO2气体中的HCl 将气体通过盛有足量NaOH溶液的洗气瓶
C 鉴别Ca(OH)2和NaOH 取样,分别滴加碳酸钠溶液
D 除去N2中的O2 通过灼热的铜网
A.A B.B C.C D.D
2.下列关于化肥的说法正确的是( )
A.过磷酸钙[Ca(H2PO4)2和CaSO4的混合物]属于氮肥
B.凡施用过化肥的蔬菜都会危害健康
C.硫酸钾与熟石灰混合、研磨,能闻到刺激性的气味
D.合理施用化肥能提高农作物的产量
3.下图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合。下列说法中错误的是( )
A.图示有4种分子 B.图示反应前后原子个数不变
C.图示发生了复分解反应 D.图示产物为混合物
4.下列哪种方式不可能用于分离饱和溶液中的溶质和溶剂( )
A.过滤 B.蒸发 C.蒸馏 D.结晶
5.化学与生活息息相关.下列说法中,不合理的是( )
A.干冰可用作环保制冷剂 B.医用酒精可用于杀菌消毒
C.小苏打可用于治疗胃酸过多 D.苛性钠可用作食品的干燥剂
6.用括号内试剂不能一次性将组内物质鉴别出来的是( )
A.NaOH固体、NH4NO3固体、NaCl固体(水)
B.稀盐酸、H2O、Ca(OH)2溶液(紫色石蕊溶液)
C.NaCl溶液、Na2CO3溶液、NaNO3溶液(AgNO3溶液)
D.Ba(NO3)2溶液、MgCl2溶液、K2CO3溶液(稀硫酸)
7.物质的鉴别、分离与除杂是化学研究常用方法,下列实验方法正确的是( )
选项 实验目的 实验方法
A 分离 K2SO4 溶液与 BaSO4 过滤
B 鉴别天然蚕丝与人造丝 取样,分别闻气味
C 区分硝酸铵与氯化钾 加足量水,观察是否溶解
D 除去稀硝酸中的少量AgNO3 加过量稀盐酸,过滤
A.A B.B C.C D.D
8.图像是化学实验分析数据的重要依据,下列图像正确的是( )
A.图A是高锰酸钾制氧气,试管中固体质量的变化
B.图B是过氧化氢与二氧化锰混合制氧气
C.图C是电解水产生的氧气和氢气的质量比
D.图D是加了二氧化锰和没加二氧化锰制氧气的对比
9.烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如图所示.
x y
A NaOH溶液 稀HCl(过量)
B 稀H2SO4 锌粒(少量)
C Ca(OH)2 CO2(适量)
D Ca(OH)2 Na2CO3(适量)
则符合该变化的一组物质是( )
A.A B.B C.C D.D
10.下列物质中,属于碱的是( )
A.HgO B.HNO3 C.KOH D.NH4Cl
11.下列物质间的转化,不能通过一步反应实现的是( )
A.CuO→Cu(OH)2 B.H2O2→O2
C.MgO→MgCl2 D.KOH→K2SO4
12.水是生命的源泉,关于水的说法不正确的是( )
A.水的天然循环是通过水的三态变化实现的,是水分子运动的结果
B.电解水时生成氢气与氧气的质量比为2:1
C.生活中常用加热煮沸的方法将硬水转化为软水
D.过滤能除掉水中不溶性泥沙,是利用了水分子比泥沙颗粒小的原理
二、填空题
13.水是人类宝贵的自然资源。
(1)天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和 (填仪器名称)。
(2)在电解水的实验中,与电源正极相连的玻璃管上方产生的是 气。
(3)甲和乙两种固体物质的溶解度曲线如图所示。
①将t1℃的甲和乙饱和溶液各100g升温至t2℃,此时两种溶液中溶剂的质量:甲 乙(填“>”、“=”或“<”)。
②乙物质中含有少量的甲,可采用 法将乙物质提纯。
14.在2019年年底开始,我国爆发了新冠肺炎,给国家和人民的财产带来巨大的损失,给人民的生命带来严重的威胁,全国人民在党中央的领导下众志成城抗击新冠肺炎。抗疫中用到了许多消毒剂,84消毒液(有效成分为次氯酸钠和二氧化氯(ClO2))是常用消毒剂。
(1)将氯气通入氢氧化钠溶液中可以得到次氯酸钠,根据反应原理推断次氯酸钠的化学式,其反应原理:Cl2+2NaOH=NaCl+H2O+ 。
(2)二氧化氯(ClO2)中氯元素的化合价 ,二氧化氯(ClO2)属于 (填字母序号)。
A、酸
B、碱
C、盐
D、氧化物
(3)84消毒液不能与洁厕灵混合使用,原因是84消毒液中的次氯酸钠与洁厕灵中的盐酸会发生化学反应,生成氯化钠、水和有毒气体氯气,写出其化学反应方程式 。
15. 下列7种物质由H、C、O、S、Ca、Fe中的一种或几种元素组成。
(1)甲在乙中燃烧,火星四射,生成黑色固体。该黑色固体的化学式是 。
(2)甲与丙的溶液反应,可生成一种在标准状况下密度最小的气体。该反应的化学方程式是 。
(3)丁可中和某些工厂污水中含有的丙。丁的溶液可用于检验无色无味的气体X。
写出上述两个反应的化学方程式 、 。
(4)戊由3种元素组成,其相对分子质量为116,工业上常用于制备一种红色物质Y。Y可与丙的溶液反应,溶液变为黄色。在空气中高温煅烧戊,只生成X和Y两种物质,其中戊、Y、X的质量比为29∶20∶11,该反应的化学方程式是 。
16.地球是太阳系八大行星之中唯被液态水所覆盖的星球。
(1)自然界的水需要经过沉降、 、吸附、消毒等多步净化处理才能成为城市生活用水(即自来水)。
(2)自来水中仍含有一些可溶性杂质,需要经过进一步净化才能符合某些实验的要求。
①若自来水中含有较多的可溶性钙和镁的化合物则为硬水。可用来区分软水和硬水的试剂是
②生活中通过 降低水的硬度。
③实验室所用的净化程度较高的水,可以通过 (填分离方法)制取。
(3)爱护水资源一方面需要节约用水,另一方面要防治水体污染。下列措施中,有助于防治水体污染的是 (填字母序号)。
A 禁止使用农药化肥
B 直接将工业废水排入大海
C 集中处理生活污水后再排放 D 园林浇灌改大水漫灌为喷灌、滴灌
17.下列与化学有关的知识,其中归纳完全正确的一组是 .
A.日常物质的区别 B.化学中常见的“三”
H2和CH4﹣﹣点燃后观察火焰颜色 硬水和软水﹣﹣加肥皂水搅拌 三种具有可燃性的气体﹣﹣H2、CO、CH4 三种构成物质的粒子﹣﹣分子、原子、离子
C.除去杂质的方法(括号内为杂质) D.灭火实例和原理
N2(O2)﹣﹣通过灼热的氧化铜 FeCl2(CuCl2)﹣﹣加入过量的铁粉 油锅着火用锅盖盖灭﹣﹣隔绝氧气 住宅失火用水熄灭﹣﹣
18.甲、乙、丙、丁是初中化学中常见的四种物质,它们有如下关系:①甲+乙→H2O,②乙+丁→CO2,③丙+乙→CO2+H2O,则甲是 ,乙中一定含 元素,丙物质是 (填一种最简单的有机化合物)。
三、综合题
19.小刚收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水。其实验过程如下所示。请回答以下问题。
(1)A物质的名称是 ,作用是 ,若经过操作①后,所得液体C中仍有浑浊,其原因可能是 (填写序号);
a.漏斗内的滤纸有破损 b.漏斗下端未靠在烧杯内壁 c.漏斗内液面高于滤纸的边缘
(2)操作②应选用的装置是 (填序号),该过程主要是 变化
(3)小刚取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是 水。操作③应选用的装置是 (填序号),
20.有同学对某铁、金合金废料中金的含量产生了兴趣.他取一定质量的铁、金合金废料,加入足量稀盐酸,充分反应后,放出0.3gH2,剩余固体质量为0.1g.
(1)求废料中铁的质量.
(2)求废料中金的质量分数.
21.A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素。其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分。它们之间的部分转化关系如下图所示(图中反应条件及部分反应物、生成物已省略)。回答下列问题:
(1)写出物质A的化学式: 。
(2)写出由物质C转化为物质B的化学方程式: ,该反应属于基本反应类型中的 反应。
(3)反应C→D可以用于 。
22.海洋中蕴含丰富的化学资源。我国海岸线长3.2万千米,拥有300万平方千米的海洋专属经济区,海洋资源开发前景十分广阔。
(1)镁被誉为海洋里宝贵的“国防元素”。下图是从海水中提取金属镁的流程图,下列说法错误的是 。
a.步骤①→步骤②是为了将氯化镁聚集起来,获得比较纯净的氯化镁
b.步骤②加入的试剂B是稀盐酸
c.步骤③的反应中化学能转化为电能
d.步骤③反应还可得到副产物氯气
(2)某化学兴趣小组的同学取50g某MgCl2溶液于一只洁净干燥的烧杯中,然后逐滴加入10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液质量的关系曲线如图所示。试回答:
①当滴入NaOH溶液20g时(即图中A点),烧杯中溶液里一定大量存在的溶质是 (写化学式)。
②当滴入10%的NaOH溶液40g时(即图中B点),试通过计算,求此时所得不饱和溶液的质量(计算结果精确至0.1g)。
答案解析部分
1.【答案】B
2.【答案】D
3.【答案】C
4.【答案】A
5.【答案】D
6.【答案】C
7.【答案】A
8.【答案】B
9.【答案】C
10.【答案】C
11.【答案】A
12.【答案】B
13.【答案】(1)玻璃棒
(2)氧气(O2)
(3)>;蒸发结晶
14.【答案】(1)NaClO
(2)+4;D
(3)
15.【答案】Fe3O4;Fe + H2SO4 = FeSO4 + H2↑;Ca(OH)2 + H2SO4 = CaSO4 + 2H2O;CO2 + Ca(OH)2 = CaCO3↓+ H2O;4FeCO3 + O2 2Fe2O3 + 4CO2
16.【答案】(1)过滤
(2)肥皂水;煮沸;蒸馏
(3)C
17.【答案】B;降低着火点
18.【答案】氢气;氧;甲烷
19.【答案】(1)明矾;生成胶状物吸附杂质,使杂质沉降来净化水;a、c
(2)Ⅱ;物理
(3)硬;Ⅰ
20.【答案】(1)解:设样品中铁的质量为x
Fe+2HCl═FeCl2+H2↑
56 2
x 0.3g
x=8.4g
(2)解:样品中金的质量分数为: ×100%≈1.2%
21.【答案】(1)O2
(2)CO2+C 2CO;化合
(3)检验二氧化碳气体
22.【答案】(1)c
(2)MgCl2、NaCl;解:设生成的氢氧化镁的质量为xx=2.9g溶液的质量为:50g+40g-2.9g=87.1g答:此时所得不饱和溶液的质量是87.1g。
同课章节目录
