6.1 奇光异彩的金属 同步练习 (含答案)2022-2023学年沪教版(上海)九年级下册化学
文档属性
| 名称 | 6.1 奇光异彩的金属 同步练习 (含答案)2022-2023学年沪教版(上海)九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 112.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-01 00:00:00 | ||
图片预览


文档简介
6.1 奇光异彩的金属 同步练习
一、单选题
1.已知X、Y、Z三种金属能发生下列反应:X+H2SO4═XSO4+H2↑,Y+Z(NO3)2═Y(NO3)2+Z,Z+X(NO3)2═Z(NO3)2+X,则X、Y、Z三种金属与氢的活动性由强到弱的顺序为( )
A.X>H>Y>Z B.Y>Z>X>H
C.Z>Y>X>H D.X>H>Z>Y
2.下列实验方案或操作不能达到目的是( )
A.用气味来区分酒精和水
B.用状态来区分铁和铜
C.用燃烧的木条比较人吸入的空气和呼出气体中二氧化碳的含量多少
D.用火柴梗迅速平放蜡烛火焰中,约 1s 后取出,比较火焰各层温度
3.自来水消毒的微观过程可用下图表示,下列说法正确的是( )
( 表示氧原子, 表示氢原子, 表示氯原子)
A.化学变化中分子不会再分
B.A,C,D都是氧化物
C.该反应属于置换反应
D.参加反应的两种分子个数比是1:1
4.归纳推理是一种重要的化学思维方法。下列叙述正确的是( )
A.活泼金属与酸反应有气体产生,则与酸反应产生气体的一定是活泼金属
B.单质一定是由同种元素组成的物质,则由同种元素组成的物质一定是单质
C.氧化物中都含有氧元素,所以含有氧元素的化合物一定是氧化物
D.化学反应伴随能量变化,所以金属腐蚀过程中一定伴随能量变化
5.如图是CO与CuO反应的实验装置,下列关于该实验说法正确的是()
①玻璃管中黑色固体变成了红色
②CO被还原为CO2
③玻璃管中发生的反应为置换反应
④既有效地防止了CO对空气的污染,又充分利用了能源
A.①② B.①④ C.②④ D.③④
6.铝是生活中常见的金属,除我们熟知的性质之外,铝还可以与NaOH溶液发生反应:,下列说法错误的是( )
A.X的化学式为H2
B.该反应不属于置换反应
C.在该反应中,铝元素与氢元素的化合价一定变化
D.铝具有很好的抗腐蚀性能是因为其化学性质很稳定
7.现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示),则三种金属活动性由强到弱的顺序是( )
A.乙、甲、丙 B.乙、丙、甲 C.丙、甲、乙 D.丙、乙、甲
8.金属M与AgNO3溶液发生反应:M+2AgNO3=M(NO3)2+2Ag,下列说法正确的是( )
A.M可能是铝
B.Ag的金属活动性比M强
C.反应前后M的化合价发生了改变
D.在金属活动性顺序里,M一定排在氢前
9.某工厂排放的废水经测定pH为3,为治理废水,需将pH调至8.为此,可向该废水中加入适量的( )
A.生石灰 B.硫酸 C.水 D.废铜屑
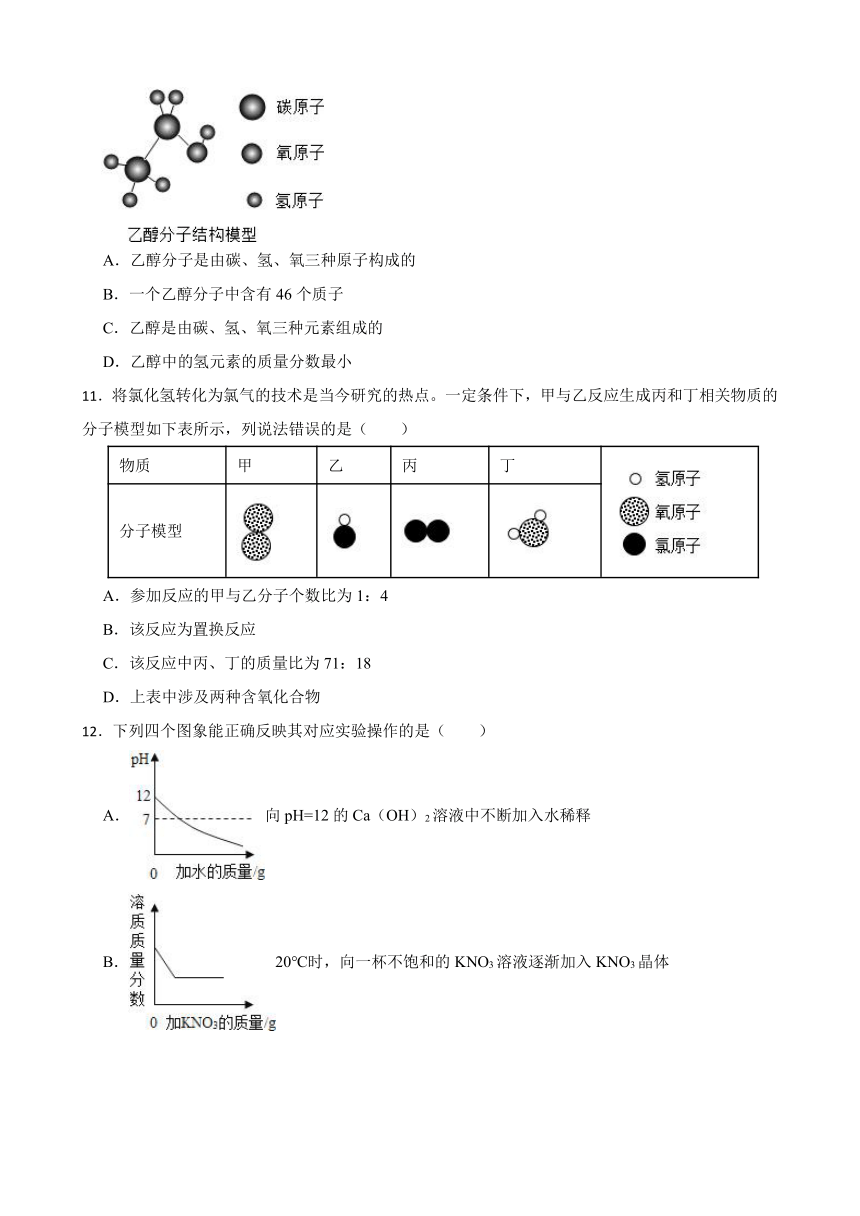
10.农作物的种子经过发酵、蒸馏可制得乙醇。乙醇的分子结构如图所示。则下列叙述错误的是( )
A.乙醇分子是由碳、氢、氧三种原子构成的
B.一个乙醇分子中含有46个质子
C.乙醇是由碳、氢、氧三种元素组成的
D.乙醇中的氢元素的质量分数最小
11.将氯化氢转化为氯气的技术是当今研究的热点。一定条件下,甲与乙反应生成丙和丁相关物质的分子模型如下表所示,列说法错误的是( )
物质 甲 乙 丙 丁
分子模型
A.参加反应的甲与乙分子个数比为1:4
B.该反应为置换反应
C.该反应中丙、丁的质量比为71:18
D.上表中涉及两种含氧化合物
12.下列四个图象能正确反映其对应实验操作的是( )
A.向pH=12的Ca(OH)2溶液中不断加入水稀释
B.20℃时,向一杯不饱和的KNO3溶液逐渐加入KNO3晶体
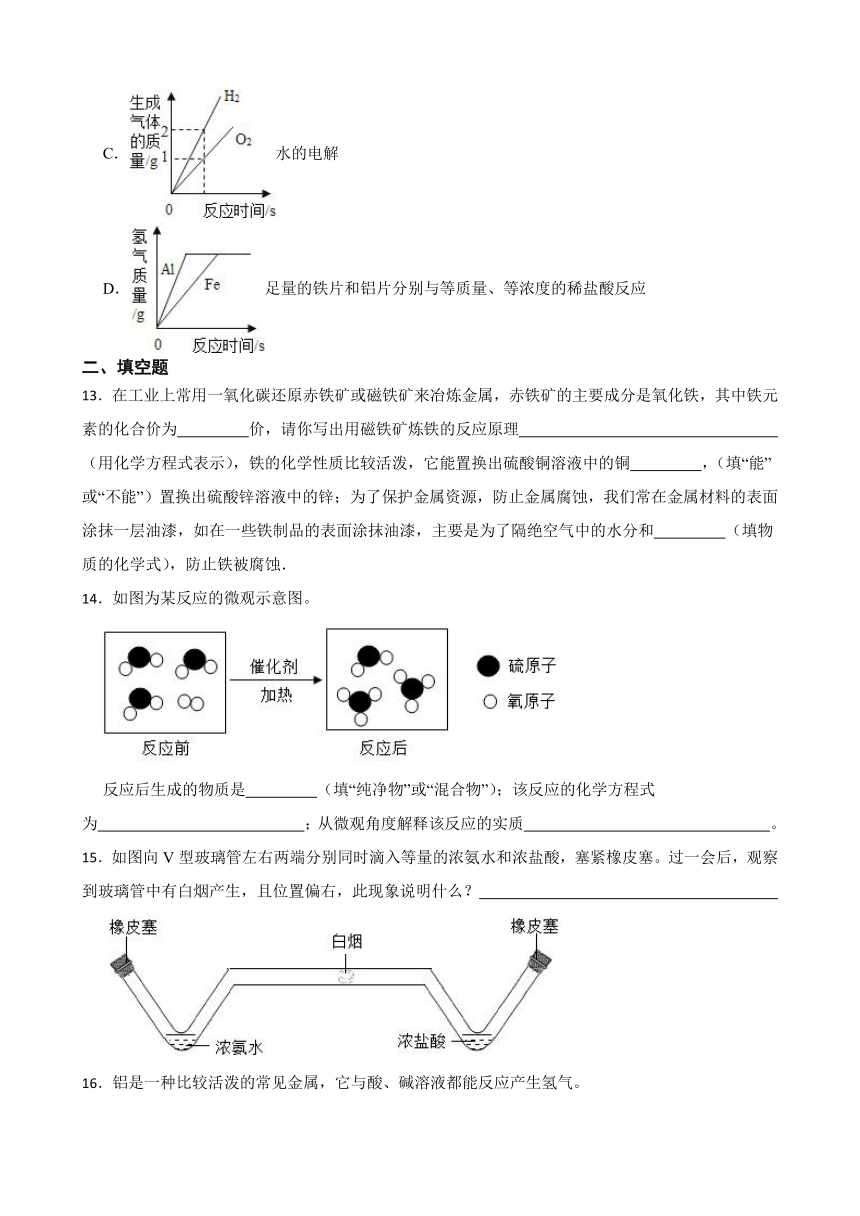
C.水的电解
D.足量的铁片和铝片分别与等质量、等浓度的稀盐酸反应
二、填空题
13.在工业上常用一氧化碳还原赤铁矿或磁铁矿来冶炼金属,赤铁矿的主要成分是氧化铁,其中铁元素的化合价为 价,请你写出用磁铁矿炼铁的反应原理 (用化学方程式表示),铁的化学性质比较活泼,它能置换出硫酸铜溶液中的铜 ,(填“能”或“不能”)置换出硫酸锌溶液中的锌;为了保护金属资源,防止金属腐蚀,我们常在金属材料的表面涂抹一层油漆,如在一些铁制品的表面涂抹油漆,主要是为了隔绝空气中的水分和 (填物质的化学式),防止铁被腐蚀.
14.如图为某反应的微观示意图。
反应后生成的物质是 (填“纯净物”或“混合物”);该反应的化学方程式为 ;从微观角度解释该反应的实质 。
15.如图向V型玻璃管左右两端分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。过一会后,观察到玻璃管中有白烟产生,且位置偏右,此现象说明什么?
16.铝是一种比较活泼的常见金属,它与酸、碱溶液都能反应产生氢气。
(1)写出铝与稀硫酸反应的化学方程式: 。
(2)完成铝与氢氧化钠溶液反应生成氢气的化学方程式:2Al+2NaOH+ ═2NaAlO2+3H2↑。
(3)已知NaAlO2与少量盐酸反应的化学方程式:NaAlO2+HCl+H2O═Al(OH)3↓+NaCl.请写出NaAlO2与过量盐酸反应的化学方程式: 。
17.某化学兴趣小组为了测定某种生铁样品中铁的质量分数,在实验室将5.8g生铁样品放入烧杯中,加入50g稀硫酸恰好完全反应(杂质不参加反应),反应后称得剩余物质的总质量为55.6g。请回答:
⑴你分析后一定能计算出产生氢气的质量为 。你上述计算的理论依据是 。
⑵请你参与这个小组,来计算出该生铁样品中铁的质量分数是多少?(结果保留一位小数)
18.金属在生产和生活中有广泛的应用。
(1)铁在潮湿的空气中易生锈的原因是 。
(2)向硝酸银溶液中加入一定量的锌和铜的混合粉末,充分反应后过滤,滤液呈蓝色,则滤出的固体中一定含有 ;滤液中一定含有的金属离子是 (写离子符号)。
(3)某同学称取黄铜(铜锌合金)样品20g放入锥形瓶中,向其中加入100g稀硫酸恰好完全反应,测得反应后剩余物的质量为119.8g,则所用稀硫酸中溶质的质量分数为 。
三、综合题
19.饺子是中国传统食品,小丽周末回家观察了妈妈包饺子的全过程,发现许多与化学知识有关的问题。
(1)包饺子所用的原料:面粉、水、食盐、芹菜、大葱、植物油、牛肉。其中芹菜富合的营养素是 ;牛肉富含的营养素是 ;
(2)煮饺子的水是硬水还是软水,可用 进行检验。日常生活中常用 的方法,降低水的硬度。
(3)煮饺子用的不锈钢锅是一种 制品,它具有良好的抗腐蚀性。
(4)饭后用洗涤灵清洗碗筷利用了洗涤灵的 作用。
20.金属在生成生活中应用广泛.
(1)最初输水管材用铸铁,目前多用塑料管和塑料金属复合管,输送热水一般用铜管.下列管材中,属于金属材料的是 (填字母序号,下同).
(2)铁生锈的条件是 .将生锈的铁片放在硫酸和硫酸铜的混合溶液中,可能发生的置换反应的化学方程式是 、 .
(3)金属的回收和利用是保护金属资源的一种有效途径.
①废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为 ;
②将铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后,对剩余固体成分的判断正确的是 .
A.肯定有银B.肯定有铜C.可能有铁D.可能是铁和银.
21.2015年8月12日23:30左右,位于天津滨海新区塘沽开发区的天津东江保税港区瑞海国际物流有限公司所属危险品仓库发生爆炸。共发现遇难者总人数升至165人,仍有8人失联 。其中公安消防人员24人,天津港消防人员75人,民警11人,其他人员55人,事故受损住宅处置协议共签约9420户。天津滨海新区危险品爆炸事故中,除硫氰化钠(NaSCN)外,还有多种危化品。许多都会遇火燃烧爆炸,且对环境有一定的危害。
(1)硫氰化钠(NaSCN)中所含的硫指的是 ,(选填“硫单质”或“硫元素”)。
(2)硫原子的相对原子质量是 。 硫原子在化学变化中容易 电子,(选填“得到”或“失去”)。请用化学符号表示其离子 。
(3)硫单质在空气中能燃烧反应生成二氧化硫,二氧化硫是一种空气污染物。你还知道其 他空气污染物吗?请任意写出两种其他空气污染物的化学式 、 。
(4)在空气中二氧化硫能继续和空气中氧气反应生成三氧化硫,三氧化硫再和空气中水蒸气反应生成硫酸形成酸雨。
①请按先后顺序写出本小题中涉及到是化学发应的符号表达式 ,
,第一个反应属于 反应类型
②硫酸中硫元素的化合价为 价。
22.在硝酸银、硝酸铜的混合溶液中加入一定量金属镁,反应停止后过滤,滤液仍为蓝色.
(1)滤液中一定含有的溶质是什么?
(2)请写出该过程中一定发生的反应的化学方程式.
(3)若向所得固体上滴加稀盐酸,则 (填“一定有”、“可能有”或“一定没 有”)气泡产生.
答案解析部分
1.【答案】B
2.【答案】B
3.【答案】D
4.【答案】D
5.【答案】B
6.【答案】D
7.【答案】D
8.【答案】C
9.【答案】A
10.【答案】B
11.【答案】D
12.【答案】D
13.【答案】+3;Fe3O4+4CO {#mathmL#}{#/mathmL#} 3Fe+4CO2;不能;O2
14.【答案】纯净物;;分子的破裂,原子的重新组合
15.【答案】分子在不断运动,不同的分子运动速率不同(或分子在不断运动,相同条件下,氨分子比氯化氢分子运动速率快)
16.【答案】(1)2Al+3H2SO4=Al2(SO4)3+3H2↑
(2)2H2O
(3)NaAlO2+4HCl=NaCl+AlCl3+2H2O。
17.【答案】0.2g;质量守恒定律;解:设生铁样品中铁的质量分数为x,则Fe + H2SO4 = FeSO4 + H2↑56 25.8gx 0.2g x=96.6%答:生铁样品中铁的质量分数为96.6%。
18.【答案】(1)铁更容易与氧气、水分充分接触
(2)Ag;Zn2+、Cu2+
(3)9.8%
19.【答案】(1)维生素;蛋白质
(2)肥皂水;煮沸
(3)合金
(4)乳化
20.【答案】(1)AB
(2)铁与水和空气并存;Fe+H2SO4=FeSO4+H2↑;Fe+CuSO4=FeSO4+Cu
(3)3CO+Fe2O3 2Fe+3CO2;AC
21.【答案】(1)硫元素
(2)32.06;得到;S2-
(3)CO;NO2(O3三个中任意写出其中两个)
(4)SO2+O2 → SO3;SO3+H2O→H2SO4;化合;+6
22.【答案】(1)解:硝酸铜和硝酸镁
(2)解:Mg+2AgNO3═2Ag+Mg(NO3)2
(3)一定没有
一、单选题
1.已知X、Y、Z三种金属能发生下列反应:X+H2SO4═XSO4+H2↑,Y+Z(NO3)2═Y(NO3)2+Z,Z+X(NO3)2═Z(NO3)2+X,则X、Y、Z三种金属与氢的活动性由强到弱的顺序为( )
A.X>H>Y>Z B.Y>Z>X>H
C.Z>Y>X>H D.X>H>Z>Y
2.下列实验方案或操作不能达到目的是( )
A.用气味来区分酒精和水
B.用状态来区分铁和铜
C.用燃烧的木条比较人吸入的空气和呼出气体中二氧化碳的含量多少
D.用火柴梗迅速平放蜡烛火焰中,约 1s 后取出,比较火焰各层温度
3.自来水消毒的微观过程可用下图表示,下列说法正确的是( )
( 表示氧原子, 表示氢原子, 表示氯原子)
A.化学变化中分子不会再分
B.A,C,D都是氧化物
C.该反应属于置换反应
D.参加反应的两种分子个数比是1:1
4.归纳推理是一种重要的化学思维方法。下列叙述正确的是( )
A.活泼金属与酸反应有气体产生,则与酸反应产生气体的一定是活泼金属
B.单质一定是由同种元素组成的物质,则由同种元素组成的物质一定是单质
C.氧化物中都含有氧元素,所以含有氧元素的化合物一定是氧化物
D.化学反应伴随能量变化,所以金属腐蚀过程中一定伴随能量变化
5.如图是CO与CuO反应的实验装置,下列关于该实验说法正确的是()
①玻璃管中黑色固体变成了红色
②CO被还原为CO2
③玻璃管中发生的反应为置换反应
④既有效地防止了CO对空气的污染,又充分利用了能源
A.①② B.①④ C.②④ D.③④
6.铝是生活中常见的金属,除我们熟知的性质之外,铝还可以与NaOH溶液发生反应:,下列说法错误的是( )
A.X的化学式为H2
B.该反应不属于置换反应
C.在该反应中,铝元素与氢元素的化合价一定变化
D.铝具有很好的抗腐蚀性能是因为其化学性质很稳定
7.现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示),则三种金属活动性由强到弱的顺序是( )
A.乙、甲、丙 B.乙、丙、甲 C.丙、甲、乙 D.丙、乙、甲
8.金属M与AgNO3溶液发生反应:M+2AgNO3=M(NO3)2+2Ag,下列说法正确的是( )
A.M可能是铝
B.Ag的金属活动性比M强
C.反应前后M的化合价发生了改变
D.在金属活动性顺序里,M一定排在氢前
9.某工厂排放的废水经测定pH为3,为治理废水,需将pH调至8.为此,可向该废水中加入适量的( )
A.生石灰 B.硫酸 C.水 D.废铜屑
10.农作物的种子经过发酵、蒸馏可制得乙醇。乙醇的分子结构如图所示。则下列叙述错误的是( )
A.乙醇分子是由碳、氢、氧三种原子构成的
B.一个乙醇分子中含有46个质子
C.乙醇是由碳、氢、氧三种元素组成的
D.乙醇中的氢元素的质量分数最小
11.将氯化氢转化为氯气的技术是当今研究的热点。一定条件下,甲与乙反应生成丙和丁相关物质的分子模型如下表所示,列说法错误的是( )
物质 甲 乙 丙 丁
分子模型
A.参加反应的甲与乙分子个数比为1:4
B.该反应为置换反应
C.该反应中丙、丁的质量比为71:18
D.上表中涉及两种含氧化合物
12.下列四个图象能正确反映其对应实验操作的是( )
A.向pH=12的Ca(OH)2溶液中不断加入水稀释
B.20℃时,向一杯不饱和的KNO3溶液逐渐加入KNO3晶体
C.水的电解
D.足量的铁片和铝片分别与等质量、等浓度的稀盐酸反应
二、填空题
13.在工业上常用一氧化碳还原赤铁矿或磁铁矿来冶炼金属,赤铁矿的主要成分是氧化铁,其中铁元素的化合价为 价,请你写出用磁铁矿炼铁的反应原理 (用化学方程式表示),铁的化学性质比较活泼,它能置换出硫酸铜溶液中的铜 ,(填“能”或“不能”)置换出硫酸锌溶液中的锌;为了保护金属资源,防止金属腐蚀,我们常在金属材料的表面涂抹一层油漆,如在一些铁制品的表面涂抹油漆,主要是为了隔绝空气中的水分和 (填物质的化学式),防止铁被腐蚀.
14.如图为某反应的微观示意图。
反应后生成的物质是 (填“纯净物”或“混合物”);该反应的化学方程式为 ;从微观角度解释该反应的实质 。
15.如图向V型玻璃管左右两端分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。过一会后,观察到玻璃管中有白烟产生,且位置偏右,此现象说明什么?
16.铝是一种比较活泼的常见金属,它与酸、碱溶液都能反应产生氢气。
(1)写出铝与稀硫酸反应的化学方程式: 。
(2)完成铝与氢氧化钠溶液反应生成氢气的化学方程式:2Al+2NaOH+ ═2NaAlO2+3H2↑。
(3)已知NaAlO2与少量盐酸反应的化学方程式:NaAlO2+HCl+H2O═Al(OH)3↓+NaCl.请写出NaAlO2与过量盐酸反应的化学方程式: 。
17.某化学兴趣小组为了测定某种生铁样品中铁的质量分数,在实验室将5.8g生铁样品放入烧杯中,加入50g稀硫酸恰好完全反应(杂质不参加反应),反应后称得剩余物质的总质量为55.6g。请回答:
⑴你分析后一定能计算出产生氢气的质量为 。你上述计算的理论依据是 。
⑵请你参与这个小组,来计算出该生铁样品中铁的质量分数是多少?(结果保留一位小数)
18.金属在生产和生活中有广泛的应用。
(1)铁在潮湿的空气中易生锈的原因是 。
(2)向硝酸银溶液中加入一定量的锌和铜的混合粉末,充分反应后过滤,滤液呈蓝色,则滤出的固体中一定含有 ;滤液中一定含有的金属离子是 (写离子符号)。
(3)某同学称取黄铜(铜锌合金)样品20g放入锥形瓶中,向其中加入100g稀硫酸恰好完全反应,测得反应后剩余物的质量为119.8g,则所用稀硫酸中溶质的质量分数为 。
三、综合题
19.饺子是中国传统食品,小丽周末回家观察了妈妈包饺子的全过程,发现许多与化学知识有关的问题。
(1)包饺子所用的原料:面粉、水、食盐、芹菜、大葱、植物油、牛肉。其中芹菜富合的营养素是 ;牛肉富含的营养素是 ;
(2)煮饺子的水是硬水还是软水,可用 进行检验。日常生活中常用 的方法,降低水的硬度。
(3)煮饺子用的不锈钢锅是一种 制品,它具有良好的抗腐蚀性。
(4)饭后用洗涤灵清洗碗筷利用了洗涤灵的 作用。
20.金属在生成生活中应用广泛.
(1)最初输水管材用铸铁,目前多用塑料管和塑料金属复合管,输送热水一般用铜管.下列管材中,属于金属材料的是 (填字母序号,下同).
(2)铁生锈的条件是 .将生锈的铁片放在硫酸和硫酸铜的混合溶液中,可能发生的置换反应的化学方程式是 、 .
(3)金属的回收和利用是保护金属资源的一种有效途径.
①废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为 ;
②将铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后,对剩余固体成分的判断正确的是 .
A.肯定有银B.肯定有铜C.可能有铁D.可能是铁和银.
21.2015年8月12日23:30左右,位于天津滨海新区塘沽开发区的天津东江保税港区瑞海国际物流有限公司所属危险品仓库发生爆炸。共发现遇难者总人数升至165人,仍有8人失联 。其中公安消防人员24人,天津港消防人员75人,民警11人,其他人员55人,事故受损住宅处置协议共签约9420户。天津滨海新区危险品爆炸事故中,除硫氰化钠(NaSCN)外,还有多种危化品。许多都会遇火燃烧爆炸,且对环境有一定的危害。
(1)硫氰化钠(NaSCN)中所含的硫指的是 ,(选填“硫单质”或“硫元素”)。
(2)硫原子的相对原子质量是 。 硫原子在化学变化中容易 电子,(选填“得到”或“失去”)。请用化学符号表示其离子 。
(3)硫单质在空气中能燃烧反应生成二氧化硫,二氧化硫是一种空气污染物。你还知道其 他空气污染物吗?请任意写出两种其他空气污染物的化学式 、 。
(4)在空气中二氧化硫能继续和空气中氧气反应生成三氧化硫,三氧化硫再和空气中水蒸气反应生成硫酸形成酸雨。
①请按先后顺序写出本小题中涉及到是化学发应的符号表达式 ,
,第一个反应属于 反应类型
②硫酸中硫元素的化合价为 价。
22.在硝酸银、硝酸铜的混合溶液中加入一定量金属镁,反应停止后过滤,滤液仍为蓝色.
(1)滤液中一定含有的溶质是什么?
(2)请写出该过程中一定发生的反应的化学方程式.
(3)若向所得固体上滴加稀盐酸,则 (填“一定有”、“可能有”或“一定没 有”)气泡产生.
答案解析部分
1.【答案】B
2.【答案】B
3.【答案】D
4.【答案】D
5.【答案】B
6.【答案】D
7.【答案】D
8.【答案】C
9.【答案】A
10.【答案】B
11.【答案】D
12.【答案】D
13.【答案】+3;Fe3O4+4CO {#mathmL#}{#/mathmL#} 3Fe+4CO2;不能;O2
14.【答案】纯净物;;分子的破裂,原子的重新组合
15.【答案】分子在不断运动,不同的分子运动速率不同(或分子在不断运动,相同条件下,氨分子比氯化氢分子运动速率快)
16.【答案】(1)2Al+3H2SO4=Al2(SO4)3+3H2↑
(2)2H2O
(3)NaAlO2+4HCl=NaCl+AlCl3+2H2O。
17.【答案】0.2g;质量守恒定律;解:设生铁样品中铁的质量分数为x,则Fe + H2SO4 = FeSO4 + H2↑56 25.8gx 0.2g x=96.6%答:生铁样品中铁的质量分数为96.6%。
18.【答案】(1)铁更容易与氧气、水分充分接触
(2)Ag;Zn2+、Cu2+
(3)9.8%
19.【答案】(1)维生素;蛋白质
(2)肥皂水;煮沸
(3)合金
(4)乳化
20.【答案】(1)AB
(2)铁与水和空气并存;Fe+H2SO4=FeSO4+H2↑;Fe+CuSO4=FeSO4+Cu
(3)3CO+Fe2O3 2Fe+3CO2;AC
21.【答案】(1)硫元素
(2)32.06;得到;S2-
(3)CO;NO2(O3三个中任意写出其中两个)
(4)SO2+O2 → SO3;SO3+H2O→H2SO4;化合;+6
22.【答案】(1)解:硝酸铜和硝酸镁
(2)解:Mg+2AgNO3═2Ag+Mg(NO3)2
(3)一定没有
