到实验室去:粗盐中难溶性杂质的去除 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学
文档属性
| 名称 | 到实验室去:粗盐中难溶性杂质的去除 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 57.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-01 00:00:00 | ||
图片预览



文档简介
到实验室去:粗盐中难溶性杂质的去除 同步练习
一、单选题
1.下列有关蒸发过程描述正确的是( )
A.蒸发需要的玻璃仪器有烧杯、玻璃棒
B.结束实验后用手拿开蒸发皿
C.蒸发过程中要用玻璃棒不停地搅拌
D.等水分完全蒸干后再停止加热
2.下列实验问题处理方法正确的是( )
①高锰酸钾制氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
②在气体发生装置上直接点燃一氧化碳气体时,必须要先检验一氧化碳气体的纯度
③实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
④给试管中的液体加热时,不时移动试管,以免暴沸伤人
⑤使用滴瓶滴加试剂后,立即用蒸馏水洗净滴管并放回原瓶
A.①②③⑤ B.①②④
C.②③⑤ D.②④⑤
3.学习化学的目的并不在于要成为化学家,重要的是善于用化学知识去分析、解决生产生活中的问题。从化学的角度看,下列关于氧气的说法中正确的是( )
A.物质与氧气发生的反应属于氧化反应
B.鱼、虾等能在水中生存,是由于氧气易溶于水
C.氧气的化学性质很活泼,能跟所有物质反应
D.氧气可以支持燃烧,可以作燃料
4.化学实验必须按规范进行操作。如图所示的实验操作规范的是( )
A.贮存呼出的气体
B.吸取液体
C.塞紧橡胶塞
D.处理废弃固体药品
5.下列各组物质的鉴别和分离方法中错误的是( )
A.用肥皂水鉴别硬水和软水
B.用二氧化锰鉴别水和过氧化氢
C.用过滤的方法分离水和铁粉
D.用燃着的木条鉴别O2、CO2、N2三种气体
6.下列化学实验操作中,先后顺序错误的是()
A.使用胶头滴管时,应先把胶头滴管伸入试剂瓶中,后用手指捏紧胶帽,赶出滴管中的空气
B.给试管中固体加热时,先预热,后集中加热
C.将玻璃管与橡胶管连接时,先用水将玻璃管润湿,后将玻璃管旋转伸入橡胶管
D.用托盘天平称量物质时,先加质量大的砝码,再加质量小的砝码
7.下列实验操作中,能达到实验目的的是()
A.向洗净的碎鸡蛋壳中加入食盐水可制得二氧化碳
B.用适量的水能区分氧化铜和二氧化锰
C.粗盐提纯实验中,蒸发结晶至有较多固体析出时停止加热
D.用pH试纸测定溶液酸碱度时,先将pH试纸用水湿润,然后再测定
8.分离下列混合物时,用到过滤操作的是( )
A.果汁和果渣 B.铁粉和铜粉 C.蔗糖和食盐 D.酒精和水
9.用足量的含不溶性固体杂质(其含量不详)的粗盐,经提纯后配制一定溶质质量分数的NaCl溶液,实验操作有①称取、②过滤、③蒸发结晶、④计算、⑤溶解、⑥干燥.其先后顺序正确的是( )
A.④、⑤、②、③、⑤、①、⑥ B.④、⑤、②、③、①、⑥、⑤
C.⑤、②、③、⑥、④、①、⑤ D.④、①、⑤、②、③、⑥、⑤
10.下列做法错误的是( )
A.用灼烧的方法区别棉花和羊毛
B.用润湿的pH试纸测白醋的pH
C.用水鉴别NH4NO3、NaOH、NaCl三种固体
D.按溶解、过滤、蒸发的主要操作顺序分离CaCl2、CaCO3的固体混合物
11.2015年3月20日联合国发布报告:到2030年,全球将有40%的国家和地区面临干旱问题.节约用水和合理开发利用水资源是每个公民应尽的责任和义务.下列关于水的认识正确的是( )
A.过滤能除去天然水中所有的杂质
B.将活性炭放入硬水中可使其软化
C.工业废水要经过处理后再排放
D.过量使用农药、化肥不会造成水体污染
12.下列观点错误的是( )
A.过滤是分离颗粒大小不同的混合物的方法
B.溶解就是溶质分子或离子通过自身不断运动分散到溶剂中的过程
C.物质都是由极其微小的粒子构成的,原子是构成物质的一种基本粒子
D.化学改变世界的途径是使物质发生化学变化,实现物质与能量的互相转化
二、填空题
13.给试管中的固体药品加热时,试管口应略 倾斜;给试管中的液体药品加热时液体的体积不得超过试管容积的 。给酒精灯里添加酒精时,酒精的量不能超过酒精灯容积的 ,熄灭酒精灯时 。
14.化学与生活息息相关。
(1)茶杯内的纱网可将茶叶与茶水分离,便于饮用。该方法利用的化学原理是 。
(2)自制净水器常加入 ,用于除去水中的异味和色素。
(3)漂白粉可用于自来水的杀菌、消毒,它的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙可发生如下反应:Ca(ClO)2+ X + H2O= CaCO3↓+ 2 HClO,则x的化学式为 ,HClO中Cl的化合价为 。
15.回答下列有关的问题
(1)硬水给人们的生活带来了许多麻烦,生活中常用 区分硬水和软水;生活中可通过 的方法使硬水软化。
(2)自来水厂常利用 的吸附性,除去水中的异味;
(3)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的 操作。
(4)“Cu”表示多种信息,如表示铜元素、金属铜单质,还能表示 。
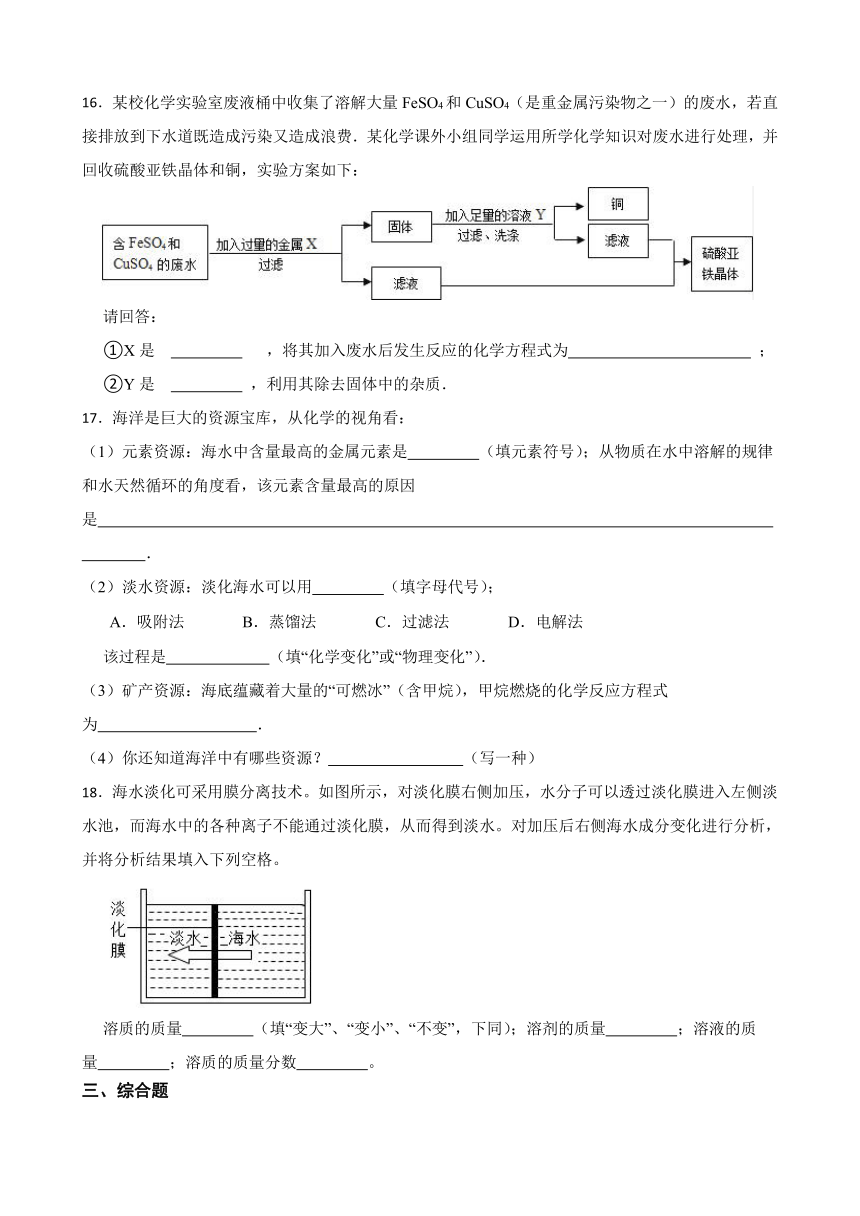
16.某校化学实验室废液桶中收集了溶解大量FeSO4和CuSO4(是重金属污染物之一)的废水,若直接排放到下水道既造成污染又造成浪费.某化学课外小组同学运用所学化学知识对废水进行处理,并回收硫酸亚铁晶体和铜,实验方案如下:
请回答:
①X是 ,将其加入废水后发生反应的化学方程式为 ;
②Y是 ,利用其除去固体中的杂质.
17.海洋是巨大的资源宝库,从化学的视角看:
(1)元素资源:海水中含量最高的金属元素是 (填元素符号);从物质在水中溶解的规律和水天然循环的角度看,该元素含量最高的原因是 .
(2)淡水资源:淡化海水可以用 (填字母代号);
A.吸附法 B.蒸馏法 C.过滤法 D.电解法
该过程是 (填“化学变化”或“物理变化”).
(3)矿产资源:海底蕴藏着大量的“可燃冰”(含甲烷),甲烷燃烧的化学反应方程式为 .
(4)你还知道海洋中有哪些资源? (写一种)
18.海水淡化可采用膜分离技术。如图所示,对淡化膜右侧加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,并将分析结果填入下列空格。
溶质的质量 (填“变大”、“变小”、“不变”,下同);溶剂的质量 ;溶液的质量 ;溶质的质量分数 。
三、综合题
19.尿素[CO(NH2)2]是农业上一种常用的氮肥。如图是以空气为原料生产尿素的流程图的一部分,请根据图示回答下列问题:
(1)NH3中氮的化合价为 ,从空气中分离出的氧气可用于 。
(2)写出合成塔①中发生反应的化学方程式: ,该反应的基本反应类型是 。
(3)合成塔②中发生反应的化学方程式是 ,X的化学式为 。
(4)农业上如果大量使用化肥,将会带来的环境问题是 (写一条即可)。
20.氯化钠是重要的化工原料,用于生产氢氧化钠、碳酸钠等,模拟流程如下。
(1)通过海水晒盐得到的粗盐中常含有NaCl、MgCl2、CaCl2等物质,“精制”过程中需要加入NaOH,目的是 。
(2)将饱和食盐水装入电解槽,可制得氢氧化钠,写出“电解槽”中发生反应的化学方程式: 。制得的氢氧化钠中常含有Na2CO3,原因是 (用化学方程式表示)。检验氢氧化钠样品中是否含有Na2CO3,下列试剂中可选择使用的是 (填序号)。
A.酚酞 B.稀盐酸 C.澄清石灰水
(3)将NH3、CO2先后通入饱和食盐水(氨气极易溶于水),可制得NaHCO3,进而获得Na2CO3.先通NH3后通CO2的原因是 。
21.请回答下面的问题:
(1)水和空气是人类宝贵的资源。从自来水中获得纯净的水,应采用的方法是 。从食盐水中分离得到食盐晶体的方法是 。除去泥水中的泥沙的方法是 。利用水可制得被称为“最清洁能源”的氢气,氢气燃烧的反应文字表达式是 ,该反应所属的基本反应类型为 。
(2)分离空气时,首先将空气加压降温成液态空气,然后逐渐升温。已知氧气的沸点是-183℃,氮气的沸点是-196℃,则在液态空气逐渐升温的过程中,最先逸出的是 。
22.氯化钠是生活中常见的盐。为除去粗盐水中的MgSO4、CaCl2杂质得到NaCl溶液,某化学小组设计如图方案。
(1)固体A的成分是 (填化学式)。
(2)溶液乙中应加入适量的 得到较纯净的NaCl溶液。
答案解析部分
1.【答案】C
2.【答案】B
3.【答案】A
4.【答案】A
5.【答案】D
6.【答案】A
7.【答案】C
8.【答案】A
9.【答案】C
10.【答案】B
11.【答案】C
12.【答案】B
13.【答案】向下;1/3;2/3;用灯帽盖灭
14.【答案】(1)过滤
(2)活性炭
(3)CO2;
15.【答案】(1)肥皂水;煮沸
(2)活性炭
(3)过滤
(4)1个铜原子
16.【答案】Fe;Fe+CuSO4═Cu+FeSO4;H2SO4
17.【答案】Na;含有钠元素的碱、盐都是易溶于水的,通过水的天然循环,土壤中的含有钠元素的物质随水进入海洋;B;物理变化;CH4+2O2CO2+2H2O ;海洋中含有溴
18.【答案】不变;变小;变小;变大
19.【答案】(1)-3;供给呼吸(答案合理即可)
(2);化合反应
(3)CO2
(4)水体污染(答案合理即可)
20.【答案】(1)除去氯化镁
(2);;BC
(3)先通入氨气是因为氨气在水中的溶解度非常大,在水中形成氨的水溶液,溶液的碱性比较强,易于吸收更多的二氧化碳,从而产生更多的纯碱。
21.【答案】(1)蒸馏;蒸发;过滤;氢气+氧气 水;化合反应
(2)氮气
22.【答案】(1)
(2)稀盐酸
一、单选题
1.下列有关蒸发过程描述正确的是( )
A.蒸发需要的玻璃仪器有烧杯、玻璃棒
B.结束实验后用手拿开蒸发皿
C.蒸发过程中要用玻璃棒不停地搅拌
D.等水分完全蒸干后再停止加热
2.下列实验问题处理方法正确的是( )
①高锰酸钾制氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
②在气体发生装置上直接点燃一氧化碳气体时,必须要先检验一氧化碳气体的纯度
③实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
④给试管中的液体加热时,不时移动试管,以免暴沸伤人
⑤使用滴瓶滴加试剂后,立即用蒸馏水洗净滴管并放回原瓶
A.①②③⑤ B.①②④
C.②③⑤ D.②④⑤
3.学习化学的目的并不在于要成为化学家,重要的是善于用化学知识去分析、解决生产生活中的问题。从化学的角度看,下列关于氧气的说法中正确的是( )
A.物质与氧气发生的反应属于氧化反应
B.鱼、虾等能在水中生存,是由于氧气易溶于水
C.氧气的化学性质很活泼,能跟所有物质反应
D.氧气可以支持燃烧,可以作燃料
4.化学实验必须按规范进行操作。如图所示的实验操作规范的是( )
A.贮存呼出的气体
B.吸取液体
C.塞紧橡胶塞
D.处理废弃固体药品
5.下列各组物质的鉴别和分离方法中错误的是( )
A.用肥皂水鉴别硬水和软水
B.用二氧化锰鉴别水和过氧化氢
C.用过滤的方法分离水和铁粉
D.用燃着的木条鉴别O2、CO2、N2三种气体
6.下列化学实验操作中,先后顺序错误的是()
A.使用胶头滴管时,应先把胶头滴管伸入试剂瓶中,后用手指捏紧胶帽,赶出滴管中的空气
B.给试管中固体加热时,先预热,后集中加热
C.将玻璃管与橡胶管连接时,先用水将玻璃管润湿,后将玻璃管旋转伸入橡胶管
D.用托盘天平称量物质时,先加质量大的砝码,再加质量小的砝码
7.下列实验操作中,能达到实验目的的是()
A.向洗净的碎鸡蛋壳中加入食盐水可制得二氧化碳
B.用适量的水能区分氧化铜和二氧化锰
C.粗盐提纯实验中,蒸发结晶至有较多固体析出时停止加热
D.用pH试纸测定溶液酸碱度时,先将pH试纸用水湿润,然后再测定
8.分离下列混合物时,用到过滤操作的是( )
A.果汁和果渣 B.铁粉和铜粉 C.蔗糖和食盐 D.酒精和水
9.用足量的含不溶性固体杂质(其含量不详)的粗盐,经提纯后配制一定溶质质量分数的NaCl溶液,实验操作有①称取、②过滤、③蒸发结晶、④计算、⑤溶解、⑥干燥.其先后顺序正确的是( )
A.④、⑤、②、③、⑤、①、⑥ B.④、⑤、②、③、①、⑥、⑤
C.⑤、②、③、⑥、④、①、⑤ D.④、①、⑤、②、③、⑥、⑤
10.下列做法错误的是( )
A.用灼烧的方法区别棉花和羊毛
B.用润湿的pH试纸测白醋的pH
C.用水鉴别NH4NO3、NaOH、NaCl三种固体
D.按溶解、过滤、蒸发的主要操作顺序分离CaCl2、CaCO3的固体混合物
11.2015年3月20日联合国发布报告:到2030年,全球将有40%的国家和地区面临干旱问题.节约用水和合理开发利用水资源是每个公民应尽的责任和义务.下列关于水的认识正确的是( )
A.过滤能除去天然水中所有的杂质
B.将活性炭放入硬水中可使其软化
C.工业废水要经过处理后再排放
D.过量使用农药、化肥不会造成水体污染
12.下列观点错误的是( )
A.过滤是分离颗粒大小不同的混合物的方法
B.溶解就是溶质分子或离子通过自身不断运动分散到溶剂中的过程
C.物质都是由极其微小的粒子构成的,原子是构成物质的一种基本粒子
D.化学改变世界的途径是使物质发生化学变化,实现物质与能量的互相转化
二、填空题
13.给试管中的固体药品加热时,试管口应略 倾斜;给试管中的液体药品加热时液体的体积不得超过试管容积的 。给酒精灯里添加酒精时,酒精的量不能超过酒精灯容积的 ,熄灭酒精灯时 。
14.化学与生活息息相关。
(1)茶杯内的纱网可将茶叶与茶水分离,便于饮用。该方法利用的化学原理是 。
(2)自制净水器常加入 ,用于除去水中的异味和色素。
(3)漂白粉可用于自来水的杀菌、消毒,它的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙可发生如下反应:Ca(ClO)2+ X + H2O= CaCO3↓+ 2 HClO,则x的化学式为 ,HClO中Cl的化合价为 。
15.回答下列有关的问题
(1)硬水给人们的生活带来了许多麻烦,生活中常用 区分硬水和软水;生活中可通过 的方法使硬水软化。
(2)自来水厂常利用 的吸附性,除去水中的异味;
(3)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的 操作。
(4)“Cu”表示多种信息,如表示铜元素、金属铜单质,还能表示 。
16.某校化学实验室废液桶中收集了溶解大量FeSO4和CuSO4(是重金属污染物之一)的废水,若直接排放到下水道既造成污染又造成浪费.某化学课外小组同学运用所学化学知识对废水进行处理,并回收硫酸亚铁晶体和铜,实验方案如下:
请回答:
①X是 ,将其加入废水后发生反应的化学方程式为 ;
②Y是 ,利用其除去固体中的杂质.
17.海洋是巨大的资源宝库,从化学的视角看:
(1)元素资源:海水中含量最高的金属元素是 (填元素符号);从物质在水中溶解的规律和水天然循环的角度看,该元素含量最高的原因是 .
(2)淡水资源:淡化海水可以用 (填字母代号);
A.吸附法 B.蒸馏法 C.过滤法 D.电解法
该过程是 (填“化学变化”或“物理变化”).
(3)矿产资源:海底蕴藏着大量的“可燃冰”(含甲烷),甲烷燃烧的化学反应方程式为 .
(4)你还知道海洋中有哪些资源? (写一种)
18.海水淡化可采用膜分离技术。如图所示,对淡化膜右侧加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,并将分析结果填入下列空格。
溶质的质量 (填“变大”、“变小”、“不变”,下同);溶剂的质量 ;溶液的质量 ;溶质的质量分数 。
三、综合题
19.尿素[CO(NH2)2]是农业上一种常用的氮肥。如图是以空气为原料生产尿素的流程图的一部分,请根据图示回答下列问题:
(1)NH3中氮的化合价为 ,从空气中分离出的氧气可用于 。
(2)写出合成塔①中发生反应的化学方程式: ,该反应的基本反应类型是 。
(3)合成塔②中发生反应的化学方程式是 ,X的化学式为 。
(4)农业上如果大量使用化肥,将会带来的环境问题是 (写一条即可)。
20.氯化钠是重要的化工原料,用于生产氢氧化钠、碳酸钠等,模拟流程如下。
(1)通过海水晒盐得到的粗盐中常含有NaCl、MgCl2、CaCl2等物质,“精制”过程中需要加入NaOH,目的是 。
(2)将饱和食盐水装入电解槽,可制得氢氧化钠,写出“电解槽”中发生反应的化学方程式: 。制得的氢氧化钠中常含有Na2CO3,原因是 (用化学方程式表示)。检验氢氧化钠样品中是否含有Na2CO3,下列试剂中可选择使用的是 (填序号)。
A.酚酞 B.稀盐酸 C.澄清石灰水
(3)将NH3、CO2先后通入饱和食盐水(氨气极易溶于水),可制得NaHCO3,进而获得Na2CO3.先通NH3后通CO2的原因是 。
21.请回答下面的问题:
(1)水和空气是人类宝贵的资源。从自来水中获得纯净的水,应采用的方法是 。从食盐水中分离得到食盐晶体的方法是 。除去泥水中的泥沙的方法是 。利用水可制得被称为“最清洁能源”的氢气,氢气燃烧的反应文字表达式是 ,该反应所属的基本反应类型为 。
(2)分离空气时,首先将空气加压降温成液态空气,然后逐渐升温。已知氧气的沸点是-183℃,氮气的沸点是-196℃,则在液态空气逐渐升温的过程中,最先逸出的是 。
22.氯化钠是生活中常见的盐。为除去粗盐水中的MgSO4、CaCl2杂质得到NaCl溶液,某化学小组设计如图方案。
(1)固体A的成分是 (填化学式)。
(2)溶液乙中应加入适量的 得到较纯净的NaCl溶液。
答案解析部分
1.【答案】C
2.【答案】B
3.【答案】A
4.【答案】A
5.【答案】D
6.【答案】A
7.【答案】C
8.【答案】A
9.【答案】C
10.【答案】B
11.【答案】C
12.【答案】B
13.【答案】向下;1/3;2/3;用灯帽盖灭
14.【答案】(1)过滤
(2)活性炭
(3)CO2;
15.【答案】(1)肥皂水;煮沸
(2)活性炭
(3)过滤
(4)1个铜原子
16.【答案】Fe;Fe+CuSO4═Cu+FeSO4;H2SO4
17.【答案】Na;含有钠元素的碱、盐都是易溶于水的,通过水的天然循环,土壤中的含有钠元素的物质随水进入海洋;B;物理变化;CH4+2O2CO2+2H2O ;海洋中含有溴
18.【答案】不变;变小;变小;变大
19.【答案】(1)-3;供给呼吸(答案合理即可)
(2);化合反应
(3)CO2
(4)水体污染(答案合理即可)
20.【答案】(1)除去氯化镁
(2);;BC
(3)先通入氨气是因为氨气在水中的溶解度非常大,在水中形成氨的水溶液,溶液的碱性比较强,易于吸收更多的二氧化碳,从而产生更多的纯碱。
21.【答案】(1)蒸馏;蒸发;过滤;氢气+氧气 水;化合反应
(2)氮气
22.【答案】(1)
(2)稀盐酸
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
