7.2 物质溶解的量 同步练习 2022-2023学年科粤版九年级下册化学(word 含答案)
文档属性
| 名称 | 7.2 物质溶解的量 同步练习 2022-2023学年科粤版九年级下册化学(word 含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 147.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-02 00:00:00 | ||
图片预览




文档简介
7.2 物质溶解的量 同步练习
一、单选题
1.运用分类思想认识物质,下列说法正确的是( )
A.柠檬酸、碳酸均属于酸,它们都能使石蕊溶液变红
B.氮气、氢气均属于非金属单质,它们都能在氧气中燃烧
C.氧化钙、氧化铝均属于金属氧化物,它们都易溶解于水
D.硝酸铵、氯化铵均属于铵盐,它们都能跟碱性肥料混合使用
2.下列关于气体性质的描述,错误的是( )
A.通常状况下,氧气是无色、无味的气体
B.氮气在低温、高压时能变为液体或固体
C.氧气极易溶于水
D.稀有气体是化学性质不活泼的气体
3.硝酸钾和氯化钠的溶解度曲线如下图所示。30℃时,分别将30g硝酸钾和氯化钠放入100 g水中,充分溶解。下列结论中,错误的是( )
A.两种溶液中溶质的质量分数相等
B.通常情况下,采取降温的方法能将两种溶液都变成饱和溶液
C.若将硝酸钾溶液降温到20℃,溶液中溶质和溶剂的质量比为3∶10
D.若将硝酸钾溶液变为10℃时的饱和溶液,溶液中溶质的质量分数一定减小
4.会发生结晶现象的溶液是( )
A.一定是浓溶液 B.一定是稀溶液
C.一定是饱和溶液 D.无法确定
5.如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
A.甲物质的溶解度一定大于乙物质的溶解度
B.t2℃时,甲、乙饱和溶液的溶质质量分数相等
C.将甲溶液从t2℃时降温到t1℃时,一定有晶体析出
D.将t2℃时乙的饱和溶液变为不饱和溶液,可采取降温的方法
6.20℃时,往50g KNO3溶液中加入5g KNO3晶体,充分搅拌后部分晶体未溶解,稍加热后,晶体全部溶解,下列说法正确的是( )
A.搅拌后加热前一定是不饱和溶液
B.搅拌后加热前一定是饱和溶液
C.加热后一定是饱和溶液
D.加热后一定是不饱和溶液
7.运用推理、归纳、类比等的方法得出下列结论,其中合理的是( )
A.化学变化常伴随着发光、放热、变色、沉淀、气体等,所以有这些现象发生一定是化学变化。
B.同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率
C.氧气可以使带火星的木条复燃,所以不能使带火星木条复燃一定不含氧气
D.化学变化中一定发生物理变化,物理变化中也一定有化学变化
8.下列有关叙述正确的是( )
A.有机物都是含碳元素的化合物,则含碳元素的化合物一定是有机物
B.保持温度一定,往氢氧化钙饱和溶液中加氧化钙,溶质、溶液的质量一定减少
C.某物质在空气中燃烧生成二氧化碳和水,说明该物质含碳、氢、氧三种元素
D.酸溶液一定显酸性,则显酸性的溶液一定是酸溶液
9.如图是M、N两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是( )
A.图中A点表示两种物质在t℃时溶解度相等
B.M中含有少量N,通常采用降温结晶的方法提纯M
C.t1℃时分别将M、N饱和溶液升温到t2℃,所得溶液的溶质质量分数相等
D.t1℃时,M溶液恒温蒸发10g水析出1g晶体,再恒温蒸发20g水析出2g晶体
10.X,Y两种固体物质的溶解度曲线如右图所示。下列说法正确的是( )
A.两种物质的溶解度X > Y
B.t2℃时,两种物质的饱和溶液中溶质的质量分数X > Y
C.将t2℃时X的饱和溶液降温至t1℃,溶质质量不变
D.将t1℃时Y的饱和溶液升温至t2℃,溶质的质量分数增大
11.下面是小华同学化学笔记中的记录,你认为错误的是()
A.在一定温度下,向溶液中加入溶质一定会使其溶质的质量分数增大
B.pH大于7的溶液一定是碱性溶液
C.盐中不一定含有金属元素
D.化学反应不一定能观察到明显的现象
12.a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
A.15℃时,a、b 的溶解度均为20g
B.加水或升温均可使b的饱和溶液变为不饱和溶液
C.将 30℃时a的饱和溶液降温至15℃,溶质的质量分数不变
D.20℃时分别向100g 水中加入20ga和 b,升温至30℃,所得溶液均为饱和溶液
二、填空题
13.1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:①NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl;②2NaHCO3Na2CO3+H2O+CO2↑;
试回答下列问题:
(1)在反应①的六种物质中,焙制糕点是时常用作发酵粉的是 ;
(2)胺盐水比食盐水更容易吸收二氧化碳的原因是 .
(3)氯化钠和碳酸钠的溶解度如图2,t2℃时,氯化钠饱和溶液溶质的质量分数 碳酸钠饱和溶液溶质的质量分数
(填“大于”“小于”“等于”之一).
(4)生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,说明这句谚语的原理: .
14.认识溶液的变化。
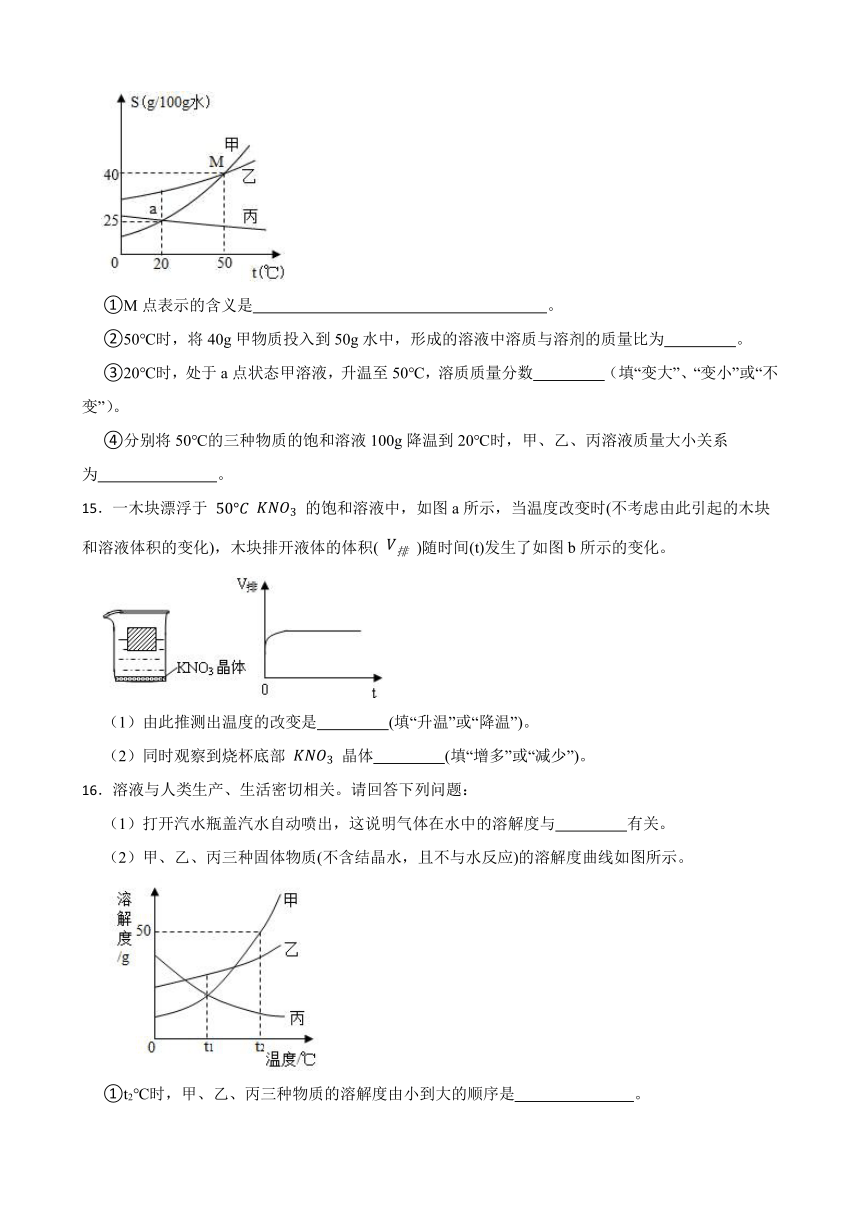
根据如图甲、乙、丙三种固体的溶解度曲线回答:
①M点表示的含义是 。
②50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为 。
③20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数 (填“变大”、“变小”或“不变”)。
④分别将50℃的三种物质的饱和溶液100g降温到20℃时,甲、乙、丙溶液质量大小关系为 。
15.一木块漂浮于 的饱和溶液中,如图a所示,当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积( )随时间(t)发生了如图b所示的变化。
(1)由此推测出温度的改变是 (填“升温”或“降温”)。
(2)同时观察到烧杯底部 晶体 (填“增多”或“减少”)。
16.溶液与人类生产、生活密切相关。请回答下列问题:
(1)打开汽水瓶盖汽水自动喷出,这说明气体在水中的溶解度与 有关。
(2)甲、乙、丙三种固体物质(不含结晶水,且不与水反应)的溶解度曲线如图所示。
①t2℃时,甲、乙、丙三种物质的溶解度由小到大的顺序是 。
②t2℃时,把50g甲放入50g水中能得到甲的饱和溶液,其中溶质与溶液的质量比为 。
③将丙的饱和溶液变为不饱和溶液,若保持溶液质量不变,可以采用 方法。
④t2℃时,甲、乙、丙三种物质的饱和溶液降温至t1℃时,这三种溶液的溶质质量分数由大到小的是 。
17.A、B、C三种固体物质的溶解度曲线如图所示,请回答:当A中混有少量B时,可采用 方法提纯A物质。t2℃时,将75 g A的饱和溶液稀释为20%的溶液,需加水的质量为 g。t2℃时,将A、B、C三种物质的饱和溶液降温至t1 ℃,所得溶液溶质的质量分数由大到小的顺序为 。
18.20℃时,氯化钠的溶解度是36g,其含义是 .其饱和溶液中溶质,溶剂,溶液的质量比是 .
三、综合题
19.根据问题填空:
(1)从溶解度曲线可以看出,大多数固体物质的溶解度随温度的升高而 ,少数固体物质的溶解度受温度的变化影响 ,极少数固体物质的溶解度随温度的升高而 。
(2)在溶质和溶剂一定的情况下, 是影响固体溶解度的重要因素。
20.在中华民族五千年的文明史上,有许多熠熠生辉的化学家,他们为推动化学的发展作出了重要贡献,取得的一系列成就在国际上也产生了重要影响。
(1)西汉刘安所著的《淮南万毕术》中记载着“曾青得铁,则化为铜”,把铁放入硫酸铜溶液中会得到铜,这一发现要比西方国家早1700多年,是湿法冶金的先驱。该反应的化学方程式为 。
(2)北宋沈括被誉为“中国整部科学史中最卓越的人物”,他所著的《梦溪笔谈》中第一次提到了“石油”这一名称,文中关于石油制品“必大行于世”的科学预见,如今读来令人叹服。石油分馏、裂解出的汽油、柴油可作为燃料,燃料燃烧的过程是将 能转化为热能。时至今日,氢气作为新能源与传统化石燃料相比,其优点是 。(写一点即可)。
(3)我国近代化学家侯德榜创立的侯氏制碱法,对化肥和制碱工业做出了杰出贡献,将制碱厂、合成氨厂、石灰厂联合起来,降低成本,极大提高了利用率。Na2CO3和NaCl的溶解度曲线如图所示。请回答下列问题:
①t1℃时,Na2CO3饱和溶液的溶质质量分数 NaCl饱和溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一)。
②t2℃时,把30gNa2CO3放入盛有100g水的烧杯中,用玻璃棒充分搅拌后,然后降温至t1℃,此时所得溶液中溶质与溶剂的质量之比为 (填最简整数比)。
③Na2CO3饱和溶液中混有少量的NaCl杂质,想要提纯Na2CO3可采用的方法是 (填“蒸发结晶”“降温结晶”之一)。
21.如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)A点的含义是 。
(2)20℃甲,乙,丙三种物质溶解度关系由小到大是 。
(3)在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液质量为 。
(4)若甲中混有少量乙,最好采用 的方法提纯甲(填“降温结晶”或“蒸发结晶”)。
(5)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数最小的物质是 。
22.化学兴趣小组对t℃的某固体物质的溶液在恒温条件下蒸发,实验记录如图所示,请回答下列问题:
(1)溶液甲~丁中,属于饱和溶液的是 (填序号)。
(2)该固体物质在t℃时的溶解度为 g。
(3)溶液甲、乙、丙、丁中,溶质质量分数的大小关系是 。
(4)给溶液丁升高温度时,固体逐渐消失,说明该物质的溶解度曲线可能是上图中的 (选填“A”或“B”)。
答案解析部分
1.【答案】A
2.【答案】C
3.【答案】B
4.【答案】C
5.【答案】B
6.【答案】B
7.【答案】B
8.【答案】B
9.【答案】D
10.【答案】B
11.【答案】A
12.【答案】D
13.【答案】碳酸氢钠 ;氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳;小于;氯化钠的溶解度随湿度变化不大,由于夏天气温高,水分蒸发快,氯化钠易结晶斩出;纯碱的溶解度随温度的变化大,冬天气温很低,使碳酸钠结晶析出
14.【答案】在50℃时,甲、乙物质的溶解度相等;2:5;不变;丙>乙>甲
15.【答案】(1)降温
(2)增多
16.【答案】(1)压强
(2)甲>乙>丙;1:3;降温;乙>甲>丙
17.【答案】降温结晶(或冷却热饱和溶液);50;B>A>C
18.【答案】20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态;9:25:34
19.【答案】(1)增大;很小;减小
(2)温度
20.【答案】(1)
(2)化学;燃烧产物是水,无污染
(3)小于;9∶50;降温结晶
21.【答案】(1)20℃时,甲、乙两种物质的溶解度相等
(2)甲=乙>丙
(3)72.5g
(4)降温结晶
(5)丙
22.【答案】(1)丙、丁
(2)30
(3)丙=丁>乙>甲
(4)A
一、单选题
1.运用分类思想认识物质,下列说法正确的是( )
A.柠檬酸、碳酸均属于酸,它们都能使石蕊溶液变红
B.氮气、氢气均属于非金属单质,它们都能在氧气中燃烧
C.氧化钙、氧化铝均属于金属氧化物,它们都易溶解于水
D.硝酸铵、氯化铵均属于铵盐,它们都能跟碱性肥料混合使用
2.下列关于气体性质的描述,错误的是( )
A.通常状况下,氧气是无色、无味的气体
B.氮气在低温、高压时能变为液体或固体
C.氧气极易溶于水
D.稀有气体是化学性质不活泼的气体
3.硝酸钾和氯化钠的溶解度曲线如下图所示。30℃时,分别将30g硝酸钾和氯化钠放入100 g水中,充分溶解。下列结论中,错误的是( )
A.两种溶液中溶质的质量分数相等
B.通常情况下,采取降温的方法能将两种溶液都变成饱和溶液
C.若将硝酸钾溶液降温到20℃,溶液中溶质和溶剂的质量比为3∶10
D.若将硝酸钾溶液变为10℃时的饱和溶液,溶液中溶质的质量分数一定减小
4.会发生结晶现象的溶液是( )
A.一定是浓溶液 B.一定是稀溶液
C.一定是饱和溶液 D.无法确定
5.如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
A.甲物质的溶解度一定大于乙物质的溶解度
B.t2℃时,甲、乙饱和溶液的溶质质量分数相等
C.将甲溶液从t2℃时降温到t1℃时,一定有晶体析出
D.将t2℃时乙的饱和溶液变为不饱和溶液,可采取降温的方法
6.20℃时,往50g KNO3溶液中加入5g KNO3晶体,充分搅拌后部分晶体未溶解,稍加热后,晶体全部溶解,下列说法正确的是( )
A.搅拌后加热前一定是不饱和溶液
B.搅拌后加热前一定是饱和溶液
C.加热后一定是饱和溶液
D.加热后一定是不饱和溶液
7.运用推理、归纳、类比等的方法得出下列结论,其中合理的是( )
A.化学变化常伴随着发光、放热、变色、沉淀、气体等,所以有这些现象发生一定是化学变化。
B.同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率
C.氧气可以使带火星的木条复燃,所以不能使带火星木条复燃一定不含氧气
D.化学变化中一定发生物理变化,物理变化中也一定有化学变化
8.下列有关叙述正确的是( )
A.有机物都是含碳元素的化合物,则含碳元素的化合物一定是有机物
B.保持温度一定,往氢氧化钙饱和溶液中加氧化钙,溶质、溶液的质量一定减少
C.某物质在空气中燃烧生成二氧化碳和水,说明该物质含碳、氢、氧三种元素
D.酸溶液一定显酸性,则显酸性的溶液一定是酸溶液
9.如图是M、N两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是( )
A.图中A点表示两种物质在t℃时溶解度相等
B.M中含有少量N,通常采用降温结晶的方法提纯M
C.t1℃时分别将M、N饱和溶液升温到t2℃,所得溶液的溶质质量分数相等
D.t1℃时,M溶液恒温蒸发10g水析出1g晶体,再恒温蒸发20g水析出2g晶体
10.X,Y两种固体物质的溶解度曲线如右图所示。下列说法正确的是( )
A.两种物质的溶解度X > Y
B.t2℃时,两种物质的饱和溶液中溶质的质量分数X > Y
C.将t2℃时X的饱和溶液降温至t1℃,溶质质量不变
D.将t1℃时Y的饱和溶液升温至t2℃,溶质的质量分数增大
11.下面是小华同学化学笔记中的记录,你认为错误的是()
A.在一定温度下,向溶液中加入溶质一定会使其溶质的质量分数增大
B.pH大于7的溶液一定是碱性溶液
C.盐中不一定含有金属元素
D.化学反应不一定能观察到明显的现象
12.a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
A.15℃时,a、b 的溶解度均为20g
B.加水或升温均可使b的饱和溶液变为不饱和溶液
C.将 30℃时a的饱和溶液降温至15℃,溶质的质量分数不变
D.20℃时分别向100g 水中加入20ga和 b,升温至30℃,所得溶液均为饱和溶液
二、填空题
13.1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:①NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl;②2NaHCO3Na2CO3+H2O+CO2↑;
试回答下列问题:
(1)在反应①的六种物质中,焙制糕点是时常用作发酵粉的是 ;
(2)胺盐水比食盐水更容易吸收二氧化碳的原因是 .
(3)氯化钠和碳酸钠的溶解度如图2,t2℃时,氯化钠饱和溶液溶质的质量分数 碳酸钠饱和溶液溶质的质量分数
(填“大于”“小于”“等于”之一).
(4)生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,说明这句谚语的原理: .
14.认识溶液的变化。
根据如图甲、乙、丙三种固体的溶解度曲线回答:
①M点表示的含义是 。
②50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为 。
③20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数 (填“变大”、“变小”或“不变”)。
④分别将50℃的三种物质的饱和溶液100g降温到20℃时,甲、乙、丙溶液质量大小关系为 。
15.一木块漂浮于 的饱和溶液中,如图a所示,当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积( )随时间(t)发生了如图b所示的变化。
(1)由此推测出温度的改变是 (填“升温”或“降温”)。
(2)同时观察到烧杯底部 晶体 (填“增多”或“减少”)。
16.溶液与人类生产、生活密切相关。请回答下列问题:
(1)打开汽水瓶盖汽水自动喷出,这说明气体在水中的溶解度与 有关。
(2)甲、乙、丙三种固体物质(不含结晶水,且不与水反应)的溶解度曲线如图所示。
①t2℃时,甲、乙、丙三种物质的溶解度由小到大的顺序是 。
②t2℃时,把50g甲放入50g水中能得到甲的饱和溶液,其中溶质与溶液的质量比为 。
③将丙的饱和溶液变为不饱和溶液,若保持溶液质量不变,可以采用 方法。
④t2℃时,甲、乙、丙三种物质的饱和溶液降温至t1℃时,这三种溶液的溶质质量分数由大到小的是 。
17.A、B、C三种固体物质的溶解度曲线如图所示,请回答:当A中混有少量B时,可采用 方法提纯A物质。t2℃时,将75 g A的饱和溶液稀释为20%的溶液,需加水的质量为 g。t2℃时,将A、B、C三种物质的饱和溶液降温至t1 ℃,所得溶液溶质的质量分数由大到小的顺序为 。
18.20℃时,氯化钠的溶解度是36g,其含义是 .其饱和溶液中溶质,溶剂,溶液的质量比是 .
三、综合题
19.根据问题填空:
(1)从溶解度曲线可以看出,大多数固体物质的溶解度随温度的升高而 ,少数固体物质的溶解度受温度的变化影响 ,极少数固体物质的溶解度随温度的升高而 。
(2)在溶质和溶剂一定的情况下, 是影响固体溶解度的重要因素。
20.在中华民族五千年的文明史上,有许多熠熠生辉的化学家,他们为推动化学的发展作出了重要贡献,取得的一系列成就在国际上也产生了重要影响。
(1)西汉刘安所著的《淮南万毕术》中记载着“曾青得铁,则化为铜”,把铁放入硫酸铜溶液中会得到铜,这一发现要比西方国家早1700多年,是湿法冶金的先驱。该反应的化学方程式为 。
(2)北宋沈括被誉为“中国整部科学史中最卓越的人物”,他所著的《梦溪笔谈》中第一次提到了“石油”这一名称,文中关于石油制品“必大行于世”的科学预见,如今读来令人叹服。石油分馏、裂解出的汽油、柴油可作为燃料,燃料燃烧的过程是将 能转化为热能。时至今日,氢气作为新能源与传统化石燃料相比,其优点是 。(写一点即可)。
(3)我国近代化学家侯德榜创立的侯氏制碱法,对化肥和制碱工业做出了杰出贡献,将制碱厂、合成氨厂、石灰厂联合起来,降低成本,极大提高了利用率。Na2CO3和NaCl的溶解度曲线如图所示。请回答下列问题:
①t1℃时,Na2CO3饱和溶液的溶质质量分数 NaCl饱和溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一)。
②t2℃时,把30gNa2CO3放入盛有100g水的烧杯中,用玻璃棒充分搅拌后,然后降温至t1℃,此时所得溶液中溶质与溶剂的质量之比为 (填最简整数比)。
③Na2CO3饱和溶液中混有少量的NaCl杂质,想要提纯Na2CO3可采用的方法是 (填“蒸发结晶”“降温结晶”之一)。
21.如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)A点的含义是 。
(2)20℃甲,乙,丙三种物质溶解度关系由小到大是 。
(3)在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液质量为 。
(4)若甲中混有少量乙,最好采用 的方法提纯甲(填“降温结晶”或“蒸发结晶”)。
(5)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数最小的物质是 。
22.化学兴趣小组对t℃的某固体物质的溶液在恒温条件下蒸发,实验记录如图所示,请回答下列问题:
(1)溶液甲~丁中,属于饱和溶液的是 (填序号)。
(2)该固体物质在t℃时的溶解度为 g。
(3)溶液甲、乙、丙、丁中,溶质质量分数的大小关系是 。
(4)给溶液丁升高温度时,固体逐渐消失,说明该物质的溶解度曲线可能是上图中的 (选填“A”或“B”)。
答案解析部分
1.【答案】A
2.【答案】C
3.【答案】B
4.【答案】C
5.【答案】B
6.【答案】B
7.【答案】B
8.【答案】B
9.【答案】D
10.【答案】B
11.【答案】A
12.【答案】D
13.【答案】碳酸氢钠 ;氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳;小于;氯化钠的溶解度随湿度变化不大,由于夏天气温高,水分蒸发快,氯化钠易结晶斩出;纯碱的溶解度随温度的变化大,冬天气温很低,使碳酸钠结晶析出
14.【答案】在50℃时,甲、乙物质的溶解度相等;2:5;不变;丙>乙>甲
15.【答案】(1)降温
(2)增多
16.【答案】(1)压强
(2)甲>乙>丙;1:3;降温;乙>甲>丙
17.【答案】降温结晶(或冷却热饱和溶液);50;B>A>C
18.【答案】20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态;9:25:34
19.【答案】(1)增大;很小;减小
(2)温度
20.【答案】(1)
(2)化学;燃烧产物是水,无污染
(3)小于;9∶50;降温结晶
21.【答案】(1)20℃时,甲、乙两种物质的溶解度相等
(2)甲=乙>丙
(3)72.5g
(4)降温结晶
(5)丙
22.【答案】(1)丙、丁
(2)30
(3)丙=丁>乙>甲
(4)A
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
