2.3 溶液的酸碱性 同步练习(含答案) 2022-2023学年鲁教版(五四制)九年级全册化学
文档属性
| 名称 | 2.3 溶液的酸碱性 同步练习(含答案) 2022-2023学年鲁教版(五四制)九年级全册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 61.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-02 00:00:00 | ||
图片预览



文档简介
2.3 溶液的酸碱性 同步练习
一、单选题
1.下列各组离子能在pH=10的溶液中大量共存的是( )
A.Na+,Mg2+,CO32﹣ B.H+,Cu2+,NO3﹣
C.NH4+,Fe3+,SO42﹣ D.K+,Ba2+,Cl﹣
2.下列仪器属于玻璃仪器,可直接加热的是( )
A.烧杯 B.蒸发皿 C.试管 D.锥形瓶
3.某化学兴趣小组探究稀盐酸和氢氧化钠溶液的反应过程。测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )
A.该pH变化过程可以证明酸和碱发生了化学反应
B.图中a点所示溶液中,含有的溶质是氯化钠和氯化氢
C.向图中c点所示溶液中滴加紫色石蕊,溶液变为红色
D.该实验是将氢氧化钠逐滴滴入到盛有盐酸溶液的烧杯中
4.下列说法正确的是( )
A.由不同种元素组成的物质一定是混合物
B.金属与酸溶液发生置换反应,溶液的质量一定增加
C.某无色溶液中滴入酚酞试液显红色,该溶液一定是碱溶液
D.某物质能与碱反应生成盐和水,则该物质一定是酸
5.下列各组混合物中加入无色酚酞溶液后,一定有明显现象是( )
A.氢氧化钙溶液、硫酸铜溶液 B.稀盐酸、氯化钠溶液
C.水、氧化钙 D.氢氧化钠溶液、稀硫酸
6.如图是X、Y、Z三种液体的对应近似pH,下列判断错误的是( )
A.X显酸性 B.Y一定是水
C.Z可能是碳酸钠溶液 D.Z可使紫色石蕊试液变蓝
7.下列化学反应都有重要的应用。其中属于中和反应的是( )
A.配制波尔多液 B.稀盐酸除铁锈
C.含小苏打的胃药治疗胃酸过多 D.氨水处理含硫酸的工业废水
8.如图是生活中一些物质的pH,下列说法正确的是( )
A.西瓜汁呈碱性
B.上述呈酸性的物质中酱油的酸性最强
C.肥皂水能使无色酚酞溶液变红
D.玉米粥的碱性比牙膏的碱性强
9.做中和反应实验时,向5mL氢氧化钠溶液中滴几滴酚酞溶液,然后再逐滴加入稀盐酸,有关分析正确的是( )
A. B.
C. D.
10.向pH=1的溶液中,滴加1~2滴紫色石蕊试液,溶液呈( )
A.红色 B.蓝色 C.紫色 D.无色
11.关于水的净化过程描述错误的是( )
A.通过过滤装置除去可溶性杂质 B.通入氯气杀菌消毒
C.加入明矾使不溶性悬浮物凝聚 D.通过活性炭吸附部分有害物质
12.小明对部分实验现象记录如下,其中错误的是( )
A.二氧化硫气体通入高锰酸钾溶液,红色褪去
B.红磷在空气中燃烧产生大量白色烟雾
C.铜片在空气中加热生成黑色固体
D.向碳酸钠溶液中滴加酚酞试液,酚酞试液变红
二、填空题
13.用量筒量液体时,量筒必须 ,视线要与量筒内液体的 保持水平.
14.我省素有“红土地”之称,红土壤偏酸性。下列农作物适宜在红土壤中种植的是 。
农作物 马铃薯 甘草 茶树 橘子 桑树
最适合生长的pH范围 5.5~6.0 7.2~8.5 5.0~5.5 5.5~6.5 7.0~8.0
A
甘草 B 橘子 C 桑树 D
15.在5mL氢氧化钠溶液中滴加2滴酚酞试液,溶液呈 色,再加入5mL稀盐酸,得到无色溶液,则无色溶液一定是 。
Ⅰ.
pH≤7 Ⅱ. pH=7 Ⅲ. pH <7 Ⅳ. pH>7
将无色溶液蒸发至干,看到的现象是 。
若将40克10%氢氧化钠溶液和足量稀盐酸反应,计算生成氯化钠的物质的量。(根据化学方程式计算)
16.柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医疗等行业,柠檬酸中碳元素的质量分数为 ,将紫色石蕊溶液滴加到柠檬酸中,溶液变红色,说明柠檬酸的pH值 7(填“>”“=”或“<”)
17.将X溶液滴入Y溶液中,在滴加过程中,Y溶液的pH值变化情况如图所示.
溶液 A B C D
X 盐酸 氢氧化钠 盐酸 氢氧化钠
Y 水 水 氢氧化钠 盐酸
(1)表格中符合这种变化情况的是 (填写编号),理由是: .
(2)写出该反应的化学方程式 .
(3)在Y溶液中滴入石蕊试液,若不断滴入X溶液,石蕊颜色的变化是 .
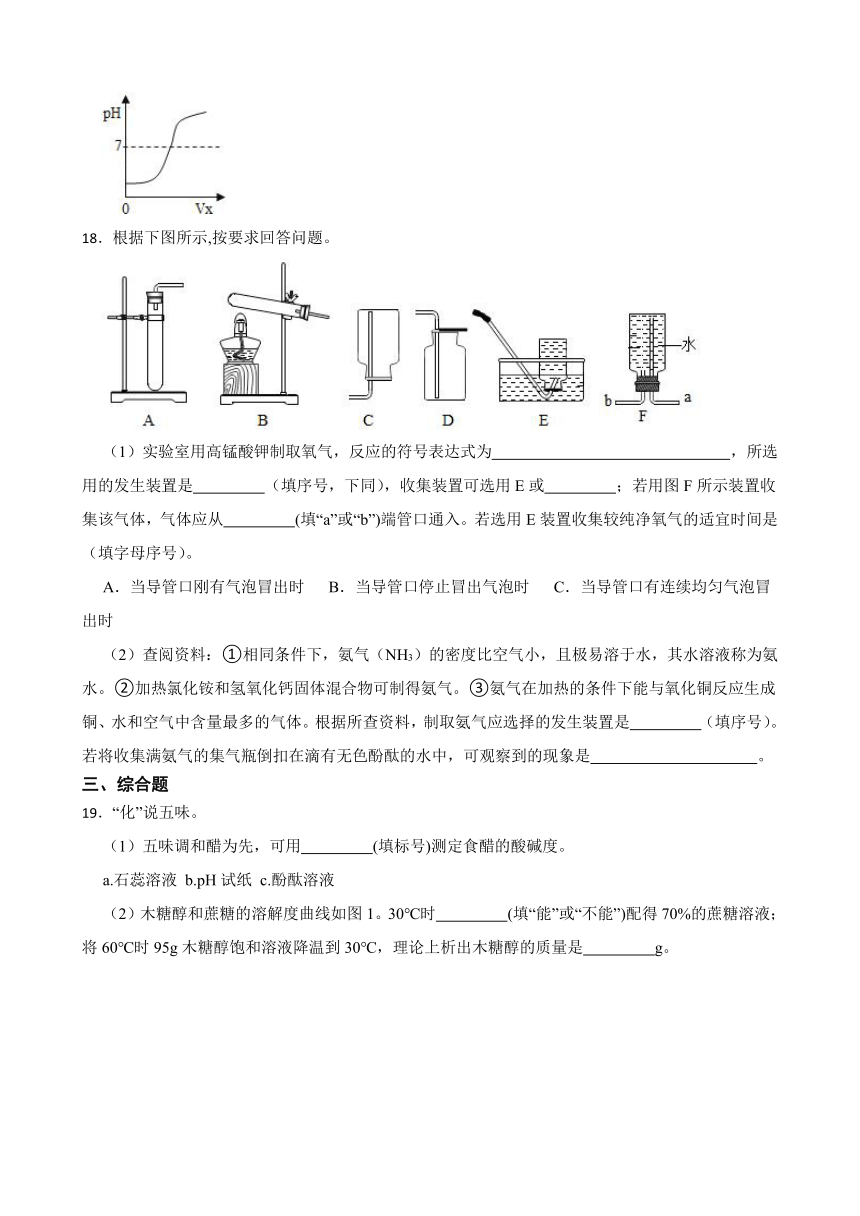
18.根据下图所示,按要求回答问题。
(1)实验室用高锰酸钾制取氧气,反应的符号表达式为 ,所选用的发生装置是 (填序号,下同),收集装置可选用E或 ;若用图F所示装置收集该气体,气体应从 (填“a”或“b”)端管口通入。若选用E装置收集较纯净氧气的适宜时间是 (填字母序号)。
A.当导管口刚有气泡冒出时 B.当导管口停止冒出气泡时 C.当导管口有连续均匀气泡冒出时
(2)查阅资料:①相同条件下,氨气(NH3)的密度比空气小,且极易溶于水,其水溶液称为氨水。②加热氯化铵和氢氧化钙固体混合物可制得氨气。③氨气在加热的条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。根据所查资料,制取氨气应选择的发生装置是 (填序号)。若将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,可观察到的现象是 。
三、综合题
19.“化”说五味。
(1)五味调和醋为先,可用 (填标号)测定食醋的酸碱度。
a.石蕊溶液 b.pH试纸 c.酚酞溶液
(2)木糖醇和蔗糖的溶解度曲线如图1。30℃时 (填“能”或“不能”)配得70%的蔗糖溶液;将60℃时95g木糖醇饱和溶液降温到30℃,理论上析出木糖醇的质量是 g。
(3)硬水有苦涩味,将其通过阳离子交换柱后可转化成软水(如图2,阴离子未画出),交换后的水仍然呈电中性。1个Ca2+可以交换出 个Na+,家庭中软化硬水的方法有 。
(4)每100g某辣椒中主要营养成分数据如下表:
营养成分 维生素C 蛋白质 脂肪 糖类 钙 铁 水
质量 171mg 1.9g 0.3g 11.6g 20mg 1.2mg 85.5g
辣椒中含量最高的营养素是 ;摄入适量 (填元素符号)可预防骨质疏松。
(5)向10g9%的氯化钠溶液中加入 g水,可稀释为0.9%的生理盐水。
20.向氢氧化钠溶液中逐滴加入盐酸,溶液pH的变化如图所示。
(1)请写出有关反应的化学方程式 。
(2)小山同学向b点溶液中滴加紫色石蕊溶液,溶液呈红色,则使石蕊溶液变红的离子是 。
21.化学源于生活,生活中很多现象蕴含着化学知识,请你填空:
(1)春天小明同学来到了邕江河边,发现河水清澈透明,如果要测定该河水的酸碱度,应选用 .(填字母号)
A,石蕊试液 B,酚酞试液 C,pH试纸
(2)医生建议胃酸过多病人须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
抗胃酸药 复方氢氧化镁片剂 铝碳酸镁片
有效成分 Mg(OH)2 AlMg(OH)3CO3
构成微粒 Mg2+、OH﹣ Al3+、Mg2+、OH﹣、CO32﹣
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异.
①Mg(OH)2起抗酸作用的微粒是 (填微粒符号,下同).该药物和盐酸反应叫 反应.
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl=MgCl2+AlCl3+4H2O+CO2↑.铝碳酸镁起抗酸作用的两种微粒是 .
22.水是生命之源,请回答下列有关水的问题:
(1)水发生部分结冰变化后形成的冰和水混合体系属于 (选填“纯净物”或“混合物”)。
(2)若要测定某工业水样的酸碱度,最适宜的是____。
A.无色酚酞试液 B.pH试纸 C.紫色石蕊试液
(3)把下列物质分别加入纯净水中,用玻璃棒不断搅拌,能形成无色溶液的是____。
A.泥沙 B.无水硫酸铜 C.氯化钠 D.花生油
答案解析部分
1.【答案】D
2.【答案】C
3.【答案】C
4.【答案】B
5.【答案】C
6.【答案】B
7.【答案】D
8.【答案】C
9.【答案】A
10.【答案】A
11.【答案】A
12.【答案】B
13.【答案】放平;凹液面的最低处
14.【答案】B;马铃薯或茶树
15.【答案】红;Ⅰ;白色固体;解:设NaCl的物质的量为x 40×10%/40=0.1mol
NaOH+HCl= NaCl + H2O
1 1
0.1mol x
1/0.1 = 1/x x=0.1mol 答:生成氯化钠的物质的量为0.1mol
16.【答案】37.5%;<
17.【答案】D;开始时Y溶液的pH<7,一定是盐酸,滴加X溶液时,混合溶液pH由小变大,直到pH>7,只能是加pH>7的溶液,即加NaOH溶液;NaOH+HCl=NaCl+H2O;红色逐渐变为紫色,再变为蓝色
18.【答案】(1);B;D;a;C
(2)B;无色酚酞溶液变红
19.【答案】(1)b
(2)不能;10
(3)2;煮沸
(4)水;Ca
(5)90
20.【答案】(1)
(2)H+或氢离子
21.【答案】(1)C
(2)①OH﹣;中和;OH﹣、CO32﹣
22.【答案】(1)纯净物
(2)B
(3)C
一、单选题
1.下列各组离子能在pH=10的溶液中大量共存的是( )
A.Na+,Mg2+,CO32﹣ B.H+,Cu2+,NO3﹣
C.NH4+,Fe3+,SO42﹣ D.K+,Ba2+,Cl﹣
2.下列仪器属于玻璃仪器,可直接加热的是( )
A.烧杯 B.蒸发皿 C.试管 D.锥形瓶
3.某化学兴趣小组探究稀盐酸和氢氧化钠溶液的反应过程。测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )
A.该pH变化过程可以证明酸和碱发生了化学反应
B.图中a点所示溶液中,含有的溶质是氯化钠和氯化氢
C.向图中c点所示溶液中滴加紫色石蕊,溶液变为红色
D.该实验是将氢氧化钠逐滴滴入到盛有盐酸溶液的烧杯中
4.下列说法正确的是( )
A.由不同种元素组成的物质一定是混合物
B.金属与酸溶液发生置换反应,溶液的质量一定增加
C.某无色溶液中滴入酚酞试液显红色,该溶液一定是碱溶液
D.某物质能与碱反应生成盐和水,则该物质一定是酸
5.下列各组混合物中加入无色酚酞溶液后,一定有明显现象是( )
A.氢氧化钙溶液、硫酸铜溶液 B.稀盐酸、氯化钠溶液
C.水、氧化钙 D.氢氧化钠溶液、稀硫酸
6.如图是X、Y、Z三种液体的对应近似pH,下列判断错误的是( )
A.X显酸性 B.Y一定是水
C.Z可能是碳酸钠溶液 D.Z可使紫色石蕊试液变蓝
7.下列化学反应都有重要的应用。其中属于中和反应的是( )
A.配制波尔多液 B.稀盐酸除铁锈
C.含小苏打的胃药治疗胃酸过多 D.氨水处理含硫酸的工业废水
8.如图是生活中一些物质的pH,下列说法正确的是( )
A.西瓜汁呈碱性
B.上述呈酸性的物质中酱油的酸性最强
C.肥皂水能使无色酚酞溶液变红
D.玉米粥的碱性比牙膏的碱性强
9.做中和反应实验时,向5mL氢氧化钠溶液中滴几滴酚酞溶液,然后再逐滴加入稀盐酸,有关分析正确的是( )
A. B.
C. D.
10.向pH=1的溶液中,滴加1~2滴紫色石蕊试液,溶液呈( )
A.红色 B.蓝色 C.紫色 D.无色
11.关于水的净化过程描述错误的是( )
A.通过过滤装置除去可溶性杂质 B.通入氯气杀菌消毒
C.加入明矾使不溶性悬浮物凝聚 D.通过活性炭吸附部分有害物质
12.小明对部分实验现象记录如下,其中错误的是( )
A.二氧化硫气体通入高锰酸钾溶液,红色褪去
B.红磷在空气中燃烧产生大量白色烟雾
C.铜片在空气中加热生成黑色固体
D.向碳酸钠溶液中滴加酚酞试液,酚酞试液变红
二、填空题
13.用量筒量液体时,量筒必须 ,视线要与量筒内液体的 保持水平.
14.我省素有“红土地”之称,红土壤偏酸性。下列农作物适宜在红土壤中种植的是 。
农作物 马铃薯 甘草 茶树 橘子 桑树
最适合生长的pH范围 5.5~6.0 7.2~8.5 5.0~5.5 5.5~6.5 7.0~8.0
A
甘草 B 橘子 C 桑树 D
15.在5mL氢氧化钠溶液中滴加2滴酚酞试液,溶液呈 色,再加入5mL稀盐酸,得到无色溶液,则无色溶液一定是 。
Ⅰ.
pH≤7 Ⅱ. pH=7 Ⅲ. pH <7 Ⅳ. pH>7
将无色溶液蒸发至干,看到的现象是 。
若将40克10%氢氧化钠溶液和足量稀盐酸反应,计算生成氯化钠的物质的量。(根据化学方程式计算)
16.柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医疗等行业,柠檬酸中碳元素的质量分数为 ,将紫色石蕊溶液滴加到柠檬酸中,溶液变红色,说明柠檬酸的pH值 7(填“>”“=”或“<”)
17.将X溶液滴入Y溶液中,在滴加过程中,Y溶液的pH值变化情况如图所示.
溶液 A B C D
X 盐酸 氢氧化钠 盐酸 氢氧化钠
Y 水 水 氢氧化钠 盐酸
(1)表格中符合这种变化情况的是 (填写编号),理由是: .
(2)写出该反应的化学方程式 .
(3)在Y溶液中滴入石蕊试液,若不断滴入X溶液,石蕊颜色的变化是 .
18.根据下图所示,按要求回答问题。
(1)实验室用高锰酸钾制取氧气,反应的符号表达式为 ,所选用的发生装置是 (填序号,下同),收集装置可选用E或 ;若用图F所示装置收集该气体,气体应从 (填“a”或“b”)端管口通入。若选用E装置收集较纯净氧气的适宜时间是 (填字母序号)。
A.当导管口刚有气泡冒出时 B.当导管口停止冒出气泡时 C.当导管口有连续均匀气泡冒出时
(2)查阅资料:①相同条件下,氨气(NH3)的密度比空气小,且极易溶于水,其水溶液称为氨水。②加热氯化铵和氢氧化钙固体混合物可制得氨气。③氨气在加热的条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。根据所查资料,制取氨气应选择的发生装置是 (填序号)。若将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,可观察到的现象是 。
三、综合题
19.“化”说五味。
(1)五味调和醋为先,可用 (填标号)测定食醋的酸碱度。
a.石蕊溶液 b.pH试纸 c.酚酞溶液
(2)木糖醇和蔗糖的溶解度曲线如图1。30℃时 (填“能”或“不能”)配得70%的蔗糖溶液;将60℃时95g木糖醇饱和溶液降温到30℃,理论上析出木糖醇的质量是 g。
(3)硬水有苦涩味,将其通过阳离子交换柱后可转化成软水(如图2,阴离子未画出),交换后的水仍然呈电中性。1个Ca2+可以交换出 个Na+,家庭中软化硬水的方法有 。
(4)每100g某辣椒中主要营养成分数据如下表:
营养成分 维生素C 蛋白质 脂肪 糖类 钙 铁 水
质量 171mg 1.9g 0.3g 11.6g 20mg 1.2mg 85.5g
辣椒中含量最高的营养素是 ;摄入适量 (填元素符号)可预防骨质疏松。
(5)向10g9%的氯化钠溶液中加入 g水,可稀释为0.9%的生理盐水。
20.向氢氧化钠溶液中逐滴加入盐酸,溶液pH的变化如图所示。
(1)请写出有关反应的化学方程式 。
(2)小山同学向b点溶液中滴加紫色石蕊溶液,溶液呈红色,则使石蕊溶液变红的离子是 。
21.化学源于生活,生活中很多现象蕴含着化学知识,请你填空:
(1)春天小明同学来到了邕江河边,发现河水清澈透明,如果要测定该河水的酸碱度,应选用 .(填字母号)
A,石蕊试液 B,酚酞试液 C,pH试纸
(2)医生建议胃酸过多病人须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
抗胃酸药 复方氢氧化镁片剂 铝碳酸镁片
有效成分 Mg(OH)2 AlMg(OH)3CO3
构成微粒 Mg2+、OH﹣ Al3+、Mg2+、OH﹣、CO32﹣
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异.
①Mg(OH)2起抗酸作用的微粒是 (填微粒符号,下同).该药物和盐酸反应叫 反应.
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl=MgCl2+AlCl3+4H2O+CO2↑.铝碳酸镁起抗酸作用的两种微粒是 .
22.水是生命之源,请回答下列有关水的问题:
(1)水发生部分结冰变化后形成的冰和水混合体系属于 (选填“纯净物”或“混合物”)。
(2)若要测定某工业水样的酸碱度,最适宜的是____。
A.无色酚酞试液 B.pH试纸 C.紫色石蕊试液
(3)把下列物质分别加入纯净水中,用玻璃棒不断搅拌,能形成无色溶液的是____。
A.泥沙 B.无水硫酸铜 C.氯化钠 D.花生油
答案解析部分
1.【答案】D
2.【答案】C
3.【答案】C
4.【答案】B
5.【答案】C
6.【答案】B
7.【答案】D
8.【答案】C
9.【答案】A
10.【答案】A
11.【答案】A
12.【答案】B
13.【答案】放平;凹液面的最低处
14.【答案】B;马铃薯或茶树
15.【答案】红;Ⅰ;白色固体;解:设NaCl的物质的量为x 40×10%/40=0.1mol
NaOH+HCl= NaCl + H2O
1 1
0.1mol x
1/0.1 = 1/x x=0.1mol 答:生成氯化钠的物质的量为0.1mol
16.【答案】37.5%;<
17.【答案】D;开始时Y溶液的pH<7,一定是盐酸,滴加X溶液时,混合溶液pH由小变大,直到pH>7,只能是加pH>7的溶液,即加NaOH溶液;NaOH+HCl=NaCl+H2O;红色逐渐变为紫色,再变为蓝色
18.【答案】(1);B;D;a;C
(2)B;无色酚酞溶液变红
19.【答案】(1)b
(2)不能;10
(3)2;煮沸
(4)水;Ca
(5)90
20.【答案】(1)
(2)H+或氢离子
21.【答案】(1)C
(2)①OH﹣;中和;OH﹣、CO32﹣
22.【答案】(1)纯净物
(2)B
(3)C
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
