3.1 海洋化学资源 同步练习(含答案) 2022-2023学年鲁教版(五四制)九年级全册化学
文档属性
| 名称 | 3.1 海洋化学资源 同步练习(含答案) 2022-2023学年鲁教版(五四制)九年级全册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 87.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-02 00:00:00 | ||
图片预览



文档简介
3.1 海洋化学资源 同步练习
一、单选题
1.海洋是一个巨大的宝藏,期待着人们的开发和利用.下列物质不经过化学变化就能从海水中获得的是( )
A.纯碱 B.单质镁 C.烧碱 D.粗盐
2.深海鱼油中的DHA(化学式为C22H32O2),俗称脑黄金,是构成大脑细胞膜的重要成分,参与脑细胞的形成和发育。下列关于DHA相关说法中正确的是( )
A.脑黄金中碳元素的质量分数最小
B.脑黄金由碳、氢、氧三种元素组成
C.脑黄金中C,H,O三种元素的质量比为11:16:1
D.脑黄金由56个原子构成
3.下列关于资源,能源说法正确的是( )
①拉瓦锡利用红磷做实验得出空气由氧气和氮气组成的结论
②煤是复杂的混合物,主要含有碳元素,焦炭、煤油、煤气都是综合利用的产品
③目前已制得的纯金属有90余种
④地球上的生物种类千差万别,体内水的质量与生物题总质量的比一般都在60%以上
⑤海水中含有80多种元素,其中含量最多的物质是氧.
A.①②③ B.②③④ C.④⑤ D.③④
4.下列关于资源、能源的叙述正确的是( )
A.使化石燃料充分燃烧,既可以减少空气污染,又可以节约化石能源
B.空气的成分按体积计大约是:氮气和氧气占99%,稀有气体占1%
C.海洋蕴藏丰富的化学资源,目前测定海水中含有的物质有80多种
D.废旧金属可回收再利用,但不包括被腐蚀的铁制品
5.下列有关资源、能源的叙述正确的是( )
A.空气中二氧化碳约占其体积分数为0.94%
B.石油炼制可得到汽油、煤焦油、航空煤油等
C.海水中含量最多的元素是钠元素
D.人们正在利用和开发的其他能源有氢能、太阳能、风能等
6.下列有关资源、能源的叙述正确的是( )
A.地壳中含量最高的金属元素是钢
B.石油炼制可得到汽油、煤焦油、航空煤油等
C.海洋中蕴藏着丰富的化学资源,海水中含有的化学元素有20多种
D.人们正在利用和开发的其他能源有氢能、太阳能、风能、地热能等
7.下列有关资源或能源的叙述正确的是( )
A.海洋中蕴藏着丰富的化学资源,海水中含有80多种物质
B.目前已经广泛用塑料来代替钢和其他合金制造管道、齿轮和汽车零部件等
C.导热、导电性最好的金属是铜
D.合金的强度和硬度一定比组成它们的纯金属更高,抗腐蚀性能等也更好
8.下列叙述中,正确的是( )
A.太阳能、核能、风能等是值得开发和利用的新能源
B.空气是一种宝贵的资源,其中含量最多的是氧气
C.海水淡化只能得到淡水,剩余物不再有利用价值
D.人类利用的能量都是通过化学反应获得的
9.下列有关资源、能源的叙述正确的是( )
A.地壳中含有最多的金属元素是铝,所以人类每年在自然界中提取最多的金属也是铝
B.石油分馏可得到汽油、柴油、煤焦油等
C.人们正在利用和开发的其他能源有太阳能、风能、地热能、可燃冰等
D.海洋中蕴藏着丰富的化学资源,海水中含有的化学元素有80多种
10.海洋是人类千万年来取之不尽,用之不竭的资源宝库,下列说法中错误的是( )
A.利用膜法可淡化海水,其原理与过滤的原理相似,都是选择合适的孔径将直径大小不同的粒子(或颗粒)分开
B.近年来海水因二氧化碳等非金属氧化物的增加而酸化。因为这些氧化物溶于海水中会使海水pH值增大
C.海水制镁时,加入石灰乳的目的是将镁离子沉降聚集
D.海水酸化严重将影响珊瑚和其他分泌碳酸钙的海洋生物生存,因为海水氢离子的浓度增加,这些海洋生物的碳酸钙外壳会遭到破坏
11.下列关于资源、能源、环保方面的叙述错误的是( )
A.海水中含有80多种元素,是巨大的资源宝库
B.世界上已有50%以上的铁和90%以上的金得到了回收利用
C.地壳中含量最多的元素是氧元素,它的质量分数接近于50%
D.世界每年因腐蚀而报废的金属设备和材料相当于年产量的50%-60%
12.下列有关说法正确的是( )
A.含氧元素质量分数最高的氧化物是水
B.空气是一种重要的自然资源,它是由氧气和氮气两种气体组成的
C.地球上的水资源是丰富的,但可利用的淡水资源只约占全球水储量的2.53%
D.海洋中含有80多种元素,其中含量最多的金属元素是钠元素
二、填空题
13.生活处处有化学,请联系学过的化学知识。回答下列问题。
(1)包饺子的食材有面粉、韭草、瘦肉、植物油、食盐等。其中富含糖类的是 。
(2)人体缺 元素能导致食欲不振、生长迟缓、发育不良。
(3)加了洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的 作用。
(4)铁锅容易生锈的主要原因是铁与空气中的 、水蒸气发生了化学反应。
14.根据如图甲、乙、丙三幅元素含量示意图,试推测元素分布领域(填图下序号):分布在人体中的是 ;分布在海水中的是 ;分布在地壳中的是 .
15.空气中含量最多的元素为 ,地壳中含量最多的元素为 ,地核中含量最多的元素为 ,太阳中含量最多的元素为 ,海水中含量最多的元素为 ;人体中含量最多的元素为 .
16.海水中有着丰富的化学资源,人们可以从海水中提取出氯化钠等多种物质。下图就是利用海水提取氯化钠的大致过程:
(1)图中①是 (填“蒸发池”或“冷却池”)。
(2)析出晶体后的母液是氯化钠的 (填“饱和溶液”或“不饱和溶液”)。
(3)实验室除去粗盐中难溶性杂质的主要实验步骤有:
Ⅰ 溶解 Ⅱ (填操作名称) Ⅲ 蒸发
上述三个步骤中,用到的同一种玻璃仪器的名称是 ,该玻璃仪器在步骤Ⅱ中的作用是 。
(4)将粗盐制成精盐后,现要配制 溶质质量分数为 的氯化钠溶液,最取蒸馏水的量筒规格应选择 (填字母)。
A. B. C. D.
(5)已知某粗盐样品中的杂质为氯化镁和泥沙。常温下,将 该粗盐样品溶解于足量水中,过滤得到不足4g泥沙和 溶液,取出 溶液进行测定,其中含有镁元素 ,氯元素 ,则原粗盐中氯化钠的质量分数为 。
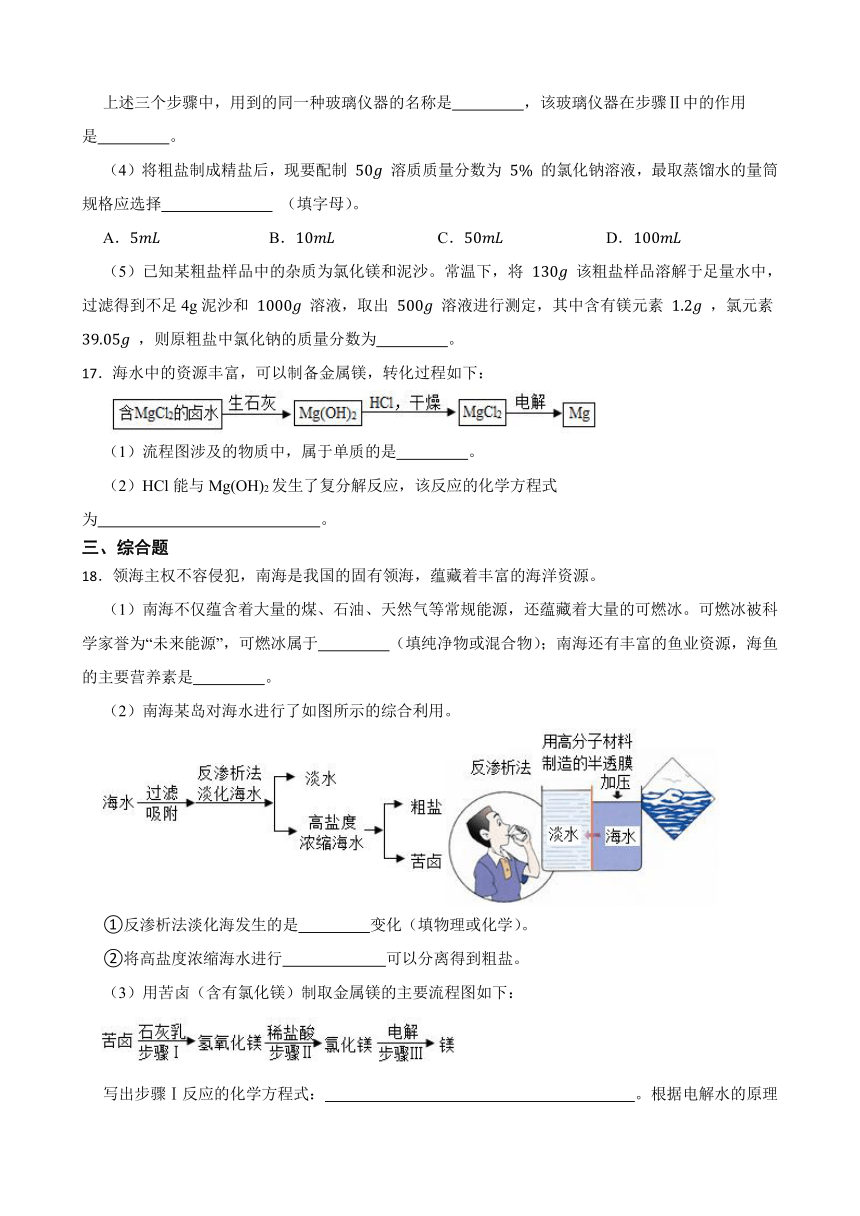
17.海水中的资源丰富,可以制备金属镁,转化过程如下:
(1)流程图涉及的物质中,属于单质的是 。
(2)HCl能与Mg(OH)2发生了复分解反应,该反应的化学方程式为 。
三、综合题
18.领海主权不容侵犯,南海是我国的固有领海,蕴藏着丰富的海洋资源。
(1)南海不仅蕴含着大量的煤、石油、天然气等常规能源,还蕴藏着大量的可燃冰。可燃冰被科学家誉为“未来能源”,可燃冰属于 (填纯净物或混合物);南海还有丰富的鱼业资源,海鱼的主要营养素是 。
(2)南海某岛对海水进行了如图所示的综合利用。
①反渗析法淡化海发生的是 变化(填物理或化学)。
②将高盐度浓缩海水进行 可以分离得到粗盐。
(3)用苦卤(含有氯化镁)制取金属镁的主要流程图如下:
写出步骤Ⅰ反应的化学方程式: 。根据电解水的原理写出步骤Ⅲ的化学方程式: 。
19.镁及其合金是一种用途广泛的金属材料,大量的金属镁是从海水或卤水中提取的,其主要步骤见下图:
(1)加入试剂①后,分离得到Mg(OH)2沉淀的方法是 ;
(2)试剂②可以选用 ;
(3)通电后,MgCl2分解生成Mg和Cl2的化学反应方程式 。
20.水是生命之源,海洋是生命的摇篮。请回答下面关于海洋的几个问题:
(1)海水中资源丰富,含量最多的金属阳离子是 (填符号),含量最多的分子是 (填符号)。
(2)下图所示是对海水的综合利用。
①反渗透法淡化海水是利用海水中各成分的 不同分离出淡水。
②从高盐度浓缩海水中分离得到粗盐的过程是 (填“物理变化”或“化学变化”)。
③用苦卤制取金属镁的流程图如下:
上述转化过程中,所发生的反应属于复分解反应类型的步骤是 (填序号),步骤II的化学方程式为 。利用苦卤提取氧化镁比“直接从海水中提取氧化镁”的优势是 。
21.化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题:
(1)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有MgCl2、Na2SO4、CaCl2等可溶性杂质,通过步骤I,再利用过滤操作进行除杂提纯。
①步骤I加入下列三种溶液正确的先后顺序为 。(填字母序号)
A.稍过量的Na2CO3溶液
B.稍过量的BaCl2溶液
C.稍过量的NaOH溶液
②理论上用过量的 溶液(填化学式)代替NaOH和BaCl2两种溶液,也可以达到相同的实验目的。
(2)步骤Ⅱ中发生反应的化学方程式为 。
(3)上述流程图中未涉及到的基本反应类型是 。
答案解析部分
1.【答案】D
2.【答案】B
3.【答案】D
4.【答案】A
5.【答案】D
6.【答案】D
7.【答案】B
8.【答案】A
9.【答案】D
10.【答案】B
11.【答案】D
12.【答案】D
13.【答案】(1)面粉
(2)锌
(3)乳化
(4)氧气
14.【答案】丙;乙;甲
15.【答案】氮;氧;铁;氢;氧;氧
16.【答案】(1)蒸发池
(2)饱和溶液
(3)过滤;玻璃棒;引流
(4)C
(5)
17.【答案】(1)Mg
(2)
18.【答案】(1)混合物;蛋白质
(2)物理;蒸发结晶
(3);
19.【答案】(1)过滤
(2)稀盐酸
(3)
20.【答案】(1)Na+;H2O
(2)颗粒大小;物理变化;I、II;Mg(OH)2+2HCl=MgCl2+2H2O;苦卤中镁离子的浓度高(或镁离子得以富集)
21.【答案】(1)CBA或BCA或BAC;Ba(OH)2
(2)CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl
(3)置换反应
一、单选题
1.海洋是一个巨大的宝藏,期待着人们的开发和利用.下列物质不经过化学变化就能从海水中获得的是( )
A.纯碱 B.单质镁 C.烧碱 D.粗盐
2.深海鱼油中的DHA(化学式为C22H32O2),俗称脑黄金,是构成大脑细胞膜的重要成分,参与脑细胞的形成和发育。下列关于DHA相关说法中正确的是( )
A.脑黄金中碳元素的质量分数最小
B.脑黄金由碳、氢、氧三种元素组成
C.脑黄金中C,H,O三种元素的质量比为11:16:1
D.脑黄金由56个原子构成
3.下列关于资源,能源说法正确的是( )
①拉瓦锡利用红磷做实验得出空气由氧气和氮气组成的结论
②煤是复杂的混合物,主要含有碳元素,焦炭、煤油、煤气都是综合利用的产品
③目前已制得的纯金属有90余种
④地球上的生物种类千差万别,体内水的质量与生物题总质量的比一般都在60%以上
⑤海水中含有80多种元素,其中含量最多的物质是氧.
A.①②③ B.②③④ C.④⑤ D.③④
4.下列关于资源、能源的叙述正确的是( )
A.使化石燃料充分燃烧,既可以减少空气污染,又可以节约化石能源
B.空气的成分按体积计大约是:氮气和氧气占99%,稀有气体占1%
C.海洋蕴藏丰富的化学资源,目前测定海水中含有的物质有80多种
D.废旧金属可回收再利用,但不包括被腐蚀的铁制品
5.下列有关资源、能源的叙述正确的是( )
A.空气中二氧化碳约占其体积分数为0.94%
B.石油炼制可得到汽油、煤焦油、航空煤油等
C.海水中含量最多的元素是钠元素
D.人们正在利用和开发的其他能源有氢能、太阳能、风能等
6.下列有关资源、能源的叙述正确的是( )
A.地壳中含量最高的金属元素是钢
B.石油炼制可得到汽油、煤焦油、航空煤油等
C.海洋中蕴藏着丰富的化学资源,海水中含有的化学元素有20多种
D.人们正在利用和开发的其他能源有氢能、太阳能、风能、地热能等
7.下列有关资源或能源的叙述正确的是( )
A.海洋中蕴藏着丰富的化学资源,海水中含有80多种物质
B.目前已经广泛用塑料来代替钢和其他合金制造管道、齿轮和汽车零部件等
C.导热、导电性最好的金属是铜
D.合金的强度和硬度一定比组成它们的纯金属更高,抗腐蚀性能等也更好
8.下列叙述中,正确的是( )
A.太阳能、核能、风能等是值得开发和利用的新能源
B.空气是一种宝贵的资源,其中含量最多的是氧气
C.海水淡化只能得到淡水,剩余物不再有利用价值
D.人类利用的能量都是通过化学反应获得的
9.下列有关资源、能源的叙述正确的是( )
A.地壳中含有最多的金属元素是铝,所以人类每年在自然界中提取最多的金属也是铝
B.石油分馏可得到汽油、柴油、煤焦油等
C.人们正在利用和开发的其他能源有太阳能、风能、地热能、可燃冰等
D.海洋中蕴藏着丰富的化学资源,海水中含有的化学元素有80多种
10.海洋是人类千万年来取之不尽,用之不竭的资源宝库,下列说法中错误的是( )
A.利用膜法可淡化海水,其原理与过滤的原理相似,都是选择合适的孔径将直径大小不同的粒子(或颗粒)分开
B.近年来海水因二氧化碳等非金属氧化物的增加而酸化。因为这些氧化物溶于海水中会使海水pH值增大
C.海水制镁时,加入石灰乳的目的是将镁离子沉降聚集
D.海水酸化严重将影响珊瑚和其他分泌碳酸钙的海洋生物生存,因为海水氢离子的浓度增加,这些海洋生物的碳酸钙外壳会遭到破坏
11.下列关于资源、能源、环保方面的叙述错误的是( )
A.海水中含有80多种元素,是巨大的资源宝库
B.世界上已有50%以上的铁和90%以上的金得到了回收利用
C.地壳中含量最多的元素是氧元素,它的质量分数接近于50%
D.世界每年因腐蚀而报废的金属设备和材料相当于年产量的50%-60%
12.下列有关说法正确的是( )
A.含氧元素质量分数最高的氧化物是水
B.空气是一种重要的自然资源,它是由氧气和氮气两种气体组成的
C.地球上的水资源是丰富的,但可利用的淡水资源只约占全球水储量的2.53%
D.海洋中含有80多种元素,其中含量最多的金属元素是钠元素
二、填空题
13.生活处处有化学,请联系学过的化学知识。回答下列问题。
(1)包饺子的食材有面粉、韭草、瘦肉、植物油、食盐等。其中富含糖类的是 。
(2)人体缺 元素能导致食欲不振、生长迟缓、发育不良。
(3)加了洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的 作用。
(4)铁锅容易生锈的主要原因是铁与空气中的 、水蒸气发生了化学反应。
14.根据如图甲、乙、丙三幅元素含量示意图,试推测元素分布领域(填图下序号):分布在人体中的是 ;分布在海水中的是 ;分布在地壳中的是 .
15.空气中含量最多的元素为 ,地壳中含量最多的元素为 ,地核中含量最多的元素为 ,太阳中含量最多的元素为 ,海水中含量最多的元素为 ;人体中含量最多的元素为 .
16.海水中有着丰富的化学资源,人们可以从海水中提取出氯化钠等多种物质。下图就是利用海水提取氯化钠的大致过程:
(1)图中①是 (填“蒸发池”或“冷却池”)。
(2)析出晶体后的母液是氯化钠的 (填“饱和溶液”或“不饱和溶液”)。
(3)实验室除去粗盐中难溶性杂质的主要实验步骤有:
Ⅰ 溶解 Ⅱ (填操作名称) Ⅲ 蒸发
上述三个步骤中,用到的同一种玻璃仪器的名称是 ,该玻璃仪器在步骤Ⅱ中的作用是 。
(4)将粗盐制成精盐后,现要配制 溶质质量分数为 的氯化钠溶液,最取蒸馏水的量筒规格应选择 (填字母)。
A. B. C. D.
(5)已知某粗盐样品中的杂质为氯化镁和泥沙。常温下,将 该粗盐样品溶解于足量水中,过滤得到不足4g泥沙和 溶液,取出 溶液进行测定,其中含有镁元素 ,氯元素 ,则原粗盐中氯化钠的质量分数为 。
17.海水中的资源丰富,可以制备金属镁,转化过程如下:
(1)流程图涉及的物质中,属于单质的是 。
(2)HCl能与Mg(OH)2发生了复分解反应,该反应的化学方程式为 。
三、综合题
18.领海主权不容侵犯,南海是我国的固有领海,蕴藏着丰富的海洋资源。
(1)南海不仅蕴含着大量的煤、石油、天然气等常规能源,还蕴藏着大量的可燃冰。可燃冰被科学家誉为“未来能源”,可燃冰属于 (填纯净物或混合物);南海还有丰富的鱼业资源,海鱼的主要营养素是 。
(2)南海某岛对海水进行了如图所示的综合利用。
①反渗析法淡化海发生的是 变化(填物理或化学)。
②将高盐度浓缩海水进行 可以分离得到粗盐。
(3)用苦卤(含有氯化镁)制取金属镁的主要流程图如下:
写出步骤Ⅰ反应的化学方程式: 。根据电解水的原理写出步骤Ⅲ的化学方程式: 。
19.镁及其合金是一种用途广泛的金属材料,大量的金属镁是从海水或卤水中提取的,其主要步骤见下图:
(1)加入试剂①后,分离得到Mg(OH)2沉淀的方法是 ;
(2)试剂②可以选用 ;
(3)通电后,MgCl2分解生成Mg和Cl2的化学反应方程式 。
20.水是生命之源,海洋是生命的摇篮。请回答下面关于海洋的几个问题:
(1)海水中资源丰富,含量最多的金属阳离子是 (填符号),含量最多的分子是 (填符号)。
(2)下图所示是对海水的综合利用。
①反渗透法淡化海水是利用海水中各成分的 不同分离出淡水。
②从高盐度浓缩海水中分离得到粗盐的过程是 (填“物理变化”或“化学变化”)。
③用苦卤制取金属镁的流程图如下:
上述转化过程中,所发生的反应属于复分解反应类型的步骤是 (填序号),步骤II的化学方程式为 。利用苦卤提取氧化镁比“直接从海水中提取氧化镁”的优势是 。
21.化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题:
(1)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有MgCl2、Na2SO4、CaCl2等可溶性杂质,通过步骤I,再利用过滤操作进行除杂提纯。
①步骤I加入下列三种溶液正确的先后顺序为 。(填字母序号)
A.稍过量的Na2CO3溶液
B.稍过量的BaCl2溶液
C.稍过量的NaOH溶液
②理论上用过量的 溶液(填化学式)代替NaOH和BaCl2两种溶液,也可以达到相同的实验目的。
(2)步骤Ⅱ中发生反应的化学方程式为 。
(3)上述流程图中未涉及到的基本反应类型是 。
答案解析部分
1.【答案】D
2.【答案】B
3.【答案】D
4.【答案】A
5.【答案】D
6.【答案】D
7.【答案】B
8.【答案】A
9.【答案】D
10.【答案】B
11.【答案】D
12.【答案】D
13.【答案】(1)面粉
(2)锌
(3)乳化
(4)氧气
14.【答案】丙;乙;甲
15.【答案】氮;氧;铁;氢;氧;氧
16.【答案】(1)蒸发池
(2)饱和溶液
(3)过滤;玻璃棒;引流
(4)C
(5)
17.【答案】(1)Mg
(2)
18.【答案】(1)混合物;蛋白质
(2)物理;蒸发结晶
(3);
19.【答案】(1)过滤
(2)稀盐酸
(3)
20.【答案】(1)Na+;H2O
(2)颗粒大小;物理变化;I、II;Mg(OH)2+2HCl=MgCl2+2H2O;苦卤中镁离子的浓度高(或镁离子得以富集)
21.【答案】(1)CBA或BCA或BAC;Ba(OH)2
(2)CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl
(3)置换反应
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
