1.3.1氧化还原反应课件(共20张PPT)2022-2023学年上学期高一化学人教版(2019)必修第一册
文档属性
| 名称 | 1.3.1氧化还原反应课件(共20张PPT)2022-2023学年上学期高一化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-02 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
银针试毒的原理:
4Ag+O2+2H2S===2Ag2S+2H2O
银白色 黑色
第三节 氧化还原反应
九年级 课本
教材P20【思考与讨论】
(1)请根据初中学过的氧化还原反应的知识,分析以下反应,完成下表。
2CuO + C = 2Cu + CO2 ↑
Fe2O3 + 3CO = 2Fe + 3CO2
物质 反应物 发生的反应(氧化反应或还原反应)
得氧物质
失氧物质
C、CO
CuO、Fe2O3
氧化反应
还原反应
在一个化学反应中,一种物质得到氧发生氧化反应,同时必然有一种物质失去氧发生还原反应。
氧化反应、还原反应是同时进行的
一、氧化还原反应的概念及其本质
反应类型 得失氧
氧化反应
还原反应
氧化还原反应
得到氧元素的反应
失去氧元素的反应
有氧得失的反应
1、从得失氧的角度认识(表观)
2CuO + C == 2Cu + CO2↑
高温
Fe2O3 + 3CO == 2Fe + 3CO2
高温
+2
0
0
+4
+3
+2
0
+4
元素化合价升高的物质发生氧化反应,化合价降低物质发生还原反应
有元素的化合价在反应前后发生变化
(判断依据)
Fe + CuSO4 == Cu + FeSO4
0
+2
0
+2
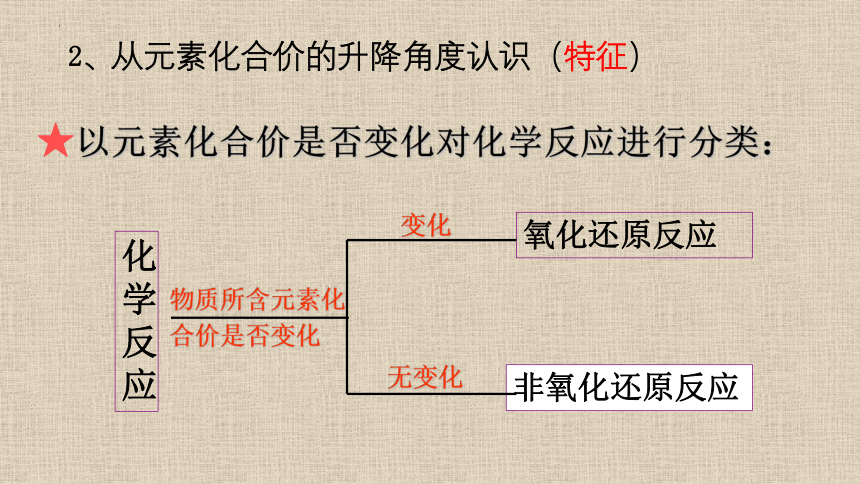
2、从元素化合价的升降角度认识(特征)
反应类型 化合价变化
氧化反应
还原反应
所含元素化合价升高的反应
所含元素化合价降低的反应
氧化还原反应
凡有元素化合价升降的反应(特征)
2、从元素化合价的升降角度认识(特征)
化学反应
氧化还原反应
非氧化还原反应
★以元素化合价是否变化对化学反应进行分类:
物质所含元素化合价是否变化
变化
无变化
4Ag+O2+2H2S===2Ag2S+2H2O
0
+1
0
-2
化合价升高,被氧化
化合价降低,被还原
在古代,由于生产技术落后,致使砒霜(三氧化二砷)中伴有少量的硫和硫化物,所以可以用银针验毒。
元素为什么会发生化合价变化?化合价的升降是什么原因引起的?
化合价的升降
电子的转移
实质
+11
+17
+17
+11
Na+ Cl-
Na
Cl
Cl-
Na+
化合物NaCl的形成过程
失2×e-,化合价升高,被氧化
得2×e-,化合价降低,被还原
0 0 +1 -1
2Na + Cl2 = 2NaCl
化合价的升降
实质
电子的得失
H Cl
+17
+1
+1
+17
H Cl
+1 -1
H
Cl
HCl
化合物HCl的形成过程
电子对偏离,化合价升高,被氧化
电子对偏向,化合价降低,被还原
2H2 + Cl2 = 2HCl
0 0 +1 -1
化合价的升降
实质
共用电子对的偏移
3、从电子转移的角度认识(本质)
反应类型 化合价变化
氧化反应
还原反应
有电子失去(或偏离)的反应
有电子得到(或偏向)的反应
氧化还原反应
有电子转移(得失或偏移)的反应
(本质) (特征)
某元素得到电子(或电子对偏向)
化合价降低
还原反应
某元素失去电子(或电子对偏离)
化合价升高
氧化反应
升---失---氧化---还原剂
降---得---还原---氧化剂
【小结】
Zn + HCl ZnCl2 + H2
0
+2
+1
0
化合价升高,失去电子,被氧化
化合价降低,得到电子,被还原
氧化剂
还原剂
氧化产物 还原产物
所含元素化合价升高的物质是 ,
所含元素化合价降低的物质是 。
还原剂
氧化剂
氧化剂 、还原剂 可以为同一物质,同样,氧化产物、还原产物也可以为同一物质。如:
不对。可以是同一种元素既被氧化、又还原。如:
Cl2 + 2NaOH = NaCl + NaClO + H2O
氧化剂
还原剂
2Mg + O2 = 2MgO
还原产物
氧化产物
在氧化还原反应中一种元素被氧化,则一定有另一种元素
被还原,这句话对吗?
二、氧化还原反应中电子转移的表示方法
双线桥表示法
+17
2
8
7
+11
2
8
1
Na
Cl
Na+
Cl-
8
NaCl
2Na + Cl2 === 2NaCl
Δ
0
0
+1
-1
失去2×e-,化合价升高,被氧化(发生氧化反应)
得到2×e-,化合价降低,被还原(发生还原反应)
H2 + Cl2 === 2HCl
点燃
+1
1
+17
2
8
7
你的电子
借我用用
Cl
H
哼!不借
6
+17
2
8
7
+11
2
8
1
Na
Cl
Na+
Cl-
8
NaCl
2Na + Cl2 === 2NaCl
Δ
0
0
+1
-1
2 e-
H2 + Cl2 === 2H Cl
点燃
+1
1
+17
2
8
7
你的电子
借我用用
Cl
H
哼!不借
6
单线桥表示法
三、氧化还原反应与四大基本反应类型关系
有单质
有单质
有单质参加的反应一定是氧化还原反应吗?不是,例如2O2 == 3O2
小结
定义
表示电子转移的方法
特征
氧化反应和还原反应同时发生的反应
四种基本反映类型与氧化还原反应的关系
本质
元素的化合价在反应前后发生变化
电子的转移(得失或偏移)
单线桥法
双线桥法
银针试毒的原理:
4Ag+O2+2H2S===2Ag2S+2H2O
银白色 黑色
第三节 氧化还原反应
九年级 课本
教材P20【思考与讨论】
(1)请根据初中学过的氧化还原反应的知识,分析以下反应,完成下表。
2CuO + C = 2Cu + CO2 ↑
Fe2O3 + 3CO = 2Fe + 3CO2
物质 反应物 发生的反应(氧化反应或还原反应)
得氧物质
失氧物质
C、CO
CuO、Fe2O3
氧化反应
还原反应
在一个化学反应中,一种物质得到氧发生氧化反应,同时必然有一种物质失去氧发生还原反应。
氧化反应、还原反应是同时进行的
一、氧化还原反应的概念及其本质
反应类型 得失氧
氧化反应
还原反应
氧化还原反应
得到氧元素的反应
失去氧元素的反应
有氧得失的反应
1、从得失氧的角度认识(表观)
2CuO + C == 2Cu + CO2↑
高温
Fe2O3 + 3CO == 2Fe + 3CO2
高温
+2
0
0
+4
+3
+2
0
+4
元素化合价升高的物质发生氧化反应,化合价降低物质发生还原反应
有元素的化合价在反应前后发生变化
(判断依据)
Fe + CuSO4 == Cu + FeSO4
0
+2
0
+2
2、从元素化合价的升降角度认识(特征)
反应类型 化合价变化
氧化反应
还原反应
所含元素化合价升高的反应
所含元素化合价降低的反应
氧化还原反应
凡有元素化合价升降的反应(特征)
2、从元素化合价的升降角度认识(特征)
化学反应
氧化还原反应
非氧化还原反应
★以元素化合价是否变化对化学反应进行分类:
物质所含元素化合价是否变化
变化
无变化
4Ag+O2+2H2S===2Ag2S+2H2O
0
+1
0
-2
化合价升高,被氧化
化合价降低,被还原
在古代,由于生产技术落后,致使砒霜(三氧化二砷)中伴有少量的硫和硫化物,所以可以用银针验毒。
元素为什么会发生化合价变化?化合价的升降是什么原因引起的?
化合价的升降
电子的转移
实质
+11
+17
+17
+11
Na+ Cl-
Na
Cl
Cl-
Na+
化合物NaCl的形成过程
失2×e-,化合价升高,被氧化
得2×e-,化合价降低,被还原
0 0 +1 -1
2Na + Cl2 = 2NaCl
化合价的升降
实质
电子的得失
H Cl
+17
+1
+1
+17
H Cl
+1 -1
H
Cl
HCl
化合物HCl的形成过程
电子对偏离,化合价升高,被氧化
电子对偏向,化合价降低,被还原
2H2 + Cl2 = 2HCl
0 0 +1 -1
化合价的升降
实质
共用电子对的偏移
3、从电子转移的角度认识(本质)
反应类型 化合价变化
氧化反应
还原反应
有电子失去(或偏离)的反应
有电子得到(或偏向)的反应
氧化还原反应
有电子转移(得失或偏移)的反应
(本质) (特征)
某元素得到电子(或电子对偏向)
化合价降低
还原反应
某元素失去电子(或电子对偏离)
化合价升高
氧化反应
升---失---氧化---还原剂
降---得---还原---氧化剂
【小结】
Zn + HCl ZnCl2 + H2
0
+2
+1
0
化合价升高,失去电子,被氧化
化合价降低,得到电子,被还原
氧化剂
还原剂
氧化产物 还原产物
所含元素化合价升高的物质是 ,
所含元素化合价降低的物质是 。
还原剂
氧化剂
氧化剂 、还原剂 可以为同一物质,同样,氧化产物、还原产物也可以为同一物质。如:
不对。可以是同一种元素既被氧化、又还原。如:
Cl2 + 2NaOH = NaCl + NaClO + H2O
氧化剂
还原剂
2Mg + O2 = 2MgO
还原产物
氧化产物
在氧化还原反应中一种元素被氧化,则一定有另一种元素
被还原,这句话对吗?
二、氧化还原反应中电子转移的表示方法
双线桥表示法
+17
2
8
7
+11
2
8
1
Na
Cl
Na+
Cl-
8
NaCl
2Na + Cl2 === 2NaCl
Δ
0
0
+1
-1
失去2×e-,化合价升高,被氧化(发生氧化反应)
得到2×e-,化合价降低,被还原(发生还原反应)
H2 + Cl2 === 2HCl
点燃
+1
1
+17
2
8
7
你的电子
借我用用
Cl
H
哼!不借
6
+17
2
8
7
+11
2
8
1
Na
Cl
Na+
Cl-
8
NaCl
2Na + Cl2 === 2NaCl
Δ
0
0
+1
-1
2 e-
H2 + Cl2 === 2H Cl
点燃
+1
1
+17
2
8
7
你的电子
借我用用
Cl
H
哼!不借
6
单线桥表示法
三、氧化还原反应与四大基本反应类型关系
有单质
有单质
有单质参加的反应一定是氧化还原反应吗?不是,例如2O2 == 3O2
小结
定义
表示电子转移的方法
特征
氧化反应和还原反应同时发生的反应
四种基本反映类型与氧化还原反应的关系
本质
元素的化合价在反应前后发生变化
电子的转移(得失或偏移)
单线桥法
双线桥法
