9.1溶液的形成课件(共18张PPT 内嵌视频)---2022-2023学年九年级化学人教版下册
文档属性
| 名称 | 9.1溶液的形成课件(共18张PPT 内嵌视频)---2022-2023学年九年级化学人教版下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 13.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-02 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
溶液的形成
第一课时
新课导入
你在海水中游过泳的话,就会发现海水又苦又咸。这是为什么呢
【实验探究一】溶液的形成
1.在20ml水中加入一药匙蔗糖,用玻璃棒搅拌,观察现象
2. 在20ml水中加入一药匙氯化钠,用玻璃棒搅拌,观察现象
【现象】搅拌后,蔗糖溶解在水中
【现象】搅拌后,NaCl溶解在水中
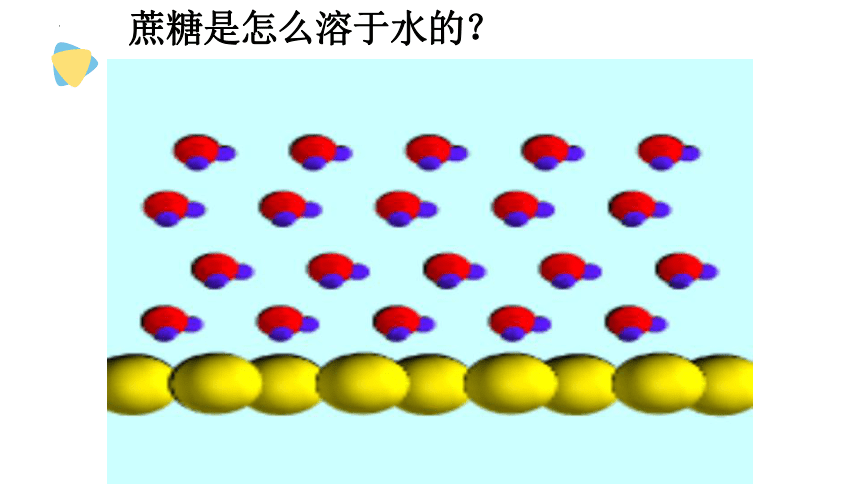
蔗糖是怎么溶于水的?
返回
氯化钠溶液中的离子运动
返回
【现象】蔗糖、NaCl均溶解在水中
【实验一】蔗糖、NaCl固体的溶解
【微观过程】
蔗糖表面的分子在水分子的作用下,向水中扩散,在水中以分子形式分散在水分子的中间。
NaCl在水分子的作用下,向水中扩散,在水中以离子形式(Na+和Cl-)存在于水分子的中间。
【注意】被溶解物在溶液中的存在形式为分子或离子
一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
一、溶液
1、定义:
溶质:
溶剂:
被溶解的物质
能溶解其它物质的物质
2、溶液的组成
溶液
思考:在蔗糖溶液和氯化钠溶液中,溶质和溶剂分别是什么?
2、溶液的组成
溶质:
溶剂:
被溶解的物质
能溶解其它物质的物质
(可以为固体、液体、气体
(通常为液体,水是最常见的溶剂,汽油、酒精也可作溶剂)
溶液
m溶液 m溶质 + m溶剂
V溶液 V溶质 + V溶剂
=
<
溶液:一种或几种物质分散到另一种物质里,
形成均一的、稳定的混合物。
3、溶液的特征:
(1)均一性:
(2)稳定性:
指溶液中任一部分的组成和性质完全相同。
指外界条件不变时,溶液组成不会改变(即溶质不会与溶剂分离开来)。
4、溶液的命名(读法)
(1)通用读法:溶质的溶剂溶液
例如:氯化钠的水溶液 碘的酒精溶液
(2)若溶剂为水,则可直接读为溶质溶液
例如:氯化钠溶液 蔗糖溶液
不同溶液里溶质与溶剂判断
溶液 溶剂 溶质
在有水的溶液里
在没有水的溶液里 气体-液体混合
固体-液体混合
液体-液体混合
水
其他物质
液体
气体
液体
固体
量多的液体
量少的液体
1.在溶质和溶剂不发生反应的溶液里:
实验9-2
实验9-2
实验现象
溶质 溶剂 现象
碘 水
碘 汽油
高锰酸钾 水
高锰酸钾 汽油
碘几乎不溶于水
碘溶于汽油,溶液为棕色
高锰酸钾溶于水,溶液为深紫红色
高锰酸钾几乎不溶于汽油
结论
同一种物质在不同溶剂中的溶解性是不同的,不同物质在同一溶剂中的溶解性也是不同的
振荡前现象
振荡后现象
静置后现象
结论
液体分层,上层无色
液体混合均匀
液体不分层
乙醇能与水互溶
[实验9-3] 乙醇能在水中溶解吗?
练习:判断下列溶液中的溶质和溶剂
溶液 溶质 溶剂
10 mL汽油 90 mL酒精
75 mL酒精 25 mL水
汽油
酒精
酒精
水
75%医用酒精
练习一:下列物质加入足量的水中能形成紫红色溶液的是( )
A.高锰酸钾 B.植物油 C. 酒精 D.大理石
A
我会做
1、下列关于溶液特征的叙述中不正确的是 ( )
A.溶液都是澄清、透明、无色的
B.当外界条件不变时,溶液长期放置溶质不会从溶液里分离出来
C.一种溶液中各部分的浓稀和性质都是一样的
D.溶液是均一、稳定的纯净物
AD
2、 下列液体属于溶液的是___________。(填序号)
①啤酒 ②水 ③泥水 ④澄清石灰水 ⑤盐酸
① ④ ⑤
溶液的形成
第一课时
新课导入
你在海水中游过泳的话,就会发现海水又苦又咸。这是为什么呢
【实验探究一】溶液的形成
1.在20ml水中加入一药匙蔗糖,用玻璃棒搅拌,观察现象
2. 在20ml水中加入一药匙氯化钠,用玻璃棒搅拌,观察现象
【现象】搅拌后,蔗糖溶解在水中
【现象】搅拌后,NaCl溶解在水中
蔗糖是怎么溶于水的?
返回
氯化钠溶液中的离子运动
返回
【现象】蔗糖、NaCl均溶解在水中
【实验一】蔗糖、NaCl固体的溶解
【微观过程】
蔗糖表面的分子在水分子的作用下,向水中扩散,在水中以分子形式分散在水分子的中间。
NaCl在水分子的作用下,向水中扩散,在水中以离子形式(Na+和Cl-)存在于水分子的中间。
【注意】被溶解物在溶液中的存在形式为分子或离子
一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
一、溶液
1、定义:
溶质:
溶剂:
被溶解的物质
能溶解其它物质的物质
2、溶液的组成
溶液
思考:在蔗糖溶液和氯化钠溶液中,溶质和溶剂分别是什么?
2、溶液的组成
溶质:
溶剂:
被溶解的物质
能溶解其它物质的物质
(可以为固体、液体、气体
(通常为液体,水是最常见的溶剂,汽油、酒精也可作溶剂)
溶液
m溶液 m溶质 + m溶剂
V溶液 V溶质 + V溶剂
=
<
溶液:一种或几种物质分散到另一种物质里,
形成均一的、稳定的混合物。
3、溶液的特征:
(1)均一性:
(2)稳定性:
指溶液中任一部分的组成和性质完全相同。
指外界条件不变时,溶液组成不会改变(即溶质不会与溶剂分离开来)。
4、溶液的命名(读法)
(1)通用读法:溶质的溶剂溶液
例如:氯化钠的水溶液 碘的酒精溶液
(2)若溶剂为水,则可直接读为溶质溶液
例如:氯化钠溶液 蔗糖溶液
不同溶液里溶质与溶剂判断
溶液 溶剂 溶质
在有水的溶液里
在没有水的溶液里 气体-液体混合
固体-液体混合
液体-液体混合
水
其他物质
液体
气体
液体
固体
量多的液体
量少的液体
1.在溶质和溶剂不发生反应的溶液里:
实验9-2
实验9-2
实验现象
溶质 溶剂 现象
碘 水
碘 汽油
高锰酸钾 水
高锰酸钾 汽油
碘几乎不溶于水
碘溶于汽油,溶液为棕色
高锰酸钾溶于水,溶液为深紫红色
高锰酸钾几乎不溶于汽油
结论
同一种物质在不同溶剂中的溶解性是不同的,不同物质在同一溶剂中的溶解性也是不同的
振荡前现象
振荡后现象
静置后现象
结论
液体分层,上层无色
液体混合均匀
液体不分层
乙醇能与水互溶
[实验9-3] 乙醇能在水中溶解吗?
练习:判断下列溶液中的溶质和溶剂
溶液 溶质 溶剂
10 mL汽油 90 mL酒精
75 mL酒精 25 mL水
汽油
酒精
酒精
水
75%医用酒精
练习一:下列物质加入足量的水中能形成紫红色溶液的是( )
A.高锰酸钾 B.植物油 C. 酒精 D.大理石
A
我会做
1、下列关于溶液特征的叙述中不正确的是 ( )
A.溶液都是澄清、透明、无色的
B.当外界条件不变时,溶液长期放置溶质不会从溶液里分离出来
C.一种溶液中各部分的浓稀和性质都是一样的
D.溶液是均一、稳定的纯净物
AD
2、 下列液体属于溶液的是___________。(填序号)
①啤酒 ②水 ③泥水 ④澄清石灰水 ⑤盐酸
① ④ ⑤
同课章节目录
