第十一单元 课题1 生活中常见的盐1(氯化钠及粗盐的提纯)课件(共24张PPT)—2022-2023学年九年级化学人教版下册
文档属性
| 名称 | 第十一单元 课题1 生活中常见的盐1(氯化钠及粗盐的提纯)课件(共24张PPT)—2022-2023学年九年级化学人教版下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-02 00:00:00 | ||
图片预览








文档简介
(共24张PPT)
指的是一类物质
食盐(主要成分氯化钠
生活中所说的盐
化学中所说的盐
据报道,我国曾发生多次将工业用盐亚硝酸钠(NaNO2)误作食盐(NaCl)用于烹饪而引起的中毒事件。
原因就是混淆了化学中的盐和生活中的盐。
一、盐的定义
在化学中,盐是指的一类化合物,即组成里含有金属离子(或铵根离子)和酸根离子的化合物。
钠盐: NaCl Na2CO3 Na2SO4 NaNO3
钾盐: KCl K2CO3 K2SO4 KNO3
碳酸盐:Na2CO3 K2CO3 CaCO3 MgCO3
铵盐: NH4Cl (NH4)2CO3 NH4NO3
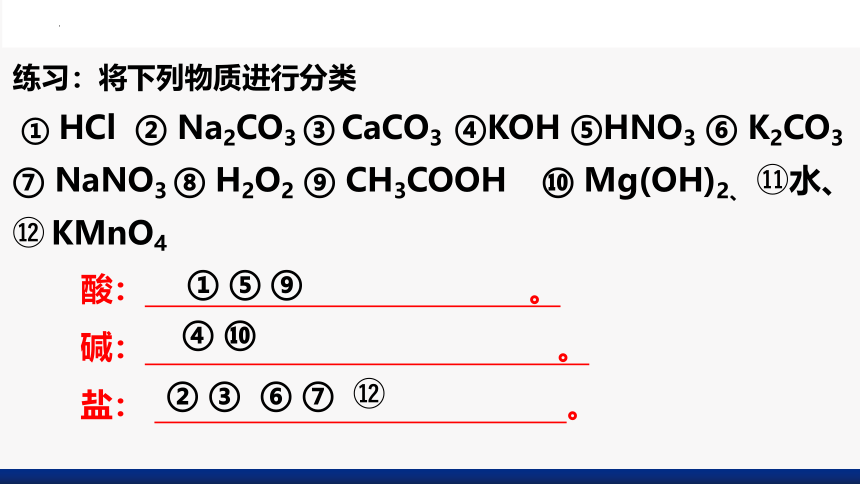
练习:将下列物质进行分类
① HCl ② Na2CO3 ③ CaCO3 ④KOH ⑤HNO3 ⑥ K2CO3
⑦ NaNO3 ⑧ H2O2 ⑨ CH3COOH ⑩ Mg(OH)2、 水、 KMnO4
酸: 。
碱: 。
盐: 。
① ⑤ ⑨
④ ⑩
② ③ ⑥ ⑦
二、氯化钠
1、食盐的主要成分是氯化钠
2、用途
(1)医疗上:
生理盐水
医疗上的生理盐水是用氯化钠配制的(100mL生理盐水中含有0.9g医用氯化钠)
(2)农业上:
选种
2、用途
(3)工业上:
化工原料
制取碳酸钠、氢氧化钠、液氯、盐酸等
2、用途
(4)生活中:
调味品
腌制食物
(5)交通上:
融雪剂
2、用途
3、氯化钠在自然界中的分布
盐湖
盐井
盐矿
海水
通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分,得到粗盐。
粗盐的成分
杂 质
NaCl
(主要成分)
难溶性的泥沙
可溶性的 CaCl2、MgCl2等
【思考】 通过什么方法可将粗盐中难溶性杂质——泥沙除去呢?
由于NaCl溶于水,而泥沙不溶于水,可通过溶解、过滤、蒸发结晶除去泥沙
①溶解
②过滤
③蒸发
步骤一:溶解
用托盘天平称取10.0g粗盐,用药匙将粗盐逐渐加入盛有10ml水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称量剩下的粗盐.
称取粗盐/g 剩余粗盐/g 溶解粗盐/g
一、实验步骤和注意事项
溶解时玻璃棒的作用
搅拌,加速溶解
步骤二:过滤
1、一贴
2、二低
3、三靠
滤纸紧贴漏斗内壁。
滤纸边缘要低于漏斗边;
液体液面要低于滤纸边缘;
烧杯嘴要紧靠玻璃棒;
玻璃棒下端要靠在三层滤纸一边;
漏斗管末端要紧靠烧杯内壁。
步骤三:蒸发
1、加热过程中,用玻璃棒不断搅动,防止由于局部温度过高, 。
2、当蒸发皿中 ,即停止加热,利用余热使滤液蒸干。
3、停止加热时,不要立即把蒸发皿直接放在实验台上,以免烫坏实验台。
造成液滴飞溅
出现较多量固体时
步骤四:计算产率
用玻璃棒把固体转移到纸上,并计算精盐的产率
精盐的产率=
溶解粗盐/g 精盐/g 精盐产率/﹪
精盐的质量
粗盐的质量
X 100%
思考:小明实验最后的产率低于老师给出的理论产率,请问可能是哪些原因?
溶解时未将食盐充分溶解;
蒸发时未用玻璃棒搅拌有液滴飞溅
转移液体或晶体时未完全转移
过滤时液滴溅出;
思考2
在实验流程中几次用到的玻璃棒,作用分别是什么?
搅拌,加速溶解
引流
搅拌,防止液滴飞溅
1、下列各组物质中,可依次通过溶解、过滤、蒸发等操作进行分离的是( )
A.水和植物油
B.氯化镁和氯化银
C.二氧化锰粉末和铁粉
D.氯化钡和硝酸镁
B
堂堂清
2、下列是关于“粗盐提纯”实验的几种说法,其中正确的是( )
A.为加快过滤速率,应用玻璃棒不断搅拌过滤器内的液体
B.粗盐经过溶解、过滤、蒸发、结晶后得到纯净的氯化钠
C.蒸发滤液时要用玻璃棒不断搅拌,用酒精灯持续加热直到蒸干为止
D.如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因
D
3、某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50g5%的氯化钠溶液
实验一:如图是同学们做粗盐提纯实验的操作示意图.
(1)操作③中用玻璃棒搅拌的作用是 。
(2)操作⑥中的错误是 .
(3)粗盐提纯实验的操作顺序为 ( 填操作序号)、称量精盐并计算产率.
(4)操作④中,当观察到 时,停止加热.
加速溶解
未用玻璃棒引流
①⑤②③⑥④
出现较多固体
指的是一类物质
食盐(主要成分氯化钠
生活中所说的盐
化学中所说的盐
据报道,我国曾发生多次将工业用盐亚硝酸钠(NaNO2)误作食盐(NaCl)用于烹饪而引起的中毒事件。
原因就是混淆了化学中的盐和生活中的盐。
一、盐的定义
在化学中,盐是指的一类化合物,即组成里含有金属离子(或铵根离子)和酸根离子的化合物。
钠盐: NaCl Na2CO3 Na2SO4 NaNO3
钾盐: KCl K2CO3 K2SO4 KNO3
碳酸盐:Na2CO3 K2CO3 CaCO3 MgCO3
铵盐: NH4Cl (NH4)2CO3 NH4NO3
练习:将下列物质进行分类
① HCl ② Na2CO3 ③ CaCO3 ④KOH ⑤HNO3 ⑥ K2CO3
⑦ NaNO3 ⑧ H2O2 ⑨ CH3COOH ⑩ Mg(OH)2、 水、 KMnO4
酸: 。
碱: 。
盐: 。
① ⑤ ⑨
④ ⑩
② ③ ⑥ ⑦
二、氯化钠
1、食盐的主要成分是氯化钠
2、用途
(1)医疗上:
生理盐水
医疗上的生理盐水是用氯化钠配制的(100mL生理盐水中含有0.9g医用氯化钠)
(2)农业上:
选种
2、用途
(3)工业上:
化工原料
制取碳酸钠、氢氧化钠、液氯、盐酸等
2、用途
(4)生活中:
调味品
腌制食物
(5)交通上:
融雪剂
2、用途
3、氯化钠在自然界中的分布
盐湖
盐井
盐矿
海水
通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分,得到粗盐。
粗盐的成分
杂 质
NaCl
(主要成分)
难溶性的泥沙
可溶性的 CaCl2、MgCl2等
【思考】 通过什么方法可将粗盐中难溶性杂质——泥沙除去呢?
由于NaCl溶于水,而泥沙不溶于水,可通过溶解、过滤、蒸发结晶除去泥沙
①溶解
②过滤
③蒸发
步骤一:溶解
用托盘天平称取10.0g粗盐,用药匙将粗盐逐渐加入盛有10ml水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称量剩下的粗盐.
称取粗盐/g 剩余粗盐/g 溶解粗盐/g
一、实验步骤和注意事项
溶解时玻璃棒的作用
搅拌,加速溶解
步骤二:过滤
1、一贴
2、二低
3、三靠
滤纸紧贴漏斗内壁。
滤纸边缘要低于漏斗边;
液体液面要低于滤纸边缘;
烧杯嘴要紧靠玻璃棒;
玻璃棒下端要靠在三层滤纸一边;
漏斗管末端要紧靠烧杯内壁。
步骤三:蒸发
1、加热过程中,用玻璃棒不断搅动,防止由于局部温度过高, 。
2、当蒸发皿中 ,即停止加热,利用余热使滤液蒸干。
3、停止加热时,不要立即把蒸发皿直接放在实验台上,以免烫坏实验台。
造成液滴飞溅
出现较多量固体时
步骤四:计算产率
用玻璃棒把固体转移到纸上,并计算精盐的产率
精盐的产率=
溶解粗盐/g 精盐/g 精盐产率/﹪
精盐的质量
粗盐的质量
X 100%
思考:小明实验最后的产率低于老师给出的理论产率,请问可能是哪些原因?
溶解时未将食盐充分溶解;
蒸发时未用玻璃棒搅拌有液滴飞溅
转移液体或晶体时未完全转移
过滤时液滴溅出;
思考2
在实验流程中几次用到的玻璃棒,作用分别是什么?
搅拌,加速溶解
引流
搅拌,防止液滴飞溅
1、下列各组物质中,可依次通过溶解、过滤、蒸发等操作进行分离的是( )
A.水和植物油
B.氯化镁和氯化银
C.二氧化锰粉末和铁粉
D.氯化钡和硝酸镁
B
堂堂清
2、下列是关于“粗盐提纯”实验的几种说法,其中正确的是( )
A.为加快过滤速率,应用玻璃棒不断搅拌过滤器内的液体
B.粗盐经过溶解、过滤、蒸发、结晶后得到纯净的氯化钠
C.蒸发滤液时要用玻璃棒不断搅拌,用酒精灯持续加热直到蒸干为止
D.如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因
D
3、某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50g5%的氯化钠溶液
实验一:如图是同学们做粗盐提纯实验的操作示意图.
(1)操作③中用玻璃棒搅拌的作用是 。
(2)操作⑥中的错误是 .
(3)粗盐提纯实验的操作顺序为 ( 填操作序号)、称量精盐并计算产率.
(4)操作④中,当观察到 时,停止加热.
加速溶解
未用玻璃棒引流
①⑤②③⑥④
出现较多固体
同课章节目录
