1.1.1-1 物质的分类 课件 (共16张PPT) 2022-2023学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 1.1.1-1 物质的分类 课件 (共16张PPT) 2022-2023学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | zip | ||
| 文件大小 | 653.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览




文档简介
(共16张PPT)
第一章 物质及其变化
第一节 物质的分类及其变化
第一课时 物质的分类
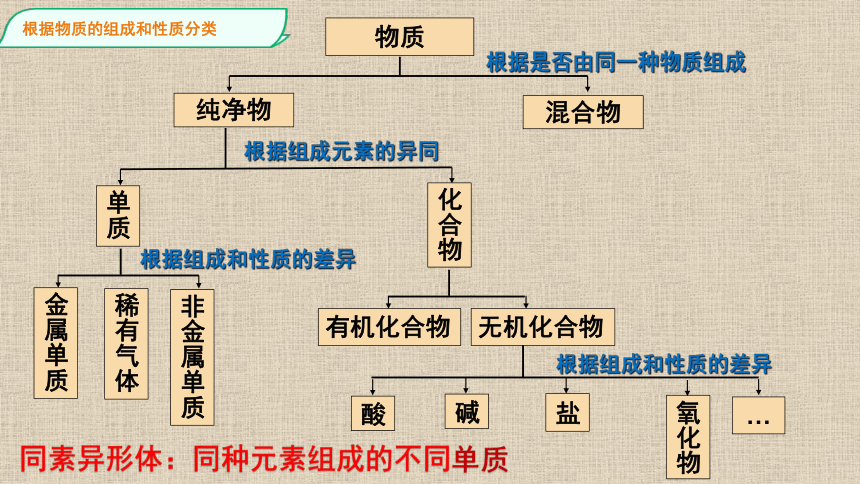
1.根据物质的组成和性质分类
美国《化学文摘》编辑部统计,已知的有机化合物的数目:
1880年约为1.2万种,
1910年约1.5万种,
1940年约为50万种,
1961年约为175万种,
1990年已超过1 000万种,
2004年,达到3 500万种以上。
要想对各物质物有条不紊地进行研究,就必须对物质分类。
方法导引
分类:根据研究对象的共同点和差异点,将它们区分为不同种类和
层次的科学方法。
意义:运用分类的方法可以发现物质及其变化的规律,预测物质的
性质及可能发生的变化。科学的分类能够反映事物的本质特
征,有利于人们分门别的的进行深入研究。
沙场练兵:请将黑板上的化学式命名并按照P7图1-3进行分类
物质
纯净物
混合物
单质
化合物
金属单质
非金属单质
氧化物
盐
碱
酸
无机化合物
有机化合物
根据是否由同一种物质组成
根据组成元素的异同
根据组成和性质的差异
根据组成和性质的差异
…
稀有气体
根据物质的组成和性质分类
同素异形体:同种元素组成的不同单质
复习
酸:阳离子全是氢离子(H+)的化合物
碱:阴离子全是氢氧根离子(OH-)的化合物
盐:由金属阳离子(或NH4+)和酸根离子构成的化合物
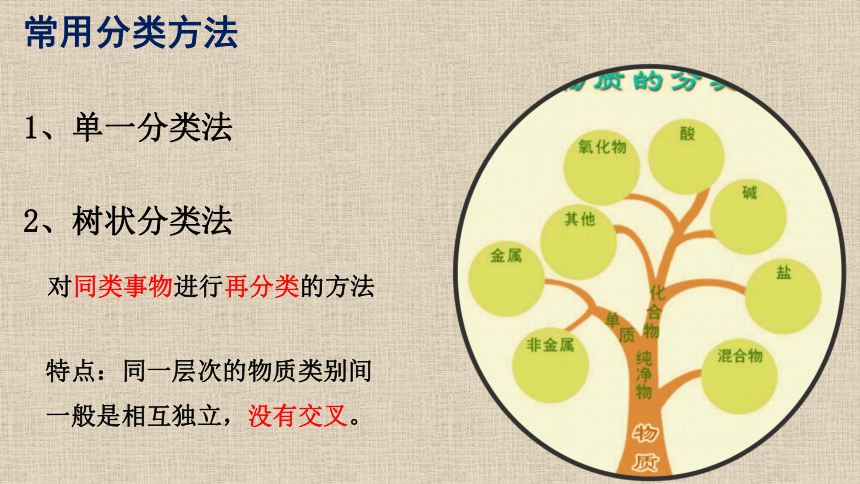
2、树状分类法
对同类事物进行再分类的方法
特点:同一层次的物质类别间一般是相互独立,没有交叉。
常用分类方法
1、单一分类法
姚明
刘翔
田亮
罗纳尔多
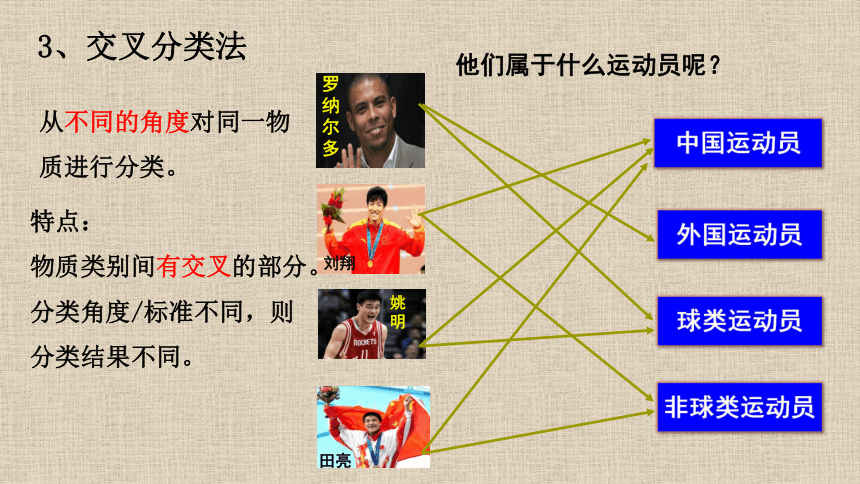
中国运动员
外国运动员
球类运动员
非球类运动员
3、交叉分类法
从不同的角度对同一物质进行分类。
特点:
物质类别间有交叉的部分。
分类角度/标准不同,则分类结果不同。
他们属于什么运动员呢?
交叉分类方法的应用练习
Na2SO4
Na2CO3
K2CO3
K2SO4
钠盐
钾盐
硫酸盐
碳酸盐
同一种事物可以按不同标准(角度)进行分类的方法
氧化物的分类:
氧化物:由氧元素与另外一种元素组成的二元化合物。
氧化物
按组成分
按性质分
金属氧化物
非金属氧化物
酸性氧化物
碱性氧化物
( SO2、CO2 、Mn2O7)
( Na2O、CaO、BaO)
( SO2、CO2 、CO、NO2)
( Na2O、CaO)
能与碱反应,只生成对应的盐和水
能与酸反应,只生成对应的盐和水
不成盐氧化物
( CO、NO、NO2)
不与酸、碱、水反应
不能得到对应的盐
两性氧化物
( Al2O3)
过氧化物
( H2O2)
树状分类方法的应用拓展
酸性氧化物和碱性氧化物的区别:
酸性氧化物
性质:能与水反应生成酸;能与碱溶液反应只生成盐和水
组成:大多数非金属元素的氧化物、某些过渡金属元素的高价氧化物
特例:Mn2O7为酸性氧化物,H2O2是过氧化物
碱性氧化物
性质:能溶于水形成可溶性碱溶液;能与酸溶液反应只生成盐和水
组成:大多数金属元素的氧化物、某些过渡金属的低价氧化物
特例:Na2O2为过氧化物,MnO为碱性氧化物
金属氧化物
碱性氧化物
非金属氧化物
酸性氧化物
碱性氧化物一定是金属氧化物!
注意!
补充:
1.酸的分类: 酸:阳离子全是氢离子(H+)的化合物
按是否含氧
酸
按提供氢离子数目
一元酸:
二元酸:
多元酸:
含氧酸、 无氧酸
HNO3
HCl
HNO3、HCl
H2SO4
能提供一个H+的酸
能提供多个H+的酸
H3PO4
按酸性强弱
强酸
HCl、H2SO4、HNO3
CH3COOH、H2CO3
能提供两个H+的酸
中强酸
H3PO4、H2SO3
弱酸
2.碱的分类: 碱:阴离子全是氢氧根离子(OH-)的化合物
1.按其在水溶液中是否溶解:
(1)可溶性碱:
(2)难溶性碱:
KOH NaOH Ba(OH)2 Ca(OH)2
Cu(OH)2 Fe(OH)3 Mg(OH)2 Zn(OH)2
2.按碱性强弱
强碱:NaOH KOH Ba(OH)2 Ca(OH)2
弱碱:NH3·H2O 、难溶性碱
3.盐的分类:
盐:由金属阳离子(或NH4+)和酸根离子构成的化合物
K+ Na+ NH4+ NO3-
(2)按是否可溶于水:
可溶性盐:
难溶性盐:
AgCl BaSO4 CaCO3
(1) 按阴、阳离子来分:
常见阳离子:
常见阴离子:
K+ Na+ NH4+ Ag+ Cu2+ Ca2+
NO3- SO42- Cl- CO32- HCO3- PO43-
(3)组成中是否有可电离的H+、OH-
正盐
酸式盐
碱式盐
Na2CO3
NaHCO3
Cu2(OH)2CO3
复盐:由两种或两种以上金属阳离子(或NH4+)和一种酸根离子构成的盐。
能电离出H+的盐
能电离出OH-的盐
不能电离出H+和OH-的盐
如KAl(SO4)2、(NH4)2Fe(SO4)2
4.单质的分类:
单质:由一种元素组成的纯净物
金属
非金属
单
质
活泼金属:
较活泼金属:
不活泼金属:
由分子构成:
由原子直接构成:
K Ca Na Mg Al Zn
Fe Sn Pb (H) Cu Hg
Ag Pt Au
金刚石、石墨
H2、Cl2、P4、O3
稀有气体:
He Ne
第一章 物质及其变化
第一节 物质的分类及其变化
第一课时 物质的分类
1.根据物质的组成和性质分类
美国《化学文摘》编辑部统计,已知的有机化合物的数目:
1880年约为1.2万种,
1910年约1.5万种,
1940年约为50万种,
1961年约为175万种,
1990年已超过1 000万种,
2004年,达到3 500万种以上。
要想对各物质物有条不紊地进行研究,就必须对物质分类。
方法导引
分类:根据研究对象的共同点和差异点,将它们区分为不同种类和
层次的科学方法。
意义:运用分类的方法可以发现物质及其变化的规律,预测物质的
性质及可能发生的变化。科学的分类能够反映事物的本质特
征,有利于人们分门别的的进行深入研究。
沙场练兵:请将黑板上的化学式命名并按照P7图1-3进行分类
物质
纯净物
混合物
单质
化合物
金属单质
非金属单质
氧化物
盐
碱
酸
无机化合物
有机化合物
根据是否由同一种物质组成
根据组成元素的异同
根据组成和性质的差异
根据组成和性质的差异
…
稀有气体
根据物质的组成和性质分类
同素异形体:同种元素组成的不同单质
复习
酸:阳离子全是氢离子(H+)的化合物
碱:阴离子全是氢氧根离子(OH-)的化合物
盐:由金属阳离子(或NH4+)和酸根离子构成的化合物
2、树状分类法
对同类事物进行再分类的方法
特点:同一层次的物质类别间一般是相互独立,没有交叉。
常用分类方法
1、单一分类法
姚明
刘翔
田亮
罗纳尔多
中国运动员
外国运动员
球类运动员
非球类运动员
3、交叉分类法
从不同的角度对同一物质进行分类。
特点:
物质类别间有交叉的部分。
分类角度/标准不同,则分类结果不同。
他们属于什么运动员呢?
交叉分类方法的应用练习
Na2SO4
Na2CO3
K2CO3
K2SO4
钠盐
钾盐
硫酸盐
碳酸盐
同一种事物可以按不同标准(角度)进行分类的方法
氧化物的分类:
氧化物:由氧元素与另外一种元素组成的二元化合物。
氧化物
按组成分
按性质分
金属氧化物
非金属氧化物
酸性氧化物
碱性氧化物
( SO2、CO2 、Mn2O7)
( Na2O、CaO、BaO)
( SO2、CO2 、CO、NO2)
( Na2O、CaO)
能与碱反应,只生成对应的盐和水
能与酸反应,只生成对应的盐和水
不成盐氧化物
( CO、NO、NO2)
不与酸、碱、水反应
不能得到对应的盐
两性氧化物
( Al2O3)
过氧化物
( H2O2)
树状分类方法的应用拓展
酸性氧化物和碱性氧化物的区别:
酸性氧化物
性质:能与水反应生成酸;能与碱溶液反应只生成盐和水
组成:大多数非金属元素的氧化物、某些过渡金属元素的高价氧化物
特例:Mn2O7为酸性氧化物,H2O2是过氧化物
碱性氧化物
性质:能溶于水形成可溶性碱溶液;能与酸溶液反应只生成盐和水
组成:大多数金属元素的氧化物、某些过渡金属的低价氧化物
特例:Na2O2为过氧化物,MnO为碱性氧化物
金属氧化物
碱性氧化物
非金属氧化物
酸性氧化物
碱性氧化物一定是金属氧化物!
注意!
补充:
1.酸的分类: 酸:阳离子全是氢离子(H+)的化合物
按是否含氧
酸
按提供氢离子数目
一元酸:
二元酸:
多元酸:
含氧酸、 无氧酸
HNO3
HCl
HNO3、HCl
H2SO4
能提供一个H+的酸
能提供多个H+的酸
H3PO4
按酸性强弱
强酸
HCl、H2SO4、HNO3
CH3COOH、H2CO3
能提供两个H+的酸
中强酸
H3PO4、H2SO3
弱酸
2.碱的分类: 碱:阴离子全是氢氧根离子(OH-)的化合物
1.按其在水溶液中是否溶解:
(1)可溶性碱:
(2)难溶性碱:
KOH NaOH Ba(OH)2 Ca(OH)2
Cu(OH)2 Fe(OH)3 Mg(OH)2 Zn(OH)2
2.按碱性强弱
强碱:NaOH KOH Ba(OH)2 Ca(OH)2
弱碱:NH3·H2O 、难溶性碱
3.盐的分类:
盐:由金属阳离子(或NH4+)和酸根离子构成的化合物
K+ Na+ NH4+ NO3-
(2)按是否可溶于水:
可溶性盐:
难溶性盐:
AgCl BaSO4 CaCO3
(1) 按阴、阳离子来分:
常见阳离子:
常见阴离子:
K+ Na+ NH4+ Ag+ Cu2+ Ca2+
NO3- SO42- Cl- CO32- HCO3- PO43-
(3)组成中是否有可电离的H+、OH-
正盐
酸式盐
碱式盐
Na2CO3
NaHCO3
Cu2(OH)2CO3
复盐:由两种或两种以上金属阳离子(或NH4+)和一种酸根离子构成的盐。
能电离出H+的盐
能电离出OH-的盐
不能电离出H+和OH-的盐
如KAl(SO4)2、(NH4)2Fe(SO4)2
4.单质的分类:
单质:由一种元素组成的纯净物
金属
非金属
单
质
活泼金属:
较活泼金属:
不活泼金属:
由分子构成:
由原子直接构成:
K Ca Na Mg Al Zn
Fe Sn Pb (H) Cu Hg
Ag Pt Au
金刚石、石墨
H2、Cl2、P4、O3
稀有气体:
He Ne
